Гемолитическая болезнь новорождённых (ГБН) — патологическое состояние новорождённого, сопровождающееся массивным распадом эритроцитов, является одной из основных причин развития желтухи у новорождённых.
Гемолитическая болезнь новорожденных диагностируется у 0,6% новорожденных. Гемолитическая болезнь новорожденных проявляется в 3 основных формах: анемической, желтушной, отечной.
Гемолитическая болезнь новорожденных (morbus haemoliticus neonatorum) — гемолитическая анемия новорожденных, обусловленная несовместимостью крови матери и плода по резус- фактору, группе крови и другим факторам крови. Заболевание наблюдается у детей с момента рождения или выявляется в первые часы и дни жизни.
Гемолитическая болезнь новорожденных, или фетальный эритробластоз, является одним из тяжелых заболеваний детей периода новорожденности. Возникая в антенатальный период, это заболевание может быть одной из причин спонтанных абортов и мертворождений. По данным ВОЗ (1970), гемолитическая болезнь новорожденных диагностируется у 0,5% новорожденных, смертность от нее составляет 0,3 на 1000 детей, родившихся живыми.
Причина гемолитической болезни новорожденных стала известна только в конце 40-х годов XX в. в связи с развитием учения о резус-факторе. Этот фактор был открыт Landsteiner и Wiener в 1940 г. у обезьян Macacus rhesus. В дальнейшем эти же исследователи установили, что резус- фактор присутствует в эритроцитах 85% людей.
Дальнейшие исследования показали, что гемолитическая болезнь новорожденных может быть обусловлена несовместимостью крови матери и плода как по резус-фактору, так и по группе крови. В редких случаях заболевание возникает в результате несовместимости крови матери и плода по другим факторам крови (М, N, М5, N3, Rell, Kidd, Luis и др.).
Резус-фактор находится в строме эритроцитов. Он не имеет связи с полом, возрастом и принадлежностью к системам АВО и MN. Имеется шесть основных антигенов системы резус, передаваемых по наследству тремя парами генов и обозначаемых либо С, с, D, d, Е, е (по Фишеру), либо rh’, hr’, Rh, hr, rh», hr» (по Виннеру). В возникновении гемолитической болезни новорожденных наиболее важное значение имеет D- антиген, отсутствующий у матери и присутствующий у плода в результате наследования его от отца.
Гемолитическая болезнь новорожденных, обусловленная несовместимостью по системе АВО, чаще встречается у детей с группами крови А(II) или В (III). У матерей этих детей имеется 0(I) группа крови, в которой содержатся агглютинины α иβ. Последние могут блокировать эритроциты плода.
Установлено, что матери, дети которых родились с проявлениями гемолитической болезни, в большинстве случаев еще до наступления данной беременности были сенсибилизированы к эритроцитарным антигенам этого плода за счет предшествующих гемотрансфузий, а также беременностей резус-поло- жительным плодом.
В настоящее время известно три вида резус-антител, образующихся в сенсибилизированном организме людей с резус- отрицательной кровью: 1) полные антитела, или агглютинины, 2) неполные, или блокирующие, 3) скрытые.
Полные антитела — это антитела, способные путем обычного контакта вызывать агглютинацию эритроцитов, специфичных для данной сыворотки; эта реакция не зависит от солевого или коллоидного состояния среды. Неполные антитела могут вызывать агглютинацию эритроцитов лишь в среде, содержащей высокомолекулярные субстанции (сыворотка, альбумин, желатин). Скрытые резус-антитела находятся в сыворотке человека с резус-отрицательной кровью в очень высокой концентрации.
В возникновении гемолитической болезни новорожденных наиболее важная роль принадлежит неполным резус-антителам, способным легко проникать через плаценту в организм плода в связи с небольшим размером молекулы.
Нормальное течение беременности предусматривает синтез женщиной антител к поступающим к ней генетически чужеродным антигенам плода отцовского происхождения. Установлено, что в плаценте и околоплодных водах материнские антитела связываются антигенами плода. При предшествующей сенсибилизации, при патологическом течении беременности барьерные функции плаценты снижаются, и материнские антитела могут поступить к плоду. Наиболее интенсивно это происходит во время родов. Поэтому гемолитическая болезнь новорожденных, как правило, начинается после рождения.
В патогенезе гемолитической болезни основное значение имеет возникновение гемолиза эритроцитов у плода или новорожденного ребенка за счет повреждения мембраны клеток красного ряда материнскими антителами. Это приводит к преждевременному внесосудистому гемолизу. При распаде гемоглобина образуется билирубин (из каждого грамма гемоглобина образуется 35 мг билирубина).
Интенсивный гемолиз эритроцитов и ферментативная незрелость печени плода и новорожденного ребенка приводят к накоплению в крови свободного (непрямого) билирубина, который обладает токсическими свойствами. Он нерастворим в воде, не выводится с мочой, зато легко проникает в ткани, богатые липидами: головной мозг, надпочечники, печень, нарушая процессы клеточного дыхания, окислительного фосфорилирования и транспорта некоторых электролитов.
Тяжелым осложнением гемолитической болезни является ядерная желтуха (kernicterus), обусловленная токсическим действием непрямого билирубина на ядра основания мозга (субталамические, гипокампа, стриарного тела, мозжечка, черепных нервов). Возникновению этого осложнения способствуют недоношенность, ацидоз, гипоальбуминемия, инфекционные заболевания, а также высокий уровень непрямого билирубина в крови (более 342 мкмоль/л). Известно, что при уровне билирубина в сыворотке крови 342-428 мкмоль/л ядерная желтуха возникает у 30% детей.
В патогенезе гемолитической болезни новорожденных определенную роль играет нарушение функции печени, легких, сердечно-сосудистой системы.
Клинически различают три формы гемолитической болезни новорожденных: отечную, желтушную и анемичную.
Отечная форма является наиболее тяжелой. Для нее хахарактерны выраженные отеки с накоплением жидкости в полостях (плевральной, брюшной), бледность кожных покровов и слизистых оболочек, значительное увеличение размеров печени и селезенки. У некоторых новорожденных наблюдаются небольшие кровоподтеки и петехии.
Большие изменения наблюдаются в составе периферической крови. У таких больных количество гемоглобина снижено до 30-60 г/л, число эритроцитов часто не превышает 1×10 12 /л, выражены анизоцитоз, пойкилоцитоз, полихромазия, нормо- и эритробластоз; общее число лейкоцитов увеличено, отмечается нейтрофилез с резким сдвигом влево. Анемия у таких детей бывает настолько выраженной, что в сочетании с гипопротеинемией и повреждением стенки капилляров приводит к развитию сердечной недостаточности, которая и считается основной причиной смерти до рождения ребенка или вскоре после него.
Желтушная форма является самой частой клинической формой гемолитической болезни новорожденных. Первым симптомом заболевания является желтуха, возникающая на 1-2-й день жизни. Интенсивность и оттенок желтухи постепенно меняются: вначале апельсиновый, потом бронзовый, затем лимонный и, наконец, цвет незрелого лимона. Отмечается желтушное прокрашивание слизистых оболочек, склер. Увеличиваются размеры печени и селезенки. Внизу живота наблюдается пастозность тканей. Дети становятся вялыми, адинамичными, плохо сосут, у них снижаются рефлексы новорожденных.
При исследовании периферической крови выявляются анемия разной степени выраженности, псевдолейкоцитоз, который возникает за счет увеличения молодых ядросодержащих клеток красного ряда, воспринимающихся в камере Горяева как лейкоциты. Значительно увеличивается количество рети- кулоцитов.
Для желтушной формы гемолитической болезни новорожденных характерным является повышение уровня непрямого билирубина в крови. Уже в пуповинной крови его уровень может быть выше 60 мкмоль/л, а в дальнейшем он достигает 265-342 мкмоль/л и более. Четкой связи между степенью желтушности кожи, тяжестью анемии и выраженностью гипер- билирубинемии обычно не бывает, но считается, что желтуш- ность ладоней свидетельствует об уровне билирубина 257 мкмоль/л и выше.
Тяжелыми осложнениями желтушной формы гемолитической болезни новорожденных являются поражение нервной системы и развитие ядерной желтухи. При возникновении этих осложнений у ребенка вначале появляются нарастающая вялость, снижение мышечного тонуса, отсутствие или угнетение рефлекса Моро, срыгивания, рвота, патологическое зевание. Затем появляются классические признаки ядерной желтухи: мышечная гипертония, ригидность затылочных мышц, вынужденное положение тела с опистотонусом, негнущимися конечностями, сжатыми в кулак кистями, резкий «мозговой» крик, гиперстезия, выбухание родничка, подергивание мышц лица, судороги, симптом «заходящего солнца», нистагм, симптом Грефе; периодически возникает апноэ.
Другим сравнительно частым осложнением является синдром сгущения желчи. Его признаками являются обесцвеченный стул, насыщенный цвет мочи, увеличение печени. При исследовании крови обнаруживают повышение уровня прямого билирубина.
Анемическая форма наблюдается у 10-15% больных гемолитической болезнью новорожденных. Ранними и постоянными симптомами ее следует считать общую выраженную вялость и бледность кожных покровов и слизистых оболочек. Бледность отчетливо выявляется к 5-8-му дню после рождения, так как в первое время она маскируется небольшой желтухой. Наблюдается увеличение размеров печени и селезенки.
В периферической крови при этой форме содержание гемоглобина снижено до 60-100 г/л, количество эритроцитов находится в пределах 2,5×10 12 /л-3,5×10 12 /л, наблюдается нормобластоз, ретикулоцитоз. Уровень билирубина нормальный или умеренно повышенный.
Диагноз гемолитической болезни новорожденных основывается на данных анамнеза (сенсибилизация матери за счет предшествующих гемотрансфузий; рождение детей в данной семье с желтухой, смерть их в периоде новорожденности; указания матери на бывшие у нее ранее поздние выкидыши, мертворождения), на оценке клинических симптомов и на данных лабораторных исследований. Последние в диагностике заболевания имеют ведущее значение.
В первую очередь проводится определение группы крови и резус-принадлежности матери и ребенка, исследуется содержание ретикулоцитов в периферической крови и уровень билирубина в венозной крови у ребенка.
При резус-несовместимости определяют титр резус-анти- тел в крови и молоке матери, проводят прямую пробу Кумбса с эритроцитами крови ребенка и непрямую с сывороткой крови матери. При несовместимости по системе АВО в крови и молоке матери определяют титр а- или р-агглютининов в солевой и белковой средах. Иммунные антитела в белковой среде имеют титр в четыре раза выше, чем в солевой. Эти антитела относятся к иммуноглобулинам класса G и проникают через плаценту, вызывая развитие гемолитической болезни новорожденных. Прямая реакция Кумбса при АВО-несовместимости, как правило, отрицательная.
Если клинико-лабораторные данные четко указывают на гемолиз, а кровь матери и ребенка совместимы по резус-фактору и системе АВО, то целесообразно поставить реакцию Кумбса, провести пробу на индивидуальную совместимость крови матери и эритроцитов ребенка, искать антитела к антигенам, редко вызывающим гемолитическую болезнь новорожденных: с, d, е, Kell, Diffy, Kidd.
Для антенатальной диагностики прогностическое значение имеет определение билирубина в околоплодных водах при сроках беременности 32-38 нед: при оптической спектрофотометрической плотности околоплодных вод (при фильтре 450 нм) 0,15-0,22 ед. развивается легкая форма гемолитической болезни новорожденных, выше 0,35 ед. — тяжелая форма. Отечную форму гемолитической болезни новорожденных в антенатальном периоде можно диагностировать с помощью ультразвукового исследования.
Выявлению сенсибилизированных к резус-антигенам женщин способствует определение титра резус-антител в крови беременных. Однако не всегда степень повышения титра резус-антител в крови беременной соответствует тяжести гемолитической болезни. Прогностически неблагоприятным считают скачущий титр резус-антител беременной женщины.
Гемолитическую болезнь новорожденных приходится дифференцировать с рядом заболеваний и физиологических состояний. В первую очередь нужно установить гемолитический характер заболевания и исключить гипербилирубинемию печеночного и механического происхождения.
Среди причин, вызывающих появление желтух второй группы у новорожденных детей, наибольшее значение имеют врожденные заболевания инфекционной природы: вирусный гепатит, сифилис, туберкулез, листериоз, токсоплазмоз, цито- мегаловирусная инфекция, а также сепсис, приобретенный не только внутриутробно, но и после рождения.
Общими признаками желтух этой группы являются следующие: отсутствие признаков гемолиза (анемии, признаков раздражения красного ряда кроветворения, повышения уровня непрямого билирубина, увеличения селезенки) и повышение уровня прямого билирубина.
Следует также помнить, что у новорожденных детей может наблюдаться механическая желтуха, которая появляется, как правило, в связи с аномалией развития желчных путей — агенезией, атрезией, стенозом и кистами внутрипеченочных желчных протоков. В этих случаях желтуха появляется обычно к концу 1-й недели, хотя может появиться и в первые дни жизни. Она прогрессивно усиливается, и кожа приобретает темно-зеленый, а в некоторых случаях и коричневатый оттенок. Кал может быть слабо окрашенным. При аномалиях развития желчных путей количество билирубина в сыворотке крови очень высокое, может достичь 510-680 мкмоль/л за счет повышения прямого билирубина. В тяжелых и далеко зашедших случаях может увеличиться и непрямой билирубин вследствие невозможности конъюгации его за счет переполнения клеток печени билирубином желчи. Моча темная и окрашивает пеленки в желтый цвет. Количество холестерина и щелочной фосфатазы обычно повышено. Печень и селезенка увеличены и с усилением желтухи уплотняются. Постепенно у детей развивается дистрофия, появляются признаки гиповитаминоза К, Д и А. Развивается билиарный цирроз печени, от которого дети умирают, не достигнув возраста 1 года.
При высоком уровне непрямого билирубина в крови и при отсутствии других признаков повышенного гемолиза эритроцитов возникает подозрение на конъюгационный характер желтухи. В таких случаях целесообразно в сыворотке крови ребенка исследовать активность лактатдегидрогеназы и ее первой фракции — гидроксибутиратдегидрогеназы. При гемолитической болезни новорожденных уровень этих ферментов резко повышен, а при конъюгационной желтухе соответствует возрастной норме.
Нельзя забывать о существовании достаточно редкого заболевания, известного как синдром Криглер — Найяра (Krigler и Najar). Это негемолитическая гипербилирубине- мия, сопровождаемая развитием ядерной желтухи. Заболевание наследуется по аутосомно-рецессивному типу. Мальчики болеют чаще девочек.
В основе синдрома Криглер — Найяра лежит резкое нарушение образования билирубиндиглюкоронида (прямого билирубина) вследствие полного отсутствия УДФ-глюкоронил- трансферазы, конъюгирующей билирубин. Основной симптом заболевания — желтуха, которая появляется в первые сутки после рождения и интенсивно нарастает, удерживаясь на протяжении жизни ребенка. Желтуха связана с резким повышением в крови непрямого билирубина, количество которого очень быстро достигает 340-850 мкмоль/л. На фоне резкого повышения в крови непрямого билирубина развиваются симптомы ядерной желтухи. Анемии не наблюдается. Количество молодых форм эритроцитов не повышено. Количество уробилина в моче в пределах нормы. Желчь лишена прямого, конъюгированного билирубина. Поражение центральной нервной системы приводит к гибели ребенка в первые месяцы жизни. Дети редко доживают до 3 лет.
Наследственные гемолитические анемии диагностируются на основании (специфических морфологических признаков эритроцитов, измерения их диаметра, осмотической стойкости, исследования активности ферментов эритроцитов (прежде всего глюкозо-6-фосфатдегидрогеназы и др.), типов гемоглобина.
Лечение гемолитической болезни новорожденных с высоким уровнем непрямого билирубина может быть консервативным или оперативным (операция заменного переливания крови).
Для новорожденных с гемолитической болезнью очень важно достаточное питание.
Консервативное лечение гемолитической болезни новорожденных включает следующие мероприятия:
- мероприятия, направленные на уменьшение гемолиза за счет стабилизации мембраны эритроцитов (внутривенные вливания 5% раствора глюкозы, назначение АТФ, эревита);
- терапию, способствующую ускорению метаболизма и экскреции билирубина из организма (прием фенобарбитала из расчета до 10 мг/кг в сутки, разделенный на три приема, внутрь);
- назначение веществ, адсорбирующих билирубин в кишечнике и ускоряющих его экскрецию с фекалиями (агар- агар по 0,1 г три раза в день внутрь; 12,5% раствор ксилита или сульфата магния внутрь по 1 чайной ложке три раза в день или аллохол по ‘/2 измельченного драже также три раза в день внутрь);
- использование средств и мероприятий по уменьшению токсичности непрямого билирубина (фототерапия); в последнее время появились сообщения об эффективности в борьбе с токсическим действием непрямого билирубина малых доз ультрафиолетового облучения.
Полезно проводить инфузионную терапию. Объем инфузионной терапии следующий: в первые сутки — 50 мл/кг и далее добавляют по 20 мл/кг в сутки, доведя до 150 мл/кг к 7-му дню.
Состав инфузионного раствора: 5% раствор глюкозы с добавлением на каждые 100 мл 1 мл 10% раствора кальция, со второго дня жизни-1 ммоль натрия и хлора, с третьих суток — 1 ммоль калия. Скорость вливания — 3-5 капель в 1 мин. Добавление 5% раствора альбумина показано лишь детям с инфекционными заболеваниями, недоношенным, при выявлении гипопротеинемии (ниже 50 г/л). Вливания гемодез и реополиглюкина при гемолитической болезни новорожденных не показаны.
Заменное переливание крови проводится по определенным показаниям. Абсолютным показанием к заменному переливанию крови является гипербилирубинемия выше 342 мкмоль/л, а также темп нарастания билирубина выше 6 мкмоль/л в 1 час, уровень его в пуповинной крови выше 60 мкмоль/л.
Показаниями к заменному переливанию крови в первые сутки жизни являются анемия (гемоглобин менее 150 г/л), нормобластоз и доказанная несовместимость крови матери и ребенка по группе или резус-фактору.
При резус-конфликте для заменного переливания крови используют кровь той же группы, что и у ребенка, резус-отрица- тельную не более 2-3 дней консервации, в количестве 150- 180 мл/кг (при уровне непрямого билирубина более 400 мкмоль/л — в объеме 250-300 мл/кг). При АВО-конфликте переливают кровь группы 0(I) с низким титром а- и ß-агглютининов, но в количестве 250-400 мл; при этом, как правило, на следующий день надо сделать повторную заменную трансфузию в том же объеме. Если у ребенка имеется одновременно несовместимость по ресуз- и АВО-антигенам, то ребенку надо переливать кровь 0(I) группы.
При проведении заменного переливания крови катетер в пупочную вену вводят на длину не более чем 7 см. Кровь должна быть подогрета до температуры не менее 28° С. Содержимое желудка до операции отсасывают. Начинают процедуру с выведения 40-50 мл крови ребенка, количество введенной крови должно быть на 50 мл больше выведенной. Операция проводится медленно (3-4 мл в 1 мин), чередуется выведение и введение по 20 мл крови. Продолжительность всей операции не менее 2 ч. Следует помнить, что на каждые 100 мл введенной крови надо ввести 1 мл 10% раствора глюконата кальция. Это делается для предупреждения цитратного шока. Через 1-3 ч после заменного переливания крови следует определить уровень глюкозы в крови.
К осложнениям заменного переливания крови относятся: острая сердечная недостаточность при быстром введении больших количеств крови, нарушения ритма сердечной деятельности, трансфузионные осложнения при неправильном подборе донора, электролитные и обменные расстройства (гиперкалиемия, гипокальциемия, ацидоз, гипогликемия), геморрагический синдром, тромбозы и эмболии, инфекционные осложнения (гепатит и др.), некротический энтероколит.
После заменного переливания крови назначают консервативную терапию. Показанием к повторному заменному переливанию крови служит темп прироста непрямого билирубина (заменное переливание крови показано при темпе прироста билирубина более 6 мкмоль/л в 1 ч).
Для проведения заменного переливания крови необходимо иметь следующий набор инструментов: стерильные полиэтиленовые катетеры № 8, 10, пуговчатый зонд, ножницы, два хирургических пинцета, иглодержатель, шелк, четыре-шесть шприцев вместимостью 20 мл и два-три шприца вместимостью 5 мл, два стакана по 100-200 мл.
Техника катетеризации пупочной вены заключается в следующем: после обработки операционного поля конец пуповинного остатка срезают поперек на расстоянии 3 см от пупочного кольца; осторожными вращательными движениями вводят катетер, направляя его после прохождения пупочного кольца вверх вдоль брюшной стенки, по направлению к печени. Если катетер введен правильно, то через него выделяется кровь.
Основные принципы профилактики гемолитической болезни новорожденных заключаются в следующем. Во-первых, учитывая большое значение предшествующей сенсибилизации в патогенезе гемолитической болезни новорожденных, к каждой девочке следует относиться как к будущей матери, в связи с чем проводить гемотрансфузии девочкам нужно только по жизненным показаниям. Во-вторых, важное место в профилактике гемолитической болезни новорожденных отводится работе по разъяснению женщинам вреда аборта. Для предупреждения рождения ребенка с гемолитической болезнью новорожденных всем женщинам, имеющим резус-отрицательный фактор крови, в первый день после аборта (или после родов) рекомендуется введение анти-О-глобулина в количестве 250-300 мкг, который способствует быстрой элиминации эритроцитов ребенка из крови матери, предотвращая синтез резус-антител матерью. В-третьих, беременных с высоким титром антирезус-антител госпитализируют на 12-14 дней в дородовые отделения в сроки 8, 16, 24, 32 нед, где им проводят неспецифическое лечение: внутривенные вливания глюкозы с аскорбиновой кислотой, кокарбоксилазой, назначают рутин, витамин Е, глюконат кальция, кислородную терапию; при развитии угрозы прерывания беременности назначают прогестерон, эндоназальный электрофорез витаминов В1, С. За 7-10 дней до родов показано назначение фенобарбитала по 100 мг три раза в день. В-четвертых, при нарастании у беременной женщины титров антирезус-антител родоразрешение проводится досрочно на 37-39-й неделе путем операции кесарева сечения.
Гемолитическая болезнь новорожденных: последствия могут быть опасными, вплоть до смерти ребёнка, могут нарушиться функции печени и почек у ребёнка. Начинать лечение надо сразу.
Прогноз гемолитической болезни новорожденных зависит от формы заболевания и адекватности проводимых профилактических и лечебных мероприятий. Больные отечной формой нежизнеспособны. Прогноз при желтушной форме благоприятен при условии проведения адекватного лечения; прогностически неблагоприятно развитие билирубиновой энцефалопатии и ядерной желтухи, поскольку в группе таких больных очень высок процент инвалидности. Анемическая форма гемолитической болезни новорожденных прогностически благоприятна; у больных этой формой наблюдается самоизлечение.
Современный уровень развития медицины, правильная диагностическая и лечебная тактика позволяют избежать выраженных последствий гемолитической болезни новорожденных.
источник
ГЕМОЛИТИЧЕСКАЯ БОЛЕЗНЬ ПЛОДА И НОВОРОЖДЕННОГО (ГБН) – изоимунная гемолитическая анемия, возникающая в случаях несовместимости крови матери и плода по эритроцитарным антигенам, при этом антигены локализуются на эритроцитах плода, а антитела на них вырабатываются в организме матери.
Эпидемиология. В России ГБН диагностируют примерно у 0,6% новорожденных.
Этиология. Конфликт возникает, если мать антиген-отрицательная, а плод антиген–положительный. При несовместимости по резус-фактору мать резус-отрицательная, а плод резус-положительный. При групповой несовместимости у матери 0(I) группа крови, а у плода А(II) или В(III). Значительно реже ГБН обусловлена несовместимостью плода и матери по другим антигенным системам (Kell, Duffi, Kidd и др.).
Патогенез. К ГБН по резус-факторам чаще приводит сенсибилизация резус-отрицательной матери к резус-D-антигену, значительно реже встречаются гемато-иммунологический конфликт по другим антигенам этой системы (С, с, е). Для этого необходимо попадание крови ребенка в кровоток матери. Сенсибилизирующими факторами являются прежде всего предыдущие беременности, в том числе закончившиеся абортами. Поэтому ГБН по резус-фактору, как правило, развивается у детей, родившихся от повторной беременности. При конфликте по группе крови этой закономерности не отмечено, и ГБН может возникнуть уже при первой беременности, но при нарушении барьерных функций плаценты, связанных с наличием у матери соматической патологии или гестоза.Эритроциты плода регулярно обнаруживаются в кровотоке матери, начиная с 16-18-й недели беременности, но общее количество из не превышает 0,1-0,2 мл. Наиболее выраженная трансплацентарная трансфузия происходит во время родов (3-4 мл крови плода). Проникшие в кровоток матери эритроциты плода, содержащие отсутствующий у матери D-антиген, стимулируют первичный иммунный ответ, результатом которого является синтез Rh-антител, относящихся к иммуноглобулинам класса М, которые не могут проникать через плаценту. В дальнейшем синтезируются антитела класса G, которые через плаценту проникают и вызывают гемолиз эритроцитов плода.
При отечной форме ГБН гемолиз начинается с 18-22 недель беременности, что приводит к выраженной анемии плода. В результате развивается тяжелая гипоксия плода, которая вызывает глубокие метаболические нарушения и повреждения сосудистой стенки, происходит снижение синтеза альбумина. Альбумин и вода перемещаются из крови плода в интерстиций ткани, что сопровождается массивными отеками. Повреждение сосудистой стенки, гипоальбуминемия лежат в основе развивающейся недостаточности кровообращения. Гепатоспленомегалия развиваются в результате эритроидной метаплазии органов. Гепатоспленомегалия является причиной высокого стояния диафрагмы, что приводит к гипоплазии легких.
При желтушной форме ГБН гемолиз начинается незадолго до родов, что приводит к значительному повышению уровня непрямого билирубина, который накапливается в головном мозге, в частности, в ядрах мозга. Большое количество непрямого билирубина в печени связаться не может, что приводит к нарушению экскреции желчи.
Анемическая форма ГБН развивается в случаях поступления небольших количеств материнских антител в кровоток плода перед родами. Гемолиз не носит интенсивного характера, а печень новорожденного ребенка достаточно активно выводит свободный билирубин.
Классификация. В зависимости от вида конфликта выделяют:
несовместимость эритроцитов матери и плода по резус-фактору;
несовместимость по системе АВ0;
несовместимость по редким факторам крови;
По клиническим проявлениям выделяют:
отечная форма (гемолитическая анемия с водянкой);
желтушная форма (гемолитическая анемия с желтухой);
анемическая форма (гемолитическая анемия без желтухи и водянки).
По степени тяжести желтухи в желтушной форме различают легкую, средней тяжести и тяжелую степень.
По наличию осложнений выделяют осложненную (ядерная желтуха, синдром сгущения желчи, геморрагический синдром, поражение почек, надпочечников и др.) и неосложненные формы ГБН.
Исследования. Общий анализ мочи, развернутый анализ крови, уровень билирубина крови и его фракции, протеинограмма, трансаминазы (АсАТ, АлАТ), холестерин, щелочная фосфатаза, ретикулоциты, определение резус-принадлежности матери и ребенка, определение группы крови матери и ребенка, определение титров антирезусных и групповых (α или β) антител, реакция Кумбса.
Табл. 2.21.Исследование беременной и плода при подозрении на ГБН
Характерные изменения при ГБ плода
Иммунологическое обследование беременной
Определение титра антирезус — АТ
Наличие титра АТ и их динамика (повышение или снижение)
Измерение объема плаценты
Измерение количества околоплодных вод
Увеличение толщины плаценты
Гепатоспленомегалия увеличение размеров живота по сравнению с размерами головки и грудной клетки. Асцит
Допплерометрия плодово-плацентарного и маточно-плацентарного кровотока
Повышение систоло-диастолического отношения и индекса резистентности
Повышение скорости кровотока
Кардиотокография с определением показателя состояния плода
Монотонный ритм при среднетяжелой и тяжелой формах ГБ и «синусоидальный» ритм при отечной форме ГБ плода
Исследование околоплодных вод (при амниоцентезе
Величина оптической плотности билирубина
Кордоцентез и исследование крови плода
Табл. 2.22.Обследование при подозрении на ГБН
Характерные изменения при ГБН
Биохимический анализ крови
Билирубин (общий, прямой, непрямой)
Гипербилирубинемия за счет непрямой фракции; увеличение прямой фракции при осложнении —
синдром сгущения желчи (холестаз)
Гипопротеинемия и альбуминемия уменьшают транспорт СБ к печени
повышен при холестазе (осложнение)
Снижен. Анемия гиперрегенаторная, нормо- или гиперхромная
М.б. повышены в ответ на гипоксию или рано начавшийся гемолиз
Rh-принадлежность при возможной Rh – сенсибилизации
Группа крови при возможной АВО-сенсибилизации
Преимущественно А(II) или В(III), АВ (IV) — реже
Иммунные в любом титре или естественные в титре 1024 и выше
Анамнез, клиника. В анамнезе: медицинские аборты, самопроизвольные выкидыши, внематочная беременность, роды, инвазивные диагностические методы исследования.
Для всех форм ГБН характерным является наличие: бледности кожных покровов и слизистых оболочек, увеличение печени и селезенки.
Для отечной формыГБН характерны: массивные отеки, развитие геморрагических проявлений, сердечно-легочная недостаточность, выраженная гепатоспленомегалия, отсутствие выраженной желтухи.
Желтушная форма ГБНпроявляется появлением желтухи при рождении или в первые сутки жизни, гепатоспленомегалией. По мере увеличения уровня билирубина нарастают вялость, сонливость, появляются изменения в неврологическом статусе. При отсутствии своевременного лечения может развиться билирубиновая энцефалопатия, которая протекает стадийно.
В I (обратимой) стадиипоявляются прогрессирующая вялость, нарушение сосания, приступы апноэ. Обычно в связи с кратковременностью ее не успевают зафиксировать, но у недоношенных младенцев смерть может наступить уже в этой стадии.
II стадияносит название ядерной желтухи и проявляется на 3-4 день жизни опистотонусом, ригидностью мышц затылка, судорогами, сопровождающимися апноэ и сердечными аритмиями, «мозговым» криком, выбуханием большого родничка, появлением симптома «заходящего солнца», вертикальным нистагмом. Чаще в эту стадию ребенок погибает.
III стадия.В дальнейшем состояние выживших детей улучшается (период мнимого благополучия).
IV стадия.Повторное ухудшение состояния наступает через несколько недель, когда начинают формироваться тяжелые и необратимые изменения со стороны нервной системы, к особенностям билирубиновой энцефалопатии следует формирование тугоухости и глухоты (механизм избирательного пораженияVIIIпары ЧМН до сих пор остается неясным).
В зависимости от выраженности анемии и гипербилирубинемии выделяют три степени тяжести данной формы ГБН.
Для анемической формыхарактерны: относительно легкое течение заболевания, бледность кожных покровов, снижение уровня гемоглобина и эритроцитов до 2 мес. жизни (максимально на 2-3-й неделе жизни), вялость, адинамия, тахикардия, гепатоспленомегалия.
Диагноз. Ранняя диагностика ГБН по резус-фактору во время беременности может осуществляться на основании наличия в сыворотке крови матери антирезус-антител. Прогностически неблагоприятным считается появление в крови беременной анти-D-антител класса G (неполных резус-антител) и рост их титра в динамике выше 1:8 – 1:16, «скачущие» титры. При этом необходимо углубленное изучение функционального состояния плода с использованием ультразвуковых методов (утолщение плаценты, многоводие, увеличение размеров живота у ребенка) и амниоцентеза (определение в околоплодной жидкости уровня билирубина, общего белка, глюкозы и др.).
ГБН может быть установлена на основании клинических и лабораторных данных как при рождении (исследование в пуповинной крови уровней гемоглобина и билирубина, выявление положительной пробы Кумбса или групповых иммунных антител, повышение в крови молодых форм эритроцитов – эритробласты, нормобласты, высокого ретикулоцитоза), так и в первые часы жизни. При исследовании уровня билирубина существенным является определение его значений в динамике с расчетом почасового прироста билирубина.
Тяжесть ГБН определяется по совокупности степени выраженности в момент рождения основных симптомов: отечности, желтухи и анемии. Оценка состояния ребенка, равная 1-3 баллам, соответствует легкой форме гемолитической болезни, 4-6 баллам – средней тяжести, от 7 до 9 баллов – тяжелой форме заболевания.
Табл.2.23.Критерии степени тяжести гемолитической болезни(Сидельникова В.М., Антонов А.Г., 2004).
Основные клинические признаки
Степень тяжести гемолитической болезни
Анемия (содержание гемоглобина в крови пуповины, г/л)
Желтуха (содержание билирубина в крови пуповины, мкмоль/л)
Пастозность подкожной клетчатки
Дифференциальный диагноз ГБН проводят с другими гемолитическими анемиями, конъюгационными желтухами новорожденных (болезнь Криглера-Найяра, Люцей-Дрискола и др.), массивными кровоизлияниями в замкнутую полость, внутриутробными инфекциями (фетальный гепатит), полицитемией.
Для исключения гемолитических анемий (сфероцитоз, талассемия и др.) необходим тщательный сбор анамнеза, определение осмотической резистентности эритроцитов, морфологии эритроцитов, уровня ферментов эритроцитов, типов гемоглобина.
Табл. 2. 24. Дифференциальный диагноз ГБН
При рождении или в первые сутки
Характер повышения билирубина
Вначале непрямой, затем прямой
Норма или незначительное повышение
Лечение. Задачи лечения: сохранение беременности до срока достижения плодом жизнеспособности, снижение выраженности гемолиза, коррекция анемии и гипербилирубинемии, лечение легочно-сердечной недостаточности, профилактика ядерной желтухи и тяжелой анемии.
Гемолитическая болезнь плода
Немедикаментозное лечение: плазмаферез, реокоррекция, иммунокоррекция.
Медикаментозное лечение: кордоцентез с внутриутробной трансфузией эритроцитарной массой в сроки беременности 24-35 недель.
Показанием для кордоцентеза является: отягощенный акушерский анамнез, положительный резус-фактор плода, положительные УЗ-признаки гемолитической болезни плода, повышение уровня билирубина в околоплодных водах, наличие титра антител 1:32 и выше, снижение HbиHtболее чем на 15% от нормы для данного гестационного срока беременности. Используют только «отмытые» эритроциты 0(I) группы крови, резус – отрицательные.
Гемолитическая болезнь новорожденного
Цели лечения: Лечение гипербилирубинемии, коррекция анемии и посиндромная терапия, направленная на восстановление функций различных органов и систем.
В роддоме новорожденных для лечения переводят в палату интенсивной терапии.
Немедикаментозное лечение. Вопрос о грудном вскармливании решают индивидуально, изучая тяжесть анемии, общее состояние ребенка и матери. Несовпадение крови матери и ребенка по группе или резус-фактору не является противопоказанием к раннему прикладыванию к груди, если во время беременности определялся титр антител. Длительное отлучение ребенка от груди с легкой формой ГБН не обосновано, т.к. количество антител, получаемых с материнским молоком, в первые дни жизни, как правило, незначительное из-за малого объема молока, а в последующем начинается естественное разрушение антител.
Основным методом лечения гипербилирубинемии при ГБН является фототерапия. В основе фототерапии лежит способность молекул билирубина под действием световой энергии изменять химическую структуру и связанные с ней физико-химические свойства. Билирубин поглощает световую энергию преимущественно в синей области видимого спектра (длина волны 450-460 нм). Под воздействием света в коже токсичные формы билирубина превращаются в менее токсичные (15% люмибилирубин и 85% водорастворимые изомеры непрямого билирубина), которые удаляется из организма с мочой.
Показания к началу светолечения изложены в табл. 2.25.
Табл.2.25.Показания к проведению фототерапии у новорожденных в зависимости от уровня непрямого билирубина, МТ и возраста(Формулярная система)
Исключение составляют дети, у которых желтуха появилась в течение первых суток жизни, в том числе вследствие гемолитической болезни новорожденного. Фототерапия этой категории детей независимо от их гестационного возраста должна начинаться с момента появления желтухи.
Наиболее часто в качестве источника света используют люминесцентные лампы синего света. Для домашнего лечения могут быть использованы «фотоодеяла». В последнем случае свет к коже ребенка передается от мощных галогеновых ламп при помощи световодов.
Принципы проведения фототерапии следующие: 1. Доза облучения должна быть не менее 8 мкВт/см 2 /нм; 2. Нельзя нарушать требования инструкции к аппарату о рекомендуемом расстоянии от источника света до ребенка; 3. Во время фототерапии ребенок должен находиться в кувезе или ОРС (каждые 2 часа следует измерять температуру тела, если кувез не поддерживает режим автоматической регулировки по кожной температуре); 4. При проведении фототерапии необходимо защищать глаза и половые органы (у мальчиков); 5. Каждые 2-6 часов необходимо изменять положение ребенка относительно источника света, поворачивая младенца вверх животом или спиной; 6. Фототерапию целесообразно проводить постоянно, делая перерывы лишь для кормления и гигиенического ухода за новорожденным, длительностью не менее 3-5 суток. Так как реакция превращения водонерастворимого изомера непрямого билирубина в водорастворимые изомеры обратима при прекращении сеанса фототерапии. 7. Суточный объем вводимой ребенку жидкости необходимо увеличить на 1 мл/кг/час (у детей с очень низкой массой тела – на 0,5 мл/кг/час) по сравнению с физиологической потребностью ребенка. 8. В случае частичного или полного парентерального питания детей использование жировых эмульсий должно быть ограничено до момента устранения угрозы билирубиновой энцефалопатии.
Всем детям, получающим фототерапию, необходимо ежедневно проводить биохимический анализ крови на билирубин (при угрозе билирубиновой энцефалопатии – каждые 6-12 ч).
Следует помнить, что фототерапия может сопровождаться побочными явлениями: пятнисто-папулезная сыпь на коже, учащение стула, появление бронзового оттенка кожи, эксикоз. В опытах на лабораторных животных было показано потенциальное повреждающее действие яркого света на сетчатку глаза и семенники яичек, что обусловило необходимость защиты глаз и половых органов во время сеансов светолечения.
Показанием к прекращению фототерапии является отсутствие признаков патологического прироста билирубина, при этом концентрация общего билирубина в сыворотке крови должна быть ниже значений, послуживших основанием для начала фототерапии. Спустя 12 часов после окончания фототерапии необходимо контрольное исследование билирубина крови.
Фототерапия обязательно сочетается с дополнительным введением жидкости (дополнительное выпаивание или инфузионная терапия при невозможности выпаивания ребенка). В состав инфузионных сред включают 10% раствор декстрозы, по показаниям (геморрагический синдром, гипоальбуминемия) могут вводиться свежезамороженная плазма, 5% раствор альбумина.
Операция заменного переливания крови(ОЗПК) показана при отечной форме ГБН и при неэффективности фототерапии для лечения желтушной формы. Существует раннее ОЗПК, которое выполняют в первые двое суток жизни, и позднее ОЗПК – с третьих суток жизни.
Показаниями к раннему ОЗПК являются: уровень билирубина в пуповинной крови выше 68 мкмоль/л; почасовой прирост билирубина у доношенных детей более 9 мкмоль/л; у недоношенных детей – более 8 мкмоль/л.
Показанием к позднему ОЗПК служит критический уровень билирубина: у доношенного ≥342 мкмоль/л, у недоношенного зависит от массы тела при рождении и возраста.
Табл. 2.26. Показания к ЗПК у недоношенных новорожденных в зависимости от уровня НБ, МТ и возраста*
источник
Анемия. Виды анемий: железодефицитная, гемолитическая, В12 дефицитная, апластическая. Причины, диагностика, степени анемии.
Анемия или пониженное количество гемоглобина в крови, а в просторечии – «малокровие». Практически каждый человек хотя бы один раз сталкивался с такой формулировкой, особенно женщины. Что же означает этот пугающий термин? Почему возникает данное состояние организма? Чем опасна анемия? Как вовремя распознать её на начальных этапах?
Анемия – это патологическое состояние организма, при котором наблюдается снижение количества гемоглобина и эритроцитов ниже нижних границ нормы. Причем уменьшение содержания гемоглобина является обязательным признаком анемии, в отличие от снижения количества эритроцитов. То есть снижение концентрации гемоглобина при анемии есть всегда, а снижение количества эритроцитов может и не быть. Однако в некоторых случаях при анемии выявляются патологические формы эритроцитов (не двояко – вогнутые).
Анемия – это не самостоятельное заболевание, а следствие основной патологии, потому, выявление сниженного уровня эритроцитов и гемоглобина, требует проведения тщательной диагностики для выявления причины!
Гидремия – разжижение крови.
Такое состояние возможно при поступлении в кровоток тканевой жидкости при схождении отека, обильном питье. Гидремия – это псевдоанемия.
Сгущение крови
Сгущение крови может происходить вследствие потери жидкой части крови, что происходит при сильном обезвоживании. Обезвоживание наблюдается в результате сильной рвоты, поноса, обильного потения. Однако в этом случае за счет сгущения крови количество гемоглобина и эритроцитов может быть в пределах нормальных значений. В таких ситуациях говорят о наличии скрытой анемии.
Специфические и неспецифические признаки анемии – что относится к ним?
В первую очередь рассмотрим, как же проявляется анемия. Существуют неспецифические проявления и специфические. Неспецифические проявления называются так, потому что эти признаки общие для всех видов анемий. Специфические же проявления строго индивидуальны и характерны только для каждого конкретного вида анемии.Сейчас мы рассмотрим только неспецифические проявления, а специфические укажем при рассмотрении видов анемий.
Итак, к неспецифическим признакам анемий, относят следующие симптомы:
- бледность кожи и слизистых оболочек
- слабость
- головокружение
- шум в ушах
- головные боли
- быстрая утомляемость
- сонливость
- одышка
- анорексия (патологическая потеря аппетита или отвращение к пище)
- нарушение сна
- нарушения менструального цикла вплоть до полного прекращения менструаций (аменореи)
- импотенция
- тахикардия (увеличение частоты сердечных сокращений)
- шумы в сердце (усиление сердечного толчка, систолический шум на верхушке сердца)
- сердечная недостаточность
- при снижении количества гемоглобина менее 50 г/л возможно развитие ацидоза (закисление крови)
- снижение содержания гемоглобина ниже нормальных показателей
- снижение содержания эритроцитов ниже нормы
- изменение цветного показателя
- изменение содержания лейкоцитов и тромбоцитов
Виды анемий – постгеморрагическая, гемолитическая, дефицитная и гипопластическая
Анемии могут вызываться совершенно разными причинами, поэтому принято все анемии делить по различным признакам, в том числе по причинам, их вызывающим. Согласно причинам (патогенезу) выделяют три вида анемии: постгеморрагические, гемолитические и связанные с нарушением кровообразования (дефицитные и гипопластические). Что это значит? Разберем подробнее.
Постгеморрагические анемии связаны с острой или хронической кровопотерей (кровотечение, ранение).
Гемолитические – развиваются в связи с усиленным разрушением эритроцитов.
Дефицитные анемии вызваны недостатком витаминов, железа или других микроэлементов, которые необходимы для кроветворения.
Гипопластические анемии – это самый тяжелый вид анемий и связан он с нарушением кроветворения в костном мозгу.
- По степени тяжести. Существует три степени тяжести анемии – легкая, средняя и тяжелая в зависимости от содержания гемоглобина и эритроцитов в крови:
| Степень тяжести | Гемоглобин, г/л | Эритроциты, Т/л | ||||||||||||||||||||||
| Легкая | > 100 г/л | > 3 Т/л | ||||||||||||||||||||||
| Средняя | 100 – 66 г/л | 3 – 2 Т/л | ||||||||||||||||||||||
| Тяжелая | 1,05) и гипохромные (ЦП 8,0 микрон) и мегалобластные (СДЭ > 9,5 микрон). Нормоцитарные анемии характеризуются нормальным диаметром эритроцитов, микроцитарные – уменьшенным диаметром эритроцитов, а макроцитарные и мегалобластные связаны с увеличением диаметра эритроцитов. К нормоцитарным анемиям относят – острую постгеморрагическую и большинство гемолитических анемий; к микроцитарным – железодефицитную анемию, микросфероцитоз и хроническую постгеморрагическую анемию. Макроцитарные анемии – это гемолитическая болезнь новорожденных, фолиево дефицитная анемии. Мегалоцитарная – В12 дефицитнаяанемия.
Мы рассмотрели, на какие типы, и по каким признакам классифицируют анемии. Перейдем к рассмотрению, как проявляются отдельные виды анемий, какие изменения при этом наблюдаются в крови и в организме человека в целом.
Симптомы острой постгеморрагической анемии, картина крови Симптомами острой постгеморрагической анемии являются такие признаки: бледность, резкое головокружение, обмороки, частый пульс, холодный пот, снижение температуры тела, иногда рвота. Потеря крови более 30% от исходного уровня является критической и опасна для жизни. Диагностика постгеморрагической острой анемии В крови увеличивается количество ретикулоцитов более 11%, также появляются «незрелые» эритроциты и эритроциты с измененной формой клетки. Со стороны лейкоцитов наблюдается увеличение их общего количества выше 12 Г/л, а в лейкоцитарной формуле идет сдвиг влево. В последующие два месяца после острой кровопотери происходит восстановление показателей эритроцитов и гемоглобина. Однако восстановление количества эритроцитов и содержания гемоглобина связано с расходованием фонда железа в организме и может повлечь за собой развитие железодефицита. Поэтому в период восстановления после кровопотери необходимо соответствующее питание, то есть в рационе должны быть продукты с высоким содержанием железа (например, гранаты, гречка, печень и т.д.). Принципы лечения острой постгеморрагической анемии Лечение острой постгеморрагической анемии должно проводиться в условиях стационара и быть направлено на восстановление количества циркулирующей крови, количества форменных элементов крови и поддержание этих показателей. В первую очередь необходимо остановить кровотечение. Затем в зависимости от количества кровопотери применяют переливание крови, эритроцитарной массы и кровезаменителей. Симптомы хронической постгеморрагической анемии Симптомы хронической постгеморрагической анемии такие же, как при железодефицитной анемии. Какие же это симптомы? Итак, признаками хронической постгеморрагической анемии являются: кожа «алебастрового» оттенка (очень белая, бледная), извращение обоняния (непереносимость запахов или, наоборот, тяга к каким-либо запахам), изменение вкуса, одутловатость лица, пастозность голеней, ломкость волос и ногтей, сухость, шершавость кожи. Также возможно образование койлонехий – истонченных и уплощенных ногтей. Помимо этих внешних признаков возможно появление одышки, тошноты, головокружения, учащения пульса, слабости, утомляемости, субфебрильной температуры (до 37° С) и прочее. Из-за дефицита железа могут проявляться нарушения со стороны желудочно-кишечного тракта – кариес, глоссит, сниженная кислотность желудочного сока, а также непроизвольное мочеиспускание при смехе, потливость. Диагностика хронической постгеморрагической анемии В крови при хронической постгеморрагической анемии появляются слабо окрашенные эритроциты маленького размера, овальные эритроциты, снижено общее количество лейкоцитов, а в лейкоцитарной формуле наблюдается незначительный лимфоцитоз. В сыворотке крови концентрация железа ниже нормы – 9,0 мкмоль/л, также ниже нормального содержание меди, кальция, витаминов А, В, С, но, однако, повышена концентрация цинка, марганца и никеля в крови. Причины хронической постгеморрагической анемии Почему же возникает такое состояние – хроническая постгеморрагическая анемия? Причины этого явления следующие:
Лечение хронической постгеморрагической анемии Именно в силу причин, приводящих к развитию хронической постгеморрагической анемии, при лечении этого состояния, прежде всего, необходимо устранить причину хронической кровопотери.Затем необходимо сбалансированное питание, содержащее продукты с высоким содержанием железа, фолиевой кислоты и витаминов. В случае тяжелой анемии необходимо принимать препараты железа (сорбифер, феррум-лек) в виде таблеток или инъекций, препараты фолиевой кислоты, витамин В12 в виде таблеток или в виде инъекций. Наиболее эффективными препаратами для восстановления уровня железа в организме являются таблетированные препараты, которые выпускаются различными фирмами. В силу этого в аптеках представлен широкий выбор препаратов железа. При выборе препарата необходимо обращать внимание на содержание железа в одной таблетке и биологическую доступность данного препарата. Препараты железа необходимо принимать совместно с аскорбиновой кислотой и фолиевой кислотой, поскольку в такой комбинации происходит наилучшее усвоение железа. Однако при выборе препарата и дозы необходимо обязательно проконсультироваться с врачом. Гемолитические анемии – это группа анемий, при которых процессы разрушения эритроцитов преобладают над процессами их производства. Иными словами разрушение эритроцитов происходит быстрее, чем образуются новые клетки, взамен разрушенных. Гемолитические анемии могут быть наследственными и приобретенными. Наследственные гемолитические анемии это:
Симптомы гемолитических анемий Общим признаком всех гемолитических анемий является желтуха. Желтуха появляется вследствие того, что при разрушении эритроцитов выделяется в кровь большое количество билирубина, который и приводит к данному симптому. Помимо желтухи имеются следующие признаки, общие для всех гемолитических анемий – увеличение печени и селезенки, увеличение концентрации билирубина в крови, темный цвет мочи и кала, лихорадка, ознобы, боли, моча цвета «мясных помоев». В связи с тем, что наиболее широкое распространение среди наследственных гемолитических анемий имеют серповидно – клеточная анемия и талассемия, более подробно рассмотрим именно их.
Серповидно – клеточная анемия вызвана тем, что синтезируется молекула гемоглобина с дефектом. Такие дефектные молекулы гемоглобина собираются в веретенообразные кристаллы (тактоиды), которые растягивают эритроцит, придавая ему серповидную форму. Такие серповидные эритроциты мало пластичны, повышают вязкость крови и закупоривают мелкие кровеносные сосуды. Кроме этого своими острыми концами такие эритроциты протыкают друг друга и разрушаются. Симптомы серповидно–клеточной анемии Серповидно – клеточная анемия внешне проявляется следующими признаками:
Диагностика серповидно–клеточной анемии В анализе крови сниженное количество гемоглобина (50 – 80 г/л) и эритроцитов (1 – 2 Т/л), увеличение ретикулоцитов до 30% и более. В мазке крови видны серповидные эритроциты и эритроциты с тельцами Жолли и кольцами Кабо. Лечение серповидно-клеточной анемии Основной принцип лечения данного вида анемии –это недопущение гемолитических кризов. Данный эффект достигается тем, что человек избегает гипоксических состояний – присутствия в разреженном воздухе, в местах с низким содержанием кислорода и прочее. Используют переливание эритроцитарной массы или кровезаменителей.
Талассемия возникает вследствие нарушения скорости образования гемоглобина. Такой незрелый гемоглобин не стабилен, в результате чего он выпадает в эритроцитах в виде включений – телец, а весь эритроцит приобретает внешний вид мишеневидной клетки. Талассемия – это тяжелое наследственное заболевание, которое невозможно вылечить, а можно лишь облегчить ее проявления. Симптомы талассемии
Диагностика талассемии В крови обнаруживаются мишеневидные эритроциты, увеличенное количество ретикулоцитов, снижение концентрации гемоглобина до 20 г/л, а эритроцитов до 1 Т/л. Также наблюдаются уменьшение количества лейкоцитов и тромбоцитов. Итак, мы рассмотрели основные виды наследственных гемолитических анемий, которые передаются от родителей к детям. Перейдем к рассмотрению приобретенных гемолитических анемий, которые возникают вследствие наличия провоцирующего фактора. Приобретенные гемолитические анемии, иммунные и не иммунные анемии Прежде всего, необходимо отметить, что приобретенные гемолитические анемии могут развиваться при участии иммунной системы (иммунные) или без ее участия (не иммунные). К анемиям, развивающимся при участии иммунной системы, относятся вирусная, сифилитическая анемия и гемолитическая болезнь новорожденных. Не иммунные гемолитические анемии – это болезнь Маркиафавы – Микелли, а также анемии, возникшие вследствие длительной маршевой ходьбы, отравления алкоголем, кислотами, солями тяжелых металлов, ядами змей, насекомых и грибов. При ожогах, составляющих более 20% поверхности тела, недостатке витамина Е и малярии, также развивается не иммунная гемолитическая анемия.
Лечение этих видов анемии, как правило, не требуется. Гемолитическая болезнь новорожденного, причины развития, симптомы заболевания, степени тяжести.
В настоящее время проводится профилактика гемолитической болезни новорожденных путем отслеживания наличия антител у матери. Если у матери выявляются антитела, то лечение проводят в стационаре. При этом производят вливание антирезусных иммуноглобулинов. Признаки не иммунных гемолитических анемий, лабораторные симптомы Не иммунные гемолитические анемии имеют следующие признаки – желтуха,увеличенные печень и селезенка,повышенная концентрация билирубина в крови, темный цвет мочи и кала, лихорадка, ознобы, боли, моча цвета «мясных помоев».В картине крови отмечается наличие эритроцитов различной формы и размеров, ретикулоцитоз до 30% и выше, сниженное количество лейкоцитов и тромбоцитов. Такие анемии сами по себе не требуют отдельного и особенного лечения, так как в первую очередь необходимо убрать фактор, вызывающий эту анемию (яды змей, соли тяжелых металлов и т.д.). Анемии, вызванные нарушением кровообразования, делятся на две большие группы – дефицитные анемии и гипопластические. Дефицитные анемии связаны с дефицитом необходимых для кроветворения элементов. К дефицитным анемиям относят – железодефицитную анемию, железорефрактерную анемию, В12 – дефицитную и фолиево дефицитную. Гипопластические анемии вызваны гибелью клеток – предшественниц в костном мозгу. Гипопластические анемии могут быть наследственными (анемия Фанкони, анемия Эстрена – Дамешика, анемия Блекфэрна — Даймонда) и приобретенными. Приобретенные гипопластические анемии развиваются либо сами по себе вследствие неизвестной причины, либо на фоне имеющегося заболевания — лучевой болезни, инфекций, повреждений иммунитета. Для большинства людей больший интерес представляют дефицитные анемии, которые могут возникнуть практически у каждого человека. Поэтому наиболее подробно остановимся именно на этом виде анемий.
Причины железодефицитной анемии Железодефицитная анемия возникает в следующих случаях:
Симптомы железодефицитной анемии Клинически железодефицитная анемия проявляется тремя основными синдромами – гипоксическим, сидеропеническим и анемическим. Что это за синдромы? Чем характеризуется каждый из них?Синдром – это устойчивая совокупность симптомов. Итак, гипоксический синдром характеризуется одышкой, головными болями, шумом в ушах, быстрой утомляемостью, сонливостью и тахикардией; анемический синдром выражается в уменьшении содержания количества эритроцитов и гемоглобина. Сидеропенический синдром напрямую связан с уменьшением количества железа в организме и проявляется так: нарушение питания кожи, ногтей, волос – кожа «алебастрового» оттенка, сухость и шершавость кожи, ломкие волосы и ногти. Затем присоединяетсяизвращение вкуса и обоняния (желание есть мел, вдыхать запах мытых бетонных полов и т.д.). Возможно появление осложнений со стороны желудочно-кишечного тракта – кариеса, дисфагии, снижения кислотности желудочного сока, непроизвольного мочеиспускания (в тяжелых случаях), потливости. Диагностика железодефицитной анемии В крови наблюдается снижение содержания гемоглобина до 60 – 70 г/л, эритроцитов до 1,5 – 2 Т/л, также снижено количество или вовсе отсутствуют ретикулоциты. Появляются эритроциты различных форм и размеров. Концентрация сывороточного железа ниже нормы. Лечение железодефицитной анемии В основе лечения железодефицитной анемии лежат принципы устранения причины ее возникновения – лечение заболеваний желудочно – кишечного тракта, а также введение сбалансированного пищевого рациона. В диете должны присутствовать продукты с высоким содержанием железа (печень, мясо, молоко, сыр, яйца, злаки и т.д.). Однако главным средством восстановления количества железа в организме на начальном этапе являются лекарственные препараты железа. В большинстве случаев такие лекарства назначают в виде таблеток. В тяжелых случаях прибегают к внутримышечным или внутривенным инъекциям. В лечении данной анемии используют, например, такие препараты: сорбифер, феррум-лек, тардиферон, тотема и другие. Выбор различных лекарственных средств, в том числе комбинированных, очень широк. При выборе необходимо консультироваться с врачом. Обычно, суточная доза для профилактики и лечения анемии легкой степени составляет 50-60 мг железа, для лечения анемии средней тяжести – 100-120 мг железа в сутки. Лечение анемии тяжелой степени проводят в стационаре и применяют препараты железа в виде инъекций. Затем переходят на таблетированные формы. Препараты железа вызывают потемнение стула, однако в данной ситуации это нормально.Если препарат железа вызывает неприятные ощущения в желудке, то его необходимо заменить.
Железорефрактерную анемию также называют сидеробластной или сидероахристической. Железорефрактерная анемия развивается на фоне нормального содержания железа в сыворотке крови и недостатка ферментов, которые участвуют в синтезе гемоглобина. То есть основная причина железорефрактерной анемии – нарушение процессов «усвоения» железа. Симптомы железорефрактерной анемии, что такое гемосидероз? Проявляется железорефрактерная анемия одышкой, головными болями, головокружением, шумом в ушах, быстрой утомляемостью, сонливостью, нарушениями сна и тахикардией. Из-за высокого содержания железа в крови тканях наблюдается гемосидероз.Гемосидероз – это отложение железа в органах и тканях вследствие его избытка. При гемосидерозе развивается недостаточность сердечно – сосудистой системы вследствие отложения железа в сердечной мышце, сахарный диабет, поражение легких и увеличиваются размеры печени и селезенки. Кожа приобретает землянистый оттенок. Диагностика железорефрактерной анемии, что такое сидеробласты? Цветной показатель крови снижен до 0,6 – 0,4, присутствуют эритроциты различных форм и размеров, количество гемоглобина и эритроцитов ниже нормы. Имеются изменения и в костном мозгу – появляются клетки – сидеробласты. Сидеробласты – это клетки, имеющие вокруг ядра венчик из железа. В норме таких клеток в костном мозгу 2,0 – 4,6%, а при железорефрактерной анемии их количество может доходить до 70%. Лечение железорефрактерной анемии Лечения, которое смогло бы устранить ее совсем, на сегодняшний день нет. Возможно применение заместительной терапии – вливание эритроцитарной массы и кровезаменителей.
Во-первых, что такое В12? В12 – это витамин, который имеет также название цианкобаламин. Цианкобаламин содержится в основном в продуктах животного происхождения – мясо, печень, почки, молоко, яйца, сыр. Уровень витамина В12 необходимо постоянно поддерживать употреблением соответствующих продуктов, поскольку происходят его естественные физиологические потери с калом и желчью. Причины В12 дефицитной анемии Итак, В12 – дефицитная анемия – это анемия, возникающая вследствие недостаточности витамина В12. Недостаток витамина В12 может быть вызван недостаточным его поступлением с пищей или нарушением его усвоения в желудочно-кишечном тракте. Недостаточное поступление цианкобаламина с пищей возможно у строгих вегетарианцев. Также недостаток В12 может проявиться при повышении потребности в нем у беременных женщин, кормящих матерей, раковых больных. Неусвоение витамина В12, поступающего с пищей в достаточном количестве, происходит при заболеваниях желудка, тонкого кишечника (дивертикулы, глисты) и лечении противосудорожными средствами или оральными контрацептивами. Симптомы В12 дефицитной анемии Симптомы проявления В12 – дефицитной анемии характеризуются нарушениями в центральной нервной системе и желудочно-кишечном тракте. Итак, рассмотрим эти две большие группы симптомов:
Диагностика В12 дефицитной анемии В системе крови происходит переход на мегалобластический тип кроветворения. Это означает, что в крови появляются гигантские эритроциты с укороченным сроком жизни, ярко окрашенные эритроциты без просветления в центре, грушевидные и овальные эритроциты с тельцами Жолли и кольцами Кабо. Также появляются гигантские нейтрофилы, уменьшается количество эозинофилов (вплоть до полного отсутствия), базофилов и общего количества лейкоцитов. В крови повышена концентрация билирубина, в связи с чем, может наблюдаться легкая желтушность кожи и склер глаз. Лечение В12 дефицитной анемии В первую очередь необходимо вылечить заболевания желудочно-кишечного тракта и наладить сбалансированное питание, с достаточным содержанием витамина В12. Применение курса инъекций витамина В12 быстро нормализует кроветворение в костном мозгу, а далее необходимо постоянное, регулярное поступление с пищей достаточного количества витамина В12.
Симптомы фолиеводефицитной анемии При фолиево дефицитной анемии страдает желудочно-кишечный тракт, поэтому и проявления данной анемии связаны с нарушениями работы желудочно-кишечного тракта. Наблюдается появление повышенной чувствительности к кислой пище, глоссита, трудностей глотания, атрофии слизистой желудка, увеличения размеров печени и селезенки. Лечение фолиеводефицитной анемии Для лечения данного вида анемии применяют таблетки фолиевой кислоты и нормализуют рацион питания, в котором должны быть продукты, содержащие достаточное количество фолиевой кислоты.
Симптомы гипопластических анемий Гипопластические анемии могут быть наследственными или приобретенными, однако все подвиды данного типа анемий характеризуются одинаковыми проявлениями. Рассмотрим эти симптомы:
Причины, вызывающие развитие гипопластической анемии Какие же причины способны вызывать подобное поражение костного мозга? Наследственные анемии, соответственно, передаются по наследству, а вот приобретенные? Все факторы, способные приводить к развитию гипопластической анемии, делятся на экзогенные (внешние) и эндогенные (внутренние). В таблице приведены основные экзогенные и эндогенные причины, способные вызвать развитие гипопластической анемии.
Принципы лечения гипопластических анемий Лечение гипопластических анемий находится строго в компетенции врача – гематолога. Могут применяться различные методы стимулирования кроветворения, или пересадка костного мозга. Итак, мы рассмотрели все основные виды анемий. Конечно, их гораздо больше, однако мы не можем объять необъятное. При появлении каких-либо признаков анемии необходимо своевременно обратиться к врачу. И регулярно сдавать анализ крови на содержание гемоглобина. источник |

 Постгеморрагические анемии могут быть острыми и хроническими. Острая постгеморрагическая анемия развивается в ответ на скоротечную и большую кровопотерю, а хроническая – развивается в ответ на длительную кровопотерю в небольших количествах.
Постгеморрагические анемии могут быть острыми и хроническими. Острая постгеморрагическая анемия развивается в ответ на скоротечную и большую кровопотерю, а хроническая – развивается в ответ на длительную кровопотерю в небольших количествах. Причины серповидно–клеточной анемии
Причины серповидно–клеточной анемии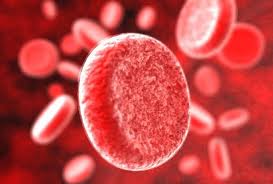 Талассемия – причины заболевания
Талассемия – причины заболевания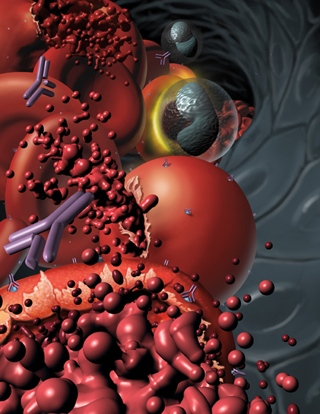 Сифилитическая и вирусная иммунные гемолитические анемии проявляются одинаково. Эти виды анемии являются вторичными, то есть возникают на фоне уже имеющегося заболевания – сифилиса или вирусной инфекции.У этих людей наблюдается лихорадка, ознобы, боли в спине, слабость, одышка, кровь в моче, увеличение печени и селезенки. В крови увеличивается концентрация билирубина и количество ретикулоцитов, а вот содержание гемоглобина может быть в норме или немного снижено, появляются эритроциты круглой формы.
Сифилитическая и вирусная иммунные гемолитические анемии проявляются одинаково. Эти виды анемии являются вторичными, то есть возникают на фоне уже имеющегося заболевания – сифилиса или вирусной инфекции.У этих людей наблюдается лихорадка, ознобы, боли в спине, слабость, одышка, кровь в моче, увеличение печени и селезенки. В крови увеличивается концентрация билирубина и количество ретикулоцитов, а вот содержание гемоглобина может быть в норме или немного снижено, появляются эритроциты круглой формы. Гемолитическая болезнь новорожденных – это заболевание, которое возникает в результате конфликта эритроцитов матери и ребенка, которые имеют несовместимые антигены группы крови или резус – фактора. В таком случае антитела матери проникают к плоду через плаценту и вызывают разрушение эритроцитов у ребенка. Тяжесть гемолитической болезни новорожденных зависит от количества антител матери, которые проникают через плаценту к плоду. Поэтому беременные женщины с отрицательным резус – фактором крови регулярно сдают анализ крови на наличие именно таких антител. Если антитела обнаруживаются, значит необходимо соответствующее лечение. Ребенок с гемолитической болезнью новорожденных рождается с отеками, асцитом, имеет высокий тон крика и высокое содержание незрелых эритроцитов (эритробластов, нормоцитов и ретикулоцитов). Гемолитическая болезнь новорожденных классифицируется по степени тяжести на легкую, среднюю и тяжелую согласно количеству гемоглобина и билирубина в крови.
Гемолитическая болезнь новорожденных – это заболевание, которое возникает в результате конфликта эритроцитов матери и ребенка, которые имеют несовместимые антигены группы крови или резус – фактора. В таком случае антитела матери проникают к плоду через плаценту и вызывают разрушение эритроцитов у ребенка. Тяжесть гемолитической болезни новорожденных зависит от количества антител матери, которые проникают через плаценту к плоду. Поэтому беременные женщины с отрицательным резус – фактором крови регулярно сдают анализ крови на наличие именно таких антител. Если антитела обнаруживаются, значит необходимо соответствующее лечение. Ребенок с гемолитической болезнью новорожденных рождается с отеками, асцитом, имеет высокий тон крика и высокое содержание незрелых эритроцитов (эритробластов, нормоцитов и ретикулоцитов). Гемолитическая болезнь новорожденных классифицируется по степени тяжести на легкую, среднюю и тяжелую согласно количеству гемоглобина и билирубина в крови.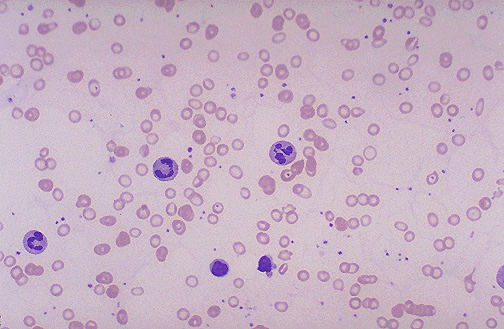 Содержание железа в организме человека – 4 – 5 г или 0,000065% от массы тела. Из них 58% железа входит в состав гемоглобина. Железо может депонироваться (откладываться в запас) в печени, селезенке и костном мозгу. В то же самое время происходят физиологические потери железа с калом, мочой, потом, с менструацией и во время кормления грудью, поэтому необходимо включать в рацион питания железосодержащие продукты.
Содержание железа в организме человека – 4 – 5 г или 0,000065% от массы тела. Из них 58% железа входит в состав гемоглобина. Железо может депонироваться (откладываться в запас) в печени, селезенке и костном мозгу. В то же самое время происходят физиологические потери железа с калом, мочой, потом, с менструацией и во время кормления грудью, поэтому необходимо включать в рацион питания железосодержащие продукты.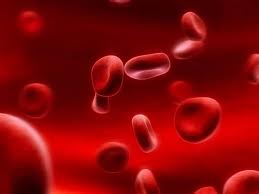 Причина железорефрактерной анемии
Причина железорефрактерной анемии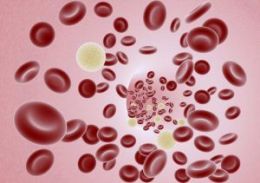 Что такое В12? Где содержится этот витамин?
Что такое В12? Где содержится этот витамин?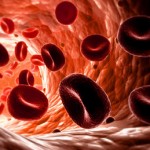 Витамин В9 –фолиевая кислота. В организм поступает с пищей – печень говяжья и куриная, салат, шпинат, спаржа, томаты, дрожжи, молоко, мясо. Витамин В9 способен накапливаться в печени. Таким образом, В9 – дефицитная анемия возникает вследствие недостатка фолиевой кислоты в организме человека. Недостаток фолиевой кислоты возможен при вскармливании детей козьим молоком, при длительной термической обработке пищи, у вегетарианцев, при недостаточном или несбалансированном питании. Также дефицит фолиевой кислоты наблюдается при повышенной потребности в ней у беременных, кормящих, недоношенных детей, подростков, раковых больных. К Вс – дефицитной анемии приводит наличие таких заболеваний как хроническая почечная недостаточность, заболевания печени. Возникновение дефицита фолиевой кислоты возможно и при нарушении всасывания данного витамина, что происходит при алкоголизме, приеме оральных контрацептивов и недостатке В12.
Витамин В9 –фолиевая кислота. В организм поступает с пищей – печень говяжья и куриная, салат, шпинат, спаржа, томаты, дрожжи, молоко, мясо. Витамин В9 способен накапливаться в печени. Таким образом, В9 – дефицитная анемия возникает вследствие недостатка фолиевой кислоты в организме человека. Недостаток фолиевой кислоты возможен при вскармливании детей козьим молоком, при длительной термической обработке пищи, у вегетарианцев, при недостаточном или несбалансированном питании. Также дефицит фолиевой кислоты наблюдается при повышенной потребности в ней у беременных, кормящих, недоношенных детей, подростков, раковых больных. К Вс – дефицитной анемии приводит наличие таких заболеваний как хроническая почечная недостаточность, заболевания печени. Возникновение дефицита фолиевой кислоты возможно и при нарушении всасывания данного витамина, что происходит при алкоголизме, приеме оральных контрацептивов и недостатке В12.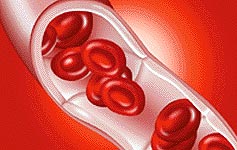 Гипопластические анемии характеризуются уменьшением содержания в крови всех клеток (панцитопенией). Панцитопения связана с гибелью клеток – предшественниц в костном мозгу.
Гипопластические анемии характеризуются уменьшением содержания в крови всех клеток (панцитопенией). Панцитопения связана с гибелью клеток – предшественниц в костном мозгу.