Анемии в результате кровопотери имеют особые проявления, они могут возникать остро или имеют хроническое течение.
Потери крови всегда чувствительны для организма, особенно если это достаточно большой объем ее за короткое время, или мелкие, но практические постоянные кровотечения. В результате такого развивается особая анемия , которую врачи называют термином — постгеморрагическая (вследствие кровопотери). Каковы причины подобного состояния и насколько оно опасно для организма?
Острая анемия вследствие кровопотери
Такой вид анемии у взрослых формируется при единовременной потери крови объемом около 500-1000мл. основными причинами таких состояний являются кровотечения — из поврежденных крупных сосудов при травмах и операциях, при патологии желудка или легких с наличием внутреннего кровотечения. Могут давать такое состояние разрывы аневризмы, прободные язвы кишечника и желудка, ранения живота, печени и т. д.
Такая кровопотеря приводит к тому, что организм одновременно утрачивает и плазму (жидкая основа крови) и форменные элементы (эритроциты, лейкоциты). При анализе крови в первые минуты и часы после потери крови может не выявлять существенных отклонений, анализ может казаться вполне нормальным, при наличии серьезных симптомов потери крови и анемии. Основные проявления при острой анемии вследствие кровопотери возникают не столько по причине дефицита гемоглобина (что дает состояние гипоксии тканей и органов), сколько выраженное снижение крови, которая может циркулировать по сосудам. В результате, организм защищается от подобного обеднения кровообращения состоянием «централизации» кровообращения. Это сохранение крови в области внутренних органов и центра тела, с обеднением кровотока по периферии. Подобное состояние без адекватной помощи медиков может стать для пациента фатальным, поэтому, помимо остановки кровотечения, чтобы устранить дальнейшую кровопотерю, необходимо еще и вливание жидкости внутрь сосудов — это могут быть заменители крови (плазма, растворы) и введение эритроцитарной массы.
Хроническая анемия из-за потери крови
Такой вид анемии возникает при небольших в объеме, но очень частых кровотечениях. Вместе с кровью происходят систематические потери железа, входящего в состав гемоглобина, что ведет к формированию его дефицита в теле. Кровопотери в объеме более 5 мл ежедневно будут постепенно, но неизбежно приводить к развитию анемии. Такого рода анемия у взрослых чаще встречается среди женщин. Это связано с регулярными физиологическими потерями крови при месячных, а также повышенном расходовании железа в периоды беременности и родов, кормления детей. Подробнее об анемии можно прочитать на нашем сайте — https://medaboutme.ru/zdorove/spravochnik/slovar-medicinskih-terminov/anemiya/ .
Другими причинами анемии среди женщин становятся кровотечения при наличии миомы, воспалительных процессов, эндометриоза или дисгормональных изменений. Поэтому, для женщины крайне важно полноценное питание с достаточным поступлением железа с пищей и полноценное его усвоение пищеварительным трактом.
Мужчины также могут страдать от постгеморрагической анемии, к такому состоянию приводят мелкие кровотечения в пищеварительном тракте. Это могут быть эзофагиты в стадии эрозирования, язвы желудка с кровотечениями, геморроидальные узлы или трещины прямой кишки. Одной из распространенных причин анемии подобного характера могут быть опухоли в стадии распада в кишечнике. При этом, потери крови в количестве 5 мл могут быть даже незаметными для пациента, выявляясь только при проведении анализа кала на скрытую кровь.
Проявления такой анемии имеют сходство со всеми остальными — это слабость и бледность, снижение работоспособности и сонливость, проблемы с аппетитом и пищеварением, нарушения роста волос и ногтей. Может страдать кожа, возникают извращение вкуса и запахов, появляются патологические вкусовые пристрастия.
источник
Этиология и патогенез. Острая кровопотеря может быть прежде всего травматического происхождения при ранении сосудов более или менее крупного калибра. Она может зависеть и от разрушения сосуда тем или иным патологическим процессом: разрыв трубы при внематочной беременности, кровотечение из язвы желудка или двенадцатиперстной кишки, из варикозных вен нижнего отрезка пищевода при атрофическом циррозе печени, из варикозных расширений геморроидальных вен. Легочное кровотечение у больного туберкулезом, кишечное — при брюшном тифе могут быть также очень обильными и внезапными и вызвать большее или меньшее малокровие.
Уже простое перечисление различных по своей этиологии кровопотерь говорит о том, что и клиническая картина, и течение, и терапия будут различными в зависимости от общего состояния больного перед наступлением кровотечения: здоровый человек, получивший ранение, здоровая до того женщина после разрыва трубы при внематочной беременности, больной язвой желудка, не знавший раньше о своей болезни, при внезапном желудочном кровотечении будут реагировать аналогично. Иначе будут переносить кровопотерю больные циррозом, брюшным тифом или туберкулезом. Основная болезнь определяет фон, от которого в значительной степени зависит дальнейшее течение малокровия.
Острая потеря крови до 0,5 л здоровым, нестарым среднего веса человеком вызывает кратковременные, нерезко выраженные симптомы: небольшая слабость, головокружение. Повседневный опыт институтов переливания крови — сдача крови донорами — подтверждает это наблюдение. Потеря 700 мл крови и больше вызывает уже более резко выраженные симптомы. Считается, что кровопотеря, превышающая 50-65% крови, или более 4-4,5% веса тела, является безусловно смертельной.
При острой кровопотере смерть наступает и при меньших количествах излившейся крови. Во всяком случае острая потеря больше трети крови вызывает обморок, коллапс и даже смерть.
Имеет значение быстрота истечения крови. Потеря даже 2 л крови, происходящая на протяжении 24 часов, еще совместима с жизнью (по Феррата).
Степень анемизации, быстрота восстановления нормального состава крови зависят не только от величины потери крови, но и от характера ранения и наличия или отсутствия инфекции. В случаях присоединения анаэробной инфекции у раненых наблюдается наиболее резко выраженная и стойкая анемия, так как к анемии от кровопотери присоединяется усиленный гемолиз, обусловленный анаэробной инфекцией. У этих раненых наблюдается особенно высокий ретикулоцитоз, желтушность покровов.
Наблюдения в период войны над течением острого малокровия у раненых уточнили наши знания о патогенезе основных симптомов острой анемии и о развивающихся при этом компенсаторных механизмах.
Кровотечение из поврежденного сосуда останавливается в результате сближения краев раненого сосуда в связи с его рефлекторным сокращением, благодаря образованию тромба в области поражения. На важные факторы, способствующие остановке кровотечения, обратил внимание Н. И. Пирогов: уменьшается «напор» крови в артерии, кровенаполнение и кровяное давление в раненом сосуде, изменяется направление кровяной струи. Кровь направляется по другим, «обходным» путям.
В результате обеднения плазмы крови белками и падения числа клеточных элементов понижается вязкость крови, ускоряется ее оборот. В связи с уменьшением количества крови сокращаются артерии и вены. Повышается проницаемость сосудистых Мембран, что способствует усилению тока жидкости из тканей в сосуды. К этому присоединяется поступление крови из кровяных депо (печень, селезенка и пр.). Все эти механизмы улучшают кровообращение и снабжение кислородом тканей.
При остром малокровии уменьшается масса циркулирующей крови. Наступает обеднение крови эритроцитами, носителями кислорода. Минутный объем крови уменьшается. Наступает кислородное голодание организма в результате понижения кислородной емкости крови и нередко остро развивающейся недостаточности кровообращения.
Тяжелое состояние и смерть при остром кровотечении зависят в основном не от потери большого количества переносчиков кислорода — эритроцитов, а от ослабления кровообращения из-за обеднения сосудистой системы кровью. Кислородное голодание при острой кровопотере — гематогенно-циркуляторного типа.
Одним из факторов, компенсирующих последствия малокровия, является также и увеличение коэффициента утилизации кислорода тканями.
Изучением газообмена при остром малокровии занимался еще В. В. Пашутин и его ученики. М. Ф. Кандаратский уже в диссертации 1888 г. показал, что при высоких степенях малокровия газообмен не изменяется.
По данным М. Ф. Кандаратского, для минимального жизнепроявления достаточно и 27% общего количества крови. Имеющееся в норме количество крови позволяет организму удовлетворить потребность при максимальной работе.
Как показал И. Р. Петров, при больших потерях крови особенно чувствительны к недостатку кислорода клетки коры головного мозга и мозжечка. Кислородным голоданием объясняется начальное возбуждение и торможение в дальнейшем функции мозговых полушарий.
В развитии всей клинической картины малокровия и компенсаторно-приспособительных реакций организма огромное значение имеет нервная система.
Еще Н. И. Пирогов обращал внимание на влияние душевных волнений на силу кровотечения: «Страх, который наводит на раненого кровотечение, также препятствует остановиться крови и нередко служит к его возврату». Отсюда Пирогов делал вывод и указывал, что «врач должен прежде всего нравственно успокоить больного».
Нам в клинике пришлось наблюдать больную, у которой регенерация была заторможена после нервного потрясения.
Под влиянием кровопотери активируется костный мозг. При больших кровопотерях желтый костный мозг трубчатых костей временно превращается в активный — красный. Резко увеличиваются в нем очаги эритропоэза. Пункция костного мозга обнаруживает большие скопления эритробластов. Количество эритробластов в костном мозгу достигает громадных размеров. Эритропоэз в нем часто преобладает над лейкопоэзом.
В отдельных случаях регенерация крови после кровопотери может быть задержана в связи с рядом причин, из которых надо выделить неполноценное питание.
Патологическая анатомия. На секции при ранней гибели больного мы находим бледность органов, малое наполнение сердца и сосудов кровью. Селезенка мала. Мышца сердца бледна (мутное набухание, жировая инфильтрация). Под эндокардом и эпикардом мелкие кровоизлияния.
Симптомы. При острой массивной кровопотере больной становится бледным, как полотно, как при смертельном испуге. Наступает непреоборимая мышечная слабость. В тяжелых случаях наступает полная или частичная потеря сознания, одышка с глубокими дыхательными движениями, подергивания мышц, тошнота, рвота, зевота (анемия головного мозга), иногда икота. Обычно выступает холодный пот. Пульс частый, еле ощутимый, кровяное давление резко понижено. Имеется полная клиническая картина шока.
Если больной оправляется от шока, если он не погибнет от обильной кровопотери, то, придя в сознание, жалуется на жажду. Он пьет, если ему дают пить, и снова впадает в забытье. Постепенно улучшается общее состояние, появляется пульс, поднимается артериальное давление.
Жизнь организма, его кровообращение возможны только при определенном количестве жидкости в кровеносном русле. Вслед за потерей крови немедленно опорожняются резервуары крови (селезенка, кожа и прочие депо эритроцитов), в кровь поступает жидкость из тканей, лимфа. Отсюда понятен основной симптом — жажда.
Температура после острого кровотечения обычно не повышается. Небольшие ее повышения на 1-2 дня наблюдаются иногда после кровотечения в желудочно-кишечный тракт (например, при кровотечении из язвы желудка и двенадцатиперстной кишки). Повышения температуры до более высоких цифр бывают при кровоизлиянии в мышцы и серозные полости (плевра, брюшина).
Бледность покровов зависит от уменьшения количества крови — олигемии — и от сокращения кожных сосудов, наступающего рефлекторно и уменьшающего емкость кровяного русла. Ясно, что в первый момент после кровопотери по уменьшенному руслу будет течь кровь более или менее прежнего состава, наблюдается олигемия в буквальном смысле слова. При исследовании крови в этот период обнаруживают свойственное больному до кровопотери количество эритроцитов, гемоглобина и обычный для него цветной показатель. Эти показатели могут быть даже большими, чем до кровопотери: с одной стороны, при указанном уменьшении кровяного русла кровь может сгуститься, с другой — в сосуды из освобождающихся кровяных дело поступает кровь, более богатая форменными элементами. Кроме того, как указано выше, при сокращении сосудов из них выдавливается больше плазмы, чем форменных элементов (последние занимают центральную часть «кровяного цилиндра»).
Малокровие стимулирует функции кроветворных органов, поэтому костный мозг начинает с большей энергией вырабатывать эритроциты и выбрасывать их в кровь. В связи с этим в последующий период изменяется состав эритроцитов. При усиленной выработке и выбрасывании в кровь неполноценных в смысле насыщенности гемоглобином эритроцитов последние бледнее нормальных (олигохромия), различной величины (анизоцитоз) и различной формы (пойкилоцитоз). Размер эритроцитов после кровотечения несколько возрастает (сдвиг кривой Прайс-Джонса вправо). В периферической крови появляются более молодые красные кровяные тельца, не потерявшие еще полностью базофилию, полихроматофилы. Процент ретикулоцитов значительно поднимается. Как правило, полихроматофилия и увеличение количества ретикулоцитов развиваются параллельно, являясь выражением усиленной регенерации и усиленного поступления молодых эритроцитов в периферическую кровь. Стойкость эритроцитов к гипотоническим растворам поваренной соли сначала на короткое время понижается, а затем повышается в связи с выходом в периферическую кровь более молодых элементов. Могут появиться эритробласты. Цветной показатель в этот период понижается.
Скорость восстановления нормального состава крови зависит от количества потерянной крови, от того, продолжается ли кровотечение или нет, от возраста больного, от состояния его здоровья до потери крови, от основного страдания, вызвавшего кровопотерю, и, главное, от своевременности и целесообразности терапии.
Наиболее быстро восстанавливается нормальное число эритроцитов. Количество гемоглобина нарастает медленнее. Постепенно приходит к норме цветной показатель.
После большой кровопотери у здорового до того человека нормальное количество эритроцитов восстанавливается в 30-40 дней, гемоглобина — в 40-55 дней.
При анемии от кровопотери, в особенности после ранений, важно устанавливать срок, прошедший после ранения и потери крови. Так, по данным Ю. И. Дымшица, через 1-2 суток после проникающего ранения грудной клетки, сопровождающегося кровоизлиянием в полость плевры, в 2/3 случаев определяется менее 3,5 млн. эритроцитов в 1 мм3. Анемия имеет гипохромный характер: в 2/3 случаев цветной показатель меньше 0,7. Но уже через 6 дней количество эритроцитов ниже 3,5 млн. в 1 мм3 наблюдается меньше чем в 1/6 случаев (у 13 из 69 обследованных).
Вслед за происшедшим кровотечением обычно наступает умеренный нейтрофильный лейкоцитоз (12 000-15 000 лейкоцитов в 1 мм3), а также нарастает число кровяных пластинок и увеличивается свертываемость крови уже через 10 минут).
Значительно увеличивается в костном мозгу процент ретикулоцитов. Форсель считал, что степень ретикулоцитоза является наиболее тонким показателем регенераторной способности костного мозга.
Лечение. При остро наступившем малокровии терапевтическое вмешательство должно быть срочным. Организм страдает от недостатка крови и жидкости, который должен быть немедленно восполнен. Ясно, что наиболее действенным средством, если кровопотеря значительна, является переливание крови.
Переливанием крови достигается пополнение утраченной организмом жидкости, питательного материала, раздражение костного мозга, усиление функций его, гемостатическое действие, введение полноценных эритроцитов и фибрин-фермента. Переливают обычно 200-250 мл крови или более массивные дозы. При продолжающемся кровотечении дозу повторно переливаемой крови снижают до 150-200 мл.
В условиях боевой травмы при шоке с кровопотерей вливают 500 мл крови. При необходимости эту дозу увеличивают до 1-1,5 л. Перед переливанием крови применяются все меры для остановки кровотечения.
При кровотечении одинаковый результат дает переливание свежей и консервированной крови. В случае необходимости оно облегчает дальнейшее оперативное вмешательство (при язве желудка, внематочной беременности). Переливание крови показано при кровотечении из брюшнотифозной язвы и противопоказано, если кровотечение обусловлено разрывом аневризмы аорты. При кровотечениях из легких у больных туберкулезом переливание крови не дает ясных результатов и обычно не применяется. Для остановки кровотечения с успехом применяют вливание в вену плазмы крови.
По данным Л. Г. Богомоловой, можно пользоваться сухой плазмой, полученной высушиванием при низкой температуре и растворяемой перед вливанием в дистиллированной стерильной воде.
Применяемые физиологический раствор хлористого натрия (0,9%) и различные смеси растворов солей заменителями крови не являются. Значительно лучшие результаты получаются при введении в вену солевых смесей, к которым прибавлены коллоиды, родственные данному организму.
Введение в вену кровезамещающих жидкостей и крови должно производиться обязательно медленно. Необходимая скорость вливания, — 400 мл в течение 15 минут при здоровом сердце и здоровой сосудистой системе. При нарушениях кровообращения необходимо применять капельный метод введения. Несоблюдение этих правил может явиться источником нежелательных реакций на вливание и осложнений.
В более поздние сроки основным методом лечения является применение железа. Хорошим подспорьем является мышьяк.
Кроме того, необходим постельный режим, полноценное питание с достаточным содержанием витаминов, в частности витамина С. Как показывают наблюдения, для быстрого восстановления крови у доноров необходимо содержание в суточном пайке не менее 50-60 мг аскорбиновой кислоты.
Небезынтересны методы остановки кровотечения, применявшиеся в прежнее время русской народно-бытовой медициной. Сок сырой морковки и редьки рекомендовалось пить при цинге. Сок редьки, свеклы и капусты употреблялся при кровохарканье у больных туберкулезом.
источник
Анемия (в просторечии называют малокровием) – патологическое состояние, о котором мы говорим, когда происходит уменьшение количества эритроцитов (красных кровяных телец), уровня гемоглобина, отвечающего за транспорт кислорода в крови и показателя, называемого гематокритом (отношение объема эритроцитов в крови к общему объему).
Болезнь диагностируют, если эти показатели падают более чем на 2 стандартных отклонения от нормального значения.
Существуют различные классификации анемии. Одна из них основывается на степени тяжести заболевания:
- Легкая анемия – уровень гемоглобина составляет от 10 до 12 г/дл;
- Средняя анемия – уровень гемоглобина составляет от 8 до 9,9 г/дл;
- Тяжелая анемия – уровень гемоглобина составляет от 6,5 до 7,9 г/дл;
- Анемия с риском для жизни – уровень гемоглобина ниже 6,5 г/дл.
Другим элементом, по которому классифицируют виды анемии – ее причины. Принимая во внимание факторы, вызывающие заболевания выделяет следующие типы анемии:
Как следует из названия, этот вид анемии является последствием острой или хронической потери крови. Острая потеря крови происходит чаще всего в результате посттравматического кровоизлияния или массивного кровотечение желудочно-кишечного тракта или половых путей.
Предполагается, что потеря примерно 20% объема циркулирующей крови может вызвать симптомы анемии. Хроническая потеря крови, как правило, связана с заболеваниями желудочно-кишечного тракта.
Анемия из-за дефицита железа является следствием слишком малого содержания железа в организме. Основные причины дефицита железа в организме человека – это его потеря вместе с кровью. Поэтому, чаще всего, анемия из-за дефицита железа имеет место у женщин, у которых железо теряется вместе с менструальной кровью, особенно при слишком частом или обильном кровотечении.
В некоторых случаях можно наблюдать увеличение спроса на железо – это период полового созревания, в период беременности и кормления грудью, а также у преждевременно родившихся детей и новорожденных некормленых молоком матери.
Причиной дефицита железа, а также может быть плохое всасывание этого элемента в желудочно-кишечном тракте. Особенно это касается пациентов после удаления желудка или участка кишечника, людей, страдающих хроническими воспалительными заболеваниями кишечника (болезнь Крона).
Многие хронические заболевания также могут привести к возникновению анемии. Это связано с процессом воспалений и нарушениями производства факторов, определяющих правильную функцию костного мозга.
Поэтому особо часто к анемии приходят при таких заболеваниях, как: рак, аутоиммунные заболевания (ревматоидный артрит, красная волчанка), хронические бактериальные воспаления, грибковые или вирусные инфекции, а также заболеваний почек, желудочно-кишечного тракта и т.д.
Название мегалобластная анемия связано с увеличением красных клеток. В первую очередь, из-за дефицита витамина B12 и фолиевой кислоты. Витамин В12 необходим для нормального синтеза ДНК.
Следовательно, его недостаток приводит к нарушению этого процесса, что быстро отражается на быстроделящихся клетках и приводит к их неправильному росту и уменьшению количества.
Фолиевая кислота, как и витамин В12, участвует в процессах синтеза ДНК и также ее недостаток приводит к нарушению деления – эритроциты получаются неестественно большими.
Причины анемии, вызванной дефицитом витамина В12:
- неправильная диета, бедная витамином В12;
- алкоголизм;
- заболевания, связанные с недостаточностью или нарушением функции фактора Касла (фактор производится клетками желудка), который отвечает за усвоение кобаламина или витамина В12;
- нарушение всасывания комплекса цианкобаламинам.
Причины анемии с дефицитом фолиевой кислоты:
- синдром нарушения всасывания;
- нехватка в рационе питания;
- хронический алкоголизм;
- период повышенного спроса, – беременность, кормление грудью, онкологические заболевания;
- прием некоторых лекарственных препаратов (например, метотрексат), противоэпилептических препаратов (например, фенитоин) и противотуберкулезных лекарственных препаратов.
Гемолитическая анемия – это очень сложная группа заболеваний, характеризующаяся неправильным, преждевременным распадом эритроцитов.
Гемолиз, то есть процесс разложения могут происходить внутри сосудов и вне сосудов (селезенка, печень). Этот тип анемии может давать симптомы в виде желтухи, потому что при чрезмерно активном разрушении красных кровяных клеток выделяется значительное количество гемоглобина, который после цикла биохимических изменений в печени, будет преобразована в билирубин, которая, при высоком уровне, придает коже и глазам характерный желтый оттенок.
Гемолитическая анемия делится на:
- врожденную, вызванную дефектом устройства кровяных клеток, например, врожденный эритроцитоз (кровяные клетки имеют не правильную клеточную мембрану), талассемия, серповидно-клеточная анемия;
- приобретенная, при которой нормальные красные кровяные тельца разрушаются под действием иммунной системы или токсинов (например, тяжелые металлы), лекарств (серосодержащие, производные платины), «механические повреждения», например, искусственный затвор сердца или инфекции (малярия, токсоплазмоз, лейшманиоз).
Апластическая анемия – это заболевание, которое включает в себя расстройства функции костного мозга и уменьшение количества элементов крови (в данном случае не только эритроцитов).
Апластическая анемия может коснуться человека в любом возрасте, у некоторых она врожденная, у других – приобретенная. Анемия иногда появляется внезапно или развивается постепенно, в течение длительного времени, даже в течение нескольких месяцев. Апластическая анемия может иметь тяжелую форму и привести к смерти.
Причины возникновения этой тяжелой болезни не до конца известны, но есть основательные подозрения, что большое значение имеют следующие факторы:
- лучевая терапия и химиотерапия – в списке их побочных эффектов значится апластическая анемия;
- контакт с инсектицидами и гербицидами;
- аутоиммунные расстройства;
- условия труда;
- вирусные инфекции;
- прием некоторых лекарственных препаратов, например, некоторых антибиотиков и средств от ревматоидного артрита;
- гемолитическая анемия;
- заболевания соединительной ткани;
- ночная гемоглобинурия.
Кроме дефицита железа и потери крови можно указать и другие причины анемии:
- недостаток витамина В12. Этот тип анемии появляется при нарушении всасывания витамина В12 из желудочно-кишечного тракта. Это может быть результатом плохого питания, вегетарианства или алкоголизма;
- трещины красных кровяных телец, вызванные атакой антител;
- инфицирование нематодой;
- заболевания костного мозга (лейкемия, множественная миелома) – костный мозг не вырабатывает достаточного количества красных кровяных клеток, что является причиной анемии;
- некоторые лекарства;
- вирус ВИЧ и СПИД .
Клинические проявления зависят, в первую очередь, от типа анемии.
Явная железодефицитная анемия в мазке периферической крови
Однако существуют некоторые общие черты, такие как:
- бледность кожи и конъюнктивы глаз;
- одышка после нагрузки;
- апатия;
- сонливость;
- скотома;
- шум в ушах;
- проблемы с памятью и концентрацией;
- поверхностное дыхание;
- обмороки;
- депрессия;
- повышенная температуру тела;
- ощущение холода;
- болезненные симптомы в области сердца.
В случае постгеморрагической анемии симптомы зависят от количества потерянной крови. Если происходит быстрая потеря крови (острое кровотечение), в объеме от 1,5 до 2 литров, это может привести к снижению температуры тела, холодному поту, беспокойству, расстройства мочеиспускания и развитию так называемого гиповолемического шока – падает артериальное давление, что приводит к нарушению сознания, и даже потере сознания. Если потеря крови хроническая, то чаще всего мы наблюдаем признаки железодефицитной анемии.
Анемия из-за дефицита железа связано с появлением общих симптомов анемии, а также других специфических, в виде: расстройства аппетита, выпячивание и сглаживания поверхности языка, болезненные трещины в углах рта (так называемый заеды), сухая и слишком бледная кожа, хрупкие ногти. Характерным симптомом может быть чрезмерное выпадение волос.
Хроническая анемия сопровождается, как правило, расстройствами, связанными с основным заболеванием. Как правило, анемия проявляется только через несколько месяцев после появления первых симптомов хронического заболевания.
Симптомы мегалобластной анемии зависят от типа дефицита. При дефиците витамина B12, могут появляться расстройства со стороны нервной системы, такие как: расстройства личности, а также парестезия (покалывание) рук и ног, ощущение прохождения тока через позвоночник при наклоне головы вперед, онемения рук и ног.
В случае тяжелой анемии могут появиться: расстройства чувствительности, нарушения походки (нарушение равновесия), нарушения мочеиспускания и ослабление зрения. Другие симптомы – потеря вкусовых ощущений, жжение языка, потеря массы тела, а также симптомы со стороны желудочно-кишечного тракта, тошнота, рвота или диарея.
Дефицит фолиевой кислоты не вызывает расстройств со стороны нервной системы, но характерным симптомом может быть окраска кожи. Дефицит фолиевой кислоты особенно опасен во время беременности, так как это может привести к врожденным дефектам у детей.
Гемолитическая анемия может быть связана с появлением желтухи и увеличением печени и селезенки.
Апластическая анемия может вызывать симптомы, связанные с поражением костного мозга и, следовательно, не только производства красных кровяных телец, а также тромбоцитов и лейкоцитов в крови. Как правило, появляется одышка и слабость.
Нарушение производства крови приводит к увеличенной склонности к кровоподтекам и – в более серьезных случаях – спонтанным кровотечениям различных органов и систем.
Одним из параметров диагностики анемии является гемоглобин (Hb). Это белок, встречающийся в эритроцитах, отвечает за «прием» кислорода в легких и транспортировку его в клетки тела, а затем прием углекислого газа и доставку его в легкие.
Допустимые значения при лабораторном исследовании довольно широкие, но колеблются в пределах: у женщины 12-16 г/дл у мужчин 14-18 г/дл, а также у новорожденных 14,5-19,5 г/дл. Следующим параметром является гематокрит. Это отношение объема элементов крови (в основном красных кровяных клеток (эритроцитов)) к объема цельной крови.
Hct принимает следующие значения:
- для женщин 35-47%;
- для мужчин 42-52%;
- а для новорожденных 44-80% (в первые дни жизни).
В результатах исследований, мы также принимается во внимание количество эритроцитов:
- для женщин 4,2-5,4 млн/мм 3 ;
- для мужчин 4,7-6,2 млн/мм 3 ;
- а для новорожденных 6,5-7,5 млн/мм 3 .
Когда значение этих показателей снижены, можно говорить об анемии.
Основой диагноза анемии ставится на исследовании морфологии периферической крови, при котором наблюдается снижение количества эритроцитов, гемоглобина и гематокрита.
Важным параметром, который может указывать на анемию – объем эритроцитов (MCV), которая должна составлять (в зависимости от нормы лаборатории) от 80 до 92 fl. Если он ниже нормы, анемия называется микроцитарная, если находится в норме – нормоцитарная, а если выше нормы – макроцитарная.
В случае постгеморрагической анемии, имеющей место в чрезвычайных ситуациях, MCV в норме. В случае хронической постгеморрагической анемии наблюдаются симптомы дефицита железа.
Анемия из-за дефицита железа связано со снижением MCV (микроцитарная анемия). Количество тромбоцитов в крови может быть правильным или уменьшенным.
Дополнительным исследованием, подтверждающим анемию из-за дефицита железа является, конечно, исследование уровня железа в крови. Происходит также снижение концентрации ферритина в крови и повышения TIBC. В диагностике причин дефицита железа важна консультация у гинеколога (женщины) и диагностика желудочно-кишечного тракта.
При анемии хронических заболеваний, MCV, как правило, в норме. Кроме того, можно наблюдать рост параметров воспаления. Поэтому требуются другие исследования, позволяющие распознать основную болезнь.
Анемия из-за дефицита витамина В12 диагностируется на основании увеличения объема эритроцитов (MCV), а также исследования уровня витамина В12 в крови. В диагностике значение имеет оценка состояния желудочно-кишечного тракта, как основной причины нарушения всасывания этого витамина. В случае анемии с дефицитом фолиевой кислоты, MCV также увеличивается.
Для диагностики апластической анемии врачи обычно рекомендуют биопсию костного мозга. Подозрение на апластическую анемию возникает также на основе определенных изменений в крови, кроме недостатка гемоглобина, происходит снижения уровня лейкоцитов (лейкопения) и тромбоцитов в крови.
В случае гемолитической анемия, MCV, как правило, находится в пределах нормы, но иногда может быть увеличен. В мазке крови можно наблюдать неправильные эритроциты. Эритроциты живут 100-120 дней. Во время своей жизни, проходят 250 км пути, постоянно перемещаются, доставляют клеткам кислород и принимают от них углекислый газ.
Иногда, однако, путешествие этих клеток заканчивается преждевременно и длится около 50 дней. Тогда говорят о преждевременном распаде эритроцитов в их гемолизе, а болезнь называется гемолитической анемией. К такому положению вещей может привести гиперспленический синдром, то есть повышенная активность селезенки.
Селезенка несет ответственность за разрушение старых эритроцитов. В случае гиперспленического синдрома селезенка «утилизирует» также и молодые клетки. Широко известной причиной гемолитической анемии является малярия, а также другие инфекции, например, токсоплазмоз, цитомегаловирус. Разрушение клеток может произойти также после переливания крови. В данном случае причиной гемолиза это несоответствие в системе антигеннов крови.
Для лечения анемии следует, конечно, учитывать ее причину. Острая постгеморрагическая анемия проявляется у взрослых после потери примерно 20% от общего объема крови. Лечение заключается, прежде всего, в задержке и остановке кровотечения, переливании концентрата эритроцитов, а также введения кровезаменительных препаратов и инфузионных растворов.
В случае анемии с дефицитом железа лечение заключается в восполнении его уровня в организме. Перед началом лечения следует определить причину потери железа. В случае тяжелой анемии применяется, как правило, железо в виде инъекций, при мягких формах, можно назначать лечение в виде пищевых добавок.
Конечно, необходимо также обогащение диеты продуктами, содержащими большое количество железа, такими как: красное мясо, овощи, продукты из цельного зерна, бобовые и чернослив, инжир.
В случае анемии с дефицитом витамина В12 необходимо подача его извне в виде инъекций (в препаратах для приема внутрь он плохо всасывается), которые во многих случаях применяются в соответствующей схеме до конца жизни. Чтобы избежать дефицита витамина В12, следует позаботиться о том, чтобы в вашем рационе были продукты животного происхождения.
Фолиевую кислоту, в отличие от железа и витамина В12 можно применять внутрь. Анемия, вызванную дефицитом фолиевой кислоты, можно предотвратить путем обогащения диеты большим количеством овощей и фруктов. Женщины, которые беременны должны помнить о ежедневном приеме препарата, содержащего кислоту.
К основным методам лечения апластической анемии относятся: пересадка костного мозга и лечение иммуносупрессантами (в случае, когда апластическая анемия появилась на фоне аутоиммунных расстройств). Кроме того, лечение включает в себя симптоматические меры, то есть переливание тромбоцитов и концентрата эритроцитов.
Больным, также назначаются антибиотики и противогрибковые препараты. С учетом нарушений иммунитета у лиц с апластической анемией рекомендуется избегать пребывания в местах больших скоплений людей, где можно легко заразиться инфекцией, а также соблюдение особой личной гигиены (мытье рук).
Лечение гемолитической анемии и состоит, если это, конечно, возможно, в лечении основной болезни, вызывающей это заболевание крови. В случае анемии на фоне аутоиммунных расстройств применяются глюкокортикоиды и иммуносупрессивные препараты.
Если есть подозрения, что причиной заболевания являются различные препараты, то, если это только возможно, необходимо приостановить их прием. Бывает, однако, что единственным выходом являются периодические переливания концентратов красных кровяных телец.
Прогноз зависит от причины анемии. Раннее выявление и быстрое развертывание программы лечения постгемморагической анемии связано с хорошим прогнозом.
В случае анемии с дефицитом железа, фолиевой кислоты или витамина В12, необходимо дополнение и изменение диеты, а также объяснение причин потери этих важных компонентов. Более плохой прогноз касается других видов анемии, при которых не всегда удается получить исцеление.
Анемия или малокровие – это опасное заболевание. Если вы подозреваете, что имеете анемию, обратитесь к врачу, чтобы начать лечение как можно скорее. Отсутствие лечения анемии может привести к истощению организма и многим осложнениям.
Для профилактики анемии особое значение имеет правильное питание, а также быстрая диагностика возможных проблем с желудочно-кишечным трактом или родовыми путями у женщин. Важно, чтобы каждый, по крайней мере, один раз в год, проходил исследование мазка крови.
источник
Различают острую и хроническую постгеморрагическую анемии.
Возникает в результате острой массивной потери крови в объеме от 5 мл/кг массы тела и выше (травма, хирургическое вмешательство, желудочные, маточные, кишечные кровотечения, разрыв фаллопиевых труб, нарушение гемостаза и др.). Сразу после потери крови вследствие уменьшения ее массы появляется общеанемические признаки — тахикардия, одышка, бледность кожных покровов и слизистых оболочек, падение АД. Содержание эритроцитов и гемоглобина снижается равномерно (нормоцитемическая гиповолемия), развивается нормохромная анемия. Изменения периферической крови носят стадийный характер. На 2–3-е сутки после кровотечения в кровь поступает тканевая жидкость, масса ее восстанавливается (гидремическая фаза), а количество эритроцитов и гемоглобина снижается, падает гематокрит, но в связи с выходом эритроцитов из депо цветовой показатель сохраняется в норме (нормохромная анемия), развивается лейкопения (утрата лейкоцитов во время кровотечения, гемодиллюция), тромбоцитопения (утрата тромбоцитов при потере крови, потребление при образовании тромба). Наблюдается умеренный анизоцитоз и пойкилоцитоз эритроцитов. Возникшая гипоксия ведет к повышению уровня эритропоэтина и на 4–5-е сутки после кровотечения активируется функция костного мозга (костномозговая фаза компенсации) появляются регенеративные формы эритроцитов — полихроматофилы, единичные нормобласты (полихроматофильные, оксифильные), ретикулоцитоз. Анемия приобретает гипохромный характер, т. к. ускоренная регенерация опережает созревание эритроцитов из-за возникшего дефицита железа. Развивается нейтрофильный лейкоцитоз со сдвигом влево по регенеративному типу.
Данные нарушения обусловлены уменьшением объема циркулирующей крови и гипоксией. В ответ на кровопотерю включаются механизмы компенсации, направленные на восстановление утерянного объема крови и на борьбу с анемическим состоянием (гипоксией).
Развивается в результате длительно повторяющихся небольших кровотечений. Является вариантом железодефицитных анемий, патогенез и проявления обусловлены нарастающим дефицитом железа.
Железо — один из важнейших микроэлементов, входящих в состав организма человека. Взрослому человеку требуется 15–18 мг/сут железа, из которых всасывается 2–2,5 мг. При этом биодоступность содержащегося в пище гемового железа существенно выше, чем негемового. Основные депо железа: печень (гепатоциты и макрофаги), костный мозг, селезёнка, мышцы. Если метаболизм железа нормален, 30–40 % нормобластов костного мозга содержат гранулы ферритина (сидеробласты). Отсутствие сидеробластов характерно для железодефицита. Избыток гранул в сидеробласте служит признаком переполнения организма железом (гемосидероз) или неспособности утилизировать его (сидеробластная анемия). На рис. 2 представлена схема метаболизма железа.
Дефицит железа в организме существует в двух формах, представляющих собой две последовательные стадии одного процесса: латентный (тканевый) дефицит железа (ЛДЖ) и собственно железодефицитная анемия (ЖДА).
ЖДА составляет около 80–90 % всех случаев анемий и является одной из самых распространенных ее форм. Женщины страдают данным заболеванием чаще, чем мужчины, поскольку запасы железа у последних значительно превышают (на 100–200 %) таковые у женщин. Явный и скрытый дефицит железа отмечается почти у 60 % женщин земного шара. Железодефицитные анемии встречаются во всех возрастных группах. Различают «истинные» ЖДА — при абсолютном дефиците железа и «ложные» — при нарушении включения железа в гемм, в отсутствие первичного истинного железодефицита.
Рисунок 2 – Схема метаболизма железа в организме
По патогенетическому принципу с учетом основных этиологических причин железодефицитные анемии делят на пять основных подгрупп (Л.И. Идельсон): 1) связанные с повышенной потерей железа; 2) связанные с недостаточным исходным уровнем железа; 3) связанные с повышенным расходованием железа; 4) связанные с нарушением всасывания железа и недостаточным поступлением его с пищей (алиментарные); 5) связанные с нарушением транспорта железа.
Таблица 3.Причины и механизмы развития железодефицитных состояний
Группы этиологических факторов
Дети недоношенные и новорожденные
Недостаточный исходный уровень железа
Интенсивный рост (пубертатный период)
Повышенное расходование железа
Хроническая кровопотеря: при частых лечебных кровопусканиях, донорстве;
При заболеваниях ССС (гипертоническая болезнь, геморрагическая телеангиэктазия и др.);
При патологии ЖКТ (варикозное расширение вен пищевода, диафрагмальная грыжа, язва желудка и 12-перстной кишки, язвенный колит, дивертикулёз, геморрой и др.);
Из органов мочеполовой системы (алкогольная нефропатия, туберкулёз почек, почечнокаменная болезнь, полипы и рак мочевого пузыря, обильные меноррагии, эндометриоз, миома матки и др.);
Из органов дыхательной системы (рак лёгкого, туберкулёз, бронхоэктазия и др.);
При заболеваниях системы крови (лейкозы, апластическая анемия и др.);
Припатологии системы гемостаза (аутоиммунная тромбоцитопения, гемофилии, ДВС-синдром и др.)
Патологические состояния и болезни
Резекция желудка и кишечника;
Гипосекреция желудочного сока;
Нарушение всасывания железа
Приобретённая гипотрансферринемия (при нарушении белоксинтезирующей функции печени)
Нарушение транспорта железа
Недостаточное поступление железа; нарушение транспорта железа; нарушение всасывания железа; потеря железа
Нарушение всасывания железа
Искусственное вскармливание грудных детей
Недостаточное поступление железа
Избыточные физические нагрузки
Повышенное расходование железа
Нередко действуют комбинации указанных факторов, вызывающих отрицательный баланс железа. Примером ЖДА, развивающейся вследствие комплексного влияния нескольких факторов, является хлороз (от греч. «хлорос» — бледно-зеленый, или «бледная немочь»). Название связано со специфическим цветом лица таких больных. При ЖДА уменьшается содержание железа в плазме крови, костном мозге и в тканевых депо.
Основным звеном патогенеза заболевания является снижение содержания железа в депо, сыворотке крови и костном мозгу. В результате нарушается синтез гемоглобина, возникают гипохромная анемия и трофические расстройства в тканях, признаками которых являются: сухость и вялость кожи, ломкость ногтей, выпадение волос, атрофия слизистой оболочки языка, повышенное разрушение зубов, дисфагия, извращение вкуса, мышечная слабость и др.. В патогенезе клинических проявлений болезни имеет значение: нарушение активности железосодержащих ферментов в тканях организма (цитохром С, цитохромоксидаза, сукцинатдегидрогеназа, пероксидаза, митохондриальная моноаминооксидаза, α-глицерофосфатоксидаза) и недостаточное снабжение тканей кислородом. Признаки гипоксии тканей появляются лишь при значительной выраженности малокровия, когда наступает истощение компенсаторных механизмов, обеспечивающих на ранних этапах развития дефицита железа нормализацию отдачи кислорода из гемоглобина тканям.
Клиническая картина складывается из двух основных синдромов: общеанемического и сидеропенического.
Общеанемический синдром проявляется симптомами, характерными для всех видов анемии: бледность, общая слабость, быстрая утомляемость, обмороки, одышка, тахикардия, систолический шум.
Сидеропенический синдром характеризуется рядом трофических нарушений. Отмечаются: сухость и трещины кожи, преждевременные морщины, ломкость ногтей, койлонихия (катлонихия) — ложкообразные ногти, ангулярный стоматит, атрофия слизистых оболочек рта, пищевода, желудка, дыхательных путей. Нарушается иммунитет, что приводит к хронизации инфекций, частым ОРЗ; развивается мышечная слабость, слабость физиологических сфинктеров. Может возникнуть извращение вкуса (поедание несъедобных продуктов — мела, бумаги и др.), пристрастие к необычным запахам (ацетон, бензин, краска). Нарушается память, концентрация внимания. При дефиците железа резко усиливается абсорбция свинца, и у детей на этом фоне развивается необратимая задержка интеллектуального развития. Нарушение проницаемости мелких сосудов ведет к отекам лица. Иногда возникает «сидеропенический субфебрилитет».
Картина крови. Основным признаком железодефицитной анемии является гипохромия со снижением цветового показателя ниже 0,8 и, соответственно, уменьшением содержания гемоглобина ниже 110 г/л. Количество эритроцитов, как правило, остается на исходном уровне, но в ряде случаев может оказаться сниженным до 2,0-1,5×10 12 /л вследствие нарушения процессов пролиферации клеток эритроидного ряда в костном мозгу и усиления неэффективного эритропоэза (в норме разрушение эритронормобластов в костном мозгу не превышает 10-15%). Ретикулоциты в норме или незначительно увеличены, при прогрессировании ЖДА их количество снижается. Важным морфологическим признаком железодефицитных анемий является анизоцитоз эритроцитов с преобладанием микроцитов.
Нередко развивается нейтропения (в результате уменьшения содержания железосодержащих ферментов в лейкоцитах). СОЭ в норме или незначительно увеличена.
Уровень тромбоцитов может быть незначительно повышен (на фоне кровотечений).
Исследование костного мозга.В КМ определяется нормобластическая гиперплазия с нарушением гемоглобинизации (преобладание базофильных и полихроматофильных нормобластов при снижении оксифильных), снижение индекса созревания нормобластов, снижение количества сидеробластов вплоть до полного их отсутствия. Миелоидный и мегакариоцитарный ростки не изменены.
Биохимический анализ крови – основной диагностический критерий при ЖДА, включающий набор тестов, при помощи которых подтверждается факт дефицита железа в организме:
снижение уровня сывороточного железа,
снижение уровня сывороточного ферритина,
снижение степени насыщения трансферрина железом,
увеличение содержания трансферрина в сыворотке,
повышение общей и латентной железосвязывающей способности сыворотки,
увеличение содержания растворимых рецепторов к трансферритину в сыворотке,
повышение свободного протопорфирина IX в эритроцитах.
Количество железа в сыворотке крови при выраженной ЖДА падает до 5,4–1,8 мкмоль/л при норме 12,5–30,4 мкмоль/л (мужчины; у женщин этот показатель на 10–15% ниже. Под общей железосвязывающей способностью сыворотки понимается количество железа, которое может связаться с трансферрином (в норме 54,0–72,0 мкмоль/л). В норме одна треть трансферрина насыщена железом, а две трети — свободны. Об уровне депонированного железа можно судить по содержанию железа в суточной моче после однократного введения больному 500 мг десферала (продукт метаболизма актиномицетов, избирательно выводящий ион железа из организма). В норме этот показатель соответствует 0,6–1,3 мг железа, а при железодефицитной анемии снижается до 0,2 мг в сутки и менее.
Сывороточный ферритин— очень точный индикатор резервных запасов железа. Он содержит примерно 15-20% общего запаса железа в организме взрослого человека. Определяется почти во всех тканях, особенно высока его концентрация и синтетическая способность в печени, селезенке и костном мозге. Белок в свободном от железа виде называется апоферритином. Ферритин состоит из белковой оболочки, которая окружает ядро трехвалентного железа в виде комплексов окиси и фосфата железа. Каждая молекула апоферритина может сорбировать до 5000 атомов железа, однако большинство молекул ферритина содержат от 1000 до 3000 атомов железа.
Анемии, ассоциированные с заболеваниями внутренних органов, включают анемии при эндокринных заболеваниях, заболеваниях печени и почек.
К числу анемий при эндокринных заболеванияхотносятся анемии при заболеваниях щитовидной и паращитовидных желез, надпочечников, половых желез, гипопитуитаризме и др., в основе патогенеза которых лежит депрессия эритропоэза при дефиците или, напротив, гиперсекреции ряда гормонов. В частности, такие гормоны, как тироксин, кортизол, тестостерон в очень высоких концентрациях вызывают угнетение пролиферативной активности эритроидных прекурсоров. В случае сгущения крови в результате дегидратации (при надпочечниковой недостаточности, гипотиреозе) диагностика анемии может быть затруднена.
К анемиям при заболеваниях печени относятся анемии, возникающие при диффузных поражениях органа (циррозе, хроническом гепатите, гемохроматозе и др.).
Патогенез анемии при заболеваниях печени отличается многообразием патогенетических факторов, что определяется особенностями патогенеза основного заболевания. Выделяют следующие механизмы развития анемии:
угнетение процессов кроветворения в костном мозгу вследствие прямого токсического влияния на клетки-предшественницы гемопоэза алкоголя (при алкогольном поражении печени) и эндогенных токсинов (при нарушениях обезвреживающей и клиренсной функции печени), при нарушениях метаболизма железа и депонирования витамина В12и фолиевой кислоты в пораженной печени;
укорочение продолжительности жизни эритроцитов в результате прямого повреждающего действия токсических продуктов экзогенного (алкоголь) и эндогенного (при эндотоксемии) происхождения, гиперспленизма, при нарушениях внутриклеточного метаболизма эритроцитов (например, в связи с дефицитом в клетках НАДФ + ) и их способности к деформации (вследствие патологии клеточной мембраны при изменениях фракционного состава фосфолипидов, снижении содержания сиаловых кислот);
кровотечения из расширенных вен желудочно-кишечного тракта (при циррозе печени), носовые, геморроидальные и иной локализации (при формирующейся недостаточности синтеза факторов свертывания крови вследствие нарушений белкового обмена).
В подавляющем большинстве случаев при заболеваниях печени регистрируется нормохромная нормоцитарная анемия, при присоединяющемся дефиците железа — микроцитарная нормоили гипохромная, при недостаточности витамина В12и фолиевой кислоты, метастазах рака желудка в печень — макроцитарная анемия нормо- или гиперхромного типа.
Анемии при заболеваниях почекмогут выявляться у больных острым гломерулонефритом, интерстициальным нефритом, хронической почечной недостаточностью. Патогенез анемии при заболеваниях почек определяется снижением продукции эритропоэтина клетками юкстагломерулярного аппарата, депрессией кроветворения в костном мозгу (в результате нарушения пролиферативной активности эритроидных клеток, торможения процессов синтеза гема) и сокращением срока жизни эритроцитов (до 40-50 дней) при действии токсических продуктов азотистого обмена.
Контрольные вопросы по теме:
Охарактеризуйте типовые формы изменений общего объема циркулирующей крови.
Какова этиология олигоцитемических и полицитемических гиповолемий?
Какова этиология олигоцитемических и полицитемических гиперволемий?
Укажите общие механизмы формирования компенсаторно-приспособительных механизмов при кровопотере.
Каков механизм формирования экстренных защитно-приспособительных реакций организма при кровопотерях?
Каков механизм формирования долговременных защитно-приспособительных реакций организма при кровопотерях?
Дайте определение понятию анемия, каковы принципы классификации?
Назовите основные фонды железа в организме?
Перечислите лабораторные показатели, характеризующие состояние красной крови при острой кровопотере?
Перечислите лабораторные показатели, характеризующие состояние красной крови при хронической кровопотере?
Какие Вы знаете анемии, ассоциированные с заболеваниями внутренних органов, какие особенности для них характерны?
Темы реферативных сообщений:
Этиологи и патогенез ювенильного хлороза (у девочек в пубертатный период) при ЖДА
источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
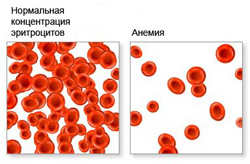
Эритроциты формируются в красном костном мозге из белковых фракций и небелковых компонентов под воздействием эритропоэтина (синтезируется почками). Эритроциты в течение трех дней обеспечивают транспорт, главным образом, кислорода и углекислого газа, а также питательных веществ и продуктов метаболизма от клеток и тканей. Срок жизни эритроцита сто двадцать дней, после чего он разрушается. Старые эритроциты накапливаются в селезенке, где утилизируются небелковые фракции, а белковые поступают в красный костный мозг, участвуя в синтезе новых эритроцитов.
Вся полость эритроцита наполнена белком, гемоглобином, в состав которого входит железо. Гемоглобин придает эритроциту красную окраску, а также помогает ему переносить кислород и углекислый газ. Его работа начинается в легких, куда эритроциты поступают с током крови. Молекулы гемоглобина захватывают кислород, после чего обогащенные кислородом эритроциты направляются сначала по крупным сосудам, а затем и по мелким капиллярам к каждому органу, отдавая клеткам и тканям необходимый для жизни и нормальной деятельности кислород.
Анемия ослабляет способность организма к газовому обмену, за счет сокращения числа эритроцитов нарушается транспортировка кислорода и углекислого газа. Вследствие этого у человека могут наблюдаться такие признаки анемии как чувство постоянной усталости, упадок сил, сонливость, а также повышенная раздражительность.
Анемия является проявлением основного заболевания и не является самостоятельным диагнозом. Многие болезни, включая инфекционные заболевания, доброкачественные или злокачественные опухоли могут быть связаны с анемией. Именно поэтому анемия является важным признаком, который требует проведения необходимых исследований для выявления основной причины, которая привела к ее развитию.
Тяжелые формы анемии вследствие тканевой гипоксии могут привести к серьезным осложнениям, таким как шоковые состояния (например, геморрагический шок), гипотония, коронарная или легочная недостаточность.
- по механизму развития;
- по степени тяжести;
- по цветному показателю;
- по морфологическому признаку;
- по способности костного мозга к регенерации.
| По патогенезу анемия может развиться вследствие кровопотери, нарушения образования эритроцитов или из-за их выраженного разрушения. По механизму развития выделяют:
|
- потеря крови (острые или хронические кровотечения);
- повышенное разрушение эритроцитов (гемолиз);
- уменьшенное производство эритроцитов.
Также следует заметить, что в зависимости от вида анемии причины ее возникновения могут отличаться.
Факторы, влияющие на развитие анемии
- гемоглобинопатии (изменение строения гемоглобина наблюдается при талассемии, серповидноклеточной анемии);
- анемия Фанкони (развивается вследствие имеющегося дефекта в кластере белков, которые отвечают за восстановление ДНК);
- ферментативные дефекты в эритроцитах;
- дефекты цитоскелета (клеточный каркас, располагающийся в цитоплазме клетки) эритроцита;
- врожденная дизэритропоэтическая анемия (характеризуется нарушением образования эритроцитов);
- абеталипопротеинемия или синдром Бассена-Корнцвейга (характеризуется нехваткой бета-липопротеина в клетках кишечника, что ведет к нарушению всасываемости питательных веществ);
- наследственный сфероцитоз или болезнь Минковского-Шоффара (вследствие нарушения клеточной мембраны эритроциты принимают шарообразную форму).
- дефицит железа;
- дефицит витамина B12;
- дефицит фолиевой кислоты;
- дефицит аскорбиновой кислоты (витамин С);
- голодание и недоедание.
Хронические заболевания и новообразования
- почечные заболевания (например, туберкулез печени, гломерулонефрит);
- заболевания печени (например, гепатит, цирроз);
- заболевания желудочно-кишечного тракта (например, язва желудка и двенадцатиперстной кишки, атрофический гастрит, неспецифический язвенный колит, болезнь Крона);
- коллагеновые сосудистые болезни (например, системная красная волчанка, ревматоидный артрит);
- доброкачественные и злокачественные опухоли (например, миома матки, полипы в кишечнике, рак почек, легких, кишечника).
- вирусные заболевания (гепатит, инфекционный мононуклеоз, цитомегаловирус);
- бактериальные заболевания (туберкулез легких или почек, лептоспироз, обструктивный бронхит);
- протозойные заболевания (малярия, лейшманиоз, токсоплазмоз).
Ядохимикаты и медикаментозные средства
- неорганический мышьяк, бензол;
- радиация;
- цитостатики (химиотерапевтические препараты, используемые для лечения опухолевых заболеваний);
- антибиотики;
- нестероидные противовоспалительные средства;
- антитиреоидные препараты (снижают синтез гормонов щитовидной железы);
- противоэпилептические препараты.
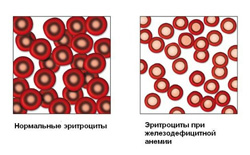
Для железодефицитной анемии характерно снижение эритроцитов, гемоглобина и цветового показателя.
Железо — это жизненно важный элемент, участвующий во многих метаболических процессах организма. У человека с весом семьдесят килограмм запас железа в организме составляет примерно четыре грамма. Данное количество поддерживается благодаря сохранению баланса между регулярными потерями железа из организма и его поступлением. Для поддержания равновесия суточная потребность железа составляет 20 – 25 мг. Большая часть поступающего железа в организм затрачивается на его нужды, остальное депонируется в виде ферритина или гемосидерина и при необходимости расходуется.
Нарушение поступления железа в организм
- вегетарианство вследствие неупотребления белков животного происхождения (мясо, рыба, яйца, молочные продукты);
- социально-экономическая составляющая (например, недостаточно денег для полноценного питания).
Нарушение усвоения железа
Всасывание железа происходит на уровне слизистых желудка, поэтому такие заболевания желудка как гастриты, язвенная болезнь или резекция желудка приводят к нарушению всасывания железа.
Повышенная потребность организма в железе
- беременность, в том числе многоплодная беременность;
- период лактации;
- подростковый возраст (за счет быстрого роста);
- хронические заболевания, сопровождающиеся гипоксией (например, хронический бронхит, пороки сердца);
- хронические нагноительные заболевания (например, хронические абсцессы, бронхоэктатическая болезнь, сепсис).
Потери железа из организма
- легочные кровотечения (например, при раке легких, туберкулезе);
- желудочно-кишечные кровотечения (например, язва желудка и двенадцатиперстной кишки, рак желудка, рак кишечника, варикозное расширение вен пищевода и прямой кишки, неспецифический язвенный колит, глистные инвазии);
- маточные кровотечения (например, преждевременная отслойка плаценты, разрыв матки, рак матки или шейки матки, прервавшаяся внематочная беременность, миома матки);
- почечные кровотечения (например, рак почек, туберкулез почек).
Питание при анемии
В питании железо делится на:
- гемовое, которое поступает в организм с продуктами животного происхождения;
- негемовое, которое поступает в организм с продуктами растительного происхождения.
Следует заметить, что гемовое железо усваивается в организме значительно лучше, нежели негемовое.
Количество железа на сто миллиграмм
Продукты питания
животного
происхождения
- печень;
- язык говяжий;
- мясо кролика;
- индюшатина;
- гусиное мясо;
- говядина;
- рыба.
- 9 мг;
- 5 мг;
- 4,4 мг;
- 4 мг;
- 3 мг;
- 2,8 мг;
- 2,3 мг.
Продукты питания растительного происхождения
- сушеные грибы;
- свежий горох;
- гречка;
- геркулес;
- свежие грибы;
- абрикосы;
- груша;
- яблоки;
- сливы;
- черешня;
- свекла.
- 35 мг;
- 11,5 мг;
- 7,8 мг;
- 7,8 мг;
- 5,2 мг;
- 4,1 мг;
- 2,3 мг;
- 2,2 мг;
- 2,1 мг;
- 1,8 мг;
- 1,4 мг.
При соблюдении диеты также следует увеличить потребление продуктов, содержащих витамин C, а также белок мяса (они повышают усвояемость железа в организме) и снизить потребление яиц, соли, кофеина и кальция (они уменьшают всасываемость железа).
Медикаментозное лечение
При лечении железодефицитной анемии больному параллельно с диетой назначается прием препаратов железа. Данные лекарственные средства предназначены для восполнения дефицита железа в организме. Они выпускаются в виде капсул, драже, инъекций, сиропов и таблеток.
Доза и длительность лечения подбирается индивидуально в зависимости от следующих показателей:
- возраста пациента;
- степени тяжести заболевания;
- причины, вызвавшей железодефицитную анемию;
- на основе результатов анализов.
Препараты железа принимаются за один час до еды или через два часа после приема пищи. Данные лекарственные средства нельзя запивать чаем или кофе, так как снижается всасываемость железа, поэтому их рекомендуется запивать водой или соком.
Принимать внутрь по одному грамму три – четыре раза в сутки.
Принимать по одной таблетке в день, с утра за тридцать минут до приема пищи.
Принимать по одной таблетке один – два раза в день.
Данные препараты рекомендуется назначать совместно с витамином C (по одной таблетке один раз в день), так как последний увеличивает всасываемость железа.
Препараты железа в виде инъекций (внутримышечных или внутривенных) применяются в следующих случаях:
- при тяжелой степени анемии;
- если анемия прогрессирует, несмотря на принимаемые дозы железа в виде таблеток, капсул или сиропа;
- если у больного имеются заболевания желудочно-кишечного тракта (например, язва желудка и двенадцатиперстной кишки, неспецифический язвенный колит, болезнь Крона), так как принимаемый препарат железа может усугубить имеющееся заболевание;
- перед оперативными вмешательствами с целью ускоренного насыщения организма железом;
- если у пациента имеется непереносимость препаратов железа при их приеме внутрь.
Хирургическое лечение
Хирургическое вмешательство производится при наличии у больного острого или хронического кровотечения. Так, например, при желудочно-кишечном кровотечении может применяться фиброгастродуоденоскопия или колоноскопия с выявлением области кровотечения и последующей его остановкой (например, удаляется кровоточащий полип, коагулируется язва желудка и двенадцатиперстной кишки). При маточных кровотечениях, а также при кровотечениях в органах, находящихся в брюшной полости, может применяться лапароскопия.
При необходимости больному может быть назначено переливание эритроцитарной массы для восполнения объема циркулирующей крови.

В норме витамин В12 поступает в организм с пищевыми продуктами. На уровне желудка В12 связывается с продуцируемым в нем белком, гастромукопротеидом (внутренний фактор Касла). Данный белок защищает поступивший в организм витамин от негативного воздействия микрофлоры кишечника, а также способствует его усвоению.
Комплекс гастромукопротеид и витамин В12 доходит до дистального отдела (нижний отдел) тонкого кишечника, где происходит распад этого комплекса, всасывание витамина В12 в слизистый слой кишечника и дальнейшее поступление его в кровь.
Из кровяного русла данный витамин поступает:
- в красный костный мозг для участия в синтезе эритроцитов;
- в печень, где происходит его депонирование;
- в центральную нервную систему для синтеза миелиновой оболочки (покрывает аксоны нейронов).
Клиническая картина В12 и фолиево-дефицитной анемии основывается на развитии у больного следующих синдромов:
- анемический синдром;
- желудочно-кишечный синдром;
- невралгический синдром.
| |
Данные симптомы развиваются вследствие атрофических изменений слизистого слоя ротовой полости, желудка и кишечника. |
|
- снижение уровня эритроцитов и гемоглобина;
- гиперхромия (выраженная окраска эритроцитов);
- макроцитоз (увеличенный размер эритроцитов);
- пойкилоцитоз (различная форма эритроцитов);
- при микроскопии эритроцитов выявляются кольца Кебота и тельца Жолли;
- ретикулоциты снижены или в норме;
- снижение уровня лейкоцитов (лейкопения);
- повышение уровня лимфоцитов (лимфоцитоз);
- снижение уровня тромбоцитов (тромбоцитопения).
В биохимическом анализе крови наблюдается гипербилирубинемия, а также снижение уровня витамина В12.
При пункции красного костного мозга выявляется повышение мегалобластов.
Больному могут быть назначены следующие инструментальные исследования:
- исследование желудка (фиброгастродуоденоскопия, биопсия);
- исследование кишечника (колоноскопия, ирригоскопия);
- ультразвуковое исследование печени.
Данные исследования помогают выявить атрофические изменения слизистой оболочки желудка и кишечника, а также обнаружить заболевания, которые привели к развитию В12-дефицитной анемии (например, злокачественные образования, цирроз печени).
Все больные госпитализируются в отделение гематологии, где проходят соответствующее лечение.
Питание при В12-дефицитной анемии
Назначается диетотерапия, при которой увеличивается потребление продуктов, богатых витамином В12.
Суточная норма витамина В12 составляет три микрограмма.
Количество витамина В12 на сто миллиграмм
Медикаментозное лечение
Медикаментозное лечение назначается больному по следующей схеме:
- В течение двух недель больной ежедневно получает по 1000 мкг Цианокобаламина внутримышечно. За две недели у пациента исчезает неврологическая симптоматика.
- В течение последующих четырех – восьми недель больной получает по 500 мкг ежедневно внутримышечно для насыщения депо витамина В12 в организме.
- Впоследствии больной пожизненно получает внутримышечные инъекции один раз в неделю по 500 мкг.
Во время лечения одновременно с Цианокобаламином больному могут назначить прием фолиевой кислоты.
Больной В12-дефицитной анемией должен пожизненно наблюдаться у гематолога, гастролога и семейного врача.
Фолиевая кислота (витамин B9) является водорастворимым витамином, который отчасти продуцируется клетками кишечника, но в основном должен поступать извне для восполнения необходимой для организма нормы. Суточная норма фолиевой кислоты составляет прием 200 – 400 мкг.
В пищевых продуктах, а также в клетках организма фолиевая кислота находится в форме фолатов (полиглутаматы).
Фолиевая кислота играет большую роль в организме человека:
- участвует в развитии организма во внутриутробном периоде (способствует формированию нервной проводимости тканей, кровеносной системы плода, предупреждает развитие некоторых пороков развития);
- участвует в росте ребенка (например, в первый год жизни, в период полового созревания);
- влияет на процессы кроветворения;
- совместно с витамином В12 участвует в синтезе ДНК;
- препятствует образованию тромбов в организме;
- улучшает процессы регенерации органов и тканей;
- участвует в обновлении тканей (например, кожи).
Абсорбция (всасывание) фолатов в организме осуществляется в двенадцатиперстной кишке и в верхнем отделе тонкого кишечника.
При фолиеводефицитной анемии у больного наблюдается анемический синдром (такие симптомы как повышенная утомляемость, сердцебиение, бледность кожных покровов, снижение работоспособности). Неврологический синдром, а также атрофические изменения слизистой оболочки ротовой полости, желудка и кишечника при данном виде анемии отсутствуют.
Также у больного может наблюдаться увеличение размеров селезенки.
При общем анализе крови наблюдаются следующие изменения:
- гиперхромия;
- снижение уровня эритроцитов и гемоглобина;
- макроцитоз;
- лейкопения;
- тромбоцитопения.
В результатах биохимического анализа крови наблюдается снижение уровня фолиевой кислоты (менее 3 мг/мл), а также повышение непрямого билирубина.
При проведении миелограммы выявляется повышенное содержание мегалобластов и гиперсегментированных нейтрофилов.
Питание при фолиеводефицитной анемии играет большую роль, больному необходимо ежедневно потреблять продукты, богатые фолиевой кислотой.
Следует заметить, что при любой кулинарной обработке продуктов фолаты разрушаются приблизительно на пятьдесят процентов и более. Поэтому для обеспечения организма необходимой суточной нормой продукты рекомендуется употреблять в свежем виде (овощи и фрукты).
| Продукты питания | Наименование продуктов | Количество железа на сто миллиграмм |
| Продукты питания животного происхождения |
|
|
| Продукты питания растительного происхождения |
|
|
Медикаментозное лечение фолиеводефицитной анемии включает прием фолиевой кислоты в количестве от пяти до пятнадцати миллиграмм в сутки. Необходимую дозировку устанавливает лечащий врач в зависимости от возраста пациента, тяжести течения анемии и результатов исследований.
Профилактическая доза включает прием одного – пяти миллиграмм витамина в сутки.
Апластическая анемия может быть врожденной или приобретенной.
Клинические проявления апластической анемии зависят от степени выраженности панцитопении.
При апластической анемии у больного наблюдаются следующие симптомы:
- бледность кожных покровов и слизистых;
- головная боль;
- учащенное сердцебиение;
- одышка;
- повышенная усталость;
- отеки на ногах;
- десневые кровотечения (вследствие снижения уровня тромбоцитов в крови);
- петехиальная сыпь (красные пятна на коже маленьких размеров), синяки на коже;
- острые или хронические инфекции (вследствие снижения уровня лейкоцитов в крови);
- изъязвления орофарингеальной зоны (поражается слизистая полости рта, язык, щеки, десна и глотка);
- желтушность кожных покровов (симптом поражения печени).
При биохимическом анализе крови наблюдается:
- повышение сывороточного железа;
- насыщение трансферрина (белок, переносящий железо) железом на 100%;
- повышение билирубина;
- повышение лактатдегидрогеназы.
При пункции красного мозга и последующем гистологическом исследовании выявляются:
- недоразвитие всех ростков (эритроцитарный, гранулоцитарный, лимфоцитарный, моноцитарный и макрофагальный);
- замещение костного мозга жировым (желтый костный мозг).
Среди инструментальных методов исследований больному может быть назначено:
- ультразвуковое исследование паренхиматозных органов;
- электрокардиография (ЭКГ) и эхокардиография;
- фиброгастродуоденоскопия;
- колоноскопия;
- компьютерная томография.
При правильно подобранном поддерживающем лечении состояние пациентов с апластической анемией существенно улучшается.
При лечении апластической анемии больному назначаются:
- иммунодепрессивные препараты (например, Циклоспорин, Метотрексат);
- глюкокортикостероиды (например, Метилпреднизолон);
- антилимфоцитарный и антитромбоцитарный иммуноглобулины;
- антиметаболиты (например, Флударабин);
- эритропоэтин (стимулирует образование эритроцитов и стволовых клеток).
Немедикаментозное лечение включает:
- трансплантацию костного мозга (от совместимого донора);
- переливание компонентов крови (эритроциты, тромбоциты);
- плазмаферез (механическое очищение крови);
- соблюдение правил асептики и антисептики с целью предотвращения развития инфекции.
Также при тяжелом течении апластической анемии больному может понадобиться хирургическое лечение, при котором производится удаление селезенки (спленэктомия).
В зависимости от эффективности проводимого лечения у больного при апластической анемии может наблюдаться:
- полная ремиссия (затухание или полное исчезновение симптомов);
- частичная ремиссия;
- клиническое улучшение;
- отсутствие эффекта от лечения.
|
|
|
|

Гемолитическая анемия может развиться вследствие наследственных или приобретенных заболеваний.
По локализации гемолиз может быть:
- внутриклеточным (например, аутоиммунная гемолитическая анемия);
- внутрисосудистым (например, переливание несовместимой крови, диссеминированное внутрисосудистое свертывание).
У пациентов с легкой степенью гемолиза уровень гемоглобина может быть нормальным, если производство эритроцитов соответствует темпу их разрушения.
Преждевременное разрушение эритроцита может быть связано со следующими причинами:
- внутренними мембранными дефектами эритроцитов;
- дефектами структуры и синтеза белка гемоглобина;
- ферментативными дефектами в эритроците;
- гиперспленомегалией (увеличение размеров печени и селезенки).
Наследственные заболевания могут вызвать гемолиз в результате отклонений мембраны эритроцита, ферментативных дефектов и отклонений гемоглобина.
Существуют следующие наследственные гемолитические анемии:
- энзимопатии (анемии, при которых наблюдается недостаток фермента, дефицит глюкозо-6-фосфатдегидрогеназы);
- наследственный сфероцитоз или болезнь Минковского-Шоффара (эритроциты неправильной шарообразной формы);
- талассемия (нарушение синтеза полипептидных цепей, входящих в строение нормального гемоглобина);
- серповидно-клеточная анемия (изменение строения гемоглобина приводит к тому, что эритроциты принимают серпообразную форму).
Приобретенные причины гемолитической анемии включают иммунные и не иммунные нарушения.
Иммунные нарушения характеризуются аутоиммунной гемолитической анемией.
Не иммунные нарушения могут быть вызваны:
- ядохимикатами (например, пестициды, бензол);
- лекарственными средствами (например, противовирусные препараты, антибиотики);
- физическим повреждением;
- инфекциями (например, малярия).
Гемолитическая микроангиопатическая анемия приводит к производству фрагментированных эритроцитов и может быть вызвана:
- дефектным искусственным сердечным клапаном;
- диссеминированным внутрисосудистым свертыванием;
- гемолитическим уремическим синдромом;
- тромбоцитопенической пурпурой.
Симптомы и проявления гемолитической анемии разнообразны и зависят от вида анемии, степени компенсации, а также от того, какое лечение получал больной.
Следует заметить, что гемолитическая анемия может протекать бессимптомно, а гемолиз выявляться случайно во время обычного лабораторного тестирования.
При гемолитической анемии могут наблюдаться следующие симптомы:
- бледность кожи и слизистых;
- ломкость ногтей;
- тахикардия;
- учащение дыхательных движений;
- снижение артериального давления;
- желтушность кожных покровов (из-за увеличения уровня билирубина);
- на ногах могут наблюдаться язвы;
- гиперпигментация кожи;
- желудочно-кишечные проявления (например, боль в животе, нарушение стула, тошнота).
Следует заметить, что при внутрисосудистом гемолизе у больного наблюдается дефицит железа из-за хронической гемоглобинурии (наличие гемоглобина в моче). Вследствие кислородного голодания нарушается сердечная функция, что приводит к развитию у пациента таких симптомов как слабость, тахикардия, одышка и стенокардия (при тяжелой форме анемии). Из-за гемоглобинурии у больного также наблюдается потемнение мочи.
Длительный гемолиз может привести к развитию желчных камней вследствие нарушения обмена билирубина. При этом пациенты могут жаловаться на боль в животе и бронзовый цвет кожи.
В общем анализе крови наблюдается:
- снижение уровня гемоглобина;
- снижение уровня эритроцитов;
- увеличение ретикулоцитов.
При микроскопии эритроцитов выявляется их серпообразная форма, а также кольца Кебота и тельца Жолли.
В биохимическом анализе крови наблюдается повышение уровня билирубина, а также гемоглобинемия (увеличение свободного гемоглобина в плазме крови).
Также необходимо сдать анализ мочи на выявление наличия гемоглобинурии.
При пункции костного мозга наблюдается выраженная гиперплазия эритроцитарного ростка.
Существует много видов гемолитической анемии, поэтому лечение может отличаться в зависимости от причины, вызвавшей анемию, а также от типа гемолиза.
При лечении гемолитической анемии больному могут назначаться следующие препараты:
- Фолиевая кислота. Профилактическая доза фолиевой кислоты назначается, потому что активный гемолиз может потреблять фолат и впоследствии привести к развитию мегалобластоза.
- Глюкокортикостероиды (например, Преднизолон) и иммунодепрессанты (например, Циклофосфан). Данные группы препаратов назначаются при аутоиммунной гемолитической анемии.
- Переливание эритроцитарной массы. Больному индивидуально подбираются отмытые эритроциты, так как существует высокий риск разрушения перелитой крови.
Спленэктомия
Спленэктомия может быть первоначальным вариантом в лечении некоторых типов гемолитической анемии, таких как, например, наследственный сфероцитоз. В других случаях, например, при аутоиммунной гемолитической анемии, спленэктомия рекомендуется тогда, когда другие методы лечения потерпели неудачу.
Терапия препаратами железа
При гемолитической анемии применение препаратов железа в большинстве случаев противопоказано. Это связано с тем, что уровень железа при данной анемии не снижается. Однако если у больного наблюдается постоянная гемоглобинурия, то происходит существенная потеря железа из организма. Поэтому при выявлении дефицита железа пациенту может быть назначено соответствующее лечение.
Проявления анемии будут зависеть от следующих факторов:
- какое количество крови было потеряно;
- с какой скоростью происходит кровопотеря.
Симптомами постгеморрагической анемии являются:
- слабость;
- головокружение;
- бледность кожных покровов;
- сердцебиение;
- одышка;
- тошнота, рвота;
- сечение волос и ломкость ногтей;
- шум в ушах;
- мелькание мушек перед глазами;
- жажда.
При острой кровопотере у больного может развиться геморрагический шок.
Выделяют четыре степени геморрагического шока.
источник