Для лечения гастрита и язвы наши читатели успешно используют Монастырский Чай. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
Около 70-80 % населения страдает от такой патологии как хронический гастрит. Актуальность и значимость проблемы определяется не только ее большой распространенностью, но и доказанной взаимосвязью с такими осложнениями как язвенная болезнь или рак. Данное поражение желудка также довольно часто диагностируется в педиатрии. Поэтому важно и полезно знать первые проявления заболевания, способы его подтверждения, методы лечения и меры профилактики.
Под хроническим гастритом понимают полиэтиологическое заболевание, в основе которого лежит длительно протекающее воспаление в слизистой оболочке желудка. Механизм развития воспалительного процесса достаточно сложен и зависит от характера провоцирующих факторов, однако, из общего – этиологический агент тормозит активность местной защиты и повреждает слизистую оболочку. В последующем в ней появляются дистрофические изменения, которые «диктуют» степень выраженности клинических проявлений.
Вызвать симптомы гастрита у взрослых способны следующие факторы:
- инфицированность Helicobacter Pylori;
- повышенная кислотность желудочного сока;
- дисфункция (слабость) сфинктера пилорического отдела желудка;
- длительное курение;
- нерациональное и несбалансированное питание (превалирование в рационе жирной, грубой, острой и жареной пищи, газированных напитков, кондитерских изделий и фаст-фуда);
- злоупотребление напитками, содержащими алкоголь;
- длительное эмоциональное перенапряжение и частые стрессовые ситуации на работе или же дома;
- продолжительный прием нестероидных противовоспалительных или гормональных средств, а также других препаратов, способных повредить стенку желудка;
- наследственная предрасположенность, аутоиммунные процессы, эндокринопатии;
- воздействие некоторых химических агентов (кислоты, щелочи) и высокая температура (кипяток).
Наиболее часто встречающейся формой является хронический гастрит типа B, который еще называют бактериальным. Он обусловлен наличием в организме человека патогенного штамма Helicobacter Pylori – микроорганизмов, живущих на стенках желудка и при определенных факторах, вызывающих в нем воспаление. Бактерия выделяет специфический фермент – уреазу, которая ощелачивает среду вокруг себя и повреждает париетальные клетки. В итоге нарушается синтез соляной кислоты и повышается кислотность желудочного сока.
К более редким формам поражения желудка относят:
- Хронический гастрит типа A. В основе его развития лежит иммунокомплексное воспаление как результат наследственного дефекта защитной системы организма. Как правило, такие люди страдают и другими видами аутоиммунных заболеваний (дерматомиозит, ревматизм, васкулиты и т.п.);
- Хронический гастрит типа C. Данный тип воспаления возникает в результате наличия дуодено-гастрального рефлюкса. Таким образом, содержимое кишечника со всеми его ферментами, желчными кислотами попадает непосредственно в полость желудка, способствуя постоянному химическому повреждению слизистой.
Еще одна классификация гастритов основывается на локализации воспаления:
- очаговый антральный;
- фундальный (поражение дна);
- поражение тела;
- диффузный или распространенный.
Стоит отметить, что симптомы гастрита желудка у взрослых зависят от степени выраженности и расположения воспалительного процесса. В некоторых случаях болезнь может практически не проявлять себя и диагностироваться лишь при развитии осложнений.
Любое хроническое воспаление характеризуется волнообразным течением, то есть со временем ремиссия сменяется обострением. Спровоцировать такой переход может сильный стресс, грубая погрешность в диете, злоупотребление алкоголем. В некоторых случаях причиной становится прием лекарственных препаратов по типу НПВП (Аспирин, Диклофенак, Нимесулид и т.п.).
При воспалении тела желудка симптомы скудные и, в основном, выражаются в ощущении тяжести в области эпигастрия, возникающей сразу после или во время еды.
При поражении антрального отдела признаки хронического гастрита проявляются сильнее и выражаются в:
- чувстве давления или полноты в собственно эпигастральной зоне;
- ноющих или спастических болях в районе желудка, появляющихся спустя 30-40 минут после употребления пищи;
- частом срыгивании и отрыжке кислым, реже – горечью;
- ощущении жжения в эпигастрии;
- периодической тошноте, изредка приводящей ко рвоте.
Кроме того, для гастрита типа B (ассоциированного с хеликобактерной инфекцией) характерны признаки «кишечной» диспепсии, проявляющиеся в виде запоров, урчания и вздутия в животе, послабления стула. Также возможно формирование язвенноподобного симптомокомплекса (голодные ночные боли, частая рвота, снижение массы тела), указывающего на высокий риск развития язвенной болезни.
Из общих расстройств выделяют астено невротический синдром с такими симптомами как слабость, боли в сердце, раздражительность, склонность к пониженному системному давлению. При длительно текущем процессе присоединяются дефицитарные анемии из-за нарушенного всасывания витамина B12 и железа (сухость и бледность кожных покровов, хроническая усталость, выраженная слабость, заеды, выпадение волос, повышенная ломкость ногтей, жжение в языке и т.п.).
При объективном осмотре врач отмечает обложенный белым налетом язык с отпечатками зубов по краям, неприятный запах изо рта, трещины в области наружных углов губ («заеды») и болезненность при пальпации желудка и эпигастрального отдела живота. Возможно вздутие и урчание кишечника.
Существует специальная инструкция (клинический протокол), согласно которой происходит обследование пациентов с вышеперечисленными жалобами. Им назначают:
- клинические и биохимическое исследование периферической крови;
- общий анализ мочи;
- ультразвуковое обследование брюшной полости;
- ФЭГДС совместно с биопсией на H. Pylori (инвазивная диагностика слизистой пищевода, желудка и начального отдела двенадцатиперстной кишки с помощью эндоскопа);
- копроцитограмма.
Примечание! H. Pylori легко передается аэрозольным путем, через поцелуи и предметы быта. Поэтому в случае диагностирования ассоциированного с хеликобактерной инфекцией хронического гастрита обследование должен пройти каждый член семьи. При нежелании выполнить ФЭГДС можно сдать венозную кровь на наличие антител к Хеликобактер или сделать дыхательный уреазный тест, который совершенно не вызывает физического дискомфорта. При положительном ответе – специфическое лечение должны пройти все, иначе велик риск рецидивирования.
Как лечить хронический гастрит – довольно актуальная тема в современной медицине. Состав и длительность терапии зависит от формы воспаления, а также от длительности процесса.
В первую очередь назначается специальная диета при хроническом гастрите (минимум на 1 месяц), которая направлена на коррекцию кислотности желудочного сока и предупреждение еще большего травмирования слизистой.
Для норм- или гиперацидного гастрита (то есть с нормальной или же повышенной продукцией соляной кислоты) назначается стол № 1, из которого исключают:
- крепкие и жирные бульоны на основе рыбы, мяса или грибов;
- жареные блюда;
- консервированные и копченые продукты;
- любые приправы, маринады;
- крепкий чай, любой кофе, соки, алкоголь, газированную воду и напитки.
В питание при хроническом гастрите рекомендуется добавить отварную рыбу и нежирное мясо, макароны из высших сортов пшеницы, яйца всмятку, галетное печенье, каши из трудноусвояемых углеводов (гречневая, рисовая, овсяная). Также разрешены кисели, суфле, овощное пюре, желе, какао и запеченные яблоки.
Диета при хроническом гастрите с пониженной секрецией носит название стол № 2 и исключает из себя:
- жирные сорта рыбы и мяса;
- соленые и острые продукты;
- свежий хлеб, сдобу, молочный шоколад;
- виноград, белокочанную капусту, цельное молоко.
Рацион необходимо разнообразить обезжиренными рыбными или мясными бульонами, рыбой (хек, минтай), разнообразной зеленью, ржаным хлебом, тушенными овощами, фруктовыми соками и кашами на молоке.
После перехода гастрита в стадию ремиссии назначают стол № 15 – ограничиваются жареные, жирные блюда, копчености, газированные напитки, алкоголь и кондитерские изделия.
При установлении хронического гастрита лечение обязательно включает в себя использование лекарственных препаратов.
Если речь идет о воспалении желудка в результате инфекции, то проводится специфическая эрадикационная терапия первой или второй линии:
- Ингибитор протонной помпы (Омез, Нольпаза) + кларитромицин (Фромилид) + амоксициллин на 7-14 дней. Или вместо Омеза назначают препараты на основе висмута (Де-нол).
- Антацид (тот же Омез) + Де-нол + амоксициллин + нифурател/фуразолидон на 10-14 дней.
Дополнительно используют седативные средства, облепиховое масло и пробиотики.
При атрофической форме воспаления с пониженной кислотностью желудочного сока используют такой препарат растительного происхождения как Плантаглюцид.
О лечении атрофического гастрита поподробнее читайте здесь.
После пройденного курса лечения, а именно через 4 недели, следует выполнить повторное эндоскопическое исследование желудка (ФЭГДС).
Болезнь легче предупредить, чем лечить, поэтому рекомендуется:
- придерживаться правильного питания (как минимум 5 приемов пищи в день, отсутствие в рационе специй, копченостей, шоколада, жареных и жирных блюд);
- отказаться от вредных привычек – курения или частого приема алкоголя;
- своевременно обращаться за медицинской помощью в случае появления каких-либо жалоб;
- при наличии хронического гастрита в анамнезе/у родственников раз в год проходить ФЭГДС (исследование также является ранним скринингом рака желудка).
Таким образом, зная, какие при хроническом гастрите симптомы и лечение у взрослых, можно обезопасить себя от возникновения тяжелых осложнений.
Эта патология может быть вызвана самыми разными факторами или их сочетанием. Их принято разделять на внешние, зависящие от условий среды и образа жизни человека, и внутренние, связанные с другими заболеваниями. Внешние причины:
- погрешности в питании – отсутствие режима приема пищи, еда всухомятку, привычка плохо пережевывать, употребление слишком горячей или, напротив, холодной еды, пристрастие к жирному, жареному, копченому, соленому, газированным напиткам или спиртному;
- психоэмоциональный фактор – хронический стресс, проявляющий себя в нарушении работы внутренних органов;
- экологическое неблагополучие – избыток в местной пище и воде токсичных примесей;
- курение;
- прием некоторых лекарственных препаратов, в том числе противовоспалительных и обезболивающих;
- носительство бактерии Helicobacter pylori.
- пернициозная анемия;
- сахарный диабет I типа;
- аутоиммунное поражение щитовидной железы;
- хроническая недостаточность коры надпочечников;
- дуодено-гастральный рефлюкс – заброс щелочного и богатого ферментами содержимого двенадцатиперстной кишки в желудок.
В настоящий момент наиболее актуальной и распространенной причиной признана хеликобактерная инфекция. Что это такое? Бактерия легко передается бытовым путем, обычно поражает всех членов семьи. По разным исследованиям ее обнаруживают у 80% пациентов, обратившихся за помощью с признаками неблагополучия верхних отделов желудочно-кишечного тракта. Одинаково часто встречается у детей и взрослых.
Этот микроорганизм поражает клетки слизистой оболочки желудка, заставляя их вырабатывать избыток соляной кислоты и гастрина, тем самым вызывая воспаление и нарушение иммунного статуса. Слишком кислый желудочный сок попадает в двенадцатиперстную кишку, вызывая изменения и в ней. В результате раскоординируется вся деятельность верхних отделов пищеварительной системы – режим выработки пищеварительных соков и проталкивания пищевого комка не соответствует приемам пищи, усугубляя состояние органов.
В зависимости от того, какая часть желудка наиболее поражена, могут проявляться в различном сочетании те или иные признаки болезни:
- боли в эпигастральной области (верхнем отделе живота, у места соединения ребер) натощак;
- ноющие боли после еды там же или в околопупочной области;
- изжога;
- отрыжка воздухом, кислым или съеденной пищей;
- чувство тяжести в животе;
- ощущение переполнения желудка;
- быстрое насыщение во время еды, даже если съедено было всего пару ложек кушанья;
- снижение аппетита;
- тошнота;
- однократная рвота, приносящая облегчение;
- неустойчивый стул – чередование запоров и поносов;
- утомляемость, головные боли;
- бледность кожи, ломкость волос и ногтей, заеды в углах рта (клиника авитаминоза);
- снижение массы тела;
- кровоточивость десен;
- потливость, эмоциональная нестабильность.
Классификация гастрита учитывает стадию заболевания, его причины и результаты диагностики. Только полный клинический диагноз по итогам всех анализов и тестов поможет правильно подобрать терапию. По состоянию желудочного эпителия может наблюдаться:
- воспаление;
- атрофия (ослабление и снижение функции клеток);
- метаплазия (новые клетки, появляющиеся взамен погибших, отличаются от должных – предраковое состояние).
По наиболее страдающему участку:
- поражение тела и дна желудка;
- поражение выходного отдела желудка;
- пангастрит (вся слизистая повреждена).
По результатам ФЭГДС гастрит бывает:
- поверхностный эритематозный – слизистая покрасневшая, отечная;
- эрозивный – имеются неглубокие дефекты поверхностного слоя по типу язвенных;
- атрофический – эпителий желудка снижает свою функцию, постепенно «вырождается»;
- геморрагический – присутствуют обильные кровоизлияния;
- гиперпластический (гипертрофический) – слизистая реагирует на длительное воспаление избыточным разрастанием, утолщением, необходимо дифференцировать от онкологического процесса.
По уровню выработки желудочного сока различают хронический гастрит:
- с нормальной кислотностью;
- с пониженной кислотностью;
- с повышенной кислотностью.
Людей трудоспособного возраста волнует вопрос, можно ли вылечить желудок без стационара. Терапия заболевания в неосложненных случаях не требует госпитализации и вполне возможна в домашних условиях. Она складывается из двух обязательных составляющих – лечебного питания и приема лекарственных препаратов.
Если установлен гастрит с пониженной кислотностью, лечение основано на диете №2, с повышенной – рекомендуется стол №1 по Певзнеру. В любом случае стоит придерживаться основных рекомендаций, касающихся лечения всех болезней пищеварительной системы.
- Питание должно быть частым и небольшими порциями. Идеально – 6 раз в день, можно выделить 3 больших приема пищи (завтрак, обед, ужин) и 3 малых (второй завтрак, полдник, вечерний перекус).
- Пища употребляется не слишком горячей и не холодной.
- Желательно, чтобы блюда были жидкие или пюреобразной консистенции. Твердые куски необходимо тщательно пережевывать.
- Хотя бы на время обострения следует отказаться от жирного, жареного, копченого, соленого, избытка специй, газированных напитков.
- Необходимо пить достаточно жидкости – простой воды без газа не менее 6 стаканов ежедневно.
- Рекомендуется вести пищевой дневник и отражать в нем все съеденное, принятые лекарственные препараты и интенсивность неприятных симптомов.
Диета №1 подразумевает также исключение из рациона мучных изделий, наваристых бульонов, макарон, бобовых, сыра, кисломолочных продуктов, свежих фруктов и ягод, кофе, какао, крепкого чая. Чем острее процесс, тем строже ограничения по набору продуктов и их механической обработке. При длительной ремиссии разрешаются вчерашний пшеничный хлеб, сухое печенье, бисквит, некислый кефир, простокваша, творог, сладкие ягоды и фрукты в протертом, вареном и печеном виде.
Диета №2 предполагает приготовление супов на некрепких бульонах, а также вторых блюд методом тушения, варения или запекания. Разрешаются кисломолочные продукты, нежирный творог и сыр.
Для терапии хронического воспаления слизистой оболочки желудка используется несколько групп медикаментов:
Для лечения гастрита и язвы наши читатели успешно используют Монастырский Чай. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
- нормализующие двигательную активность желудочно-кишечного тракта (Метоклопрамид, Домперидон);
- снижающие кислотность желудочного сока – антациды (Маалокс, Гевискон, Фосфалюгель и др.);
- снижающие выработку соляной кислоты (Ранитидин, Фамотидин, Омепразол, Эзомепразол и др.);
- антибиотики для борьбы с хеликобактерной инфекцией (Амоксициллин, Кларитромицин);
- спазмолитики для снятия схваткообразных болей;
- препараты, улучшающие обмен веществ в слизистой оболочке желудка (витамины);
- цитопротекторы – защищают клетки от ракового перерождения;
- растительные средства для стимуляции секреции;
- легкие успокоительные препараты.
Как видите, в практической медицине достаточно большой арсенал лекарств, чтобы помочь больному. Вовсе не нужно применять их все, чтобы навсегда победить недуг. Врач по результатам полного обследования порекомендует, как лечить гастрит индивидуально подобранной комбинацией 3 – 5 средств на курс, разъяснит назначение и особенности приема каждого из них. Не забудьте сообщить, если у вас хотя бы раз в жизни возникали аллергические реакции на те или иные препараты.
Хронический гастрит – это длительное прогрессирующее заболевание, вылечить которое можно с помощью коррекции питания и грамотного приема лекарств. Не занимайтесь самолечением – так вы рискуете не только зря потратить время и деньги, но и получить нежелательные побочные эффекты и осложнения.
Желудок – это сложный, незащищенный отдел желудочно-кишечного тракта. Поверхность органа слизистая, внутри – желудочный сок. Главный компонент сока – соляная кислота. С ее помощью пища перемешивается, расщепляется, всасывается. Из заболеваний желудочно-кишечного тракта 80% приходится на острые и хронические виды гастрита.
В мире 90% людей на протяжении жизни хотя бы раз почувствовали признаки болезни. При неблагоприятных условиях хроническая стадия может перейти в язву или рак желудка, который стоит на первом месте по частоте случаев в онкологии.
Чем опасен гастрит с повышенной кислотностью: симптомы, причины возникновения
Гастрит – это комплекс изменений, патологий, связанных с воспалением внутренней слизистой оболочки желудка. В зависимости от размеров поражения и времени воздействия опасных факторов различают острую и хроническую степень заболевания. Подразделяют гастрит с пониженной и повышенной кислотностью.
Течение острой стадии гастрита – стремительное однократное воспаление слизистой после воздействия ядов, лекарств, недоброкачественной пищи, алкоголя. Заболевание по характеру возникновения делят на виды:
- катаральный гастрит отличается легким, поверхностным поражением слизистой, болевым синдромом, который быстро проходит после принятия лекарств;
- эрозивный гастрит характеризуется сильным поражением слизистой, наличием эрозийных включений, ярким болевым синдромом, присутствием рвоты с примесью крови;
- фибринозный гастрит обуславливается образованием белковой пленки – фибрина после инфекции или отравления тяжелыми металлами;
- коррозивный гастрит – этот вид развивается при сильном отравлении химическими веществами, поражаются глубокие слои стенок желудка, в рвотной массе присутствуют кровь, слизь;
- флегмонозный гастрит – это развитие гнойного воспаления на фоне распространения бактерий.
Состояние ухудшается, поднимается температура, бьет озноб, путается сознание.
Хронический гастрит – результат болезни острой формы. Его развитие – медленное, длительное течение со смазанными признаками.
Гастрит бывает: поверхностный, когда поражена только поверхностная часть; атрофический – заболевание в запущенной фазе с атрофией части органа.
Осложнения при заболевании гастритом хронического вида серьезные и требуют пристального внимания:
- внутренние кровотечения;
- перерождение гастрита в язву;
- перерождение гастрита в рак желудка;
- полипы в кишечнике;
- начальная стадия анемии при малых и постоянных кровотечениях.
При нарушениях пищеварения наступает апатия, снижается работоспособность. Человек быстро устает, нервничает. Гастрит имеет следующие признаки, симптомы:
- ощущение тяжести в области живота;
- боли различного характера в животе, при ощущении голода или после приема еды;
- постоянная тошнота, рвота по утрам;
- сильная изжога;
- кислый, дурной запах изо рта;
- сухость во рту или обильное слюноотделение;
- перебои в работе кишечника (понос, запоры);
- слабость, головокружение, низкое давление, раздражительность;
- выделение крови при эрозийном гастрите острого течения;
- анемия при хронической форме;
- отрыжка;
- метеоризм.
Причины возникновения хронического гастрита бывают внешние и внутренние. Основной причиной болезни считается наличие бактерий, способных жить в кислой среде (Helicobacter pylori), которые при слабом иммунитете вызывают гастрит. Внешние причины:
- несбалансированное питание, нехватка витаминов и клетчатки, переедание, недоедание,
- преобладание жирной и острой пищи;
- вредные привычки, такие как алкоголь, курение;
- прием лекарственных препаратов без контроля;
- стрессовые ситуации;
- вредные условия труда;
- недостаточное пережевывание пищи;
- заболевания, связанные с обменом веществ;
- заболевание почек, печеночная недостаточность.
- наследственность;
- болезнь желчного пузыря, когда часть желчи забрасывается в желудок;
- нарушение со стороны иммунной системы;
- нарушения гормонального характера.
Начинать лечение надо с выявления состояния слизистой оболочки по результатам ФГСД (фиброгастродуоденоскопия – обследование желудка и двенадцатиперстной кишки).
О причинах возникновения гастрита и его лечении — в тематическом видеоматериале:
В период обострения болезни и при хронической стадии необходима специальная диета. Питаться надо часто и небольшими порциями. Еду принимать в теплом виде.
Категорически запрещен прием алкоголя, жирной, острой, соленой пищи. В этот момент лучше питаться кашами на воде, отварным рисом и картофельным пюре.
Гастрит лечится в домашних условиях, при помощи народных средств, рецептов и лечебного питания:
- Вода. Перед завтраком выпивать простой, желательно комнатной температуры воды 1–2 стакана, чтобы начать работу желудка.
- Мед. Брать свежий, лучше цветочный мед. Употреблять перед едой по 1–2 столовых ложки утром и вечером с теплой водой, чаем. Можно пить утром медовую воду. Через 15–20 минут принимать мягкую пищу. Курс 1 месяц.
- Результат лечения усиливается, если в мед добавить молоко. Для этого в теплом молоке растворяют 2 столовые ложки меда. При сильных болях в желудке пить такой состав весь день. На завтрак употреблять нежирный кефир, легкий йогурт, молочный омлет. После меда вечером ничего не есть. В течение курса исключить острое и кофе.
- Полезно пить мед с соком алоэ при сильном газообразовании. В равных количествах смешивается мед с соком алоэ и принимается по одной чайной ложке не более трех раз в день.
- Масло (нерафинированное), лучше оливковое, полезно для пищеварения выпивать по одной столовой ложке утром. Через две недели наступает облегчение. Курс два месяца.
- Сок картофеля считается наиболее эффективным способом лечения. Картофель тщательно промывают под проточной водой, с кожурой натирают на терке, отжимают сок. Выпивать натощак утром один стакан свежего сока, полежать 30 мин, подождать ещё 30 минут и позавтракать. Принимать 10 дней и перерыв 10 дней.
- Молоко в объеме 5 л помещают в теплом месте. После скисания процеживают и отделяют творог. Остается сыворотка, в нее добавляют в неочищенный овес, предварительно просеянный и промытый. Сыворотки берется пять частей, а овса одна часть. Варят в течение трех часов в эмалированной кастрюле, на малом огне. Остужают, процеживают, туда же добавляют 300 г меда и 125 г спирта, тщательно перемешивают, хранят все в прохладном месте (на полке холодильника). Принимают по 30 г за 15 минут до еды, предварительно встряхивая. Выпить три таких состава.
- Морковный сок прекрасно понижает кислотность. Морковь очистить, натереть на терке или приготовить сок с помощью соковыжималки. Пить натощак по 1,5 стакана до еды за час.
Сборы состоят из трав, которые заживляют раны, снимают воспаление, обладают обволакивающим действием. Готовые травяные сборы продаются в аптеке или приготавливаются самостоятельно:
- Отличное средство при заболеваниях гастрита (с повышенной кислотностью) – лопух. Листья лопуха сушат, потом приготавливают отвар. В 200 г крутого кипятка закладывают 2 чайных ложки сырья, дают настояться два часа и процеживают. Рекомендуется пить после приема пищи по 2 столовых ложки.
- Например – сбор, состоящий из равных частей валерьянового корня, корешков ревеня, травы зверобоя и травки сушеницы болотной. Все компоненты перемешиваются. В емкость наливают литр красного сухого вина, добавляют три столовых ложки травяной смеси. Оставляют настой на три недели на солнце, процеживают, обязательно добавляют 3 столовых ложки сока растения золотой ус. Принимать по утрам и вечерам по 2 столовые ложки.
- Другой сбор – травы шалфея, к нему добавляют корень гречанки, дополняют перечную мяты и корицу. Составляющие берутся в равных пропорциях и смешиваются. Смесь 1/2 столовой ложки заваривают в 200 г кипятка, настаивают до полного остывания. За 24 часа выпить 400 г этого отвара. Принимать две недели. Нормализуется кислотность.
При лечении этой сложной болезни надо тщательно соблюдать комплексное лечение: медикаментозную терапию, прием разрешенных продуктов, дробное питание и применение народных средств. И тогда болезнь можно держать под контролем.
Расскажите друзьям! Расскажите об этой статье своим друзьям в любимой социальной сети с помощью социальных кнопок. Спасибо!
источник
Воробьев С.А. Морфологические особенности и секреторная функция желудка у больных хроническим гастритом на фоне В12-дефицитной анемии. Эксперементальная и клиническая гастроэнтерология. – 2006. – № 4. – с. 11–16.
Морфологические особенности и секреторная функция желудка у больных хроническим гастритом на фоне В12-дефицитной анемии
Известно, что у больных В12-дефицитной анемией нередко наблюдается хронический гастрит, характеризующийся развитием атрофии слизистой оболочки преимущественно в теле желудка и выраженным снижением продукции соляной кислоты вплоть до анацидного состояния [4,8,11,13]. Это связывается с появлением антител к париетальным клеткам желудка и запуском аутоиммунного воспаления [2,7,12]. На основании выявления противожелудочных антител принято обозначать этот гастрит как аутоиммунный или гастрит типа А [17].
Однако, как известно, В12-дефицитная анемия не является однородным по этиологии и патогенезу заболеванием [3,5,14]. В ее развитии, помимо наследственного дефицита внутреннего фактора Кастла и аутоиммунных процессов, имеют значение алиментарный дефицит цианкобаламина, заболевания кишечника, глистная инвазия, препятствующие достаточному поступлению витамина в организм [4,6,11].
Остается до конца не решенным вопрос, является ли наличие аутоантител к париетальным клеткам и внутреннему фактору Кастла у больных В12-дефицитной анемией причиной атрофии слизистой оболочки желудка или же ее следствием [1,2,7,12]. По данным А.Б. Островского [9], лишь у 50% пациентов с В12-дефицитной анемией имеются в крови антитела к париетальным клеткам слизистой оболочки желудка, а ряд исследователей находили их у больных атрофическим гастритом без пернициозной анемии и даже у здоровых людей [7,12,16].
В литературе мы не встретили сведений, касающихся состояния секреторной функции желудка у больных с В12-дефицитной анемией различной этиологии.
С учетом изложенного возникает необходимость дальнейшего детального изучения различных факторов, участвующих в формировании атрофии слизистой оболочки и секреторной недостаточности желудка у больных мегалобластной анемией.
В связи с этим целью работы было выяснение особенностей морфологического состояния, кислото-, пепсиногено-, гастромуко-протеидообразующей функций желудка у больных хроническим гастритом, ассоциированным с В12-дефицитной анемией различной этиологии.
Обследованы 45 больных хроническим гастритом, лечившихся в терапевтическом отделении 4-й городской больницы Твери, и 15 здоровых лиц (добровольцев) для отработки собственных нормативов.
У 25 пациентов (21 женщина и 4 мужчин, средний возраст — 68,5 ± 77 года) хронический гастрит сочетался с В12-дефицитной анемией, а у 20 (17 женщин и 3 мужчин, средний возраст — 66,4 ± 8,4 года) — с железодефицитной анемией.
Больные железодефицитной анемией были обследованы как контрольная группа сравнения для выяснения влияния характера анемического синдрома на морфофункциональное состояние желудка. Учитывая, что у всех больных В12-дефицитной анемией имелся атрофический гастрит, в группу сравнения включались пациенты с железодефицитной анемией, у которых при эндоскопическом и гистологическом исследовании биоптатов слизистой оболочки желудка выявлялось ее атрофическое поражение.
Пациенты с В12-дефицитной анемией в зависимости от возможных этиологических особенностей были разделены на 3 группы: 10 больных имели в анамнезе указание на алиментарный дефицит B12 (строгое соблюдение постов и материальный недостаток). У 8 пациентов — болезнь, вероятнее всего, имела аутоиммунную природу, поскольку клинически проявлялась ярко выраженной типичной триадой симптомов (анемия, гастрит, фуникулярный миелоз) и сочеталась с такими аутоиммунными заболеваниями, как тиреоидит, ревматоидный артрит. У 7 обследованных при колоноскопии была выявлена патология кишечника (у 2 — доброкачественные полипы сигмовидной кишки, у 5 — дивертикулез толстого кишечника).
Диагноз анемии выставлялся с учетом данных клинического анализа крови, оценки эритроцитарных индексов, определения сывороточного железа и общей железосвязывающей способности сыворотки крови, наличия признаков мегалобластного кроветворения в стернальном пунктате.
Данные исследования клинического анализа крови у больных с анемическим синдромом приведены в табл.1.
Таблица 1. Показатели клинического анализа крови у обследованных больных хроническим гастритом с сопутствующим анемическим синдромом
| Показатели | Здоровые | В12-дефицитная анемия | р | Железодефицитная анемия | р1 |
| Лейкоциты, 10 9 /л | 6,2±1,6 | 4,5±1,3 | 6,5±2,1 | 0,001 | |
| Эритроциты, 10 12 /л | 4,6±0,5 | 2,2±0,6 | 3,5±0,6 | ||
| Гемоглобин, г/л | 136±15,2 | 79,5±17,2 | 79,3±13,1 | >0,05 | |
| Гематокрит, % | 41,2±3,2 | 22,1±4,4 | 26,3±4,3 | ||
| Тромбоциты, 10 9 /л | 280±44,1 | 202,2±50,4 | 306,7±81,9 | ||
| Средний размер эритроцита, фл | 88,2±7,3 | 11,5±7,4 | 65,7±4,5 | ||
| Среднее содержание гемоглобина в эритроците, пг | 29,3±2,5 | 37,5±6,5 | 24,7±2,7 | ||
| Средняя концентрация гемоглобина в эритроците, г/дл | 35,1±1,7 | 38,7±1,2 | 29,5±1,3 | ||
| Цветной показатель | 0,91±0,1 | 1,2±0,2 | 0,7±0,1 | ||
| СОЭ, мм/ч | 8,3±4,2 | 21,7±16,5 | 22,5±16,9 | >0,05 |
Примечание: р — достоверность различий со здоровыми лицами; р1 — достоверность различий между группами.
Из данных табл. 1 следует, что в обеих группах у больных подтверждался анемический синдром, имеющий особенности в зависимости от характера заболевания.
Помимо общеклинического обследования, всем больным проводились фиброгастроскопия с прицельной биопсией и гистологическим изучением биоптатов слизистой желудка по визуально-аналоговой шкале Сиднейской модифицированной системы [1], исследование обсемененности слизистой оболочки желудка Helicobacter pylori (HP) и другими микроорганизмами в мазках-отпечатках, окрашенных по Граму, ставился уреазный тест.
Исследование кислотообразующей функции желудка проводили методом внутрижелудочной рН-метрии по В.Н. Чернобровому [15] с использованием аппарата ИАГМ-1 с помощью стандартных рН-зондов и титровочных растворов фирмы «Исток-система».
Результаты рН-метрии по протяженности желудка распределяли в соответствии с функциональными интервалами (ФИ рН) базальной рН-граммы желудка: рН 7,0-7,5 (анацидность — ФИ рН6), рН 3,6-6,9 (выраженная гипоацидность — ФИ рН5), рН 2,3-3,5 (гипоацидность — ФИ рН4), рН 1,6-2,2 (нормоацидность — ФИ рН3), рН 1,3-1,5 (гиперацидность — ФИ рН2), рН 0,9-1,2 (выраженная гиперацидность — ФИ pH1).
При анализе рН-метрии выделяли ФИ рН, на который приходится наибольшее количество точек замера рН по протяженности желудка, так называемый доминирующий функциональный интервал рН-ДФИ.
О пепсиногенобразующей функции желудка судили по содержанию пепсиногена (методика В.Н. Туголукова), а гастромукопротеидобразующей — фукомукопротеидов в сыворотке крови [10]. Забор крови поводили непосредственно перед проведением рН-метрии. Показатели выражали в единицах системы СИ.
Для статистической обработки данных применяли критерий Стьюдента, однофакторный дисперсионный анализ и критерий z (для процентных соотношений). В работе использовали пакет программ «Biostatics» и «Microsoft Office Excel XP».
Установлено, что у всех больных В12-дефицитной анемией при фиброгастроскопии и последующем гистологическом исследовании биоптатов слизистой оболочки желудка выявлен атрофический гастрит. Гастрит на фоне В12-дефицитной анемии характеризовался сочетанным поражением антрального и фундального отделов желудка, в то время как у пациентов на фоне железодефицитной анемии атрофия была менее выражена и в 70% случаев локализовалась только в антральном его отделе (рис. 1).
При микроскопическом исследовании биопатов слизистой оболочки желудка (по визуально-аналоговой шкале Сиднейской модифицированной системы) у больных хроническим гастритом на фоне железодефицитной анемии наблюдалась выраженная лимфоплазмоцитарная и слабая, реже умеренная, нейтрофильная инфильтрация собственной пластинки, слабая и умеренная атрофия желез, в единичных случаях (15%) — кишечная метаплазия. В мазках-отпечатках выявлялась очень низкая обсемененность слизистой оболочки микрофлорой с преимущественным выявлением единичных скоплений стрептококков, стафилококков, энтеробактерий. HP регистрировался в 25% случаев. Уреазный тест был положительным у 30% пациентов.
Хронический гастрит на фоне В12-дефицитной анемии гистологически отличался умеренной или выраженной атрофией, частым (44%) выявлением кишечной метаплазии, слабой, реже умеренной, как лимфоплазмоцитарной, так и нейтрофильной инфильтрацией. В мазках-отпечатках отмечалась низкая обсемененность слизистой оболочки микрофлорой с выявлением единичных скоплений стрептококков, стафилококков, энтеробактерий, лактобактерий, лептотрихий. HP регистрировался в 16% случаев. Уреазный тест был положительным у 24% пациентов. По данным других исследователей [1,16], HP при хроническом гастрите на фоне железодефицитной анемии встречается в 76,9% случаев, а на фоне B12-дефицитной — в 6,5% случаев.
Изучение кислотообразующей функции желудка по анализу результатов интрагастральной рН-метрии показало (рис. 2), что в обеих группах больных хроническим гастритом на фоне анемического синдрома, по сравнению со здоровыми лицами, доминирующие ФИ рН достоверно (р 0,05).
Таблица 2. Пепсиноген плазмы и фукомукопротеиды сыворотки крови у больных атрофическим гастритом на фоне В12— и железодефицитной анемии
| Показатели | Здоровые лица | анемия | р | Железодефицитная анемия | р | р1 |
| Пепсиноген плазмы, мг/л | 75,2±17 ,91 | 29,2±10,2 | 52,7±7,2 | |||
| Фукомукопротеиды сыворотки крови, мг/л | 150,2±32 | 68,0±18,1 | 102,1±22,7 |
Примечание: р — достоверность различий со здоровыми; р1 — между группами больных.
Суммируя изложенное, следует констатировать, что хронический гастрит на фоне В12-дефицитной анемии во всех случаях носил атрофический характер и в большинстве случаев одновременно поражал антральный и фундальный отделы желудка.
Заболевание протекало с существенным снижением кислото-, пепсиногено- и гастромукопротеидообразующей функции желудка, которое имело незначительные особенности в зависимости от этиологии В12-дефицитной анемии.
Только аутоиммунными механизмами трудно объяснить развитие выраженного атрофического процесса и глубокое снижение секреторной функции слизистой оболочки желудка при В12-дефицитной анемии, так как оно имело место и при алиментарном дефиците цианкобаламина и при патологии кишечника.
По-видимому, в развитии гастрического процесса на фоне В12-дефицитной анемии, помимо аутоиммунных механизмов, имеют значение действия различных эндогенных и экзогенных факторов, в том числе влияние гемической гипоксии, нарушения синтеза ДНК и клеточного обновления из-за дефицита цианкобаламина, изменения вегетативной регуляции при фуникулярном миелозе, а также расстройства системного гемостаза и микро-циркуляции. Это позволяет объяснить сходные морфофункциональные нарушения желудка при В12-дефицитной анемии различной этиологии.
Полученные данные указывают на необходимость дальнейшего детального исследования особенностей морфологических и функциональных изменений желудка при хроническом гастрите, протекающем на фоне анемии, в зависимости от ее характера, длительности и степени тяжести, а также с учетом нарушения гемостаза и микрогемоциркуляции.
1. Хронический атрофический гастрит на фоне В12-дефицитной анемии в 68% случаев характеризуется одновременным поражением антрального и фундального отделов желудка, а атрофические изменения на фоне железодефицитной анемии в 70% случаев происходят только в антральном его отделе. Степень выраженности атрофии больше при мегалобластной анемии.
2. Хронический гастрит на фоне В12-дефицитной анемии сопровождается существенным снижением кислото-, пепсиногено- и гастромукопротеиодообразования, более выраженным, чем при сочетании гастрического процесса с железодефицитной анемией.
3. Более выраженное снижение секреторной функции желудка у больных хроническим гастритом на фоне В12-дефицитной анемии, по сравнению с заболеванием, ассоциированным с железодефицитной анемией, может быть обусловлено большей степенью атрофического процесса в слизистой оболочке желудка и частым одновременным поражением его антрального и фундального отделов.
4. Полученные данные следует учитывать при ведении данного контингента больных, выборе лечебного питания и медикаментозной терапии.
1. Аруин Л.И. Морфологическая диагностика болезней желудка и кишечника / Л.И. Аруин, Л.Л. Капуллер, В.А. Исаков. — М.: Триада-Х, 1998. — 496 с.
2. Аруин Л.И. Иммуноморфология желудка / Л.И. Аруин, О.Л. Шаталова // Клин. мед. 1981. № 7. С. 8-14.
3. Григорьев П.Я. Клиническая гастроэнтерология / П.Я. Григорьев, А.В. Яковенко. — М.: МИА, 2001. — 704 с.
4. Демидова А.В. Вопросы диагностики и терапии B12-дефицитной анемии / А.В. Демидова, НА. Сысоева // Клин. мед. 1996. № 1. С. 59-60.
5. Долгов В.В. Лабораторная диагностика анемий / В.В. Долгов, СА. Луговская, В.Т. Морозова, М.Н. Почтарь. — Тверь: Губернская медицина, 2001. — 88 с.
6. Идельсон Л.И. Ошибки в диагностике В12— и фолиеводефицитной анемии / Л.И. Идельсон // Тер. арх. 1986. № 9. С. 144-150.
7. Kиpeeвa O.B. Аутоимунные процессы у больных хроническим гастритом / О.В. Киреева, A.M. Раскин, Б.Г. Лисочкин // Тер. архив. 1974. № 11. С. 104-107.
8. Логинов А.С. Хронический гастрит. Современные аспекты (обзор литературы) / А.С. Логинов, В.Ф. Алексеев, О.С. Радбиль. — М. 1987. — 56 с.
9. Островский А.Б. Иммунопатология хронического гастрита при В12-дефицитной анемии / А.Б. Островский // Тер. архив. 1984. № 10. С. 49-52.
10. Рабинович П.Д. Содержание некоторых Сахаров, связанных с биополимерами в секрете тканей желудка, сыворотке крови и моче при язвенной болезни. / П.Д. Рабинович, СИ. Вайстух, Н.М. Лошакова и др. // Вопр. мед. химии. 1972. № 6. С. 52-58.
11. Рысс Е.С. Анемии и желудочно-кишечный тракт / Е.С. Рысс — М.: Медицина, 1972. — 192 с.
12. Салупере В.П. Проблема хронического гастрита / В.П. Салупере. — Таллин: Валгус, 1978. — 143 с.
13. Циммерман Я.С. Хронический гастрит и язвенная болезнь (Очерки клинической гастроэнтерологии) / Я.С. Циммерман. — Пермь: Изд-во Перм. гос. мед. академии, 2000. — 256 с.
14. Циммерман Я.С. Анемии (вопросы этиологии, классификации, диагностики и дифференцированного лечения) / Я.С. Циммерман, Г.Д. Бабушкина. — Пермь: Изд-во Перм. гос. мед. академии, 2004. — 125 с.
15. Чернобровый В.Н. Экспресс-методика внутрижелудочной рН-метрии / В.Н. Чернобровый // Лаб. дело. 1990. № 3. С. 113-117.
16. Шамгунова Б.А. Клинико-морфологические особенности хронического геликобактерного гастрита у больных железодефицитной и смешанной (железо- и В12-дефицитной) анемией / БА. Шамгунова // Дисс. . канд. мед. наук. — Астрахань. 2001. С. 23.
17. Hamashinma V. Immunohistopathology / V. Hamashinma. — Stuttgart. 1976.
18. Strickland, R.G. / R.G. Strickland, J.R. Mackay // Am. J. Dig. Dis. 1973. Vol. 18. P. 426-440.
Морфологические особенности и секреторная функция желудка у больных хроническим гастритом на фоне В12-дефицитной анемии.
Тверская медицинская академия.
Эксперементальная и клиническая гастроэнтерология. 2006, № 4, с. 11-16.
источник
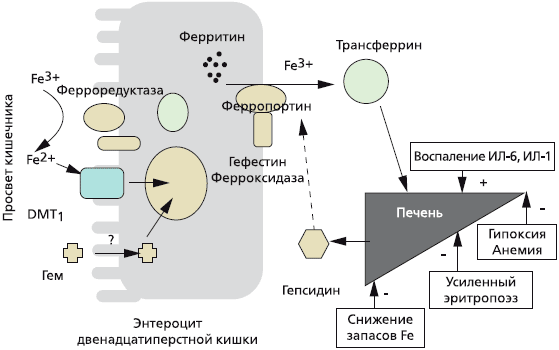
Железодефицитная анемия – наиболее частая форма анемий в гастроэнтерологии, и причиной ее развития являются кровотечения, нарушения всасывания железа, диетические ограничения. Ряд хронических заболеваний пищеварительной системы сопровождается развитием анемии различной степени тяжести. Анемия может являться первым признаком основного заболевания, в частности, опухолевого процесса пищевого канала, а также быть причиной снижения качества жизни пациентов.
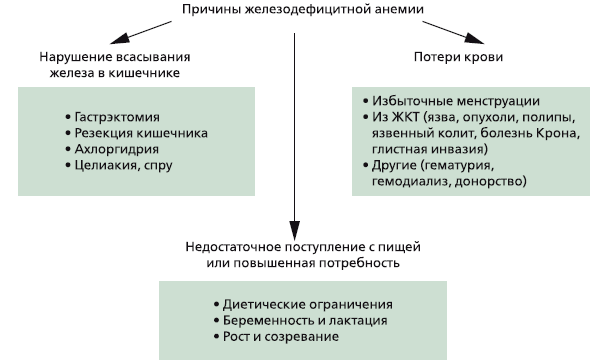
Выделяют три глобальные причины развития дефицита железа в организме:
- Недостаточное поступление с пищей или повышенная потребность.
- Нарушение всасывания железа в кишечнике.
- Хронические потери крови.
Заболевания желудочно-кишечного тракта являются одной из основных причин развития железодефицитной анемии, что обусловлено нарушением всасывания железа в кишечнике или его потерями вследствие эрозивно-язвенных, опухолевых или аутоиммунных воспалительных поражений слизистой оболочки кишечника.
Перечень заболеваний пищеварительного тракта, сопровождающихся развитием анемии, достаточно широк. Причиной железодефицитных состояний часто выступают болезни верхних отделов желудочно-кишечного тракта и толстой кишки.
Одной из важных причин развития железодефицитной анемии является нарушение процессов всасывания железа в двенадцатиперстной кишке и проксимальном отделе тощей кишки. Различные заболевания тонкой кишки, сопровождающиеся синдромом мальабсорбции (энтерит, амилоидоз, целиакея, идеопатическая стеаторея), а также оперативные вмешательства на желудке и тонкой кишке (состояние после тотальной гастроэктомии, субтотальной резекции желудка, ваготомии с гастроэктомией, резекция тонкой кишки) приводят к развитию дефицита железа.
Накапливаются данные о потенциальной связи инфекции H. pylory с железодефицитной анемией, которая может быть следствием скрытых кровотечений при эрозивном гастрите и язвенной болезни, нарушение всасывания железа при хеликобактерном атрофическом пангастрите, а также снижения содержания аскорбиновой кислоты в желудке и конкурентного захвата и утилизации железа самой бактерией. Таким образом, эрадикация H. pylory может стать еще одним подходом к лечению железодефицитной анемии в отсутствии других явных ее причин.
Этиологическим фактором анемии может стать прием нестероидных противовоспалительных препаратов (НПВП). Врачам хорошо известна возможность как массивных, так и скрытых кровотечений из эрозий и язв желудка и двенадцатиперстной кишки при НПВП-гастропатии. Однако, железодефицитная анемия может быть следствием НПВП-энтеропатии, другими клиническими проявлениями которой могут служить гипоальбуминемия, мальабсорбция и наличие измененной крови в кале.
Причиной нарушения всасывания гемопоэтических факторов являются и заболевания тонкой кишки. К ним можно отнести целиакию (половина пациентов с неясной этиологией железодефицитной анемии, резистентной к терапии препаратами железа), резекцию участка тонкой кишки, синдром избыточного бактериального роста в тонкой кишке, диабетическую энетропатию, амилоидоз, склеродермию, болезнь Уиппла, туберкулез, лимфому тонкой кишки, тропическое спру, паразитарные заболевания (лямблиоз) и гельминтозы (дифиллоботриоз).
Воспалительные заболевания кишечника, прежде всего, неспецифический язвенный колит и болезнь Крона, часто сопровождаются развитием анемии. Ведущими механизмами при этом выступают кровопотеря у пациентов с язвенным колитом и болезнью Крона, а также мальабсорбция при вовлечении в процесс тощей и подвздошной кишки при болезни Крона.
Ведущей причиной анемии при патологии нижних отделов желудочно-кишечного тракта, особенно у пациентов старше 50 лет, служит колоректальный рак. Хроническая кровопотеря наблюдается при полипах толстой кишки, дивертикулезе, ишемическом колите, геморрое и анальных трещинах.
Анемический синдром часто делает необходимым тщательное обследование желудочно-кишечного тракта. Для уточнения вида анемии проводят исследования общего и биохимического анализа крови.
Среди причин железодефицитной анемии (почти 30-50% всех случаев) прежде всего рассматривают острые или хронические кровопотери из желудочно-кишечного тракта.
Причины железодефицитной анемии
Как показали результаты открытого мультицентрового исследования, проведенного в Украине в 2008 году и базировавшиеся на анализе 1299 историй болезней больных железодефицитной анемией, основной причиной развития были эрозивно-язвенные поражения пищевого канала (44,58%) и заболевания, сопровождающиеся синдромом мальабсорбции. Циррозы печени являлись причиной железодефицитной анемии в 10,39% случаев, воспалительные заболевания кишечника – 4,54% больных.
Диагностируется железодефицитная анемия у больных с гастроэнтерологическими заболеваниями по совокупности анамнестических данных (указания на оперативные вмешательства на желудке или кишечнике, прием нестероидных или гормональных противовоспалительных препаратов, антикоагулянтов и антиагрегантов, язвенный анамнез, наличие хронических заболеваний печени и воспалительных заболеваний кишечника и т.д.), клинических проявлений (наличие специфического сидеропенического синдрома, проявляющегося сухостью и истончением кожи, ангулярный хейлит, дисфагия, ломкость ногтей, их поперечная исчерченность, вогнутость ногтевой пластинки, извращение вкуса и обоняния, симптом «голубых склер», мышечная слабость) и лабораторных показателей.
Диагностика анемии основывается, главным образом, на данных лабораторных исследований, в первую очередь – на результатах клинического исследования крови с определением концентрации гемоглобина.
| Параметры | Значения при ЖДА | Норма | |
| Железо сыворотки, мкг/дл | 3 | 5 | Примечание. НПВС — нестероидные противовоспалительные средства. Среди причин ЖДА (почти 30-50 % всех случаев) прежде всего рассматривают острые или хронические кровопотери из ЖКТ. Основной причиной ЖДА у женщин до менопаузы являются беременность и менструации, у женщин после менопаузы и у мужчин — хронические (латентные) потери крови из ЖКТ. Анализ кала на скрытую кровь — основной скрининговый метод выявления скрытого желудочно-кишечного кровотечения (тест положительный при выделении не менее 10 мл крови в сутки). При потере не менее 30 мл крови в сутки тест на скрытую кровь бывает положительным в 93 % случаев [8]. Наиболее часто при хронической ЖДА и особенно в случаях положительного результата кала на скрытую кровь выполняют эзофагогастродуодено- (ЭФГДС) и колоноскопию. В 5-10 % случаев анемий, связанных с заболеваниями ЖКТ, при ЭФГДС и колоноскопии не удается выявить очага поражения [9]. В 25 % случаев это обусловлено небольшим размером пораженного участка, который обнаруживается при повторном осмотре, в остальных случаях необходимо обследование тонкой кишки. В последние годы наиболее часто для выявления источника кровотечения из тонкой кишки используется беспроводная капсульная эндоскопия. В 10-17 % случаев причиной ЖДА у мужчин и женщин старше 40 лет являются онкологические заболевания ЖКТ; прежде всего колоректальный рак. ЖДА в течение длительного времени может быть единственным проявлением рака толстой кишки правосторонней локализации, при этом размер опухоли обычно превышает 3 см. Другая наиболее частая причина ЖДА -язвенная болезнь желудка и двенадцатиперстной кишки. При скрытых кровопотерях, обусловленных поражением тонкой кишки, наиболее часто в возрасте до 40 лет выявляют опухоли (лимфому, карциноид, аденокарциному, полипоз), ангиоэктазию артерий (Dieulafoy’s поражение), целиакию и болезнь Крона, в возрасте старше 40 лет -патологию сосудов различной природы и прием НПВС. У трети больных воспалительными заболеваниями кишечника (болезнь Крона, язвенный колит) выявляется анемия, имеющая сложный генез (сочетание ЖДА и анемии хронических заболеваний). При этом дефицит железа становится следствием нескольких причин: Лечение Суточная терапевтическая доза элементарного железа при лечении ЖДА для взрослых составляет в среднем 100— 200 мг в 2—3 приема. Поливитаминные комплексы, содержащие железо, не рекомендуют в качестве лечения ЖДА, т. к. они содержат недостаточное количество железа либо оно плохо всасывается в кишечнике. При адекватном лечении уже в течение первых 3 суток наблюдается увеличение числа ретикулоцитов в крови, на 7—10-й день отмечается ретикулоцитарный криз (пик ретикулоцитоза). К 3—4-й неделе лечения имеет место увеличение уровня гемоглобина на 20 г/л. Прием препаратов железа необходимо продолжать еще в течение 3—6 месяцев после нормализации уровня гемоглобина — пока насыщение трансферрина железом не превысит 30 % и концентрация ферритина не достигнет 50 нг/мл (показатель восстановления тканевых запасов железа). Среди 20—30 % пациентов в результате приема препаратов железа отмечаются различные диспептические расстройства (тошнота, дискомфорт в эпигастрии, диарея или запор). Риск развития желудочно-кишечных расстройств можно снизить, принимая препарат во время еды или на ночь, а также при постепенном увеличении дозы. Среди причин неэффективности пероральных форм железа рассматривают целый ряд факторов [10]: недостаточное поступление железа; Нарушение всасывания железа: Продолжающиеся потери крови или повышенная потребность в железе: Сопутствующие заболевания или состояния: Неправильный диагноз или наличие других причин анемии: Выделяют следующие показания к парентеральному введению, преимущественно внутривенному, препаратов железа: Основная опасность при парентеральном введении железа — развитие тяжелых аллергических реакций, включая анафилактических шок с летальным исходом, которые наблюдаются в 0,6—1,0 % случаев. Данные реакции, в основном, характерны для препаратов железа, содержащих декстран. Среди парентеральных препаратов железа широкое распространение, особенно в комплексной терапии воспалительных заболеваний кишечника, получили сахарат железа и железа карбоксимальтозат (Феринжект), которые в отличие от декстрана железа ассоциируются с минимальным риском развития анафилактических и других аллергических реакций [11—13]. Так, в 2011 г. были опубликованы результаты рандомизированного контролируемого исследования применения железа карбоксимальтозата пациентами с железодефицитной анемией, обусловленной воспалительными заболеваниями кишечника (FERGIcor — a Randomized Controlled Trial on Ferric Carboxymaltose for Iron Deficiency Anemia in Inflammatory Bowel Disease) [14]. В исследовании сравнивали эффективность и безопасность нового режима фиксированной дозы железа карбоксимальтозата (Феринжекта) и индивидуально рассчитываемых доз сахарата железа (СЖ) для пациентов с воспалительными заболеваниями кишечника и ЖДА. В исследование были включены 485 пациентов с ЖДА (уровень ферритина ЛИТЕРАТУРА источник |