Вынесенное в заголовок определение включает в себя большую группу заболеваний, которые отличаются друг от друга по причинам возникновения, механизмам развития болезни в организме, внешним проявлениям и схемам лечения. Основным и единым для них признаком является ускоренный распад и сокращение продолжительности жизни эритроцитов.
Если в нормальных условиях существования продолжительность жизни эритроцитов составляет, как правило, 100—120 дней, то при наличии гемолитической анемии они усиленно разрушаются и срок их жизни сокращается до 12—14 дней.
Буквальное разрушение эритроцитов (определяется как патологический гемолиз) происходит преимущественно внутри сосудов. Внутри клеток распад эритроцитов возможен только в селезенке. Процесс внутриклеточного разрушения сразу заявляет о себе повышением в сыворотке крови свободного билирубина и увеличением выделения уробилина с экскрементами. В дальнейшем это может сказаться камнями в желчных протоках и желчном пузыре.
Согласно превалирующей в настоящее время классификации гемолитические анемии разделяют на две группы:
Различаются две группы тем, что наследственные анемии люди получают вследствие действия дефектных генетических факторов на жизнь эритроцитов, а приобретенные развиваются под действием внешних причин, способных разрушить изначально здоровые эритроциты.
Назван так в честь исследователей, впервые его описавших еще в 1900 году. Причина болезни – в генетическом дефекте мембранного белка эритроцита. Неполноценная мембрана пропускает внутрь эритроцита чрезмерное количество ионов натрия и способствует накоплению в нем воды. В результате образуются сфероциты. Сфероциты, или сферические эритроциты, не в состоянии протискиваться в узких просветах кровотока, например, при проходе в синусы селезенки, что ведет к застою движения эритроцитов, от которых отщепляются частички их поверхности, а из них в свою очередь образуются микросфероциты. Кстати, отсюда и название болезни – микросфероцитоз. Разрушенные эритроциты утилизируются макрофагами селезенки.
Процесс постоянного гемолиза эритроцитов в селезенке вынуждает ее разрастаться, наращивать пульпу, чтобы справиться с ситуацией. Поэтому орган со временем ощутимо увеличивается в размерах, обычно выступая из-под подреберья на 2—3 см. Распад эритроцитов в сыворотке способствует росту свободного билирубина в крови, откуда он поступает в кишечник и выводится из организма естественными путями в виде стеркобилина, суточное количество которого при данной болезни двадцатикратно превышает норму.
Внешние проявления заболевания зависят от выраженности процесса разрушения эритроцитов. Чаще всего первые симптомы болезни выявляются в юношеском возрасте, а у детей она обычно обнаруживается при обследовании по поводу заболевания их родственников.
Вне обострения процесса жалобы могут отсутствовать, по мере усугубления ситуации у больного появляются жалобы на слабость, головокружение, повышение температуры. Для врача основным клиническим симптомом служит желтуха, которая длительное время может оставаться единственным внешним проявлением заболевания. Интенсивность желтухи зависит от двух факторов: от скорости гемолиза и от способности печени перерабатывать непрестанно поступающий свободный билирубин. Поэтому чем здоровее изначально печень, тем менее выражена желтуха.
При лабораторном исследовании мочи свободный билирубин в ней не находят. Кал интенсивного темно-коричневого цвета. Характерная для болезни склонность к камнеобразованию может спровоцировать приступ печеночной колики. При механической закупорке общего желчного протока развивается картина обтурационной желтухи: кожный зуд, желчные пигменты в моче и пр.
Печень при спокойном течении заболевания без осложнений, как правило, нормальных размеров, лишь изредка у больных, долгое время страдающих гемолитической анемией, отмечается ее увеличение. У детей наблюдаются симптомы замедленного развития. Также отмечаются изменения лицевого скелета по типу башенного черепа, формирование седловидного носа, узких глазниц, высокого стояния неба и нарушения прикуса зубов.
У каждого больного степень выраженности болезни различна. Если у некоторых больных чаще отмечается незначительное уменьшение количества гемоглобина, то у других больных малокровие вообще отсутствует. В пожилом возрасте порой встречаются трудно поддающиеся лечению трофические язвы голени, что связано с гемолизом эритроцитов в мелких капиллярах нижних конечностей.
Заболевание протекает с характерными гемолитическими кризами, которые выражаются в резком усилении обычных симптомов. По мере роста жалоб повышается температура тела больного, вызванная усиленным распадом эритроцитов, нарастает интенсивность желтухи, присоединяются сильные боли в животе и рвота. Гемолитические кризы обычно бывают спровоцированы сторонней инфекцией, переохлаждением, а у женщин развиваются в связи с беременностью. Частота кризов строго индивидуальна, у некоторых они вообще отсутствуют.
Для врача диагноз наследственного микросфероцитоза ясен при наличии у обследуемого пациента чередования кризов и ремиссий, желтухи, увеличенной в размерах селезенки (спленомегалия), болей в правом подреберье, признаков малокровия, подтвержденных показателями лабораторного исследования крови (нормохромная анемия, ретикулоцитоз, микросфероцитоз). Дополнительным подтверждением правильности диагноза может служить ряд лабораторных тестов. Например, установлению верного диагноза помогает проба Кумбса, с помощью которой выявляют зафиксированные на эритроцитах аутоантитела при гемолитических аутоиммунных анемиях.
Важное социальное значение несет целенаправленное обследование специалистом близких родственников заболевших. При этом у некоторых из них могут быть выявлены едва уловимые признаки разрушения эритроцитов, определяемые врачом как микросфероцитоз без выраженных клинических проявлений. Вероятность развития заболевания у детей, если один из родителей болен микросфероцитозом, чуть менее 50%.
К сожалению, единственным эффективным способом лечения больных наследственным микросфероцитозом является хирургическое удаление селезенки – спленэктомия. Удаление дает практически полное излечение, несмотря на то что эритроциты сохраняют свои болезнетворные свойства – микросфероцитоз и снижение осмотической резистентности.
Но операция возможна не у всех больных. Ее проводят только при наличии частых гемолитических кризов, инфарктах селезенки, прогрессирующем развитии анемии, частых приступах печеночной колики. По возможности вместе с селезенкой хирурги стараются удалить желчный пузырь. Прогноз жизни при наследственном микросфероцитозе благоприятен: большинство больных доживают до старости.
В понятие талассемии объединена целая группа гемолитических анемий, передаваемых по наследству. Общей для них чертой является отчетливая гипохромия красных кровяных телец (эритроцитов), диагностируемая на фоне нормального или даже повышенного содержания ионов железа в кровяной сыворотке. Вместе с тем довольно часто у больных отмечается повышенный билирубин в крови и умеренный ретикулоцитоз. Селезенка, как правило, увеличена и легко прощупывается. Клинические проявления у конкретного больного напрямую зависят от того, каким образом произошло наследование болезни: от одного из родителей или от обоих. На общую картину болезни влияет и тип нарушения одной из четырех цепочек гемоглобина.
Причины ускоренного гемолиза эритроцитов вызваны измененной структурой клетки, что происходит в результате патологического изменения соотношения цепей глобина внутри самой клетки. При талассемии, кроме укорочения жизни эритроцитов, гибнут клетки костного мозга – эритрокариоциты, ответственные за эффективное кровообразование. Эритропоэз становится неэффективным.
Внешние и внутренние проявления талассемии, передаваемой от обоих родителей, складываются в клиническую картину тяжелой гипохромной анемии с резко выраженным анизоцитозом эритроцитов и наличием в крови так называемых мишеневидных форм эритроцитов. «Мишени» образуются тогда, когда на месте нормального просветления в центре эритроцита формируется пятно гемоглобина, напоминающее мишень. Болезненные изменения, происходящие в организме, виновны в формировании у больного башенного черепа и седловидного носа, в изменении расположения зубов и неправильном прикусе. Раннее малокровие сказывается на умственном и физическом развитии ребенка, его кожные покровы обычно желтушного оттенка, увеличена селезенка. К сожалению, при тяжелом течении анемии дети умирают, не дожив до года. Но встречаются и менее тяжелые формы гомозиготной талассемии, дающие больным детям возможность при правильном и своевременном лечении дожить до зрелого возраста.
Талассемия, передающаяся от одного родителя, или гетерозиготная, способна протекать с менее выраженными ухудшениями показателей крови. Гипохромное малокровие может быть умеренным, ретикулоцитоз – незначительным, а признаки ускоренного гемолиза эритроцитов – отсутствовать; желтуха лишь слегка выражена, а селезенка мало увеличена в размерах.
Диагностическим признаком талассемии служат нормальные или повышенные цифры содержания железа в сыворотке крови. Другая важная для диагностики проба заключается в том, что при железодефицитном малокровии прием железосодержащих лекарств неизбежно приводит к росту количества ретикулоцитов в крови уже к середине второй недели терапии, а при талассемии, какое бы количество железа ни употреблял больной, уровень ретикулоцитов остается неизменным.
Конкретная форма талассемии определяется только при специальном исследовании всех четырех цепочек гемоглобина.
Лечение тяжелого гомозиготного малокровия заключается в попытках переливанием эритроцитов скорректировать картину крови. Нужное количество крови для переливания рассчитывают так, чтобы удержать уровень гемоглобина на 85 г/л. Переизбыток железа из организма выводится.
Лечебное воздействие способна оказать пересадка (трансплантация) костного мозга. Спленэктомия – хирургическое удаление селезенки, показана исключительно при тяжелых формах гемолиза и катастрофическом увеличении органа. Но врачи к ней прибегают редко, стараясь в полной мере использовать бескровные методы терапии.
Профилактика: табу на инцест.
В общей основе возникновения патологии лежит дефицит активности некоторых ферментов эритроцитов, в результате чего они (эритроциты) становятся болезненно чувствительными к воздействию различных веществ растительного происхождения, в том числе и лекарственных препаратов. Самой распространенной из несфероцитарных гемолитических анемий является острая гемолитическая анемия, обусловленная дефицитом специфического фермента со сложным обозначением Г-6-ФДГ. У детей с его недостаточностью может проявиться фавизм.
Фавизм – это острая гемолитическая анемия, отличающаяся бурным течением. Развивается у детей с дефицитом указанного фермента при употреблении в пищу конских бобов или вдыхании пыльцы растения Vicia Fava. Впервые заболевание было описано более полувека назад, тогда и было указано на его семейный характер.
Фавизм возникает у детей преимущественно дошкольного возраста, чаще у мальчиков. Развивается обычно бурно. После вдыхания пыльцы цветов растения Vicia Fava симптомы болезни появляются уже через несколько минут, а после употребления в пищу конских бобов – в течение 5—24 часов. Возникают озноб, высокая температура, тошнота, рвота, головная боль, возможны помрачение сознания и состояние, близкое к коллапсу. Постепенно нарастает желтуха, увеличиваются печень, селезенка. У многих больных развивается гемоглобинурия. Количество эритроцитов в течение нескольких суток снижается до 1 ґ 1012 клеток/л. Иногда определяют высокий нейтрофильный лейкоцитоз. Уровень непрямого билирубина повышен. Осмотическая резистентность эритроцитов нормальная или снижена. Реакция Кумбса, как прямая, так и непрямая, бывает положительной у большинства больных в течение первой недели заболевания. Острый период обычно продолжается от двух до шести дней, несколько дольше длится желтуха. После восстановления состава периферической крови развивается иммунитет, который сохраняется 6 недель. Прогноз для жизни медики в основном дают благоприятный.
Гемолитический криз могут вызвать самые разные причины. Например, прием даже обычных анальгетиков, сульфаниламидных и противомалярийных препаратов, витамина K, некоторых химиотерапевтических препаратов, таких как ПАСК или фурадонин. Употребление в пищу бобовых и стручковых растительных продуктов питания также может завершиться гемолитическим кризом. Тяжесть грянувшего гемолитического процесса напрямую зависит от количества фермента Г-6-ФДГ и от дозы препарата или количества продукта, спровоцировавшего криз. Особенностью реакции является то, что гемолиз эритроцитов наступает не сразу, а растянут по времени, обычно на два-три дня с момента приема препаратов-провокаторов.
В тяжелых случаях у больных повышается до верхних пределов температура тела, наступает резкая слабость, выраженная одышка, сердцебиение, появляются боли в животе и спине, сопровождающиеся обильной рвотой. Состояние больного быстро ухудшается вплоть до коллаптоидного состояния. Типичным признаком приближающегося коллапса служит появление мочи темного, вплоть до черного, цвета. Такое окрашивание мочи диктуется выведением из организма гемосидерина, образующегося в результате внутрисосудистого распада эритроцитов, который, неустанно прогрессируя, способен вылиться в приступ острой почечной недостаточности. Одновременно проявляется желтушность кожных покровов и видимых слизистых оболочек, прощупывается увеличенная селезенка, реже можно прощупать нижний край печени в правом подреберье. Как правило, спустя неделю распад эритроцитов прекращается. Гемолиз прекращается независимо от того, продолжается ли прием препарата, вызвавшего приступ, или нет.
Диагноз острой гемолитической анемии, связанной с дефицитом Г-6-ФДГ, достаточно прост для квалифицированного врача: четкая типичная клиническая картина в сочетании с лабораторными показателями острого гемолиза и дефицита в крови названного фермента при явной связи приступа с приемом лекарств однозначно говорит об этой форме гемолитической анемии. Лишним подтверждением служит выявленная нехватка фермента в эритроцитах крови у близких родственников.
Основным методом лечения данной разновидности малокровия служат вполне очевидные манипуляции: многократные, один или два раза в неделю, трансфузии в количестве до полулитра свежей крови одной группы и внутривенные вливания больших количеств 5%-ного раствора глюкозы или физиологического раствора. Для снятия и предупреждения развития шока используют преднизолон, промедол или морфин. Подчас требуется применение кордиамина и камфоры. В случае если течение болезни усугубляется острой почечной недостаточностью, проводят обычный комплекс терапевтических процедур. При отсутствии эффекта неизбежно проведение искусственного гемодиализа.
Чтобы предупредить гемолитические кризы, следует скрупулезно собрать сведения у больного. Это необходимо сделать до введения лекарственных препаратов, способных спровоцировать ухудшение. Со стороны сбор анамнеза напоминает исповедь – врач спрашивает, а больной чистосердечно отвечает, помогая тем самым себе и своему лечащему врачу. Это очень ответственное мероприятие.
Прогноз для жизни и здоровья больного при данной форме анемии неутешителен в том случае, если развивается почечная недостаточность и анурия. Смерть может наступить при молниеносном течении заболевания от острой аноксии или шока.
Среди группы приобретенных гемолитических анемий чаще других встречается аутоиммунная гемолитическая анемия. В медицинской литературе начало развития этой болезни обычно связывают с появлением в организме антител к собственным эритроцитам. Организм ополчается на свои же эритроциты и «бьет» их как чужих из-за поломки системы опознавания «свой – чужой»: иммунная система воспринимает эритроцитарный антиген как чужеродный и начинает вырабатывать к нему антитела. После фиксации аутоантител на эритроцитах последние захватываются клетками ретикулогистиоцитарной системы, где подвергаются агглютинации и распаду. Гемолиз эритроцитов происходит главным образом в селезенке, печени, костном мозге.
Различают симптоматические и идиопатические гемолитические аутоиммунные анемии. Симптоматические аутоиммунные анемии сопровождают различные заболевания, связанные с нарушениями в иммунной системе человека. Наиболее часто они встречаются при хроническом лимфолейкозе, лимфогранулематозе, остром лейкозе, при циррозе, хронических гепатитах, ревматоидном артрите, при системной красной волчанке.
В тех же случаях, когда врачам не удается увязать образование аутоантител с тем или иным патологическим процессом, принято говорить об идиопатической аутоиммунной гемолитической анемии. Подобный диагноз выносится врачами примерно в половине случаев.
Аутоантитела к эритроцитам принадлежат к различным типам. По серологическому принципу аутоиммунные гемолитические анемии делятся на несколько форм:
• анемии с неполными тепловыми агглютининами;
• анемии с тепловыми гемолизинами;
• анемии с полными холодовыми агглютининами;
• анемии с двухфазными гемолизинами;
• анемии с агглютининами против нормобластов костного мозга.
Каждая из этих форм имеет свои особенности в клинической картине и диагностике. Наиболее часто встречаются анемии с неполными тепловыми агглютининами, составляющие до 4/5 всех случаев аутоиммунных гемолитических анемий. По клиническому течению выделяют острую и хроническую формы данного заболевания.
Острую форму отличает внезапное начало: наваливается резкая слабость, кожные покровы быстро желтеют, больного бьет лихорадка, донимают одышка и приступы сердцебиения.
При хроническом течении заболевания приступ развивается неспешно, подкрадывается исподволь. При этом общее состояние больных мало изменяется, несмотря на выраженную анемичность больного. Такие симптомы, как одышка и сердцебиение, могут вообще отсутствовать. Секрет тут в том, что при неспешном развитии болезни организм больного постепенно адаптируется к состоянию хронической гипоксии. При желании можно прощупать у больного край увеличенной селезенки, немного реже – печени.
При аутоиммунной анемии, связанной с холодовой аллергией, которая характеризуется плохой переносимостью минусовых температур с развитием симптомов крапивницы, синдрома Рейно и гемоглобинурии, течение заболевания отличается склонностью к обострениям или гемолитическим кризам. Ухудшение провоцируют вирусные инфекции вкупе с переохлаждением. При лабораторных исследованиях крови выявляется нормохромная или умеренно гиперхромная анемия различной степени, ретикулоцитоз, нормоцитоз. Для холодовой аутоиммунной гемолитической анемии характерна реакция агглютинации (склеивания) эритроцитов сразу после взятия крови и непосредственно в мазке, которая исчезает при согревании. СОЭ сильно увеличена. Число тромбоцитов неизменно. Также фиксируется увеличение количества непрямого билирубина. В кале повышен уровень стеркобилина.
Диагноз аутоиммунной гемолитической анемии возможен при сочетании двух признаков: наличия симптомов повышенного гемолиза и обнаружения фиксированных на поверхности эритроцитов антител. Аутоантитела на эритроцитах выявляют с помощью уже упоминавшейся пробы Кумбса. Различают прямую и непрямую пробы Кумбса. Прямая проба выпадает положительной в большинстве случаев аутоиммунной гемолитической анемии. Отрицательный результат прямой пробы означает отсутствие антител на поверхности эритроцита и не исключает наличия свободных циркулирующих антител в плазме. Для выявления свободных антител применяют непрямую пробу Кумбса.
Аутоиммунные гемолитические анемии хорошо поддаются лечению глюкокортикоидными гормонами, которые способны прекратить распад эритроцитов в большинстве случаев болезни. После наступления ремиссии доза гормонов постепенно уменьшается. Поддерживающая доза составляет 5—10 мг/сут. Лечение проводится на протяжении двух-трех месяцев, до исчезновения всех клинических признаков гемолиза и отрицательных результатов пробы Кумбса. У некоторых больных эффект оказывают иммунодепрессанты (6-меркаптопурин, азатиоприн, хлорамбуцил), а также противомалярийные препараты (делагил, резохин). При рецидивирующих формах заболевания и отсутствии эффекта от применения глюкокортикоидов и иммунодепрессантов показана опять же спленэктомия – удаление селезенки. Гемотрансфузии у больных аутоиммунной гемолитической анемией следует проводить только по жизненным показаниям (резкое падение гемоглобина, потеря сознания).
источник
Гемолитические анемии связаны с усиленным разрушением эритроцитов. Все гемолитические состояния характеризуются увеличением в крови содержания продуктов распада эритроцитов — билирубина или свободного гемоглобина или появлением гемосидерина в моче. Важный признак — значительное нарастание в крови процента «новорожденных» эритроцитов — ретикупоцитов за счет повышения продукции клеток красной крови. Костный мозг при гемолитических анемиях характеризуется значительным увеличением числа клеток красного ряда.
Наследственный микросфероцитоз. Этиология, патогенез. Болезнь наследуется по доминантному типу. В основе гемолиза лежит дефект структуры мембраны эритроцитов, что вызывает ее повышенную проницаемость и способствует проникновению внутрь эритроцитов избытка натрия и накоплению воды. Эритроциты приобретают сферическую форму, повреждаясь при прохождении через узкие пространства синусов селезенки. Поврежденные клетки захватываются макрофагами (внутриклеточный гемолиз); превращение в них гемоглобина в билирубин ведет к непрямой гипербилирубинемии, желтухе.
Клиническая картина. Желтуха, увеличение селезенки, анемию, склонность к образованию камней в желчном пузыре, характерные морфологические изменения эритроцитов, ретикупоцитоз. Весьма редкий и неспецифический признак болезни — образование трофических язв на голенях. Отмечаются деформация челюстей с неправильным расположением зубов, высокое небо, выступающий лоб, легкая микрофтапьмия. Селезенка пальпируется всегда.
Картина крови: микросфероцитоз эритроцитов, высокий ретикупоцитоз, обычно исчисляемый десятками процентов, нор-мохромная анемия разной выраженности, иногда число эритроцитов и гемоглобин нормальные. В период гемолитического криза возможен нейтрофильный лейкоцитоз. Очень резко возникают так называемые арегенераторные кризы, когда повышенный гемолиз в течение нескольких дней не сопровождается эритропоэзом; ретикулоциты исчезают из крови, быстро нарастает анемия, уровень билирубина падает. Сфероцитозу эритроцитов соответствует их пониженная осмотическая стойкость. Средний диаметр эритроцитов уменьшается, соответственно увеличивается их толщина, в связи с чем в большинстве клеток не видно центрального просветления, так как эритроцит из двояковогнутого превращается в шаровидный.
Лечение. Радикальный метод — спленэктомия.
Талассемии — группа наследственных гемолитических анемий, характеризующихся выраженной гипохромией эритроцитов при нормальном или повышенном уровне железа в сыворотке крови. Часто повышено содержание билирубина в крови, отмечаются умеренный ретикулоцитоз, увеличение селезенки. Патогенез повышенной гибели эритроцитов связан с нарушенной структурой клетки из-за неправильного соотношения цепей глобина в ней. Кроме укорочения жизни эритроцитов при талассемии происходит гибель эритрокариоцитов костного мозга — так называемый неэффективный эритропоэз.
Клиническая картина гомозиготной талассемии характеризуется тяжелой гипохромной анемией, резко выраженным анизоцитозом эритроцитов, наличием мишеневидных форм (вместо нормального просветления в центре определяется пятно гемоглобина, напоминающее мишень). Гетерозиготная талассемия может протекать с умеренной гипохромной анемией, небольшим ретикулоцитозом, легкой желтушностью, незначительным увеличением селезенки.
Картина крови при талассемиях характеризуется описанной выше морфологией эритроцитов, низким цветовым показателем. Число эритроцитов нормальное или слегка увеличенное, лейкограмма, число тромбоцитов не меняются. Диагностический признак — нормальные или повышенные цифры сывороточного железа.
Серповидно-клеточная анемия. В большой группе заболеваний, обусловленных нарушениями аминокислотного состава глобина,— гемоглобинопатий наиболее распространенной является серповидно-клеточная анемия. Болезнь встречается в двух формах: гомозиготной (тяжелой) и гетерозиготной; последняя осложняется анемическим кризом лишь в особых условиях кислородного голодания.
Клиническая картина гомозиготной формы складывается из ранней тяжелой гемолитической анемии, имеющей нормохромный или гиперхромный характер. Физическая и некоторая умственная отсталость, связанная с рано развившимся и глубоким анемическим синдромом, сопровождается нарушениями скелета; дети худые с удлиненными конечностями, череп своеобразно деформированный, высокий, суженный, имеет часто утолщенный шов лобных частей в виде гребня. Характерны тромботические осложнения. Гемолитический криз обычно протекает с высокой температурой, выраженным нейтрофильным лейкоцитозом с омоложением формулы, тромбоцитозом. Массивный внутрисссудистый гемолиз при кризе сопровождается выделением темной мочи, в которой определяется гемосидерин. Нередко встречаются язвы голеней. В начале болезни часто увеличена селезенка, в дальнейшем из-за повторных инфарктов она сморщивается и перестает пальпироваться. Печень увеличена.
Картина крови: нормохромная анемия, выраженный анизоцитоз эритроцитов, присутствие своеобразных форм, напоминающих полудиск, небольшое число мишеневидных эритроцитов. Настоящие серповидные эритроциты выявляются лишь при специальной пробе с метабисульфитом натрия, который, действуя как восстановитель, вызывает недостаток кислорода в эритроцитах, что ведет к кристаллизации гемоглобина в них и появлению серповидных форм. Снятие покровного стекла с препарата — доступ кислорода — ведет к восстановлению нормальной формы эритроцитов.
Клинические проявления гетерозиготной формы наблюдаются лишь при гемолитических кризах, спровоцированных аноксическими состояниями (полет в самолете без герметизации кабины, тяжелая пневмония, наркоз и т. п.). Криз сопровождается множественными тромботическими осложнениями. В крови анемия, нейтрофильный лейкоцитоз, тромбоцитоз. Эритроциты претерпевают те же изменения, что и при гомозиготной форме, та же проба выявляет серповидность.
Лечение. В период гемолитического криза — госпитализация больного и согревание, так как при низкой температуре признаки серповидное выражены больше. Внутрь назначают ацетилсалициловую кислоту (в качестве дезагреганта и фактора, меняющего сродство гемоглобина к кислороду) в дозе 0,5 г 3 раза в день. При тяжелой анемии переливают эритроцитную массу.
Кроме серповидно-клеточной гемоглобинопатий, встречаются и другие аномалии гемоглобина, обычно дающие гемолитический синдром лишь в гомозиготном состоянии: отмечаются небольшая желтуха, увеличение селезенки, анизоцитоз и иноща мишеневидность эритроцитов, ретикулоцитоз. Аутоиммунные гемолитические анемии. В основе патологического процесса лежит срыв иммунолитической нечувствительности к собственному антигену.
Клиническая картина болезни складывается из признаков анемического синдрома; тяжесть состояния больных определяется выраженностью и остротой развития анемии. При хроническом, медленно развивающемся процессе первым признаком болезни может быть небольшая желтуха (за счет непрямого билирубина); одновременно выявляется и анемия. В других случаях начало болезни характеризуется бурным гемолизом с быстро нарастающей анемией и желтухой. Нередко повышается температура тела. Часто увеличивается селезенка. Возможно увеличение печени за счет холелитиаза, жировой дистрофии.
Картина крови характеризуется нормохромной анемией (при остром гемолизе уровень гемоглобина может падать до катастрофических цифр, больной может впадать в анемическую кому). Морфология эритроцитов существенно не меняется. При остром гемолизе в крови могут определяться единичные эритрокариоциты. Уровень ретикулоцитов высок. Белая кровь существенно не меняется. Однако встречается аутоиммунный цитолиз, касающийся двух ростков — тромбоцитарного и эритроцитарного (синдром Ивенса — Фишера). В этом случае клинически определяются признаки гемолитической анемии и тромбоцито-пенической пурпуры. Костный мозг при аутоиммунной гемолитической анемии характеризуется раздражением красного ростка (при сочетании гемолиза с тромбоцитопенией в костном мозге отмечается высокий мегакариоцитоз), но нередко можно встретить высокий процент ретикулярных клеток — своеобразных элементов с грубоструктурным ядром с нуклеолой и широкой цитоплазмой, содержащей скудную азурофильную зернистость. Биохимические исследования обнаруживают, помимо гипербилирубинемии, увеличение содержания гамма-глобулинов, которые в отдельных случаях могут иметь моноклоновый характер.
Лечение. Начинают терапию обычно с назначения 60 мг преднизолона (для взрослых) в день. При тяжелом гемолитическом процессе с бурно прогрессирующей анемией дозу преднизолона быстро увеличивают до 100—200 мг в день. Неэффективность стероидной терапии, выявляемая по нарастанию анемии, процента ретикулоцитов, может потребовать проведения спленэктомии уже в самом начале болезни.
Дата добавления: 2015-02-19 ; просмотров: 414 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
источник
- Наследственная форма гемолитической анемии, обусловленная нарушением мембраны эритроцитов
- Наследственная форма гемолитической анемии, обусловленная нарушением активности ферментов эритроцитов
- Наследственная форма гемолитической анемии, обусловленная нарушением синтеза или структуры гемоглобина
- Анемия, обусловленная влиянием антител
- Анемия, обусловленная изменением структуры мембраны, вызванной соматической мутацией
- Анемия, обусловленная механическим повреждением оболочки эритроцитов
- Анемия, вызванная химическим повреждением эритроцитов
- Анемия, вызванная дефицитом витаминов (фолиевой кислоты и цианокобаламина)
- Анемия, вызванная разрушением эритроцитов паразитами
Болезнь Минковского-Шоффара (наследственный микросфероцитоз) – группа наследственных гемолитических анемий, характеризующихся образованием микросфероцитов (шаровидных эритроцитов) и обусловленных дефектом протеинов цитоскелета эритроцитов. При этом эритроциты теряют часть мембраны, уменьшается соотношение площади поверхности к объему, в результате чего эритроцит превращается в микросфероцит. Как правило, патология наследуется по аутосомно-доминантному признаку. Распространенность наследственного микросфероцитоза составляет примерно 1 случай на 1000-4500 человек.
При наследственном микросфероцитозе генетические нарушения влияют на протеины цитоскелета, преимущественно на те, которые объединяют цитоскелет с мембраной эритроцита. У большинства больных отмечается значительный дефицит спектрина, и только в некоторых случаях этот дефицит обусловлен генетическими дефектами самого спектрина.
Главные признаки наследственного микросфероцитоза – анемия, желтуха, спленомегалия (увеличенная селезенка). Анемия возникает из-за внутриклеточного распада эритроцитов. Желтуха развивается посредством непрямой гипербилирубинемии, может быть непостоянной и, как правило, слабо выражена у детей раннего возраста. Повышенное содержание билирубина в желчи часто является причиной образования пигментных желчных камней (даже у детей). Увеличение селезенки (спленомегалия) отмечается практически во всех случаях. При системных инфекционных патологиях интенсивность гемолиза может увеличиваться, в результате чего развивается спленомегалия.
Тяжелые формы наследственного микросфероцитоза характеризуются деформацией скелета: изменение расположения зубов, акрокефалия (башенный череп), высокое верхнее небо, микрофтальмия (уменьшение глазного яблока). В некоторых случаях отмечаются укороченные мизинцы. Могут образовываться трофические язвы на ногах.
Наследственный микросфероцитоз сопровождается апластическими кризами, которые провоцируются инфекцией (особенно парвовирусной).
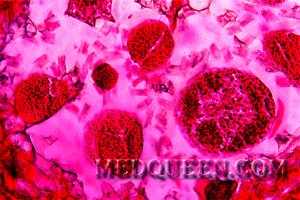
Микросфероцитоз – характерное изменение формы эритроцитов при этой патологии. При анализе мазка крови в биологическом материале наблюдаются микросфероциты в виде мелких клеток без центрального просветления (см рисунок 1). Отметим, что обнаружение микросфероцитов в мазках не всегда является признаком наследственного сфероцитоза.
Рисунок 1. Наследственный микросфероцитоз. Микросфероциты в мазке периферической крови (окр. по Романовскому-Гимзе, ув. ×100)
Такой признак обнаруживается при аутоиммунной гемолитической анемии с неполными тепловыми агглютинами, при наследственных дизэритропоэтической анемии. Средний объем эритроцитов, как правило, остается в норме или незначительно снижен. Показатель среднего содержания гемоглобина в эритроцитах в норме или незначительно повышен. Средняя концентрация гемоглобина в эритроцитах повышена почти у 50% пациентов.
Количественным показателем сферичности эритроцитов является осмотическая устойчивость (она снижена). Уровень ретикулоцитов в крови при гемолитическом кризе может значительно повышаться. Миелограмма показывает резкое раздражение красного ростка. Дифференциальный диагноз проводят с аутоиммунной гемолитической анемией, для которой характерна положительная проба Кумбса, отсутствие этой патологии среди родственников пациента и отсутствие данных о начале заболевания в детском возрасте.
Основной метод лечения анемии при наследственном микросфероцитозе – спленэктомия, с помощью которой устраняется анемия; при этом нельзя устранить морфологический дефект эритроцитов.
Наследственная гемолитическая анемия, обусловленная дефицитом глюкозо-6-фосфат дегидрогеназы эритроцитов – наиболее распространенная ферментопатия эритроцитов из группы ферментопатий пентозофосфатного пути метаболизма глюкозы. Глюкозо-6-фосфатдегидрогеназа эритроцитов – олигомер (в зависимости от условий может быть димер или тетрамер), который состоит из субъединиц с молекулярной массой 56 000 D. По данным ВОЗ (Всемирной организации здравоохранения) во всем мире количество людей, страдающих этой патологией, составляет более 200 млн. Наиболее широкое распространение этого заболевания характерно для Средиземноморского региона (Сицилия, Греция, Сардиния), негроидной расы, жителей Ближнего и Дальнего востока.
Клиническая картина при наследственной форме гемолитической анемии полиморфна: степень тяжести патологии может колебаться от гемолитической анемии, возникающей спонтанно после рождения, до гемолитических кризов. Гемолитический криз, который может провоцироваться метаболическим ацидозом или гипогликемией, развивается за несколько часов. В тяжелых случаях у больного развивается гемоглобинурия и шок. Также наблюдаются желтуха, моча приобретает бурый или черный цвет, одышка, диарея, рвота, снижение артериального давления, развивается тяжелая анемия, увеличиваются печень (гепатомегалия) и селезенка (спленомегалия).
Тяжелый гемолитический криз может спровоцировать развитие ДВС-синдрома (диссеминированного внутрисосудистого свертывания крови). Некоторые пациенты не переносят конские бобы (Viciafaba), после употребления которых происходит молниеносное развитие гемолитического криза (это явление также известно, как фовизм или примахиновая анемия).
Дефицит глюкозо-6-фосфат дегидрогеназы эритроцитов необходимо подозревать во всех случаях острого гемолиза, особенно у лиц негроидной расы и жителей средиземноморского региона. Диагноз подтверждается путем проведения лабораторных анализов. Острый гемолиз характеризуется быстрым снижением гематокрита с одновременным повышением уровня гемоглобина и непрямого гемоглобина, а также снижением уровня гаптоглобина. Анализ мазка крови показывает наличие фрагментов эритроцитов. Основой диагностики считается качественное (при необходимости – количественное) определение активности глюкозо-6-фосфат дегидрогеназы эритроцитов. У пациентов с вариантом «А-» явление аномального гемолиза проходит, как правило, самостоятельно – такие больные не нуждаются в специальном лечении. В случае развития тяжелого гемолитического криза необходимо проводить форсированный диурез, профилактику ДВС-синдрома, плазмаферез (с целью удаления продуктов гемолиза).
В случае возникновения качественной гемоглобинопатии происходит изменение аминокислотной последовательности цепей глобина. Талассемия (количественная гемоглобинопатия) характеризуется снижением образования цепей глобина без изменения их цепей. Нужно отметить, что разница между качественной и количественной гемоглобинопатиями не абсолютна.
Талассемия (анемия Кули) – группа патологий, обусловленных генетическим нарушением синтеза одной из цепей глобина. В норме процесс синтеза глобиновых цепей сбалансирован, поэтому свободных цепей глобина нет. В случае нарушения синтеза одной из цепей глобина баланс нарушается, образуются лишние цепи, которые агрегируют и откладываются в эритрокариоцитах. Среди жителей Средиземноморья наиболее распространена β-талассемия.
«Большая талассемия» (болезнь Кули, β-талассемия) – наследственная гемолитическая анемия, впервые описанная американскими педиатрами-гематологами Томасом Бентоном Кули (Thomas Benton Cooley) и Ли (P. Lee) в статье «Серия случаев спленомегалии у детей с анемией и необычными изменениями костей» («A Series of Cases of Splenomegaly in Children, with Anemia and Peculiar Bone Changes»), где были приведены случаи у выходцев из стран Средиземноморья. Для анемии Кули характерна тяжелая степень течения с самого детства, задержка роста и изменения костей в результате увеличения объема костного мозга, возникающие в случае отсутствия соответствующего лечения). Также при этой патологии у больного наблюдаются гепатомегалия, спленомегалия, гиперспленизм, деформации черепа (монголоидное лицо, башенный череп); желтуха, бледность и отложение меланина придают коже особый медный оттенок. Кроме этого, наблюдается перегрузка железом сердца, легких, печени, поджелудочной железы и других органов эндокринной системы, переломы костей, сдавления периферических нервов, разного рода инфекционные осложнения.
Результаты лабораторных исследований периферической крови показывают гипохромную анемию, ретикулоцитоз, мишеневидные эритроциты (см рис 2-4).
Рисунок 02. Анемия Кули (большая талассемия). Периферическая кровь. Микроцитоз, выраженная гипохромия, мишеневидные нормобласты и эритроциты (окр. по Романовскому-Гимзе, ув. ×100)
Рисунок 03. Анемия Кули (большая талассемия). Периферическая кровь (окр. по Романовскому-Гимзе, ув. ×50)
Рисунок 04. Анемия Кули (большая талассемия). Периферическая кровь. Множественные мишеневидные эритроциты (окр. по Романовскому-Гимзе, ув. ×100)
Миелограмма демонстрирует раздражение «красного ростка» и повышение количества сидеробластов. Также наблюдается повышение осмотической резистентности эритроцитов и количества билирубина за счет непрямой фракции. В крови повышается содержание железа и ферритина, развивается гемосидероз (чрезмерное отложение гемосидерина в тканях) внутренних органов. При гомозиготной β-талассемии необходимо проводить пренатальную диагностику – забор клеток плода из амниотической жидкости на предмет выявления мутации генов, отвечающих за кодирование β-цепи глобина, с применением метода полимеразной цепной реакции.
Без соответствующего лечения больные анемией Кули умирают в детском возрасте. Продлить жизнь, предупредить деформации костей и задержку роста можно путем регулярных трансфузий эритроцитарной массы (лучше переливать отмытые или размороженные эритроциты) при условии поддержания достаточно высокого уровня гемоглобина. В случае значительной спленомегалии и явлениях гиперспленизма больному показана спленэктомия (удаление селезенки). С целью предотвращения развития гемосидероза пациентам периодически назначают Деферазирокс (Эксиджад) или Дефероксамин (Десферал). Излечение возможно при аллогенной трансплантации костного мозга.
Серповидноклеточная анемия обусловлена носительством гемоглобина, который меняет свою структуру в условиях гипоксии. Самой распространенной аномалией структуры гемоглобина является гемоглобинопатия Sα2β26 глу+вал. При гомозиготном носительстве можно говорить о серповидноклеточной анемии; при гетерозиготном носительстве – серповидноклеточная аномалия. Патология наследуется по аутосомно-доминантному признаку. При серповидноклеточной анемии наблюдается мутация, в результате которой в цепи глобина глутаминовая кислота заменяется валином. В результате растворимость гемоглобина S при отдаче кислорода снижается, что приводит к образованию геля.
Серповидноклеточная анемия наиболее распространена среди населения Центральной Африки, Турции, Индии, Кубы. У больных диагностируется анемия, тромботические осложнения, поражения костей и суставов (отмечаются некрозы плечевой и бедренной костей). Кроме этого, тромбозы осложняются инфарктами (сердца, легких, почек, селезенки, головного мозга), приступами сильной боли в области живота. У детей отмечаются нарушения физического (отставание в росте) и полового развития, ночное недержание мочи, нарушение зрения (тромбозы сосудов сетчатки). Также могут развиваться гемолитический, апластический и секвестрационные кризы, при этом в селезенке происходит резкое накопление эритроцитов, что вызывает гиповолемический шок и резкое снижение уровня гемоглобина.
Для анализов крови при апластической анемии характерны низкий уровень гемоглобина, наличие серповидных эритроцитов (рисунок 5), базофильная пунктация эритроцитов, их мишеневидность, повышение уровня ретикулоцитов и непрямого билирубина. Миелограмма демонстрирует раздражение «красного ростка».
Рисунок 5. Серповидноклеточная анемия. Периферическая кровь. Серповидные и мишеневидные эритроциты. выраженная гипохромия эритроцитов (окр. по Романовскому-Гимзе, ув. ×100)
В качестве лечения применяют адекватную инфузионную терапию, переливания эритроцитарной массы, оксигенотерапии.
К приобретенным гемолитическим анемиям относится группа заболеваний разного патогенеза, которые объединяет внутрисосудистый гемолиз (гемолиз эритроцитов в периферической крови). В зависимости от механизма эритролиза приобретенная гемолитическая анемия может носить иммунный и неиммунный характер. Но, несмотря на разные патогенетические механизмы, клинические признаки этих анемий часто совпадают.
Гемолитическая анемия у пациентов с протезированными клапанами сердца и сосудами развивается примерно в 10% случаев при протезированном аортальном клапане. При использовании стеллитовых запирательных элементов частота гемолиза незначительно увеличивается (по сравнению с селиконовыми). Также некоторое увеличение частоты гемолиза отмечается при наличии околоклапанной регургитации и при малом диаметре клапана. Биопротезы (свиные клапаны) в редких случаях являются причиной механического гемолиза. Гораздо реже причиной гемолиза может быть также протезированный митральный клапан, так как трансклапанный градиент давления в этом случае ниже.
Гемолиз протезированными клапанами происходит в результате одновременного действия сразу нескольких факторов:
- Значительная сила сдвига, которая при турбулентном токе крови действует на мембрану эритроцитов, особенно когда под высоким давлением кровь проходит через маленькое отверстие (например, при околоклапанной регургитации)
- Отложения фибрина на участках неплотного прилегания кольца клапана к тканям сердца
- Прямое механическое повреждение эритроцитов при закрытии запирательного элемента
Значительное разрушение эритроцитов может наблюдаться после закрытия дефекта межпредсердной перегородки типа ostium primum заплатой из синтетического материала. Умеренное сокращение жизни эритроцитов с легкой анемией или без нее может наблюдаться при значительном обызвествлении аортального клапана. Механический гемолиз обнаруживается также у пациентов, перенесших аортокоронарное и аортобедренное шунтирование.
Тяжелые случаи механического гемолиза сопровождаются тяжелой анемией, ретикулоцитозом, обнаруживаются фрагментированные эритроциты (шизоциты), гемоглобинемия и гемоглобинурия, повышается активность лактатдегидрогеназы, снижается уровень гаптоглобина. Выведение железа из организма с мочой в виде гемосидерина или гемоглобина может вызвать дефицит железа в организме. В случае развития дефицита железа пациенту назначается пероральный прием препаратов железа. Терапия препаратами железа способствует повышению уровня гемоглобина и способствует снижению сердечного выброса и снижению интенсивности гемолиза. Отметим, что ограничение физической активности также способствуют снижению интенсивности распада эритроцитов. Если предпринимаемые меры не приводят к желаемому результату, нужно полностью устранить околоклапанную регургитацию или заменить протез.
источник
а) болезнь Минковского-Шоффара б) болезнь Маркиафавы-Микели в) талассемия г) анемия при гиперспленизме д) аутоиммунная гемолитическая анемия
27. Причиной развития железодефицитной анемии являются:
б) острое нарушение мозгового кровообращения
в) хронический обструктивный бронхит
г) остеохондроз шейного отдела позвоночника
а) головокружение, слабость
в) признаки фуникулярного миелоза
а) хронической кровопотери
в) В12 – фолиеводефицитной анемии
г) сидероахрестической анемии
30. Какое из перечисленных клинических проявлений характерно для железодефицитной анемии? а) желтуха б) спленомегалияв) ретикулоцитоз г) извращениевкусад) жидкий стул
32. Где депонируется железо:
33. Гипорегенераторный характер анемии указывает на:
а) наследственный сфероцитоз
в) недостаток железа в организме
34. Признаками дефицита железа являются:
35. В организме взрослого содержится:
36. Сфероцитоз эритроцитов:
а) встречается при болезни Минковского-Шоффара
б) характерен для В-12 –дефицитной анемии
в) является признаком внутрисосудистого гемолиза
37. Лейкемоидные реакции встречаются:
б) при септических состояниях
38. Препараты железа назначаются:
39. После спленэктомии при наследственном сфероцитозе:
а) в крови не опреляются сфероциты
в) возникает тромбоцитопения
40. Укажите уровень гемоглобина соответствующий тяжелой степени анемии:
Схема решения ситуационных задач:
1.Выделите основные клинические синдромы.
2.Поставьте предварительный диагноз.
3.Назначьте план обследования.
4.На основании клинических и лабораторных данных сформулируйте клинический диагноз, обоснуйте его.
5.Определите основные направления терапии и тактику ведения.
6.Определите мероприятия, направленные на профилактику имеющегося у больного заболевания.
Больная М., 46 лет, поступила в клинику с жалобами на слабость, головокружение, боли давящего характера в области сердца. Ухудшение в течение 2-х недель, когда постепенно стали нарастать слабость, головокружение, в течение 2-х дней беспокоят неинтенсивные боли в области сердца давящего характера, без иррадиации. На момент осмотра обращала внимание выраженная бледность кожных покровов, тахикардия до 96 в мин, АД 130/80 мм рт ст. В легких дыхание везикулярное, хрипов нет. В течение 3-х месяцев беспокоят продолжительные и обильные менструации, по 7-10 дней, с перерывом в 20 дней. В общем анализе крови — эритроциты 2,8*10л12/л, гемоглобин 88 г/л, ЦП 0,7, анизоцитоз ++ , лейкоциты 7,6*10л12/л, П-1, С-68, Л-25, М-6, СОЭ 5 мм/ч, сывороточное железо — 7,2 мкмоль/л. Осмотрена гинекологом — фибромиома матки, нарушение менструального цикла. По ЭКГ — острой коронарной патологии не выявлено.
Больной В., 50 лет. Три года назад перенес обширную резекцию желудка по поводу язвенной болезни. После операции уровень гемоглобина составлял 133,5 г/л. В течение последнего года состояние ухудшилось, появились резкая слабость, мелькание мушек перед глазами, одышка при ходьбе. Анализ крови: Нв-6.2 г/л, эр-3000000, цв.л.-0.62, л-3700, п-2%, э-2%, с-56%, лимф-34%, мон-6%, СОЭ 7мм/ч. Эритроциты гипохромны. Анизоцитоз (микро- и макро), пойкилоцитоз. Сывороточное железо-30мкг.
Как объяснить появление наряду с микроцитами, макроцитов?
Какое лечение показано больному в настоящее время?
Какие профилактические мероприятия необходимы в будущем?
Больная А., 37 лет, поступила с жалобами на слабость, быструю утомляемость, головокружение, плохой аппетит, затрудненное глотание пищи, желание есть мел, штукатурку. Из анамнеза известно, что во время беременности 5 лет назад у больной отмечалось снижение гемоглобина до 8 г %. Больной назначались препараты железа. Объективно: бледность кожных покровов и видимых слизистых, питание хорошее. Периферические л/у не увеличены. В легких везикулярное дыхание. Пульс 96 уд. мин., ритмичен. Тоны сердца звучные, негрубый систолический шум на верхушке и легочной артерии. А/Д 110/70 мм рт. ст. Язык нормальной окраски, сосочки сглажены. Живот болезненный в эпигастрии. Печень и селезенка не увеличены. При исследовании желудочного сока выявлена ахилия. При рентгенологическом исследовании желудка — симптомы гастрита. Гинекологический статус нормальный. Менструации регулярные, по 4 дня необильные. Анализ крови: эр-3400000, Нв 7 г%, ретикулоциты 2%, л-4700, э-2%, п-3%, с-64%, лимф-26, мон-5%, СОЭ 7мм/ч. Сывороточное железо 30мг%.
1.Назовите характер изменений со стороны ОАК.
2.Поставьте клинический диагноз.
3.Какое лечение показано больной.
4.Какова продолжительность лечения.
5.Какие профилактические мероприятия необходимы больной в будущем?
ТЕМЫ УЧЕБНО-ИССЛЕДОВАТЕЛЬСКОЙ РАБОТЫ СТУДЕНТОВ:
1.Причины приобретенных анемий, механизмы развития клинических проявлений, диагностика на современном этапе развития медицины.
2.Дифференциально-диагностические признаки различных видов анемий.
3.Сидеропенический синдром, клинические проявления, диагностика.
4.Анемический синдром, клинические проявления, диагностика.
5.Профилактика железодефицитных анемий.
6.Синтез гема, биохимические механизмы, клинические проявления нарушения синтеза гема, методы специфической диагностики.
7.Железо, его роль в организме.
8.Лечебное питание при железодефицитной анемии.
Название темы: ХРОНИЧЕСКИЙ ЛИМФОЛЕЙКОЗ
1. Этиологию и патогенез хронического лимфолейкоза.
2. Классификацию хронического лимфолейкоза по стадиям.
3. Клиническую картину этого заболевания по синдромам.
4. Осложнения и течение хронического лимфолейкоза.
5. Методы диагностики хронического лимфолейкоза.
6. Методы медикаментозной терапии, вторичной профилактики обострений, показания и противопоказания к применению препаратов.
1. Последовательно собрать жалобы, анамнез заболевания, анамнез жизни больного.
2. Выполнить объективное обследование больного с хроническим лимфолейкозом.
3. На основании клинического, лабораторного, инструментального методов обследования составить клинический диагноз с учетом современной классификации.
4. Составить план лечения на основании современных протоколов ведения больных с хроническим лимфолейкозом.
5. Оценивать эффективность лечения на основании динамики клинико-лабораторных данных.
ВОПРОСЫ ДЛЯ САМОПОДГОТОВКИ:
1. Определение хронического лимфолейкоза.
2. Этиология и патогенез хронического лимфолейкоза.
3. Формы хронического лимфолейкоза.
4. Особенности клинического течения различных вариантов хронических лимфолейков.
5. Основные клинические проявления хронического лимфолейкоза.
6. Диагностика хронического лимфолейкоза.
7. Лабораторно-морфологическая диагностика. Диагностические критерии болезни.
8. Основные принципы лечения хронического лимфолейкоза.
1. Какой из перечисленных препаратов показан для лечения больных хроническим лимфолейкозом:
Г. Нуклеиновокислый натрий
2. Какие из перечисленных признаков можно отнести к кардинальным при хроническом лимфолейкозе?
Б. Увеличение лимфатических узлов
3. Какой из названных признаков не характерен для хронического лимфолейкоза?
Б. Увеличение лимфатических узлов
Д. Гемморагический синдром
4. Добракачественное течение заболевания характерно для:
Б. Хронического миелолейкоза
В. Хронического лимфолейкоза
5. Тени Гумпрехта представляют собой:
А. Разрушенные при приготовлении мазка ядра лимфоцитов, в которых среди глыбок хроматина можно заметить нуклеолы
6.В течении хронического лимфолейкоза выделяют стадии:
А. Начальная, развернутая, терминальная
Б. Начальная, прогрессирующая, ремиссия
В. Обострение, развернутая, ремиссия
Г. Начальная, периодическая, терминальная
7. Какие осложнения характерны для хронического лимфолейкоза: 1) гемморагические; 2) аутоиммунные; 3) инфекционные или гнойно-воспалительные; 4) артериальная гипертония; 5) все перечисленное.
8. Наиболее информативным методом для подтверждения лимфопролиферативного синдрома при хроническом лимфолейкозе является:
А. лейкоцитарная формула крови
Б. пункция лимфатического узла
Г. биопсия лимфатического узла
9. Наиболее характерный клинический симптом хронического лимфолейкоза:
Г. увеличение лимфатических узлов
10. Хронический лимфолейкоз (выберите одно правильное утверждение):
А. самый распространенный вид гемобластоза
Б. характеризуется доброкачественным течением
В. возникает в старшем и пожилом возрасте, во многих случаях не требует цитостатической терапии
11. Субстратом опухоли при хроническом лимфолейкозе являются:
12. Какие лимфоциты чаще являются субстратом опухоли при хроническом лимфолейкозе?
13. Для хронического лимфолейкоза характерно:
А. отсутствие признаков опухолевой прогрессии
Б. наличие признаков опухолевой прогрессии
14. Какие стадии хронического лимфолейкоза выделяют, кроме:
15. Лимфопролиферативный синдром обусловлен следующими причинами, кроме:
В. лимфоидной пролиферацией костного мозга
16. Синдром осложнений при хроническом лимфолейкозе проявляется следующими состояниями, кроме:
17. Гемолитическая анемия и тромбоцитопения при хроническом лимфолейкозе является показанием для назначения:
В. сочетания преднизолона с высокими дозами цитостатиков
Г. низких доз цитостатиков
18. Полихимиотерапия при хроническом лимфолейкозе — это:
А. комплекс цитостатиков и преднизолон
Б. комплекс преднизолона и антибиотиков
В. комплекс цитостатиков и антибиотиков
Г. комплекс цитостатиков и гемотрансфузий
19. Какова причина аутоиммунной анемии и тромбоцитопении при хроническом лимфолейкозе:
А. недостаток выработки эритропоэтина почками
Б. выработка неполноценных эритроцитов и тромбоцитов в костном мозге
В. появление аутоантител к собственным нормальным эритроцитам и тромбоцитам
20. Какое количество лимфоцитов в пунктате костного мозга является патогномоничным для хронического лимфолекоза?
21. Острый или хронический характер лейкоза определяется: 1) характером начала болезни (быстрое или постепенное); 2) характером и длительностью лечения; 3) эффективностью или устойчивостью к цитостатическим препаратам; 4) видом и особенностями клеток, составляющих субстрат опухоли (видом подавляющего большинства опухолевых клеток); 5) видом клеток родоначальников опухолевого клона.
22. Хронический лимфолейкоз – это опухоль, возникающая из:
А. клеток ранних предшественников миелопоэза, не способных дифференцироваться до ранних форм
Б. клеток ранних предшественников миелопоэза, дифференцирующихся до зрелых форм
В. полипотентных клеток гемопоэза, не спосбных к созреванию
Г. В-лимфоцитов, продуцирующих парапротеины
Д. клеток предшественников миелопоэза, сохраняющих способность дифференцироваться до зрелых форм с преимущественной пролиферацией эритроидного костного мозга
23. Для начальной стадии хронического лимфолейкоза характерно: 1) моноклоновость опухолевой пролиферации; 2) поликлоновость опухолевой пролиферции; 3) генерализация опухолевого процесса; 4) ограниченность опухоли местом ее возникновения; 5) отсутствие выраженной клиники заболевания; 6) яркая клиника заболевания.
24. Для развернутой стадии хронического лимфолейкоза характерно: 1) моноклоновость опухолевой пролиферации; 2) поликлоновость опухолевой пролиферции; 3) генерализация опухолевого процесса; 4) ограниченность опухоли местом ее возникновения; 5) отсутствие выраженной клиники заболевания; 6) яркая клиника заболевания.
25. Для терминальной стадии хронического лимфолейкоза характерно: 1) моноклоновость опухолевой пролиферации; 2) поликлоновость опухолевой пролиферции; 3) генерализация опухолевого процесса; 4) явная выраженность клинической картины заболевания; 5) отсутствие выраженной клиники заболевания; 6) анемия и тромбоцитопения; 7) бластные кризы; 8) рефрактерность к цитостатикам.
26. Для развернутой стадии хронического лимфолейкоза со стороны крови характерны: 1) лейкопения; 2) гиперлейкоцитоз нейтрофильный; 3) гиперлейкоцитоз лейкоцитарный; 4) тени Гумпрехта; 5) наличие или увеличение эознофилов и/или базофилов; 6) относительная гранулоцитопения; 7) гипертромбоцитоз; 8) тромбоцитопения.
27. Для хронического лимфолейкоза наиболее характерно: 1) увеличение и безболезненность лимфоузлов; 2) увеличение и болезненность лимфоузлов; 3) кожный зуд; 4) эритромелалгия; 5) склонность к тромбообразованию; 6) развитие мочекаменной болезни; 7) частые инфекционные осложнения; 8) склонность к аутоиммунным осложнениям (гемолиз, цитопения).
28. Спленэктомия показана при хроническом лимфолейкозе: 1) во всех случаях; 2) при резкой анемии; 3) при тромбоцитопении; 4) при резкой и нарастающей спленомегалии; 5) при инфарктах селезенки; 6) при цитостатической цитопении; 7) при иммунной (не цитостатической) цитопении.
29. Для какой формы хронического лимфолейкоза характерно значительное увеличение лимфатических узлов при невысоком лейкоцитозе?
30. Задачи лечения хронического лимфолейкоза следующие: 1) уничтожение всех элементов опухоли; 2) замедление опухолевой прогрессии; 3) сохранение соматической компенсации больного; 4) нормализация патогенных характеристик лейкозных клеток; 5) лечение инфекционных, аутоиммунных и других осложнений.
31. Какое количество лимфоцитов в пунктате лимфоузла и селезенки характерно для хронического лимфолейкоза?
32. Начальная стадия хронического лимфолейкоза характеризуется следующими клиническими проявлениями, кроме:
А. умеренная лимфоаденопатия
Б. умеренная спленомегалия
В.симптомы лимфоидной пролиферации крови и костного мозга
33. К общим симптомам, обусловленным интоксикацией, разрастанием лейкозных клеток в костном мозге и селезенке при ХЛЛ относятся следующие, кроме:
Г. боли в костях, селезенке и печени
34. Тяжесть в левом подреберье у больных ХЛЛ обусловлена:
А. расширением петель толстого кишечника
35. В периферической крови у больного ХЛЛ обнаруживается: 1) выраженные лейкоцитоз; 2) выраженная лейкопения; 3) содержание лимфоцитов до 80-90%; 4) отсутствие лимфоцитов; 5) лимфоциты малого размера с узкой полоской цитоплазмы. Выберите правильную комбинацию ответов.
36. В какую стадию ХЛЛ появляются анемия и тромбоцитопения?
37. Сочетание проявлений хронического лимфолейкоза с поражением кожи – это:
38. Какие больные чаще болеют хроническим лимфолейкозом:
39. Какая жалоба наиболее характерна для начальной стадии хронического лимфолейкоза:
В. увеличение шейных, подмышечных, паховых лимфоузлов
40. Показанием для гемотрансфузий у больных с ХЛЛ является:
А. выраженная анемия, не купирующаяся приемом препаратов железа
источник