Многие годы безуспешно боретесь с ГИПЕРТОНИЕЙ?
Глава Института: «Вы будете поражены, насколько просто можно вылечить гипертонию принимая каждый день.
Железодефицитная анемия знакома довольно большой части населения земного шара. В странах Европы проблему недостатка железа в организме решает Всемирная Организация Здравоохранения, у которой представлена оздоровительная программа «Гемоглобиновое оздоровление населения». В нашей стране, к сожалению, терапия и профилактика ЖДА находятся в зачаточном состоянии. Хотя ведутся непрерывные исследования, разрабатываются новые препараты, нет системно налаженного процесса терапии и профилактики, что приводит к понижению уровня железа.
Для лечения гипертонии наши читатели успешно используют ReCardio. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
В первую очередь необходимо разобраться, что такое железодефицитная анемия, в чем выражается механизм ее образования.
Поскольку железодефицитная форма анемии напрямую связана именно с дефицитом железа, необходимо разобраться, как происходит обмен этого элемента в организме. Он поступает вместе с пищей, солями и комплексами, содержащими железо, а также бывает гемовым (то есть помогает выработке гемоглобина) и негемовым. Элемент всасывается зачастую в двенадцатиперстной кишке, усваивается такое количество железа, которое нужно для стабильного функционирования органов. При железодефицитной анемии человек особенно остро нуждается в микроэлементе, поэтому всасывание происходит и в остальных отделах кишечника.
Когда железо попадает в кровь, оно соединяется с особым белком — плазменным трансферрином, который образуется в печени. Этот белок примерно на тридцать процентов насыщается железом и переносит его к клеткам костного мозга, в которые микроэлемент попадает при помощи эндоцитоза, а затем участвует в процессе образования гемоглобина.
Кроме внешних источников получения железа с пищей и витаминными комплексами, организм использует также резервный путь: после распада эритроцитов в селезенке остается некоторое количество железа, которое трансферрин также переносит к костному мозгу.
Таким образом, весь процесс обмена железа в организме представлен следующими процессами:
- усвоение элемента кишечником;
- транспорт вещества к клеткам при помощи трансферрина;
- разрушение эритроцитов и хранение образованного железа в печени и селезенке (депонирование);
- удаление железа из организма естественным путем.
Теоретически, получить анемию может каждый человек, но, как и с каждым заболеванием, существуют определенные группы людей, которые больше подвержены такому заболеванию:
- Чаще всего анемией страдают женщины, среди которых заболевают молодые представительницы слабого пола, беременные и девочки-подростки. Это обусловлено ежемесячной потерей крови женщинами при менструации.
- В подростковом возрасте анемия встречается практически у всех людей, поскольку начинается период быстрого роста, он может достигать целых пятидесяти процентов, при этом в большей мере железодефицитной анемией страдают девочки, у которых начинаются менструации.
- Среди младенцев тоже существует своя статистика, согласно которой близнецы при многоплодной беременности, а также дети, значительно опережающие сверстников в росте до первого года жизни, с вероятностью в шестьдесят процентов получат диагноз «железодефицитная анемия».
- К более пожилому возрасту (примерно к шестидесяти годам) гендерные рамки стираются и теперь анемией страдают в основном не женщины, а мужчины.
Железодефицитные анемии можно классифицировать разными способами.
По степени тяжести выделяют такие формы заболевания:
- легкая, при которой недостаток железа выражен неярко, содержание гемоглобина равно примерно 90/100 граммам на литр крови;
- средняя, при которой в крови в среднем содержится семьдесят/девяносто грамм гемоглобина на литр;
- сильная, при которой уровень гемоглобина понижается до семидесяти грамм на литр.
Классическая клиническая классификация, которой характеризуется анемия железодефицитная, включает в себя разные формы:
- Постгеморрагическую анемию, вызванную небольшими повторными кровопотерями.
- Малокровие беременных, связанное с тем, что в этот волнительный период жизни питание часто становится несбалансированным, а большая часть железа передается развивающемуся плоду. Возможно также появление малокровия в период кормления ребенка грудью.
- Анемию, появившуюся на фоне каких-либо патологий ЖКТ. Причиной такого состояния является нарушение всасывательной функции кишечника, неспособного усваивать железо в достаточном количестве. Такое заболевание появляется особенно часто после гастрэктомии и других оперативных вмешательств.
- Вторичную анемию, являющуюся следствием инфекций, опухолей или воспалений. Причина заключается в том, что большая часть железа теряется во время распада опухолевых клеток, могут возникать кровотечения различных масштабов, а также нужда в микроэлементе увеличивается в районе воспалительных очагов.
- Эссенциальную (или идиопатическую) анемию. Она представляет собой особый случай, при котором даже тщательные исследования не позволяют определить первопричину заболевания. Чаще всего при такой анемии наблюдаются индивидуальные особенности усвоения железа кишечником.
- Ювенильную форму, которая развивается чаще всего у девушек, а у юношей встречается достаточно редко.
Существует также классификация по стадиям развития железодефицитной анемии:
- При I стадии происходит превышение уровня потери железа над его получением, кишечник начинает усиленно всасывать железо из пищи.
- При II стадии запасы микроэлемента истощаются настолько, что это начинает мешать нормальному образованию красных кровяных клеток — эритропоэзу.
- III стадия характеризуется возникновением легкой степени анемии.
- IV стадия — уже вполне выраженная анемия средней степени, при которой наблюдается заметный недостаток эритроцитов.
- V стадия — возникает тяжелая степень анемии с нарушениями циркуляции крови, гипоксией в тканях.
Кроме того, выделяют еще два типа малокровия:
- гипохромная анемия, характеризующаяся снижением числа гемоглобина в эритроцитах, при этом изменяется цветовой показатель крови;
- микроцитарная анемия, когда нарушается процесс встраивания железа в костном мозге, образования эритроцитов.
Чаще всего железодефицитное малокровие представляет собой комбинацию, куда входит и микроцитарная, и гипохромная анемия.
Для предупреждения появления болезни важно знать, какие существуют причины железодефицитной анемии, поскольку только так можно определить свою принадлежность к группам риска.
Железодефицитная форма анемии может возникнуть, если у ребенка при рождении уже был недостаток железа.
Чаще всего это дети, которые родились раньше срока, если была многоплодная беременность с одним или более ребенком. Вероятность заболевания возрастает, если у матери тоже была диагностирована нехватка железа либо возникали кровотечения в последнем триместре или в процессе родов.
Другим фактором считается нарушение процесса поступления железа и его всасывания ЖКТ.
Причинами такого состояния могут быть:
- исключительно вегетарианская диета без употребления красного мяса;
- однообразная диета, в которой присутствует повышенное количество жиров и углеводов;
- нарушение процесса всасывания железа вследствие индивидуальных и наследственных особенностей организма.
Кроме этих причин, процесс усвоения железа может быть нарушен из-за наличия отклонений со стороны ЖКТ:
- рак желудка;
- оперативное вмешательство с целью частичного удаления желудка либо кишечника;
- хронический панкреатит;
- муковисцидоз, представляющий собой наследственное заболевание, поражающее системы желёз;
- целиакия, обусловлена тем, что белок глютен повреждает внутренние стенки кишечника, вследствие чего происходит дисфункция усвоения полезных элементов;
- энтеропатии, которые характеризуются как хронические болезни кишечника, протекающие без воспалительного процесса, и при которых возникают нарушения выработки ферментов, наблюдаются аномалии в строении ЖКТ.
Железодефицитная анемия и причины другие также может иметь: наиболее распространенными являются кровотечения различного происхождения и масштаба, среди которых выделяют кровоизлияния во внешнюю и внутреннюю среду. При этом в первом случае зачастую происходят кровотечения из ЖКТ в результате эрозий и язв, а также варикоза кишечника. По причине таких кровопотерь, даже если они будут незначительны, возникает потеря железа и, как следствие, гемоглобина.
Кровоизлияния во внутреннюю среду чаще всего выражаются в виде изолированного гемосидероза легких, при котором возникают периодические кровоизлияния в альвеолы, а гемоглобин, находившийся в этом потерянном количестве крови, повторно не используется.
Кроме вышеперечисленных причин железодефицитной анемии у взрослых, можно также выявить наличие в организме сильного воспалительного процесса или опухолей, при этом резко увеличивается уровень потребления дефицитного железа тканями.
Тем людям, кто подозревает у себя развитие малокровия, необходимо знать симптоматику, поскольку, как правило, неприятные ощущения и недомогания появляются при средней степени анемии, от которой необходимо систематически лечиться.
В целом заболевание клинически проявляется в двух вариантах: анемическом и сидеропеническом.
Анемический синдром обусловлен недостатком гемоглобина и эритроцитов, им сопровождается железодефицитная анемия, и симптомы при этом чаще всего наблюдаются такие:
- упадок сил;
- апатия;
- усталость;
- может шуметь в ушах;
- черные точки перед глазами.
Во время движения быстро появляется одышка, ускоряется сердцебиение, могут появиться частые обмороки. При более тяжелой стадии может ухудшиться память и мозговая работоспособность, а также появится постоянная сонливость.
Недостаток важных элементов в крови приводит к тахикардии и аритмии, тона сердца глухие при прослушивании. При внешнем осмотре больного анемическим синдромом можно заметить белесость кожных покровов и слизистых, по утрам часто возникает отек лица.
Сидеропенический синдром (или гипосидероз) характеризуется острой нехваткой железа в тканях, вследствие чего понижается активность большинства ферментов.
При этом синдроме наблюдаются сопутствующие признаки железодефицитной анемии:
- Извращение вкуса, при котором людей тянет съесть малосъедобное или вовсе не пригодное в пищу. Чаще всего такое проявление наблюдается у подростков, хотя свойственно и зрелым женщинам.
- Хочется съесть соленые, острые, кислые блюда, а также использовать много пряностей.
- Извращенное обоняние, когда человеку нравятся те ароматы, которые остальные люди считают невыносимыми.
- Недостаток мышечной силы, сильная утомляемость, вызванная недостатком миоглобина и гипоксией тканей.
- Пересыхание, отшелушивание кожного покрова, появление трещинок, сухие, ломкие и тусклые волосы, легко ломающиеся истонченные ногти, наблюдается их ложкообразная вогнутость.
- Трещины и «заеды» в уголках рта — ангулярный стоматит, встречается примерно у пятнадцати процентов больных.
- Глоссит, при котором наблюдается неприятное, распирающее чувство в языке, кончик красного цвета, он становится гладким, поскольку атрофируются сосочки. Зачастую появляются проблемы с зубами.
- Наблюдается сухость слизистой пищевода, трудно и больно глотать пищу, развивается гастрит и энтерит.
- Склеры окрашиваются в голубоватый цвет, что обусловлено истончением их оболочки по причине недостаточного образования коллагена в организме, начинают просвечивать кровеносные сосуды.
- Возникает слабость сфинктеров мочевыводящих путей, при этом часто невозможно удержать мочу при смехе, чихании и кашле, а также может возникнуть ночное недержание.
- Может на длительное время увеличиться температура тела до 37—38 градусов.
Кроме того, человек становится восприимчив к респираторно-вирусным и инфекционным заболеваниям, поскольку снижается способность лейкоцитов к фагоцитозу и, как следствие, понижается уровень иммунитета. Нарушается регенеративная функция организма, плохо заживают повреждения кожи и слизистых оболочек.
Кроме клинических проявлений этих двух синдромов, симптомы железодефицитной анемии также делятся на пять степеней заболевания:
- Легкая степень протекает с отсутствием симптоматических проявлений.
- Средняя степень: упадок сил, тяжело сфокусировать внимание, падает активность мозга, бледность слизистых и кожи.
- Тяжелая степень: при движениях возникает одышка, учащается сердцебиение, возникает аритмия, появляется головная боль и головокружение, наблюдается шум в ушах, нарушается нормальный сон, снижается аппетит и появляется желание съесть кусочек мела, грязи или другого несъедобного вещества. А также начинают нравиться запахи краски, ацетона, бензина, пациент часто болеет простудами и ОРВИ, при внешнем осмотре наблюдается бледная окраска кожи и слизистых, ногти и волосы ломкие, хрупкие.
- Анемическая прекома характеризуется наличием одышки даже при отсутствии физической нагрузки, постоянной тахикардии, прогрессирующей сонливости и слабости, кожные покровы с синюшным оттенком. Могут появиться галлюцинации, депрессия и другие расстройства психики.
- Самой тяжелой стадией считается анемическая кома: важно знать, чем опасна такая форма заболевания. Резко падает артериальное давление, возникает частое поверхностное дыхание, больной не может глубоко дышать, появляется рвота, пациент может упасть в обморок. Может отсутствовать реакция на внешние раздражители.
При обращении в больницу врач в первую очередь должен собрать анамнез и опросить больного на предмет его самочувствия, а также наличия похожих симптомов у родственников. После этого должен быть произведен внешний осмотр кожных покровов и слизистых, особое внимание обращается на их цвет.
Основным способом выявления анемии является, разумеется, общий и биохимический анализ крови, в ходе которых выявляется уровень гемоглобина, цветной показатель крови, количество эритроцитов и так далее.
Кроме того, может быть произведена:
Для лечения гипертонии наши читатели успешно используют ReCardio. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
- пункция кости с целью исследования костного мозга для оценки процесса кроветворения;
- при наличии тахикардии или аритмии назначается электрокардиограмма.
После точной установки диагноза можно начинать лечение железодефицитной анемии. В традиционной медицине используют методы восполнения дефицитного железа в организме, направленные на общее улучшение состояния больного.
Это устранение первопричины возникновения анемии, поскольку качественно излеченное заболевание, вызвавшее дефицит железа, является первым шагом на пути к избавлению от недомоганий.
Необходимо также изменить свой распорядок дня в более активную сторону:
- больше гулять на свежем воздухе;
- заниматься спортом.
Изменить принципы питания, в первую очередь — увеличить употребление белка, есть больше творога, рыбы, мяса, яиц. Перестать употреблять жирные блюда, восполнять недостаток жиров в организме при помощи растительных масел.
Употреблять меньше молока и крепко заваренного чая, поскольку они замедляют процесс усвоения железа кишечником.
Нет необходимости ограничивать себя в углеводах, рекомендуются:
- разнообразные каши;
- пудинги;
- варенье;
- блюда из фруктов, овощей и бобовых;
- ввести в рацион как можно больше блюд, которые содержат витамины B и С: мясо, рыба, творог, дрожжи, капуста, отруби.
И, разумеется, важнейшим принципом смены диеты является постоянное употребление продуктов, содержащих большое количество железа:
- печень;
- икра;
- красное мясо;
- крольчатина и индюшатина;
- персики;
- черника;
- гречневая, овсяная, ячневая и пшеничная каша.
Железосодержащие препараты необходимо употреблять между основными приемами пищи, при этом необходимо запивать их соком или водой, но не молоком. Если анемия развилась до тяжелой формы, то назначаются уколы препаратов железа внутривенно либо внутримышечно, а также может быть произведено переливание эритроцитарной массы из донорской крови.
Все вышеперечисленные методы являются основным ответом на вопрос, как лечить железодефицитную анемию, — и при неукоснительном следовании всем врачебным рекомендациям болезнь отступит.
Методы профилактики заболевания делятся на две основные части:
- Профилактические меры до возникновения заболевания (первичная профилактика). Для этого людям, которые потенциально входят в группы риска по заболеваемости анемией, назначаются железосодержащие препараты. А также рекомендуется смена основ питания: повышенное количество продуктов животного происхождения в рационе, содержащих много белков, дробное питание маленькими порциями пять раз в день. Следует отказаться от жирного, острого, соленого и слишком горячего, добавить употребление поливитаминных комплексов. К мерам первичной профилактики можно отнести и профилактику заболеваний ЖКТ, дабы не вызвать нарушения в процессе усваивания полезных веществ организмом.
- Вторичная профилактика производится уже после того, как заболевание было диагностировано, и представляет собой в основном периодические обследования больных анемией и принятие мер по излечению рецидивов.
Если не обращать внимания на симптомы и лечение заболевания, вполне вероятно скорое развитие осложнений:
- Помимо ухудшения психологического состояния может возникнуть сильное нарушение концентрации внимания, снижение памяти, частая раздражительность и эмоциональная неустойчивость.
- В более тяжелых случаях может возникнуть анемическая кома, которая характеризуется отсутствием реакции на внешние раздражители и дефицитом кислорода в головном мозге вследствие сильного недостатка гемоглобина, переносящего кислород ко всем тканям организма.
- Кроме анемической комы, могут возникнуть общие нарушения в работе внутренних органов, например, сердца, печени, почек, и ухудшение их состояния, особенно если были выявлены хронические заболевания со стороны этих органов.
Информацию о железодефицитной анемии необходимо знать каждому, поскольку заболевание не такое простое и безобидное, как кажется.
При своевременном определении уровня гемоглобина в крови и быстро проведенном лечении можно предотвратить многие серьезные осложнения, которые могут привести даже к коме.
Здоровье каждого человека находится в его руках. Стоит внимательно следить за своим организмом, который подает тревожные звоночки при любом патологическом процессе, и таком как железодефицитная анемия, и лечение тогда не будет изнурительным, долгим.
источник
Анемия из-за дефицита железа, фолиевой кислоты и витамина В12 – это болезнь, которую можно вылечить, изменив рацион питания. Анемией не следует пренебрегать, так как нарушение функционирования крови всегда является сигналом серьезных нарушений в работе организма.
Анемия из-за дефицита витамина В12 или фолиевой кислоты вызывает нарушение синтеза ДНК и разрушает созревание клеток. Анемия из-за дефицита фолиевой кислоты особенно опасна у беременных женщин.
Выделяют следующие симптомы анемии из-за дефицита железа:
- бледная кожа;
- запор;
- выпадение волос;
- усталость;
- трещины уголков рта;
- трудности с дыханием;
- трудности с концентрацией внимания;
- ломкие ногти;
- слабое половое влечение;
- покалывание в ногах и руках;
- апатия.
Анемия из-за дефицита железа, иначе называемая микроцитарная анемия, является следствием нарушений всасывания этого элемента, хронических кровотечений, возникающие из-за различных причин, у женщин очень обильные менструации.
Явная железодефицитная анемия в мазке периферической крови
Люди, которые имеют мало железа в крови, должны принимать препараты железа каждый день, во время еды и обогатить рацион красным мясом, лиственными овощами, продуктами из цельного зерна, бобовыми, черносливом, инжиром.
Если врач считает, что у человека развилась анемия из-за дефицита железа, не следует сразу начинать прием препаратов железа, так как они могут быть опасными для здоровья. Стоит помнить о том, чтобы отказаться употребления молока вместе с железом, так как кальций останавливает его всасывание. Аналогичное действие имеют кофе и чай.
Люди с анемией из-за дефицита железа должны употреблять препараты из пурпурной эхинацеи и крапивы, которые помогают усвоить железо из потребляемых продуктов и блюд.
Витамин В12 необходим для функционирования организма, однако, анемия из-за дефицита витамина В12 может не проявляться годами. Для правильного усвоения витамина В12 в организме, необходим специальный фактор (называемый внутренний фактор Касла), вырабатываемый слизистой оболочкой желудка.
Когда внутренний фактор не доступен в достаточных количествах, например, вследствие частичного урезания желудка или атрофии слизистой оболочки желудка, усвоение витамина В12 в организме снижается.
Недостаток витамина В12 приводит к развитию мегалобластной анемии, которая характеризуется наличием больших кровяных клеток в периферической крови (MCV). Витамин B12 играет важную роль в процессах метаболизма быстро делящихся клеток, например, клеток желудочно-кишечного тракта.
При длительном дефиците витамина В12 могут развиться неврологические нарушения в виде шатающейся походки, расстройства чувствительности к вибрациям и нарушения поз конечностей.
Недостаток витамина В12 приводит к трудностям с концентрацией внимания, апатии, болезненных язв в углах рта, преждевременному седенью, желтизне белков, метеоризму и диарее, отвращению к жареным блюдам и мясу, психическим расстройствам, а также изменениям в мозге и нервной системе.
Анемии с дефицитом витамина В12 более подвержены курильщики. Риск возникновения этого недуга повышен у жителей Северной Европы, особенно у женщин.
Причины анемии из-за дефицита витамина B12:
- неправильная диета, бедная витамином В12;
- алкоголизм;
- заболевания, связанные с недостаточностью или нарушением функции фактора Касла, который отвечает за усвоение кобаламина;
- нарушение всасывания комплекса цианкобаламин;
- инфицирование широким лентецом;
- дефицит транскобаламина II и другие.
Недостаток витамина В12 в организме приводит к развитию болезненных изменений в различных органах и системах: желудочно-кишечного тракта, кроветворной и нервной системе.
К типичным симптомам мегалобластной анемии из-за дефицита витамина B12 относятся: бледность кожи, оттенок желтого лимона рядом с местом обесцвечивания, пожелтение белков глаз, воспалительные изменения желудка, слизистой оболочки языка, пищевода, кишечника, разглаживание языка, заеды в углах рта, жжение языка, потеря аппетита. На тяжелых стадиях анемии могут возникать такие симптомы, как: сердцебиение, головокружение, затрудненное дыхание, шум в ушах.
Неврологические расстройства, возникающие из-за дефицита витамина В12, заключаются, прежде всего, в возникновении судорог конечностей и ослабления мышц ног, нарушениях памяти и концентрации внимания, раздражительности и эмоциональной лабильности.
Иногда первые симптомы дефицита витамина В12 вытекают из демиелинизации нервов спинного мозга и коры головного мозга. К ним относятся: периферическая невропатия, артроз цепочек спинного мозга, демиелинизация серого вещества мозга.
Чтобы избежать дефицита витамина В12, следует позаботиться о том, чтобы в рационе присутствовал белок животного происхождения. Лучшим источником витаминов группы B являются ростки, желтые и зеленые овощи, пивные дрожжи, орехи, миндаль, мука грубого помола, горох, капуста, чечевица, темный рис, печень телячья, фасоль, патока и кунжут.
Анемия из-за дефицита витамина В12, железа и фолиевой кислоты негативно влияет на функционирование организма, поэтому стоит ее предотвратить путем использования разнообразной диеты, богатой этими питательными веществами.
Для диагностики мегалобластной анемии из-за дефицита витамина В12 необходимо провести исследование крови. Морфология при анемии с дефицитом витамина B12 содержит в себе увеличенные эритроциты и их чрезмерную окраску. Для подтверждения диагноза необходимо выполнить биопсию костного мозга, которая нужна для исключения других возможных причин анемии.
В определении диагноза анемии с дефицитом витамина B12 помогает также выявление повышенных значений билирубина в крови и пониженного числа тромбоцитов и лейкоцитов. При злокачественной анемии отмечается снижение абсорбции витамина В12 без фактора Касла и правильное усвоение после введения этого фактора.
В диагностике причин дефицита витамина B12 помогает расширенный тест Шиллинга. Он позволяет отличить, является ли причиной уменьшения поглощения дефицит фактора Касла или нарушено всасывание витамина в кишечнике.
Лечение анемии, вызванной дефицитом витамина В12, заключается в подаче витамина в виде инъекций внутривенно в дозе 1000 мкг 1 раз в день в течение 10 – 14 дней, а затем, после изменения лабораторных показателей, 100-200 мкг 1 раз в неделю до конца жизни.
Первые результаты лечения можно наблюдать уже через неделю лечения – в периферической крови увеличивается количество ретикулоцитов, гемоглобина, улучшается гематокрит. Нормализация параметров периферической крови происходит примерно после 2 месяцев лечения.
В случае удаления желудка или после резекции тонкой кишки витамин В12 назначается профилактически в дозе 100 мкг внутримышечно 1 раз в месяц.
Дефицит фолиевой кислоты или витамина B4, приводит к тошноте, диарее и воспалению языка. Фолиевая кислота – это чрезвычайно важный элемент для беременных женщин, младенцев и созревающих девочек. Стоит отметить, что на уровень фолиевой кислоты в организме влияют гормональные препараты и употребление больших доз витамина C.
Такого рода анемия вызывает нарушение синтеза ДНК. Фолиевая кислота необходима для правильной работы эритроцитов. Ее отсутствие особенно опасно во время беременности, так как это может привести к повреждению нервной системы плода.
Причины анемии с дефицитом фолиевой кислоты:
- синдром нарушения всасывания;
- нехватка фолиевой кислоты в рационе питания;
- хронический алкоголизм;
- период повышенного спроса: беременность, кормление грудью, онкологические заболевания;
- прием некоторых лекарственных препаратов, например, метотрексатов, противоэпилептических препаратов (например, фенитоин) и противотуберкулезных лекарственных препаратов.
Анемию, вызванную дефицитом фолиевой кислоты, можно предотвратить путем обогащения диеты большим количеством овощей и фруктов, а также отказом от алкоголя.
Женщина, которая планирует беременность должна принимать профилактически пищевые добавки с витамином B4 за 2 месяца до зачатия и в период вынашивания ребёнка.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Приведены рекомендации по применению лекарственных препаратов железа при железодефицитной анемии в различных клинических ситуациях.
Рассматриваются причины неэффективности терапии препаратами железа, а также особенности путей введения.
The paper gives recommendations for the use of iron drugs in iron deficiency anemia in different clinical situations.
It considers the causes of ineffective therapy with iron preparations and the specific ways of their administration.
Л. И. Дворецкий – ММА им. И.М. Сеченова
L. I. Dvoretsky – I. M. Sechenov Moscow Medical Academy
Ж елезодефицитная анемия (ЖДА) — клинико-гематологический синдром, характеризующийся нарушением синтеза гемоглобина в результате дефицита железа, развивающегося на фоне различных патологических (физиологических) процессов, и проявляющийся признаками анемии и сидеропении.
В основе развития ЖДА лежат разнообразные причины, среди которых основное значение имеют следующие:
— хронические кровопотери различной локализации (желудочно-кишечные, маточные, носовые, почечные) вследствие различных заболеваний;
— нарушение всасывания поступающего с пищей железа в кишечнике (энтериты, резекция тонкого кишечника, синдром недостаточного всасывания, синдром «слепой петли»);
— повышенная потребность в железе (беременность, лактация, интенсивный рост и др.);
— алиментарная недостаточность железа (недостаточное питание, анорексии различного происхождения, вегетарианство и др.).
При выявлении причины развития ЖДА основное лечение должно быть направлено на ее устранение (оперативное лечение опухоли желудка, кишечника, лечение энтерита, коррекция алиментарной недостаточности и др.). В целом ряде случаев радикальное устранение причины ЖДА не представляется возможным, например, при продолжающихся меноррагиях, наследственных геморрагических диатезах, проявляющихся носовыми кровотечениями, у беременных и при некоторых других ситуациях. В таких случаях основное значение приобретает патогенетическая терапия железосодержащими лекарственными препаратами. Лекарственные препараты железа (ПЖ) являются средством выбора для коррекции дефицита железа и уровня гемоглобина у больных ЖДА. ПЖ следует предпочитать пищевым продуктам, содержащим железо.
Таблица 1. Основные лекарственные препараты железа для приема внутрь
| Препарат | Дополнительные компоненты | Лекарственная форма | Количество двухвалентного железа, мг |
| Хеферол | Фумаровая кислота | Капсулы | |
| Никотинамид | |||
| Витамины группы В | |||
| Иррадиан | Аскорбиновая кислота | ||
| Фолиевая кислота | |||
| Цианкобаламин | |||
| Цистеин, | Драже | ||
| фруктоза, дрожжи | |||
| * Железо находится в виде трехвалентного в форме сложного комплекса (как в ферритине), не обладающего прооксидантными свойствами | |||
В настоящее время в распоряжении врача имеется большой арсенал лекарственных ПЖ, характеризующихся различным составом и свойствами, количеством содержащегося в них железа, наличием дополнительных компонентов, влияющих на фармакокинетику препарата, лекарственной формой. В клинической практике лекарственные ПЖ применяются внутрь или парентерально. Путь введения препарата у больных ЖДА определяется конкретной клинической ситуацией.
Лечение препаратами железа для приема внутрь
В большинстве случаев для коррекции дефицита железа при отсутствии специальных показаний ПЖ следует назначать внутрь. На российском фармацевтическом рынке имеется широкий выбор ПЖ для приема внутрь. Они различаются количеством содержащихся в них солей железа, в том числе двухвалентного железа, наличием дополнительных компонентов (аскорбиновая и янтарная кислоты, витамины, фруктоза и др.), лекарственными формами (таблетки, драже, сиропы, растворы), переносимостью, стоимостью. Основными принципами лечения ПЖ для приема внутрь являются следующие:
— предпочтительное назначение больным ЖДА при отсутствии специальных показаний к применению ПЖ парентерально;
— назначение ПЖ с достаточным содержанием двухвалентного железа;
— назначение ПЖ, содержащих вещества, усиливающие всасывание железа;
— избегать одновременного приема пищевых веществ и лекарственных препаратов, уменьшающих всасывание железа;
— нецелесообразность одновременного назначения витаминов группы В, В12, фолиевой кислоты без специальных показаний;
— избегать назначения ПЖ внутрь при наличии признаков нарушения всасывания в кишечнике;
— достаточная продолжительность насыщающего курса терапии (не менее 1-1,5 мес);
— необходимость проведения поддерживающей терапии ПЖ после нормализации показателей гемоглобина в соответствующих ситуациях.
В табл.1 представлены основные лекарственные ПЖ для приема внутрь, зарегистрированные в России.
При выборе конкретного препарата и оптимального режима дозирования необходимо иметь в виду, что адекватный прирост показателей гемоглобина при наличии ЖДА может быть обеспечен поступлением в организм от 30 до 100 мг двухвалентного железа. Учитывая, что при развитии ЖДА всасывание железа увеличивается по сравнению с нормой и составляет 25 — 30% (при нормальных запасах железа — всего 3 — 7%), необходимо назначать от 100 до 300 мг двухвалентного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. Таким образом, минимальная эффективная доза составляет 100 мг, а максимальная — 300 мг двухвалентного железа в сутки. Индивидуальные колебания в количестве необходимого железа обусловлены степенью дефицита железа в организме, истощения запасов, скоростью эритропоэза, всасываемостью, переносимостью и некоторыми другими факторами. С учетом этого при выборе лекарственного ПЖ следует ориентироваться не только на содержание в нем общего количества, но главным образом на количество двухвалентного железа, которое только и всасывается в кишечнике. Так, например, при назначении препарата с низким содержанием двухвалентного железа (ферроплекс) количество принимаемых таблеток должно быть не менее 8 — 10 в сутки, в то время как препараты с высоким содержанием двухвалентного железа (ферроградумент, сорбифер дурулес и др.) можно принимать в количестве 1 — 2 таблетки в сутки.
С помощью современной технологии в настоящее время выпускаются ПЖ с замедленным высвобождением из них железа благодаря наличию инертных субстанций, из которых через мелкие поры постепенно поступает железо. К таким препаратам относятся ферроградумент, сорбифер-дурулес, фенюльс. Это обеспечивает пролонгированный эффект всасывания и снижает частоту нарушений со стороны желудочно-кишечного тракта. Входящие в состав многих лекарственных форм ПЖ аскорбиновая кислота, цистеин, фруктоза усиливают всасывание железа. Необходимо учитывать, что всасывание железа может уменьшаться под влиянием некоторых содержащихся в пище веществ (фосфорная кислота, соли, кальций, фитин, танин), а также при одновременном применении ряда медикаментов (тетрациклины, альмагель, соли магния). Для лучшей переносимости ПЖ следует принимать во время еды. В то же время всасывание железа лучше при приеме лекарственных препаратов перед едой.
В случаях назначения ПЖ в достаточной дозе на 7 -10-й день от начала лечения наблюдается повышение количества ретикулоцитов. Нормализация уровня гемоглобина отмечается в большинстве случаев через 3 — 4 нед от начала лечения. В ряде случаев сроки нормализации показателей гемоглобина затягиваются до 6 — 8 нед. Иногда наблюдается резкое скачкообразное повышение гемоглобина. Эти индивидуальные колебания нормализации гемоглобина могут быть обусловлены выраженностью ЖДА, степенью истощения запасов железа, а также не полностью устраненной причины (хронические кровопотери и др.).
Среди побочных проявлений на фоне применения ПЖ внутрь наиболее часто возникают тошнота, анорексия, металлический вкус во рту, запоры, реже — поносы. Развитие запоров обусловлено, по всей вероятности, связыванием в кишечнике сероводорода, являющегося одним из стимулов кишечной перистальтики. В большинстве случаев современные ПЖ вызывают незначительные побочные явления, требующие их отмены и перехода на парентеральный путь введения.
Диспептические расстройства могут уменьшаться при приеме препаратов после еды или уменьшении дозы.
Причины неэффективности терапии ПЖ для приема внутрь:
— отсутствие дефицита железа (неправильная трактовка природы гипохромной анемии и ошибочное назначение ПЖ);
— недостаточная дозировка ПЖ (недоучет количества двухвалентного железа в препарате);
— недостаточная длительность лечения ПЖ;
— нарушение всасывания ПЖ, назначаемых внутрь у больных с соответствующей патологией;
— одновременный прием препаратов, нарушающих всасывание железа;
— продолжающиеся хронические (невыявленные) кровопотери, чаще всего из желудочного тракта;
— сочетание ЖДА с другими анемическими синдромами (В12-дефицитной, фолиеводефицитной).
Лечение ПЖ для парентерального введения
ПЖ могут применяться парентерально при следующих клинических ситуациях:
— нарушение всасывания при патологии кишечника (энтериты, синдром недостаточности всасывания, резекция тонкого кишечника, резекция желудка по Бильрот II с включением двенадцатиперстной кишки);
— обострение язвенной болезни желудка или двенадцатиперстной кишки;
— непереносимость ПЖ для приема внутрь, не позволяющая дальнейшее продолжение лечения;
— необходимость более быстрого насыщения организма железом, например у больных ЖДА, которым предстоят оперативные вмешательства (миома матки, геморрой и др.).
В табл. 2 представлены ПЖ, использующиеся для парентерального введения.
В отличие от ПЖ для приема внутрь в инъекционных препаратах железо всегда находится в трехвалентной форме.
Общая ориентировочная доза ПЖ для внутримышечного введения, необходимая для коррекции дефицита железа и анемии, может быть рассчитана по формуле: А = К • (100 — 6 • Нв) • 0,0066, где А — число ампул, К — масса больного в кг, НВ — содержание гемоглобина в гр%. При расчете необходимого количества ампул феррум ЛЕК для внутривенного введения можно также пользоваться приведенной формулой. При этом в 1-й день вводят 1/2 ампулы (2,5 мл), во 2-й день — 1 ампулу (5 мл), в 3-й день — 2 ампулы (10 9 мл). В последующем препарат вводят 2 раза в неделю до достижения необходимой рассчитанной общей дозы.
На фоне парентерального лечения ПЖ, особенно при внутривенном применении, нередко возникают аллергические реакции в виде крапивницы, лихорадки, анафилактического шока. Кроме того, при внутримышечном введении ПЖ может возникать потемнение кожи в местах инъекций, инфильтраты, абсцессы. При внутривенном введении возможно развитие флебитов. Если ПЖ для парентерального введения назначают больным гипохромной анемией, не связанной с дефицитом железа, имеется повышенный риск возникновения тяжелых нарушений из-за «перегрузки» железом различных органов и тканей (печень, поджелудочная железа и др.) с развитием гемосидероза. В то же время при ошибочном назначении ПЖ внутрь никогда не наблюдается возникновение гемосидероза.
Тактика лечения ЖДА при различных клинических ситуациях
Лечение больных ЖДА имеет свои особенности в зависимости от конкретной клинической ситуации с учетом многих факторов, в том числе характера основного заболевания и сопутствующей патологии, возраста больных (дети, старики), выраженности анемического синдрома, дефицита железа, переносимости ПЖ и др. Далее приводятся наиболее часто встречающиеся в клинической практике ситуации и некоторые особенности лечения больных ЖДА.
ЖДА у новорожденных и детей. Основной причиной ЖДА у новорожденных считается наличие ЖДА или скрытого дефицита железа у матери во время беременности. У детей раннего возраста наиболее частой причиной ЖДА является алиментарный фактор, в частности вскармливание исключительно молоком, поскольку содержащееся в женском молоке железо всасывается в незначительных количествах. Среди ПЖ, которые показаны новорожденным и детям наряду с соответствующей коррекцией питания (витамины, минеральные соли, животный белок), следует назначать препараты для приема внутрь, содержащие малые и средние дозы двухвалентного железа (ферроплекс, фенюльс). Предпочтительнее назначение ПЖ в каплях или в виде сиропа (актиферрин, мальтофер). У детей раннего возраста удобно применение ПЖ в виде жевательных таблеток (мальтоферфол).
ЖДА у девушек-подростков является чаще всего следствием недостаточных запасов железа в результате дефицита железа у матери во время беременности. При этом имеющийся у них относительный дефицит железа в период интенсивного роста и с появлением менструальных кровопотерь может приводить к развитию клинико-гематологических признаков ЖДА. Таким больным показана терапия ПЖ для приема внутрь. Целесообразно использование препаратов, содержащих различные витамины (фенюльс, иррадиан и др.), так как в период интенсивного роста повышается потребность в витаминах группы А,В,С. После восстановления показателей гемоглобина до нормальных значений следует рекомендовать повторные курсы лечения, особенно если устанавливаются обильные месячные или имеются другие незначительные кровопотери (носовые, десневые).
ЖДА у беременных является самым частым патогенетическим вариантом анемий, возникающих во время беременности. Чаще всего ЖДА диагностируется во II — III триместре и требует коррекции лекарственными ПЖ. Целесообразно назначать препараты, содержащие аскорбиновую кислоту (ферроплекс, сорбифер дурулес, актиферин и др.). Содержание аскорбиновой кислоты должно превышать в 2 — 5 раз количество железа в препарате. С учетом этого оптимальными препаратами могут быть ферроплекс и сорбифер дурулес. Суточные дозы двухвалентного железа у беременных с нетяжелыми формами ЖДА могут не превышать 50 мг, так как при более высоких дозах вероятно возникновение различных диспептических расстройств, к которым и без того склонны беременные. Комбинации ПЖ с витамином В 12 и фолиевой кислотой, а также ПЖ, содержащих фолиевую кислоту (фефол, ирровит, мальтоферфол), не оправданы, так как фолиеводефицитная анемия у беременных возникает редко и имеет специфические клинико-лабораторные признаки.
Парентеральный путь введения ПЖ у большинства беременных без специальных показаний следует считать нецелесообразным. Лечение ПЖ при верификации ЖДА у беременных должно проводиться до конца беременности. Это имеет принципиально важное значение не только для коррекции анемии у беременной, но главным образом для профилактики дефицита железа у плода.
По рекомендации ВОЗ все беременные на протяжении II — III триместров беременности и в первые 6 мес лактации должны получать ПЖ.
ЖДА у женщин, страдающих меноррагиями. Независимо от причины меноррагий (миома, эндометриоз, дисфункция яичников, тромбоцитопатии и др.) и необходимости воздействия на соответствующий фактор, необходима длительная терапия ПЖ для приема внутрь. Доза, режим дозирования и конкретный ПЖ подбираются индивидуально с учетом содержания железа в препарате, его переносимости и т.д. При выраженной анемии с клиническими признаками гипосидероза целесообразно назначение препаратов с высоким содержанием двухвалентного железа, что позволяет, с одной стороны, осуществлять адекватную компенсацию дефицита железа, а с другой — облегчает и делает более удобным прием ПЖ (1 — 2 раза в сутки). После нормализации уровня гемоглобина необходимо проводить поддерживающую терапию ПЖ в течение 5 — 7 дней после окончания менструации. При удовлетворительном состоянии и стабильных показателях гемоглобина возможны перерывы в лечении, которые, однако, не должны быть длительными, так как продолжающиеся у женщин меноррагии быстро истощают запасы железа с риском рецидива ЖДА.
Таблица 2. ПЖ для парентерального введения
источник
Распространенность данного заболевания крови в мире трудно оценить. Дело в том, что большинство людей получают достаточное количество фолиевой кислоты с пищей. Даже временная ее нехватка (в течение нескольких недель) не ведет к ярким клиническим проявлениям. В случае же развития анемии и появления характерных симптомов первопричину заболевания не всегда удается обнаружить. В наши дни фолиеводефицитная анемия встречается чаще всего в слаборазвитых странах, для которых актуальна проблема голода, высокая частота заболеваний желудочно-кишечного тракта (ЖКТ), высокая распространенность кишечных паразитов. В развитых странах это заболевание встречается в основном среди так называемых «групп риска» — людей, предрасположенных к развитию такой анемии.
Интересные факты
- Первые описания мегалобластных анемий датируются еще серединой XIX века. Тогда эти анемии называли злокачественными, так как эффективного лечения не существовало, и подавляющее большинство пациентов погибало.
- Первым лекарством от таких анемий стал дрожжевой экстракт, в котором позже обнаружили высокое содержание фолиевой кислоты.
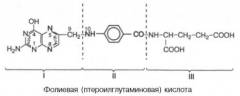
- Впервые фолиевую кислоту как отдельное вещество получили в 1941 году из шпината. Она даже названа была в честь листьев, в которых содержалась (folium с латыни – лист).
- В наши дни смерть на фоне анемии при недостатке фолиевой кислоты возможна только в исключительном случае, при позднем вмешательстве врачей и тяжелых сопутствующих заболеваниях.
- Запасов фолиевой кислоты в здоровом организме хватает примерно на 4 месяца, даже если полностью исключить ее поступление с едой.
- Активная профилактика фолиеводефицитной анемии проводится в обязательном порядке среди беременных и кормящих женщин.
- Примерно 50% фолиевой кислоты, которая содержится в продуктах питания, разрушается при кулинарной обработке. Всасывается в организме тоже лишь 25 – 50% этого вещества.
- В некоторых странах закон обязывает производителей специально добавлять в мучные изделия фолиевую кислоту. Таким образом проводится массовая профилактика анемий среди населения.
Основными задачами эритроцитов являются:
- транспортировка кислорода от легких ко всем органам и тканям;
- транспортировка углекислого газа от тканей к легким;
- транспорт аминокислот (структурные части белков организма);
- транспорт антител и некоторых лекарственных веществ;
- разнесение по организму некоторых токсинов.
Самой важной ролью эритроцитов в обмене веществ является, разумеется, поддержание дыхательной функции. Ее выполнение возможно благодаря особому белку — гемоглобину, который содержится внутри эритроцитов.
Гемоглобин – это сложный белок, содержащий в своей структуре атомы железа. Он находится в цитоплазме эритроцитов и заполняет их объем приблизительно на 96%. Гемоглобин состоит из глобина – белковой части и гема – небелковой части. Одна молекула гема способна перенести четыре молекулы кислорода. Кислород связывается только с двухвалентным железом, в результате чего образуется оксигемоглобин.
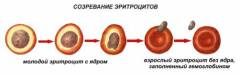
Образование, рост и созревание эритроцитов происходит в костном мозге. Это особая ткань, присутствующая в костях черепа, в ребрах, в грудине и позвоночнике. В детском возрасте он обнаруживается еще в длинных костях рук и ног. Разрушение и гибель эритроцитов происходит в печени и селезенке (большая часть). Прежде чем выйти в кровь, эритроциты проходят стадии роста и дифференцирования. Они получаются в результате цепочки клеточных превращений. Только достигшие зрелости клетки способны выполнять нормально все функции.
На процесс образования и созревания эритроцитов влияют следующие вещества:
- витамин В12;
- фолиевая кислота;
- эритропоэтин;
- железо;
- другие гормоны и ферменты, содержащиеся в костном мозге.
Таким образом, можно заметить, что фолиевая кислота является одним из важных элементов в процессе созревания эритроцитов.
Определенную роль в синтезе и усвоении фолиевой кислоты и витамина В12 играет нормальная микрофлора кишечника. Большинство бактерий, населяющих нижние отделы ЖКТ, с помощью своих ферментов временно связывают, активизируют и даже самостоятельно производят эти вещества.
Всасывание фолиевой кислоты или фолатов (соединений, содержащих эту кислоту) происходит в норме в тощей и в подвздошной кишке. Это наиболее длинные отделы тонкого кишечника. Из-за проблем с желудком может не происходить достаточной выработки гастромукопротеина. Это специальный белок, необходимый для всасывания витамина В12 в кишечнике.
Как уже говорилось, витамин В12 принимает активное участие в развитии анемии. Дело в том, что только в его присутствии возможно превращение фолиевой кислоты в ее активную форму – фолиновую кислоту. Из-за недостатка витамина этого превращения зачастую не происходит, хоть кислота и попадает в организм в нужном количестве. Дефицит В12 и отсутствие активной формы фолиевой кислоты приводят к нарушению синтеза ДНК в кроветворных клетках. В первую очередь страдают так называемые эритробласты (промежуточная форма развития красных кровяных телец — эритроцитов). Нарушается клеточное деление, и эритроциты не приобретают нормальную форму в процессе созревания. Впоследствии эритробласты увеличиваются в размерах и превращаются в так называемые мегалобласты (отсюда название – мегалобластная анемия).
Мегалобласты – это клетки, являющиеся родоначальниками эритропоэза – процесса кроветворения, в ходе которого образуются эритроциты. Они отличаются крупными размерами и аномальной формой. Эритропоэз принимает мегалобластический характер, возвращаясь на путь эмбрионального развития. Мегалобласты редко вызревают до своей конечной формы. Большинство из них погибают и разрушаются в костном мозге, не выходя в кровь. Вследствие этого уровень зрелых эритроцитов значительно падает. Возникают проблемы с переносом кислорода и углекислого газа. Постепенно появляются характерные симптомы, и развивается клиническая картина анемии.
Данная причина встречается в медицинской практике очень часто. Основным источником фолиевой кислоты для человеческого организма являются продукты питания. Если рацион пациента скудный, то это вещество может не поступать в необходимом количестве. Тогда для развития анемии потребуется несколько месяцев (пока не истощатся внутренние запасы фолиевой кислоты). Если же у пациента имеются еще какие-либо заболевания или нарушения, то процесс будет развиваться быстрее. Именно сочетание скудного рациона и определенных хронических патологий ведет к появлению выраженной клинической картины.
Наиболее богаты фолиевой кислотой следующие продукты питания:
- сырые овощи (морковь, шпинат, листья салата и др.);
- бобовые;
- хлеб с отрубями (грубого помола);
- некоторые цитрусовые (особенно авокадо);
- яйца;
- мед;
- дрожжевое тесто;
- некоторые сыры;
- говяжья печень.
Если не употреблять эти продукты, то организм не будет получать нормальной суточной дозы фолиевой кислоты, и ее запасы начнут постепенно истощаться. Следует, однако, отметить, что в небольших количествах это вещество содержится и в других продуктах питания. Поэтому только бедный рацион без других сопутствующих факторов не приведет к выраженным нарушениям на уровне целого организма.
Случаи фолиеводефицитной анемии у маленьких детей отмечались, если их в первый год жизни пытались перевести с молока матери на козье молоко. В отличие от коровьего оно почти не содержит фолиевой кислоты, и, учитывая возраст ребенка, быстро ведет к развитию тяжелой анемии.
Проблемы с ЖКТ являются, вероятно, наиболее распространенной причиной фолиеводефицитной анемии. Дело в том, что даже в полностью здоровом организме усваивается не весь объем этого вещества, поступающий с пищей. Если же на фоне болезней ЖКТ ухудшается пищеварение, усвоение фолиевой кислоты снижается еще больше. Кроме того, сам воспалительный процесс увеличивает потребности организма. При любом воспалении происходит разрушение клеток, а в их восстановлении участвует и фолиевая кислота.
Наиболее распространенными заболеваниями, которые могут привести к фолиеводефицитной анемии, являются:
- гастриты;
- язва желудка или двенадцатиперстной кишки;
- перенесенные операции на ЖКТ (укорачивается кишечник, удаляется часть желудка, в области швов образуется соединительная ткань, и всасывание питательных веществ не происходит);
- хронические гепатиты или цирроз печени;
- хронические энтериты и гастроэнтериты;
- болезнь Крона;
- непереносимость глютена (целиакия);
- другие заболевания, сопровождающиеся синдромом мальабсорбции (нарушением всасывания).
При всех этих патологиях может иметь место повреждение слизистой оболочки тонкого кишечника. Из-за этого нарушается всасывание питательных веществ в целом и фолиевой кислоты в частности. Людей, страдающих вышеперечисленными болезнями, относят к так называемой группе риска. Им рекомендуется сдавать анализ крови не реже чем раз в 6 месяцев, чтобы обнаружить признаки анемии на ранних стадиях.
Бактерии, в норме населяющие кишечник человека, являются симбиотическими. Это значит, что они способны приносить определенную пользу хозяину. Одной из их функций является участие в метаболизме витамина В12 и фолиевой кислоты. Безобидная микрофлора кишечника способствует выделению этих веществ из продуктов питания и их легкому всасыванию эпителием кишечника. Доказано, что некоторые виды микробов способны даже сами синтезировать витамины.
При дисбактериозе кишечника нарушается нормальное содержание полезных микроорганизмов. Их место занимают болезнетворные (патогенные) бактерии. Эти бактерии уже не способствуют всасыванию витаминов из кишечника. Поэтому при длительном дисбактериозе могут обнаруживаться проблемы с образованием эритроцитов. Чаще всего они не вызывают тяжелые формы болезни.
Причинами дисбактериоза кишечника могут быть:
- тяжелые кишечные инфекции (сальмонеллез, дизентерия, эшерихиоз и др.);
- длительное применение антибиотиков;
- острые и хронические заболевания ЖКТ;
- заболевания печени и болезни поджелудочной железы;
- нарушения иммунной системы.
Еще более тяжелое течение болезнь принимает при некоторых паразитарных инфекциях. Паразиты представляют собой многоклеточные организмы, которые живут и размножаются в теле хозяина, но не приносят ему никакой пользы. Некоторые паразиты поглощают сами всю фолиевую кислоту и другие витамины, попадающие с пищей. Из-за этого анемия развивается быстрее, а состояние пациента становится все более тяжелым. Доказано, что особо характерны мегалобластные анемии при дифиллоботриозе. Особи этого паразита могут достигать очень больших размеров, до нескольких метров в длину. Даже одного такого паразита достаточно, чтобы вызвать тяжелую анемию.
В ряде случаев фолиеводефицитная анемия может развиться даже при нормальном поступлении этого вещества и при условии нормального всасывания. Дело в том, что существует ряд физиологических и патологических состояний, при которых организму требуется повышенное количество фолиевой кислоты в связи с ее повышенным расходом. Чаще всего таким особым состояниям становится беременность.
Во время роста и развития плода идет активное деление клеток. При этом происходит усиленное потребление фолиевой кислоты. Материнскому организму приходится обеспечивать этим веществом и растущего ребенка. Считается, что в период беременности и лактации потребности матери в фолиевой кислоте возрастают в полтора — два раза. При ее нехватке будет страдать как материнский организм (развитие мегалобластной анемии), так и организм еще не рожденного ребенка (высокая вероятность различных пороков развития). Таким образом, беременные и кормящие женщины также относятся к группе риска.
Некоторые авторы замечают аналогичный механизм развития анемии при некоторых хронических воспалительных заболеваниях. Специальные исследования, например, показали, что при псориазе также расходуется фолиевая кислота и повышен риск развития мегалобластной анемии. Также это возможно при злокачественных опухолях, некоторых видах дерматитов.
Прием некоторых лекарственных средств может сильно снижать всасывание фолиевой кислоты в кишечнике либо увеличивать ее потребление организмом. Это происходит не только при неправильном приеме (передозировке), но даже в нормальных дозах, предписанных лечащим врачом.
Препаратами, которые могут вызвать фолиеводефицитную анемию, являются:
- дифенин;
- фенобарбитал;
- метотрексат;
- триамтерен;
- циклосерин;
- изониазид.
Проблема заключается в том, что отмена этих препаратов приведет к резкому ухудшению состояния пациента. Длительные курсы лечения вышеперечисленными медикаментами назначаются при судорожном синдроме, туберкулезе, злокачественных опухолях и др. Все эти заболевания имеют значительно более плохой прогноз, чем фолиеводефицитная анемия. Единственно верным решением в таких случаях является параллельное назначение препаратов фолиевой кислоты для профилактики анемии. Периодически берется анализ крови для оценки количества эритроцитов и гемоглобина.
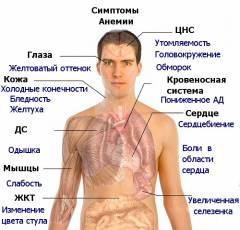
Анемический синдром объясняется нарушением транспорта кислорода к органам, вызванным уменьшением содержания гемоглобина и/или эритроцитов в единице объема крови. Наиболее выраженными являются нарушения в работе сердечно-сосудистой, дыхательной и центральной нервной систем. Несколько меньшее значение имеют изменения со стороны кожи и ее придатков. Данный синдром является общим для всех анемий, независимо от механизма их возникновения.
Возможными проявлениями анемического синдрома при фолиеводефицитной анемии являются:
- слабость;
- головокружение;
- шум в ушах;
- одышка;
- тахикардия;
- пальпитации;
- бледность кожи с желтушным оттенком;
- ломкость ногтей и сухость кожи.
Сухость кожи и поражение ее придатков (ногтей и волос) являются проявлениями атрофии. Из-за длительных нарушений в поставке кислорода клетки не производят структурные вещества. Процессы регенерации, увлажнения кожи, образования новых клеток замедлены. Ногти становятся ломкими, слоятся, тяжело и долго растут. Волосы теряют блеск, становятся сухими и безжизненными. Даже мелкие царапины могут заживать неделями. Без адекватного лечения повышается риск развития бактериальной или грибковой инфекции.
Желудочно-кишечный синдром обусловлен нарушением функций печени, желудка и кишечника. Чаще всего он не является следствием самой анемии, а развивается параллельно. Как уже отмечалось выше, причиной анемии может быть нарушение всасывания фолиевой кислоты на уровне ЖКТ. Эти-то заболевания и проявляются желудочно-кишечным синдромом. Однако, в редких случаях, при выраженной анемии может нарушаться кровоснабжение слизистой оболочки ЖКТ. Тогда ее клетки уплощаются, и всасывание питательных веществ нарушается.
При фолиеводефицитной анемии основными методами диагностики являются:
- общий анализ крови;
- биохимический анализ крови;
- общий анализ мочи;
- анализ на фолиевую кислоту;
- пункция костного мозга;
- паразитологический анализ кала;
- специальные анализы крови;
- рентгенография;
- фиброэзофагогастродуоденоскопия (ФЭГДС).
Общий анализ крови является важнейшим анализом, который подтверждает наличие анемии и помогает определить степень тяжести патологического процесса. Во время лечения он назначается, чтобы определить динамику состояния больного.
Общий анализ крови представляет собой лабораторное исследование, позволяющее получить информацию о картине всех форменных элементов крови. Кровь для общего анализа берется из пальца (капиллярная кровь). Исследование желательно проводить в первой половине дня. На результаты не влияет прием пищи, но может повлиять обезвоживание.
При диагностике фолиеводефицитной анемии наиболее важными являются следующие показатели:
- Уровень гемоглобина. В норме в крови человека должно содержаться от 120 до 160 г/л. Этот показатель может отличаться в зависимости от пола, возраста и при некоторых физиологических состояниях, таких как беременность или кормление грудью. При анемии уровень гемоглобина падает ниже нормального уровня. Для женщин среднего возраста этой границей будет служить уровень в 120 г/л, для мужчин среднего возраста – 130 г/л, для беременных и кормящих женщин допустим показатель 110 г/л. Снижение его уровня ниже 70 г/л соответствует тяжелой анемии (III степени), которая представляет опасность для жизни.
- Количество эритроцитов. Количество эритроцитов определяется на единицу объема крови. В норме оно составляет 3,7 – 4,9 × 10 12 в 1 л. Возможны колебания границ в зависимости от возраста, при беременности или при кормлении грудью. При фолиеводефицитной анемии количество эритроцитов снижается ниже наименьшего значения нормы для данного возраста и пола. Помимо общего количества красных кровяных телец общий анализ крови позволяет оценить форму и размер эритроцитов. Все эти характеристики могут в разной степени изменяться при различных видах анемии, что помогает в дифференциальной диагностике (различия анемий между собой). Например, в легких случаях количество эритроцитов может и не снижаться, но начинают появляться аномальные формы этих клеток (пойкилоцитоз).
- Цветовой показатель. Цветовой показатель характеризует насыщенность эритроцитов гемоглобином. В норме он должен быть в пределах 0,85 – 1,15. При анемии этот показатель понижается ниже нижней границы нормы. Это говорит о плохом насыщении эритроцитов гемоглобином. То есть, клетки либо не созрели до конца, либо настолько изменены, что не могут присоединить молекулы гемоглобина. В обоих случаях они будут неспособны переносить достаточное количество кислорода.
- Уровень тромбоцитов. Одним из специфических осложнений может стать изменение уровня тромбоцитов. Его следует определить заранее, чтобы при необходимости предупредить образование тромбов или возможные кровотечения.
- Уровень лейкоцитов. Уровень лейкоцитов при мегалобластных анемиях может быть снижен. Характерным признаком является так называемая гиперсегментация нейтрофилов. Под микроскопом их ядра имеют не 3 – 4, а 6 и более сегментов. Могут встречаться клетки нейтрофильного типа, но больших размеров.
- Уровень ретикулоцитов. Проводится не при всех заболеваниях. При анемиях он может быть понижен.
Этот анализ не является специфическим исследованием в диагностике фолиеводефицитной анемии. Он позволяет составить полноценную картину о состоянии организма на данный момент. Ввиду того, что при фолиеводефицитной анемии нарушается функции печени, желудка и тонкого кишечника, в результатах биохимического анализа будут изменения, характерные для пораженного какого-либо органа. Забор крови на биохимический анализ крови производится натощак из вены.
Наиболее важными показателями являются:
- мочевина;
- креатинин;
- билирубин (свободный и связанный);
- печеночные трансаминазы;
- амилаза;
- глюкоза;
- белки крови.
Изменения этих показателей будут указывать на проблемы с печенью, почками, поджелудочной железой или другие заболевания. О них необходимо знать, так как они могут быть первопричиной анемии. Во-вторых, наличие острых и хронических заболеваний, даже не связанных с основным диагнозом, влияет на подбор лечения.
Существует и специальный анализ для определения фолиевой кислоты в крови. Его проводят при подозрении на мегалобластную анемию (понижение уровня гемоглобина и эритроцитов с соответствующими клиническими симптомами). В норме содержание фолиевой кислоты в сыворотке крови колеблется между 3 и 16 нг/л. Этот анализ требует применения специальных химических реактивов и проводится далеко не во всех лабораториях.
Современные методы диагностики позволяют раздельно определять концентрацию фолиевой кислоты в сыворотке и внутри эритроцитов (здесь она колеблется от 100 до 425 нг/л). Для этого используются радиоиммунологические методы. Из-за высокой стоимости они пока что редко применяются в медицинской практике.
Если обнаруживается недостаток фолиевой кислоты, рекомендуется проверить также уровень витамина В12. Чтобы диагностировать его недостаток проверяют два основных показателя. Нормальный уровень самого витамина В12 в крови колеблется между 160 и 700 пг/л. Для второго вещества — гомоцистеина, норма составляет 5 – 15 ммоль/л.
Из менее дорогостоящих анализов для определения фолиевой кислоты иногда проводят специальный микробиологический тест. Он позволяет отличить анемии при дефиците фолиевой кислоты от других мегалобластных анемий (при дефиците витамина В12). В ходе этого теста измерения проводят косвенно, исследуя нормальную микрофлору тонкого кишечника. В качестве тестового микроба можно брать Streptococcus faecalis или Lactobacillus casei.
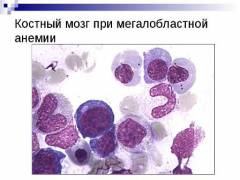
Пункция костного мозга проводится обычно на уровне грудины. Ее выполняют в гематологических отделениях специальной иглой после предварительной подготовки пациента. Целью исследования является оценка гемопоэза (процесса созревания кровяных телец). Пунктат исследуют под микроскопом, применяя различные методы окраски. В результате обнаруживаются гигантские мегалобластные клетки. Это говорит о наличии мегалобластного типа гемопоэза, и вкупе с низким уровнем фолиевой кислоты подтверждает диагноз.
Для получения достоверного результата при пункции нужно иметь в виду, что на фоне лечения мегалобластный тип гемопоэза может исчезнуть уже на 2 – 3 день. Поэтому пункция делается до начала приема препаратов фолиевой кислоты.
К специальным анализам крови в данном случае будет относиться определение группы крови и резус-фактора Rh (позитивный или негативный). Это необходимо не только для госпитализации. Дело в том, что пациентам с анемией в перспективе может понадобиться срочное переливание крови. Чтобы не тратить время на ее определение потом, группу рекомендуется определять при первом обращении к врачу.
Из этих же соображений проводятся серологические тесты на антитела к наиболее опасным инфекциям, которые могут передаваться с кровью. Это инфекция ВИЧ/СПИД, а также вирусные гепатиты В и С.
Рентгенография с контрастом может быть назначена для выявления заболеваний ЖКТ. Контраст представляет собой кашицеобразную массу, содержащую барий. Эта масса при проглатывании равномерно распределяется по стенкам пищевода, желудка, двенадцатиперстной кишки. После этого на рентгеновском снимке верхние отделы ЖКТ становятся хорошо видны. Данное исследование является недорогим и безопасным для пациента. Единственная проблема может быть с проглатыванием контрастного вещества (у некоторых пациентов при этом возникает рвотный рефлекс). Тогда возможно введение контраста через специальный катетер.
С помощью рентгенологического исследования иногда можно заподозрить язву желудка, двенадцатиперстной кишки, наличие сужений или расширений пищеварительного тракта на разных уровнях. Это помогает определить первопричину заболевания, объясняя плохое всасывание фолиевой кислоты.
ФЭГДС является одним из самых информативных исследований при заболеваниях верхних отделов ЖКТ. При нем врач вводит в пищевод пациента специальный аппарат (фиброскоп). Это достаточно толстый гибкий провод с маленькой камерой на конце. Камера по мере продвижения вниз по ЖКТ передает изображение на монитор. Врач может своими глазами оценить состояние слизистой оболочки, выявить наличие патологических сужений, расширений или других проблем. В рамках диагностики при фолиеводефицитной анемии это исследование назначают, чтобы найти первопричину болезни. Как уже говорилось выше, это могут быть гастриты, гастродуодениты, язва желудка и другие патологии верхних отделов ЖКТ.
ФЭГДС является достаточно сложным и неприятным для пациента исследованием. Даже при предварительном обезболивании и приеме противорвотных препаратов процедура может быть болезненной. Перед ней нельзя принимать пищу или пить, чтобы уменьшить вероятность рвоты во время введения прибора. В связи с этим ФЭГДС назначают далеко не всем пациентам с анемией. Она показана только при наличии других симптомов со стороны ЖКТ (рвота, тошнота, длительные запоры или диарея). Если же их нет, а анемия хорошо поддается лечению, это исследование не проводят.

Госпитализация пациента рекомендуется в следующих случаях:
- тяжелые анемии с уровнем гемоглобина менее 70 г/л;
- больные преклонного возраста (старше 60 лет);
- больные с тяжелыми сопутствующими заболеваниями;
- сопутствующий недостаток витамина В12;
- трудности в постановке окончательного диагноза;
- наличие осложнений.
В этих случаях больного рекомендуется госпитализировать для полноценного обследования. Обычно в условиях стационара лишь начинают лечение. После постановки окончательного диагноза и ликвидации самой анемии пациента выписывают (при отсутствии осложнений и сопутствующих болезней на 2 – 3 день).
Само лечение во многом зависит от состояния пациента. Решающую роль играют причины заболевания и уровень гемоглобина при обращении к врачу. Принципы лечения в амбулаторных условиях и в условиях стационара одни и те же.
Лечение фолиеводефицитной анемии предполагает следующие методы:
- устранение причины анемии;
- восстановление уровня эритроцитов;
- лечение препаратами фолиевой кислоты;
- профилактика анемии.
Данное направление в лечении может считаться главным, так как даже переливания крови и препараты фолиевой кислоты будут лишь временной мерой, если не устранить причину болезни. Если из анамнеза (опроса) больного следует, что причиной могло стать неправильное питание, пациенту попросту объясняют особенности диеты. Более сложные методы лечения могут понадобиться, если фолиеводефицитная анемия развилась вторично, на фоне других заболеваний.
Лечение причин анемии может проводиться следующим образом:
- Противопаразитарные препараты. Если анализ кала указывает на присутствие паразитов или чрезмерное развитие болезнетворных микробов, назначаются соответственно противопаразитарные препараты или антибиотики. Выбор конкретного медикамента зависит от того, какой микроорганизм или паразит обнаружен. Лечение обычно длится 1 – 2 недели, после чего необходимо еще несколько недель на восстановление нормальной микрофлоры кишечника.
- Лечение заболеваний ЖКТ. Если у больного имеются заболевания желудки или кишечника, которые препятствуют нормальному усвоению фолиевой кислоты, необходимо провести их полноценное лечение. Оно может заключаться в антибиотикотерапии (при язве желудка, вызванной Helicobacter Pylori), назначении противовоспалительных препаратов. При нарушениях работы поджелудочной железы назначают ферментные препараты. Может потребоваться и хирургическое лечение. Однако следует учитывать, что удаление верхних отделов тонкой кишки только усугубит дефицит фолиевой кислоты.
- Лечение дисбактериоза. Лечение дисбактериоза кишечника проводится специальными препаратами — эубиотиками. Кроме того, при этом нужно придерживаться специальной диеты. Обычно лечение дисбактериоза (при отсутствии хронических инфекций ЖКТ) длится несколько недель.
- Лечение алкоголизма. Из всех причин фолиеводефицитной анемии алкоголизм является, возможно, наиболее серьезной. До сих пор лечение данной проблемы сопряжено с множеством трудностей. Эффективную помощь при данной проблеме могут оказать врачи-наркологи. Она включает не только медикаментозное лечение, но также психотерапевтическую помощь, благоприятный социальный фон.
После устранения причины фолиеводефицитной анемии состояние пациентов обычно быстро улучшается. Прием необходимых лекарств восстанавливает уровень эритроцитов и гемоглобина, симптомы постепенно исчезают.
Экстренное восстановление уровня эритроцитов в крови проводится путем переливания донорской крови. Чаще всего при этом используется специальный концентрат — так называемая эритроцитарная масса. Дело в том, что при фолиеводефицитной анемии нет потерь жидкости, как при кровотечениях. Переливание обычной донорской крови восстановит уровень эритроцитов и гемоглобина, но приведет к перегрузке организма жидкостью.
Переливания крови необходимы только в очень тяжелых случаях или при серьезных сопутствующих заболеваниях. Если нет прямой угрозы для жизни, то гемотрансфузия при фолиеводефицитной анемии считается неоправданным риском. В случае необходимости переливание делается только в отделении интенсивной терапии в присутствии врача-реаниматолога. Это объясняется относительно высокой частотой тяжелых осложнений.
Основным лечением при анемии, вызванной недостатком фолиевой кислоты, является использование препаратов, содержащих это вещество. В более легких случаях назначают 1 – 5 мг фолиевой кислоты перорально (в виде таблеток). При невозможности перорального приема (тяжелые заболевания ЖКТ с нарушением всасывания) возможно также внутривенное или внутримышечное введение в аналогичных дозах. Курс лечения длится в среднем 4 – 6 недель. За этот период постепенно растет уровень гемоглобина в крови, и исчезают симптомы. Первые изменения в лучшую сторону можно заметить уже на 5 – 7 день лечения.
В тяжелых случаях, при затруднениях в постановке диагноза, лечение начинают с увеличенных доз (беременным перорально до 15 мг/сут в первые дни). Одновременно назначают препараты витамина В12. Длительность лечения может составлять до 2 – 3 месяцев. Единственным адекватным критерием выздоровления является нормальный уровень эритроцитов и гемоглобина в крови при повторных анализах крови. Эти анализы должны проводиться регулярно (раз в 6 месяцев в течение 3 лет).
Как следует из всего вышеперечисленного, фолиеводефицитная анемия не предполагает серьезного развернутого лечения. Также в наши дни она редко представляет серьезную опасность для жизни пациентов. Однако при данном заболевании может возникать ряд других проблем, которые отразятся на здоровье и благополучии пациента. В связи с этим рекомендуется обращать больше внимания на профилактику фолиеводефицитной анемии. У беременных и кормящих женщин в соответствии с рекомендациями Всемирной Организации Здравоохранения (ВОЗ) она проводится в обязательном порядке (до 5 мг/сут перорально).
В целом профилактика фолиеводефицитной анемии основывается на следующих принципах:
- адекватное питание (продукты, содержащие фолиевую кислоту);
- профилактический прием фолиевой кислоты (по назначению врача, для пациентов, у которых повышен риск ее возникновения);
- умеренное употребление алкоголя;
- употребление лекарств только в дозах, назначенных лечащим врачом;
- своевременная диагностика и лечение хронических заболеваний.
Сопутствующими нарушениями при фолиеводефицитной анемии могут быть:
- невропатия;
- повышенная свертываемость крови;
- нарушение созревания сперматозоидов;
- врожденные нарушения развития.
У пациентов с выраженной анемией на фоне нехватки фолиевой кислоты повышен риск образования тромбов. Это объясняется повышенным (реже пониженным) уровнем тромбоцитов, который наблюдается у многих пациентов. В связи с этим необходимо проведение тестов на свертываемость крови. Если они показывают склонность к образованию тромбов, в лечение анемии добавляют антикоагулянты (вещества, препятствующие свертыванию крови).
Непосредственно тромбоз у пациентов с фолиеводефицитной анемией встречается не так часто. Для этого осложнения необходимо наличие и других заболеваний (варикозное расширение вен, сердечные аритмии).
Врожденные нарушения развития у детей являются наиболее серьезным последствием фолиеводефицитной анемии у их матерей во время беременности. Дело в том, что фолиевая кислота очень важна для развивающегося плода. При недостаточном поступлении этого вещества в организм могут возникнуть проблемы с развитием костной и нервной систем. Наиболее специфичным именно для фолиеводефицитной анемии является незаращение канала костного мозга, гидроцефалия, анэнцефалия. Могут наблюдаться и другие аномалии развития.
Помимо пороков развития плода, вызванных недостатком фолиевой кислоты, в тяжелых случаях наступают проблемы с течением беременности. Эти проблемы уже вызваны низким уровнем эритроцитов и гемоглобина в крови. При анемии II – III степени наблюдается хроническая гипоксия плода. Из-за этого он медленнее растет и набирает вес. Повышается вероятность преждевременных родов, токсикоза, отслойки плаценты и других осложнений беременности.
Из вышеперечисленных проблем только врожденные аномалии развития у детей являются необратимыми. Поэтому в большинстве стран проводят специфическую профилактику фолиеводефицитной анемии на протяжении беременности. Остальные же осложнения являются обратимыми и постепенно исчезают по ходу курса лечения.
источник