Железодефицитная анемия – клинико-гематологический синдром, обусловленный недостатком железа в организме человека, что влечет нарушение нормального синтеза гемоглобина и гипоксию тканей.
Патология широко распространена. По статистическим данным, у 8-10% женщин детородного возраста диагностируется железодефицитная анемия, а у 30% женщин – латентный дефицит железа. В раннем детском возрасте признаки железодефицитной анемии выявляются у каждого второго ребенка. В структуре всех анемий на долю железодефицитной приходится 90%.
В основе развития железодефицитной анемии лежит отрицательный баланс обмена железа. К этому могут приводить разные факторы, но чаще всего причиной дефицита железа становится хроническая кровопотеря:
- кровотечения из геморроидальных узлов или анальных трещин;
- дисфункциональные маточные кровотечения;
- обильные менструации;
- желудочно-кишечные кровотечения (из эрозий и язв слизистой оболочки желудка или кишечника).
Другие причины кровопотери:
- гельминтозы;
- гемосидероз легких;
- геморрагические диатезы (болезнь Виллебранда, гемофилия);
- гемоглобинурия;
- обширные травмы и операции;
- частая сдача крови (донорство).
Нередко железодефицитная анемия развивается и у пациентов с хронической почечной недостаточностью, находящихся на программном гемодиализе.
При железодефицитных состояниях происходит снижение активности IgA; в результате у пациентов зачастую возникают кишечные и респираторные инфекции.
Недостаток железа в организме также может сформироваться в результате недостаточного поступления его из пищи по следующим причинам:
- низкий уровень жизни;
- вегетарианство;
- соблюдение диеты, ограничивающей употребление мясных продуктов;
- анорексия;
- искусственное вскармливание детей грудного возраста, особенно при позднем введении прикорма.
Ряд заболеваний и патологических состояний органов пищеварительной системы может приводить к нарушению всасывания железа и развитию железодефицитной анемии:
- гастерэктомия;
- состояние после резекции тонкой кишки;
- синдром мальабсорбции;
- хронический энтерит;
- гипоацидный гастрит;
- кишечные инфекции.
Железодефицитная анемия развивается и у пациентов, страдающих хроническими гепатитами или циррозом печени. В данном случае нарушается транспорт железа из депо.
Железодефицитная анемия может также появиться на фоне повышенной потребности в железе (в период полового созревания, беременности либо лактации) или при значительных потерях этого элемента (при онкологических, инфекционных заболеваниях).
В зависимости от причины железодефицитные анемии делятся следующим образом:
- алиментарные;
- постгеморрагические;
- связанные с нарушением транспорта железа, недостаточностью его резорбции или повышенным расходом;
- обусловленные врожденным (исходным) дефицитом железа.
По степени выраженности лабораторных и клинических признаков железодефицитные анемии бывают:
- легкими (гемоглобин выше 90 г/л);
- средней тяжести (гемоглобин от 70 до 90 г/л);
- тяжелыми (гемоглобин менее 70 г/л).
Железодефицитная анемия легкой степени в большинстве случаев протекает без-каких либо клинических проявлений или с минимальной их выраженностью. Тяжелая форма сопровождается развитием гематологического, сидеропенического и циркуляторно-гипоксического синдромов.
В течении железодефицитной анемии выделяют несколько стадий:
- Предлатентный железодефицит – истощается депонированное железо, гемоглобиновые и транспортные запасы сохранены.
- Латентный железодефицит – происходит снижение запасов содержащегося в плазме крови транспортного железа.
- Собственно железодефицитная анемия – истощение всех метаболических запасов железа (эритроцитарного, транспортного и депонированного).
В клинической картине железодефицитной анемии выделяют синдромы:
- циркуляторно-гипоксический;
- сидеропенический;
- астеновегетативный.
Возникающие на фоне железодефицитной анемии циркуляторно-гипоксические нарушения ухудшают течение сопутствующих заболеваний сердечно-сосудистой и дыхательных систем.
Развитие циркуляторно-гипоксического синдрома обусловлено нарушением синтеза гемоглобина, в результате чего страдает транспорт кислорода и развивается тканевая гипоксия. Клинически это проявляется:
- общей слабостью;
- сонливостью;
- головокружениями;
- шумом в ушах;
- преходящими обмороками;
- учащенным сердцебиением;
- повышенной чувствительностью к низкой температуре;
- одышкой, возникающей при физических нагрузках, а при тяжелой анемии – и в состоянии покоя.
Механизм развития сидеропенического синдрома связан с дефицитом железосодержащих тканевых ферментов (цитохромов, пероксидазы, каталазы). Недостаток названных ферментов становится причиной наблюдаемых на фоне железодефицитной анемии трофических расстройств со стороны слизистых оболочек и кожных покровов. Признаки сидеропенического синдрома:
- сухость кожи;
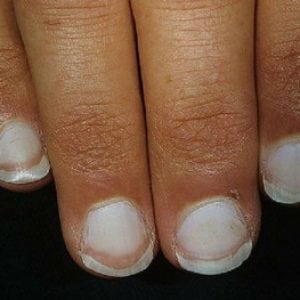
- деформация, повышенная ломкость и поперечная исчерченность ногтей;
- выпадение волос;
- атрофический гастрит;
- дисфагия;
- ангулярный стоматит;
- глоссит;
- искажения вкуса (желание употреблять в пищу несъедобные предметы, например глину или зубной порошок);
- дизурические расстройства;
- диспепсия;
- мышечная слабость.
Астеновегетативный синдром характеризуется эмоциональной лабильностью, повышенной раздражительностью, ухудшением памяти, снижением работоспособности.
Клиническая картина железодефицитной анемии у детей неспецифична, преобладает один из следующих синдромов:
- Астеновегетативный. Связан с кислородным голоданием тканей нервной системы. Проявляется снижением мышечного тонуса и задержкой психомоторного развития ребенка. При тяжелой степени железодефицитной анемии и отсутствии необходимой терапии возможна интеллектуальная недостаточность. К другим проявлениям астеновегетативного синдрома относят энурез, обморочные состояния, головокружение, раздражительность и плаксивость.
- Эпителиальный. Характеризуется изменениями со стороны кожи и ее придатков. Кожные покровы становятся сухими, в области коленей и локтей развивается гиперкератоз, волосы теряют блеск и активно выпадают. Часто развиваются хейлит, глоссит, ангулярный стоматит.
- Диспепсический. Снижается аппетит вплоть до полного отказа от еды, наблюдаются неустойчивость стула (поносы, чередующиеся с запорами), вздутие живота, дисфагия.
- Сердечно-сосудистый. Развивается на фоне тяжелой железодефицитной анемии и проявляется одышкой, снижением артериального давления, тахикардией, шумами в сердце и дистрофическими изменениями в миокарде.
- Синдром иммунодефицита. Характеризуется немотивированным повышением температуры до субфебрильных значений. Дети подвержены респираторным кишечным инфекциям с тяжелым и (или) затяжным течением.
- Гепатолиенальный. Наблюдается на фоне выраженной железодефицитной анемии, особенно сочетающейся с другими видами анемий или рахитом. Проявляется увеличением размеров печени и селезенки.
В раннем детском возрасте признаки железодефицитной анемии выявляются у каждого второго ребенка.
Диагностика состояния, а также определение степени его тяжести осуществляются по результатам лабораторных исследований. Для железодефицитной анемии характерны следующие изменения:
- снижение содержания гемоглобина в крови (норма для женщин – 120–140 г/л, для мужчин – 130–150 г/л);
- пойкилоцитоз (изменение формы эритроцитов);
- микроцитоз (наличие в крови аномально маленьких по своим размерам эритроцитов);
- гипохромия (цветовой показатель – менее 0,8);
- снижение концентрации сывороточного железа (норма для женщин – 8,95–30,43 мкмоль/л, для мужчин – 11,64–30,43 мкмоль/л);
- уменьшение концентрации ферритина (норма для женщин – 22–180 мкг/л, для мужчин – 30–310 мкг/л);
- уменьшение насыщения трансферрина железом (норма – 30%).
Для эффективного лечения железодефицитной анемии важно установить причину, ее вызвавшую. С целью обнаружения источника хронической кровопотери показано проведение:
- ФЭГДС;
- рентгенографии желудка с контрастированием;
- колоноскопии;
- ирригоскопии;
- ультразвукового исследования органов малого таза;
- исследования кала на скрытую кровь.
По статистическим данным, у 8-10% женщин детородного возраста диагностируется железодефицитная анемия, а у 30% женщин – латентный дефицит железа.
В сложных диагностических случаях выполняют пункцию красного костного мозга с последующим гистологическим и цитологическим исследованием полученного пунктата. Значительное снижение в нем сидеробластов свидетельствует о наличии железодефицитной анемии.
Дифференциальная диагностика проводится с другими видами гипохромных анемий (талассемией, сидеробластной анемией).
Принципы терапии железодефицитной анемии:
- устранение источника хронической кровопотери;
- коррекция рациона;
- восполнение недостатка железа.
Важную роль играет диетотерапия. В рацион включают язык, печень, мясо кролика, баранину, говядину, телятину – продукты, богатые гемовым железом. Для улучшения всасывания железа из желудочно-кишечного тракта необходимы аскорбиновая, янтарная и лимонная кислоты, которые в большом количестве содержатся в свежих фруктах и ягодах. Исключают шоколад, молоко, соевый протеин, чай, кофе, поскольку они ингибируют всасывание железа.
Но только лишь диетой восполнить уже образовавшийся дефицит железа невозможно. Пациенты с железодефицитной анемией проходят заместительную терапию ферропрепаратами длительным курсом (не менее 2-2,5 месяцев).
При тяжелой форме железодефицитной анемии и выраженном циркуляторно-гипоксическом синдроме возникают показания к проведению гемотрансфузии.
Возникающие на фоне железодефицитной анемии циркуляторно-гипоксические нарушения ухудшают течение сопутствующих заболеваний сердечно-сосудистой и дыхательных систем.
При железодефицитных состояниях происходит снижение активности IgA; в результате у пациентов зачастую возникают кишечные и респираторные инфекции.
На фоне длительного течения тяжелой формы железодефицитной анемии у больных может развиться миокардиодистрофия.
Прогноз благоприятный при условии своевременной коррекции дефицита железа и устранения причины развития анемии.
Профилактика железодефицитной анемии включает:
- полноценное рациональное питание;
- ежегодный контроль содержания гемоглобина в крови;
- своевременное устранение источников хронической кровопотери;
- профилактический прием препаратов железа лицами из группы риска.
Видео с YouTube по теме статьи:
Образование: окончила Ташкентский государственный медицинский институт по специальности лечебное дело в 1991 году. Неоднократно проходила курсы повышения квалификации.
Опыт работы: врач анестезиолог-реаниматолог городского родильного комплекса, врач реаниматолог отделения гемодиализа.
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
источник
В.Ю. Сельчук, С.С. Чистяков, Б.О. Толокнов, Л.В. Манзюк, мгмсу М.П. Никулин, Т.В. Юрьева, П.В. Кононец, Г.В. Титова
МГМСУ
Реферат: обсуждаются вопросы современного лечения железодефицитных анемий, включая препарат для внутривенного введения — карбоксимальтозат железа, который быстро восстанавливает дефицит железа, не вызывает реакции гиперчувствительности, характерные для препаратов, содержащих декстран, и обеспечивает медленное высвобождение железа, что снижает риск токсических эффектов.
Ключевые слова: железодефицитная анемия, лечение, карбоксимальтозат железа
Анемия — это клинико-гематологический синдром, характеризующийся уменьшением количества эритроцитов и гемоглобина в крови. Снижение содержания гемоглобина до уровня менее 120 г/л рассматривается как анемия [Aapro, 2008]. Самые разнообразные физиологические и патологические процессы могут служить основой развития анемических состояний, в связи с чем анемии в большинстве случаев рассматриваются как симптом, а не основное заболевание. Анемии наблюдаются при многих терапевтических, хирургических, онкологических и других заболеваниях. Различают железодефицитные, сидероахрестические (с избытком железа), В12— и фолиеводефицитные, гемолитические, анемии при костномозговой недостаточности, постгеморрагические, анемии, связанные с перераспределением железа, комбинированные анемии. Однако 80% всех анемий связано с дефицитом железа. Железо в организме человека участвует в регуляции обмена веществ, в процессах переноса кислорода, в тканевом дыхании и оказывает огромное влияние на состояние иммунологической резистентности.
Почти все железо в организме человека входит в состав различных белков и ферментов. Можно выделить две его основные формы: гемовое (входящее в состав гема — составной части гемоглобина и миоглобина) и негемовое. Железо гема мясных продуктов всасывается без участия соляной кислоты. Однако ахилия может в определенной мере способствовать развитию железодефицитной анемии (ЖДА) при наличии значительных потерь железа и высокой потребности в нем.
Всасывание железа осуществляется преимущественно в двенадцатиперстной кишке и верхних отделах тощей кишки. Степень всасывания железа зависит от потребности организма в нем. При выраженном дефиците железа всасывание его может происходить и в остальных отделах тонкого кишечника. При уменьшении потребности организма в железе происходит снижение скорости поступления его в плазму крови и увеличивается отложение в энтероцитах в виде ферритина, который элиминируется при физиологическом слущивании эпителиальных клеток кишечника. В крови железо циркулирует в комплексе с плазменным трансферрином. Этот белок синтезируется преимущественно в печени. Трансферрин захватывает железо из энтероцитов, а также из депо в печени и селезенке и переносит его к рецепторам на эритрокариоцитах костного мозга. В норме трансферрин насыщен железом приблизительно на 30%. Комплекс трансферрин-железо взаимодействует со специфическими рецепторами на мембране эритрокариоцитов и ретикулоцитов костного мозга, после чего путем эндоцитоза проникает в клетки, и железо переносится в их митохондрии, где включается в протопорфирин и таким образом участвует в образовании гема. Освободившийся от железа трансферрин неоднократно участвует в переносе железа. Количество железа, которое расходуется на эритропоэз, составляет 25 мг/сут., что значительно превышает возможности всасывания железа в кишечнике. В связи с этим для гемопоэза постоянно используется железо, освобождающееся при распаде эритроцитов в селезенке. Хранение (депонирование) железа осуществляется в депо в составе белков ферритина и гемосидерина.
Наиболее распространенная форма депонирования железа в организме — ферритин. Ферритин представляет собой водорастворимый гликопротеиновый комплекс, в центре которого расположено железо, покрытое белковой оболочкой из апоферритина. Каждая молекула ферритина содержит от 1000 до 3000 атомов железа. Ферритин определяется почти во всех органах и тканях, но наибольшее его количество обнаруживается в макрофагах печени, селезенки, костного мозга, эритроцитах, сыворотке крови, слизистой оболочке тонкой кишки. При нормальном балансе железа в организме устанавливается своеобразное равновесие между содержанием ферритина в плазме и депо (прежде всего в печени и селезенке). Уровень ферритина в крови отражает количество депонированного железа. Ферритин создает запасы железа в организме, которые могут быстро мобилизоваться при повышении потребности тканей в железе.
Другая форма депонирования железа — гемосидерин. Это малорастворимое производное ферритина с более высокой концентрацией железа, состоящее из агрегатов кристаллов железа, не имеющих апоферритиновой оболочки. Гемосидерин накапливается в макрофагах костного мозга, селезенки, купферовских клетках печени.
Общепринято выделять две формы железодефицитных состояний: латентный дефицит железа и ЖДА. Латентный дефицит железа характеризуется уменьшением количества железа в его депо и снижением уровня транспортного железа крови при нормальных показателях гемоглобина и эритроцитов. ЖДА — гипохромная микроцитарная анемия, развивающаяся вследствие дефицита железа в сыворотке крови, костном мозге и депо — печени и селезенке. ЖДА возникает как правило, при хронической потере крови и (или) недостаточном поступлении железа в организм.
По данным Всемирной организации здравоохранения (ВОЗ), дефицит железа в организме человека является одним из наиболее распространенных дефицитов питательных веществ в организме человека во всем мире [Benoist B. et al., 2008; WHO, 2001]. Анемия относится к числу глобальных проблем современного здравоохранения. В мире анемией страдают около 1,6 млрд человек, или 24,8% от общего населения. Частота встречаемости анемии оказалась высокой во всех группах и составила 25,4-47,4% у детей дошкольного и школьного возраста, 41,8% — у беременных женщин, 30,2% — у небеременных женщин репродуктивного возраста, 23,9% — у пожилых людей и 12,7% — у мужчин.
Хотя среди взрослого населения анемия чаще всего развивалась у женщин во время беременности, тем не менее в популяции основную долю пациентов с анемией составляли небеременные женщины репродуктивного возраста (468 млн человек). По крайней мере в половине случаев причиной анемии служит дефицит железа [WHO, 2001], который может быть следствием хронической кровопотери (менструации, оккультные кровотечения при опухолях желудочно-кишечного тракта (ЖКТ), неспецифические и специфические воспалительные заболевания тонкой и толстой кишки, другие причины), недостаточного поступления железа с пищей или нарушения его усвояемости (например, при хроническом алкоголизме), повышенной потребности (детский и подростковый возраст, беременность, послеродовый период), нарушения всасывания.
Дефицит железа бывает не только абсолютным, но и функциональным. Последний возникает, когда адекватное или даже повышенное общее содержание железа в организме оказывается недостаточным у больных при увеличении потребности в железе костного мозга на фоне стимуляции эритропоэза. Важную роль в регуляции обмена железа играет гепсидин — гормон, который образуется в печени, взаимодействует с ферропортином (белком, осуществляющим транспорт железа) и подавляет всасывание железа в кишечнике, а также его высвобождение из депо и макрофагов. Повышение уровня гепсидина, отмечающееся при воспалении, считают основной причиной анемии при хронических заболеваниях. Кроме того, уровень гепсидина повышается при хронической болезни почек, что способствует развитию нефрогенной анемии и резистентности к стимуляторам эритропоэза. При усилении эритропоэза под действием эритропоэтина скорость мобилизации железа из депо становится недостаточной для обеспечения возросших потребностей костного мозга. Пролиферирующим эритробластам необходимо все большее количество железа, что приводит к истощению лабильного пула железа и снижению сывороточного уровня ферритина. Для мобилизации и растворения железа из гемосидерина требуется определенное время. В результате количество поступающего в костный мозг железа уменьшается, что вызывает развитие его функционального и абсолютного дефицита.
В соответствии с Международной классификацией болезней 10-го пересмотра (МКБ-10) учитывают следующие формы анемий, связанных с абсолютным и относительным дефицитом железа:
Классификация, клиника и диагностика ЖДА
Общепризнанной классификации ЖДА не существует. Имеются клиническая классификация ЖДА и классификация по стадиям и тяжести протекания анемии.
Клиническая классификация ЖДА:
1. ЖДА постгеморрагические. Эту группу составляют анемии, развивающиеся на почве повторных небольших кровопотерь, — метроррагии, эпистаксис, гематурия и т.д.
2. ЖДА беременных. Причины возникновения анемий данной группы различны: дисбаланс питания беременных и связанное с этим ухудшение утилизации железа, передача организмом матери значительного его количества развивающемуся плоду, потери железа в период лактации и др.
3. ЖДА, связанные с патологией ЖКТ. К ним относятся анемии, возникающие после гастрэктомии, обширных резекций тонкой кишки, при различных энтеропатиях. По своей сути это ЖДА, обусловленные грубым, тяжелым нарушением функции всасывания железа -проксимальном отделе двенадцатиперстной кишки.
4. ЖДА вторичные, возникающие при инфекционных, воспалительных или опухолевых болезнях. Анемии в этих случаях развиваются вследствие больших потерь железа при гибели клеток опухолей, распаде тканей, микро- и даже макрогеморрагиях, повышении потребности в железе в очагах воспаления.
5. Эссенциальная (идиопатическая) ЖДА, при которой самый тщательный анамнестический и лабораторный поиск не выявляет общеизвестные причины возникновения дефицита железа. У большинства больных имеет место особая форма нарушения всасывания железа.
6. Ювенильная ЖДА — анемия, развивающаяся у молодых девушек (и чрезвычайно редко — у юношей). Данная форма железодефицитного малокровия связана с генетическими или фенотипическими дисгормональными явлениями.
7. ЖДА сложного генеза. В эту группу входят анемии алиментарные.
ЖДА также классифицируют по стадиям и тяжести протекания.
I стадия — потеря железа превышает его поступление, постепенное истощение запасов, всасывание в кишечнике компенсаторно увеличивается;
II стадия — истощение запасов железа (уровень сывороточного железа — ниже 50 мкг/л, насыщение трансферрина — ниже 16%) препятствует нормальному эритропоэзу, эритропоэз начинает падать;
III стадия — развитие анемии легкой степени (100-120 г/л гемоглобина, компенсированной), с незначительным снижением цветового показателя и других индексов насыщения эритроцитов гемоглобином;
IVстадия — выраженная (менее 100 г/л гемоглобина, субкомпенсированная) анемия с явным снижением насыщения эритроцитов гемоглобином;
Vстадия — тяжелая анемия (60-80 г/л гемоглобина) с циркуляторными нарушениями и тканевой гипоксией.
Клиническая картина ЖДА
Клиническими проявлениями ЖДА являются два важнейших синдрома — анемический и сидеропенический.
Анемический синдром обусловлен снижением содержания гемоглобина и уменьшением количества эритроцитов, недостаточным обеспечением тканей кислородом и представлен неспецифическими симптомами. Больные жалуются на общую слабость, повышенную утомляемость, снижение работоспособности, головокружение, шум в ушах, мелькание мушек перед глазами, сердцебиения, одышку при физической нагрузке, появление обморочных состояний. Может появляться снижение умственной работоспособности, ухудшение памяти, сонливость. Субъективные проявления анемического синдрома вначале беспокоят больных при физической нагрузке, а затем и в покое (по мере развития анемии).
При объективном исследовании обнаруживается бледность кожи и видимых слизистых оболочек, нередко — некоторая пастозность в области голеней, стоп, лица. Характерны утренние отеки — «мешки» вокруг глаз. Анемия обусловливает развитие синдрома миокардиодистрофии, который проявляется одышкой, тахикардией, часто аритмией, умеренным расширением границ сердца влево, глухостью тонов сердца, негромким систолическим шумом во всех аускультативных точках. При тяжелой и длительной анемии миокардиодистрофия может привести к выраженной недостаточности кровообращения. ЖДА развивается постепенно, поэтому организм больного адаптируется к низкому уровню гемоглобина, и субъективные проявления анемического синдрома не всегда бывают ярко выражены.
Сидеропенический синдром (синдром гипосидероза) обусловлен тканевым дефицитом железа, что приводит к снижению активности многих ферментов (цитохромоксидаза, пероксидаза, сукцинат-дегидрогеназа и др.). Сидеропенический синдром проявляется многочисленными симптомами, такими как:
Лабораторные данные
Диагностика латентного дефицита железа
Латентный дефицит железа диагностируется на основании следующих признаков:
Диагностика ЖДА
При снижении содержания гемоглобинового железа появляются характерные для ЖДА изменения общего анализа крови:
Наиболее часто используемыми в практике критериями ЖДА являются:
— низкий цветовой показатель;
— гипохромия эритроцитов, микроцитоз;
— снижение уровня сывороточного железа;
— повышение ОЖСС;
— снижение содержания ферритина в сыворотке.
При биохимическом исследовании крови, кроме снижения уровня сывороточного железа и ферритина, выявляются также изменения, обусловленные основным онкологическим или другим заболеванием.
Лечение
В настоящее время существует следующие этапы лечения ЖДА:
Не так давно гемотрансфузия являлась одним из самых распространенных способов коррекции анемии даже легкой степени у больных после операционной кровопотери и кровопотери при других клинических ситуациях (роды, маточные кровотечения, геморрой, опухоли ЖКТ и др.). Считалось, что надо остановить кровотечение и перелить донорскую кровь или эритроцитную массу. Необходимое для переливания количество эритроцитов определяли исходя из объема кровопотери и уровня гемоглобина. Однако ориентация на достижение нормального уровня гемоглобина иногда приводила к переливанию значительных количеств (до 5-6 л) донорской крови, что сопровождалось развитием синдрома массивной трансфузии, рецидивом кровотечения, появлением признаков полиорганной недостаточности с высокой смертностью.
В последнее время получила распространение новая трансфузионная тактика — компонентная гемотерапия, в связи с чем переливание эритроцитной массы заняло доминирующее место в лечении не только хронической, но и острой кровопотери. Однако отсутствие детально разработанных и сформулированных показаний к гемотерапии с учетом индивидуальных особенностей пациентов нередко приводит к необоснованным, неоправданным трансфузиям, которых, к сожалению, еще много. В современных условиях оправдана тенденция к ограничению переливания препаратов крови в связи с ростом числа таких осложнений, как перенос инфекций, формирование ложных групповых антител, подавление эндогенного эритропоэза.
Лечебная программа при ЖДА включает:
При выявлении причины развития ЖДА основное лечение должно быть направлено на ее устранение (оперативное лечение опухоли желудка, кишечника, лечение энтерита, коррекция алиментарной недостаточности и др.). В целом ряде случаев радикальное устранение причины ЖДА не представляется возможным, например, при продолжающихся меноррагиях, наследственных геморрагических диатезах, проявляющихся носовыми кровотечениями, у беременных и в некоторых других ситуациях. В таких случаях основное значение приобретает патогенетическая терапия железосодержащими лекарственными препаратами.
Путь введения препарата больному ЖДА определяется конкретной клинической ситуацией. При проведении купирующей терапии применяются пероральное и парентеральное введение препаратов железа (ПЖ) больному.
Первый путь — пероральный — является наиболее распространенным, хотя и дающим более отсроченные результаты.
Основными принципами лечения ПЖ для приема внутрь являются следующие:
— назначение ПЖ с достаточным содержанием трехвалентного железа;
— нецелесообразность одновременного назначения витаминов группы В (в том числе В12), фолиевой кислоты без специальных показаний;
— избегание назначения ПЖ внутрь при наличии признаков нарушения всасывания в кишечнике;
— достаточная продолжительность насыщающего курса терапии (не менее 3-5 мес.);
— необходимость проведения поддерживающей терапии ПЖ после нормализации показателей гемоглобина в соответствующих ситуациях.
Для адекватного прироста показателей гемоглобина у больных необходимо назначать от 100 до 300 мг трехвалентного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. Индивидуальные колебания в количестве необходимого железа обусловлены степенью его дефицита в организме, истощения запасов, скоростью эритропоэза, всасываемостью, переносимостью и некоторыми другими факторами. С учетом этого при выборе лекарственного ПЖ следует ориентироваться не только на содержание в нем общего количества, но и, главным образом, на количество трехвалентного железа, которое только и всасывается в кишечнике.
Причины неэффективности терапии ПЖ для приема внутрь:
— отсутствие дефицита железа (неправильная трактовка природы гипохромной анемии и ошибочное назначение ПЖ);
— недостаточная дозировка ПЖ (недоучет количества трехвалентного железа в препарате);
— недостаточная длительность лечения ПЖ;
— нарушение всасывания ПЖ, назначаемых внутрь больным с соответствующей патологией;
— одновременный прием препаратов, нарушающих всасывание железа;
— наличие хронических (оккультных) кровопотерь, чаще всего из органов ЖКТ;
— сочетание ЖДА с другими анемическими синдромами (В12-дефицитной, фолиеводефицитной).
Второй путь введения ПЖ — парентеральное введение, которое может быть внутримышечным и внутривенным. Показаниями для применения ПЖ парентерально могут быть следующие клинические ситуации:
— нарушение всасывания при патологии кишечника (энтериты, синдром недостаточности всасывания, резекция тонкого кишечника, резекция желудка по методу Бильрот II с выключением двенадцатиперстной кишки);
— обострение язвенной болезни желудка или двенадцатиперстной кишки;
— непереносимость ПЖ для приема внутрь, не позволяющая дальнейшее продолжение лечения;
— необходимость более быстрого насыщения организма железом, например, у больных ЖДА, которым предстоят оперативные вмешательства (миома матки, геморрой и др.).
В отличие от ПЖ для приема внутрь в инъекционных препаратах железо всегда находится в трехвалентной форме. Лечение больных с ЖДА имеет свои особенности в зависимости от конкретной клинической ситуации с учетом многих факторов, в том числе характера основного заболевания и сопутствующей патологии, возраста больных (дети, пожилые люди), выраженности анемического синдрома, дефицита железа, переносимости ПЖ и др. Общая ориентировочная доза ПЖ для внутримышечного введения, необходимая для коррекции дефицита железа и анемии, может быть рассчитана по формуле:
А = KxF (100 — 6 Х Hb) F = 0,0066,
где А — число ампул, К — масса больного в кг, НЬ — содержание гемоглобина в г %.
При парентеральном введении ПЖ возможны развитие флебитов, инфильтратов, потемнение кожи в местах инъекций, аллергических реакций, в том числе тяжелых (анафилактический шок). Внутримышечные инъекции болезненны, в некоторых случаях они ассоциировались с развитием саркомы ягодичной мышцы [Grasso P, 1973; Greenberg G., 1976]. По мнению некоторых авторов [Auerbach M. et al., 2007], от внутримышечного введения ПЖ следует отказаться.
В последнее время особенно большой интерес вызывают ПЖ для внутривенного введения с целью терапии постгеморрагических анемий. В нескольких работах показано, что внутривенное введение ПЖ более эффективно при сравнении с приемом железа внутрь при тех же показаниях. Помимо этого, внутривенная терапия позволяет избежать возникновения как побочных эффектов со стороны ЖКТ, наблюдающихся при приеме ПЖ внутрь, так и некоторых осложнений, вызываемых при внутримышечном введении ПЖ, однако требует определенного уровня реанимационной службы учреждения, в котором вводятся препараты.
ПЖ для внутривенного введения
Для внутривенного введения в России применяют карбоксимальтозат железа (Феринжект®), сахарат железа (Венофер), глюконат железа и декстран железа, которые представляют собой сферические железоуглеводные коллоиды. Углеводная оболочка придает комплексу стабильность, замедляет высвобождение железа и поддерживает образующиеся формы в коллоидной суспензии.
Внутривенное введение декстрана железа вызывает большое число анафилактических реакций, сопровождающихся летальностью в 13,5% случаев [Faich G. еt Strobos J., 1999], и в настоящее время применяется ограниченно. Применение натриевого комплекса глюконата железа в сукрозе вызывает значительно меньше осложнений и, как правило, не сопровождается смертельными исходами. Однако токсические эффекты, связанные с поступлением свободного железа в организм, существенно ограничивают применение препарата в ежедневной практике терапии ЖДА.
Сахарат железа (III) (Венофер®) является популярным препаратом для лечения синдрома ЖДА. Это связано с безопасностью и высокой переносимостью комплекса трехвалентного железа с сахаратом в отличие от декстрана железа и глюконата железа. Данный препарат одобрен для применения, в том числе и в период беременности. Венофер следует вводить только в учреждениях, располагающих оборудованием для сердечно-легочной реанимации, так как часто могут отмечаться сердечно-сосудистые осложнения в виде гипотонии. Максимальная разовая парентеральная доза сахарата железа (III) составляет 500 мг, предпочтительно развести препарат в 100 мл 0,9% раствора NaCl для введения в форме инфузии. Продолжительность инфузии составляет приблизительно 4,5 ч с использованием внутривенного доступа (следует помнить, что высокая скорость инфузии связана с риском развития гипотензивной реакции). В зависимости от исходных значений уровня гемоглобина внутривенное введение повторяют 1-3 раза/нед. до повышения уровня гемоглобина >105 г/л. Затем пациента можно перевести на прием пероральных ПЖ для поддерживающей терапии. Оснований ожидать возможной передозировки железом не имеется.
Комплекс железа с карбоксимальтозой (Феринжект®) — новый недекстрановый комплекс железа, преимуществом которого является возможность введения высоких доз (до 1000 мг за 1 введение) в короткий промежуток времени (на 1 инфузию требуется 15 мин.). Благодаря этому отсутствует необходимость в дорогостоящих повторных инфузиях небольших доз железа, при этом Феринжект® характеризуется хорошей переносимостью. Феринжект® также одобрен для применения, в том числе и в период беременности. На сегодняшний день (как и в случае сахарата железа) не проводилось масштабных рандомизированных исследований для оценки безопасности применения данного препарата для плода. По этой причине перед назначением любых ПЖ внутривенно необходимо тщательно оценить соотношение пользы и рисков.
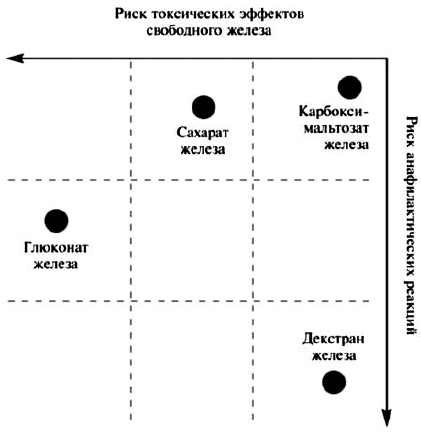
Эффективность и безопасность внутривенного введения ПЖ зависят от их молекулярной массы, стабильности и состава. Комплексы с низкой молекулярной массой, такие как глюконат железа, менее стабильны и быстрее высвобождают в плазму железо, которое в свободном виде может катализировать образование реактивных форм кислорода, вызывающих перекисное окисление липидов и повреждение тканей. Значительная часть дозы подобных препаратов выводится через почки в первые 4 ч после приема и не используется для эритропоэза. Хотя декстран железа обладает высокими молекулярной массой и стабильностью, его недостатком является повышенный риск развития аллергических реакций. Карбоксимальтозат железа сочетает в себе положительные свойства высокомолекулярных комплексов железа, но не вызывает реакции гиперчувствительности, наблюдающиеся при применении препаратов, содержащих декстран, и, в отличие от сахарата и глюконата железа, может вводиться в более высокой дозе [Geisser P., 2009]. Схема оценки риска токсических эффектов и анафилактических реакций препаратов свободного железа для внутривенного введения представлена на рисунке 1 [С.В. Моисеев, 2012].
Рис. 1. Риск токсических эффектов и анафилактических реакций при применении внутривенных препаратов железа
Из рисунка 1 видно, что глюконат железа может вызывать анафилактические реакции и одновременно обладает выраженным токсическим эффектом. Декстран железа, не являясь препаратом с выраженными токсическими эффектами, способен вызывать анафилаксию. Сахарат железа не приводит к развитию анафилактических реакций у больных с ЖДА, но обладает токсическими свойствами. Карбоксимальтозат железа — Феринжект® характеризуется сниженным риском возникновения как токсических эффектов свободного железа, так и анафилактических реакций.
Применение карбоксимальтозата железа позволяет вводить за 1 инфузию до 1000 мг железа (внутривенно капельно в течение 15 мин.), в то время как максимальная доза железа в виде сахарата составляет 500 мг и вводится в течение 4,5 ч, а длительность инфузии декстрана железа достигает 6 ч. Причем в двух последних случаях перед началом инфузии необходимо ввести тестовую дозу препарата. Введение большой дозы железа позволяет сократить необходимое число инфузий и затраты на лечение. Карбоксимальтозат железа отличается не только удобством применения, но и низкой токсичностью, а также отсутствием оксидативного стресса, которые определяются медленным и физиологичным высвобождением железа из стабильного комплекса с углеводом, по структуре сходного с ферритином.
Также, Феринжект® вводят внутривенно в виде болюса (максимальная доза — 4 мл, или 200 мг железа, не более 3 раз/нед.) или капельно (максимальная доза -20 мл, или 1000 мг железа, не чаще 1 раза/нед.). Перед началом лечения необходимо рассчитать оптимальную кумулятивную дозу препарата, которую не следует превышать. Кумулятивную дозу, необходимую для восстановления уровня гемоглобина в крови и восполнения запасов железа в организме, вычисляют по формуле Ганзони:
Кумулятивный дефицит железа (мг) = масса тела (кг) х (целевой НЬ — фактический НЬ) (г/дл) х 2,4 + содержание депонированного железа (мг), где целевой уровень гемоглобина (НЬ) у человека с массой тела или = 35 кг 15 г/дл (9,3 ммоль/л), соответственно, депо железа у человека с массой тела >35 кг и = 35 кг = 500 мг и ЛИТЕРАТУРА
1. Worldwide prevalence of anaemia 1993-2005. WHO global database of anaemia. Edited by de Benoist В. et al. World Health Organisation. 2008.
2. Iron deficiency anaemia: assessment, prevention, and control. A guide for programme managers. Geneva, WHO, 2001 (WH0/NHD/01.3).
3. Grasso P. Sarcoma after intramuscular iron injection // Br. Med. J. 1973. Vol. 2. Р. 667.
4. Greenberg G. Sarcoma after intramuscular iron injection // Br. Med. J. 1976. Vol. 1. Р. 1550-1550.
5. Auerbach M, Ballard H., Glaspy J. et al. Clinical update: intravenous iron for anaemia // Lancet. 2007. Vol. 369. Р. 1502-1504.
6. Geisser P. The pharmacology and safety profile of ferric carboxymaltose (Ferinjecf): structure/reactivity relationships of iron preparations // Port.. J. Nephrol. Hypert. 2009. Vol. 23 (1). Р. 11-16.
7. Моисеев С.В. Железа карбоксимальтозат (Феринжект) — новый внутривенный препарат для лечения железодефицитной анемии // Клиническая фармакология и терапия. 2012. № 21 (2). С. 2-7.
8. Faich G., Strobos J. //Am. J. Kidney Dis. 1999. Vol. 33. No. 3. P. 464-470.
9. Beshara S., Sorensen J., Lubberink M. et al. Pharmacokinetics and red cell utilization of 52Fe/59Fe-labelled iron polymaltose in anaemic patients using positron emission tomography// Br. J. Haematol. 2003. Vol. 120. Р. 853-859.
источник
Железодефици́тная анеми́я (ЖДА) — гематологический синдром, характеризующийся нарушением синтеза гемоглобина вследствие дефицита железа и проявляющийся анемией и сидеропенией. Основными причинами ЖДА являются кровопотери и недостаток богатой гемом пищи и питья.
Причиной дефицита железа является нарушение его баланса в сторону преобладания расходования железа над поступлением, наблюдаемое при различных физиологических состояниях или заболеваниях:
кровопотери различного генеза;
повышенная потребность в железе;
нарушение усвоения железа;
врождённый дефицит железа;
нарушение транспорта железа вследствие дефицита трансферрина.
Кровопотери различного генеза
Повышенное расходование железа, вызывающее развитие гипосидеропении, чаще всего связано с кровопотерей или с усиленным его использованием при некоторых физиологических состояниях (беременность, период быстрого роста). У взрослых дефицит железа развивается, как правило, вследствие кровопотери. Чаще всего к отрицательному балансу железа приводят постоянные небольшие кровопотери и хронические скрытые кровотечения (5 — 10 мл/сут). Иногда дефицит железа может развиться после однократной массивной потери крови, превышающей запасы железа в организме, а также вследствие повторных значительных кровотечений, после которых запасы железа не успевают восстановиться.
По статистическим данным, у 20 — 30 % женщин детородного возраста наблюдается скрытый дефицит железа, у 8 — 10 % обнаруживается железодефицитная анемия. Основной причиной возникновения гипосидероза у женщин, кроме беременности, являются патологическая менструация и маточные кровотечения. Полименорея может быть причиной уменьшения запасов железа в организме и развития скрытого дефицита железа, а затем и железодефицитной анемии. Маточные кровотечения в наибольшей мере увеличивают объем кровопотери у женщин и способствуют возникновению железодефицитных состояний. Существует мнение о том, что фибромиома матки, даже при отсутствии менструальных кровотечений, может привести к развитию дефицита железа. Но чаще причиной анемии при фибромиоме является повышенная кровопотеря.
Развитие постгеморрагической железодефицитной анемии, также вызывают кровопотери из пищеварительного канала, которые часто имеют скрытый характер и трудно диагностируются. Такие кровопотери могут быть обусловлены заболеваниями органов пищеварения и болезнями других органов. Нарушения баланса железа могут сопровождать повторные острые эрозивные или геморрагические эзофагиты и гастриты, язвенная болезнь желудка и двенадцатиперстной кишки с повторными кровотечениями, хронические инфекционные и воспалительные заболевания пищеварительного канала. При гигантском гипертрофическом гастрите (болезни Менетрие) и полипозном гастрите слизистая оболочка легко ранима и часто кровоточит. Частой причиной скрытых труднодиагностируемых кровопотерь является грыжа пищевого отверстия диафрагмы, варикозное расширение вен пищевода и прямой кишки при портальной гипертензии, геморрой, дивертикулы пищевода, желудка, кишок, протока Меккеля, опухоли. Легочные кровотечения — редкая причина развития дефицита железа. К развитию дефицита железа иногда могут приводить кровотечения из почек и мочевых путей. Очень часто сопровождаются гематурией гипернефромы.
В некоторых случаях кровопотери различной локализации, являющиеся причиной железодефицитной анемии, связаны с гематологическими заболеваниями (коагулопатиями, тромбоцитопениями и тромбоцитопатиями), а также с поражением сосудов при васкулитах, коллагенозах, болезни Рандю — Вебера — Ослера, гематомах.
Дефицит железа алиментарного происхождения может развиться у детей и взрослых при недостаточном его содержании в пищевом рационе, что наблюдается при хроническом недоедании и голодании, при ограничении питания с лечебной целью, при однообразной пище с преимущественным содержанием жиров и сахаров. У детей может наблюдаться недостаточное поступление железа из организма матери как следствие железодефицитной анемии во время беременности, преждевременных родов, при многоплодности и недоношенности, преждевременной перевязке пуповины до прекращения пульсации.
Нарушение усвоения железа
Длительное время считали основной причиной развития дефицита железа отсутствие хлористоводородной кислоты в желудочном соке. Соответственно выделяли гастрогенную или ахлоргидрическую железодефицитную анемию. В настоящее время установлено, что ахилия может иметь только дополнительное значение в нарушении всасывания железа в условиях повышенной потребности в нем организма. Атрофический гастрит с ахилией возникает вследствие дефицита железа, обусловленного снижением активности ферментов и клеточного дыхания в слизистой оболочке желудка.
К нарушению всасывания железа могут приводить воспалительные, рубцовые или атрофические процессы в тонкой кишке, резекция тонкой кишки. Существует ряд физиологических состояний, при которых потребность в железе резко увеличивается. К ним относятся беременность и лактация, а также периоды усиленного роста у детей. Во время беременности расходование железа резко повышается на потребности плода и плаценты, кровопотерю при родах и лактацию. Баланс железа в этот период находится на грани дефицита, и различные факторы, уменьшающие поступление или увеличивающие расход железа, могут приводить к развитию железодефицитной анемии.
Железодефицитная анемия иногда, особенно в грудном и пожилом возрасте, развивается при инфекционных и воспалительных заболеваниях, ожогах, опухолях, вследствие нарушения обмена железа при сохранённом его общем количестве.
Клиническая картина и стадии развития болезни
ЖДА является последней стадией дефицита железа в организме. Клинических признаков дефицита железа на начальных стадиях нет, и диагностика предклинических стадий железодефицитного состояния стала возможной лишь благодаря развитию методов лабораторной диагностики. В зависимости от выраженности дефицита железа в организме различают три стадии:
прелатентный дефицит железа в организме;
латентный дефицит железа в организме;
Прелатентный дефицит железа в организме
На этой стадии в организме происходит истощение депо. Основной формой депонирования железа является ферритин — водорастворимый гликопротеиновый комплекс, который содержится в макрофагах печени, селезенки, костного мозга, в эритроцитах и сыворотке крови. Лабораторным признаком истощения запасов железа в организме является снижение уровня ферритина в сыворотке крови. При этом уровень сывороточного железа сохраняется в пределах нормальных значений. Клинические признаки на этой стадии отсутствуют, диагноз может быть установлен лишь на основании определения уровня сывороточного ферритина.
Латентный дефицит железа в организме
Если не происходит адекватного восполнения дефицита железа на первой стадии, наступает вторая стадия железодефицитного состояния — латентный дефицит железа. На этой стадии в результате нарушения поступления необходимого металла в ткани отмечается снижение активности тканевых ферментов (цитохромов, каталазы, сукцинатдегидрогеназы и др.), что проявляется развитием сидеропенического синдрома. К клиническим проявлениям сидеропенического синдрома относится извращение вкуса, пристрастие к острой, соленой, пряной пище, мышечная слабость, дистрофические изменения кожи и придатков и др.
На стадии латентного дефицита железа в организме более выражены изменения в лабораторных показателях. Регистрируются не только истощение запасов железа в депо — снижение концентрации ферритина сыворотки, но и снижение содержания железа в сыворотке и белках-переносчиках.
Сывороточное железо — важный лабораторный показатель, на основании которого возможно проведение дифференциальной диагностики анемий и определение тактики лечения. Так, если при анемии отмечается снижение уровня сывороточного железа наряду со снижением ферритина сыворотки, это свидетельствует о железодефицитной этиологии анемии, и основной тактикой лечения является устранение причин потери железа и восполнение его дефицита. В другом случае сниженный уровень сывороточного железа сочетается с нормальным уровнем ферритина. Это встречается при железоперераспределительных анемиях, при которых развитие гипохромной анемии связано с нарушением процесса высвобождения железа из депо. Тактика лечения перераспределительных анемий будет совершенно другой — назначение препаратов железа при данной анемии не только нецелесообразно, но может причинить вред больному.
Общая железосвязывающая способность сыворотки (ОЖСС) — лабораторный тест, который дает возможность определить степень так называемого «Fe-голодания» сыворотки. При определении ОЖСС в исследуемую сыворотку добавляют определенное количество железа. Часть добавленного железа связывается в сыворотке с белками-переносчиками, а железо, которое не связалось с белками, удаляют из сыворотки и определяют его количество. При железодефицитных анемиях сыворотка пациента связывает больше железа, чем в норме, — регистрируется увеличение ОЖСС.
Железодефицитное состояние зависит от степени дефицита железа и скорости его развития и включает признаки анемии и тканевого дефицита железа (сидеропении). Явления тканевого дефицита железа отсутствуют лишь при некоторых железодефицитных анемиях, обусловленных нарушением утилизации железа, когда депо переполнены железом. Таким образом, железодефицитная анемия в своем течении проходит два периода: период скрытого дефицита железа и период явной анемии, вызванной дефицитом железа. В период скрытого дефицита железа появляются многие субъективные жалобы и клинические признаки, характерные для железодефицитных анемий, только менее выраженные. Больные отмечают общую слабость, недомогание, снижение работоспособности. Уже в этот период могут наблюдаться извращение вкуса, сухость и пощипывание языка, нарушение глотания с ощущением инородного тела в горле (синдром Пламмера — Винсона), сердцебиение, одышка..
При объективном обследовании больных обнаруживаются «малые симптомы дефицита железа»: атрофия сосочков языка, хейлит («заеды»), сухость кожи и волос, ломкость ногтей, жжение и зуд вульвы. Все эти признаки нарушения трофики эпителиальных тканей связаны с тканевой сидеропенией и гипоксией.
Скрытый дефицит железа может быть единственным признаком недостаточности железа. К таким случаям относятся нерезко выраженные сидеропении, развивающиеся на протяжении длительного времени у женщин зрелого возраста вследствие повторных беременностей, родов и абортов, у женщин — доноров, у лиц обоего пола в период усиленного роста. У большинства больных при продолжающемся дефиците железа после исчерпания его тканевых резервов развивается железодефицитная анемия, являющаяся признаком тяжелой недостаточности железа в организме. Изменения функции различных органов и систем при железодефицитной анемии являются не столько следствием малокровия, сколько тканевого дефицита железа. Доказательством этого служит несоответствие тяжести клинических проявлений болезни и степени анемии и появление их уже в стадии скрытого дефицита железа.
Больные железодефицитной анемией отмечают общую слабость, быструю утомляемость, затруднение в сосредоточении внимания, иногда сонливость. Появляются головная боль после переутомления, головокружение. При тяжелой анемии возможны обмороки. Эти жалобы, как правило, зависят не от степени малокровия, а от продолжительности заболевания и возраста больных.
Железодефицитная анемия характеризуется изменениями кожи, ногтей и волос. Кожа обычно бледная, иногда с легким зеленоватым оттенком (хлороз) и с легко возникающим румянцем щек, она становится сухой, дряблой, шелушится, легко образуются трещины. Волосы теряют блеск, сереют, истончаются, легко ломаются, редеют и рано седеют. Специфичны изменения ногтей: они становятся тонкими, матовыми, уплощаются, легко расслаиваются и ломаются, появляется исчерченность. При выраженных изменениях ногти приобретают вогнутую, ложкообразную форму (койлонихия).
В общем анализе крови при ЖДА будут регистрироваться снижение уровня гемоглобина и эритроцитов. Умеренная эритроцитопения может проявляться при Hb 1,05) — содержание гемоглобина в эритроцитах повышено. В мазке крови эти эритроциты имеют более интенсивную окраску, просвет в центре значительно уменьшен либо отсутствует. Гиперхромия связана с увеличением толщины эритроцитов и часто сочетается с макроцитозом;
полихроматофилы — эритроциты, окрашенные в мазке крови в светло-фиолетовый, сиреневый цвет. При специальной суправитальной окраске это — ретикулоциты. В норме могут быть единичными в мазке.
Биохимический анализ крови
При развитии ЖДА в биохимическом анализе крови будут регистрироваться:
уменьшение концентрации сывороточного ферритина;
уменьшение концентрации сывороточного железа;
уменьшение насыщения трансферрина железом.
Лечение проводится только длительным приёмом препаратов двухвалентного железа внутрь в умеренных дозах, причём существенный прирост гемоглобина, в отличие от улучшения самочувствия, будет не скорым — через 4—6 недель.
Обычно назначается любой препарат двухвалентного железа — чаще это сульфат железа — лучше его пролонгированная лекарственная форма, в средней лечебной дозе на несколько месяцев, затем доза снижается до минимальной ещё на несколько месяцев, а затем (если причина малокровия не устранена), продолжается приём поддерживающей минимальной дозы в течение недели ежемесячно многие годы. Так, эта практика хорошо оправдала себя при лечении тардифероном женщин с хронической постгеморрагической железодефицитной анемией вследствие многолетней гиперполименорреи — одна таблетка утром и вечером 6 месяцев без перерыва, затем одна таблетка в день ещё 6 месяцев, затем несколько лет каждый день в течение недели в дни месячных. Это обеспечивает нагрузку железом при появлении затянутых обильных месячных в период климакса. Бессмысленным анахронизмом является определение уровня гемоглобина до и после месячных.
Беременным с дефицитом железа и малокровием (небольшое снижение уровня гемоглобина и числа эритроцитов физиологично вследствие умеренной гидремии и не требует лечения) назначается средняя доза сульфата железа внутрь до родов и в период кормления грудью, если у ребёнка не возникнет диарея, что обычно случается редко.
периодическое наблюдение за картиной крови;
употребление пищи с высоким содержанием железа (мясо, печень и др.);
профилактический прием препаратов железа в группах риска.
оперативная ликвидация источников кровопотерь.
источник
Железодефицитная анемия (ЖДА) — одно из наиболее часто диагностируемых патологических состояний кровеносной системы, да и вообще самый распространенный вид анемии.
Статистические исследования показали, что около 2,5 млрд. пациентов во всем мире имеют этот диагноз.
Для того чтобы остановить прогрессирование заболевания и избежать осложнений, необходимо выявить первопричины его появления и своевременно начать лечение.
Анемия характеризуется пониженным содержанием в кровеносной системе человека красных кровяных телец — эритроцитов, и, как следствие, падением гемоглобина.
Если низкий уровень этих элементов связан с недостатком железа в организме, то в данном случае речь идет о железодефицитной анемии (ЖДА).
Как правило, патология не является самостоятельным заболеванием. В большинстве случаев железодефицитная анемия возникает вслед за какими-либо другими негативными изменениями в организме человека.
ДЛЯ СПРАВКИ! Норма содержания железа в организме у взрослых в среднем составляет около 4 грамм. У мужчин и женщин в разном возрасте этот показатель может иметь различное значение. Так, например, железодефицитная анемия у взрослых гораздо чаще проявляется у представительниц слабого пола. Прежде всего, это связано с регулярными потерями крови, происходящими во время менструаций. А наиболее сильная концентрация железа наблюдается у новорожденных младенцев, поскольку они имеют усиленную подпитку этим микроэлементом в утробе матери.
Дефицит железа плохо сказывается на жизнеспособности человека в целом. Кроме того, развитие этой недостаточности чревато сбоями в образовании эритроцитов, а также нарушением реакций окисления и восстановления, механизма деления клеток и нормального течения некоторых других реакций.
Железо является основой гемоглобина, выполняющего функции снабжения кислородом всех тканей и органов в теле человека, а также играющего важную роль в синтезе белка и гормонов. Если дефицит железа не восполняется в течение длительного времени, у пациента начинает развиваться анемический синдром.
Причины развития железодефицитной анемии могут заключаться в нехватке железа, поступающего в организм извне, или в сбоях потребляющих его процессов, ведь самостоятельно организм человека не может вырабатывать этот микроэлемент. Ими могут стать:
- несбалансированное питание: не грамотно подобранная диета, отказ от употребления мяса (вегетарианство);
- регулярные значительные кровопотери. Помимо менструаций у женщин хронические потери крови могут быть связаны с наличием различных заболеваний: язва желудка, геморрой, распадающиеся опухоли и другие. Также сюда можно отнести донорство крови, которое происходит чаще, чем 3-4 раза за один год;
- врожденные факторы, возникшие при внутриутробном развитии: наличие ЖДА у матери, многоплодная беременность, недоношенность;
- сбои в работе желудочно-кишечного тракта, в результате которых нарушается процесс всасывания железа в двенадцатиперстной кишке. Это может быть связано с наличием различных заболеваний кишечника (энтерит, гастрит, целиакия, рак желудка, болезнь Крона и т.д.);
- болезни печени, приводящие к нарушениям в выработке трансферрина – белка, осуществляющего транспортные функции: поступающие с пищей микроэлементы не распределяются по организму, из-за чего возникает дефицит железа. Синтез трансферрина происходит в клетках печени;
- прием лекарственных препаратов, оказывающих влияние на всасывание и переработку железа в превышенных дозах. Среди них могут быть: нестероидные противовоспалительные препараты, антациды, железосвязывающие препараты. Людям, имеющим предрасположенность к железодефицитной анемии, перед применением этих видов лекарств необходимо проконсультироваться с врачом.
Железодефицитная анемия у детей может развиваться в результате различных патологий при беременности, раннему переходу на искусственное кормление, ускоренным темпом роста (в случае недоношенности плода).
Усиленная потребность организма в железе и является главным провоцирующим фактором для развития железодефицитной анемии. Она может быть связана с такими жизненными процессами, как:
- беременность. При беременности женщине для нормального развития плода необходимо почти в два раза больше железа, чем в обычной жизни;
- грудное вскармливание. Как и в период беременности, во время кормления ребенка женский организм расходует гораздо больше железа, чем может получить.
Патогенез этой разновидности анемии выражается двумя основными периодами:
- Латентный (скрытый) период характеризуется уменьшением запасов железа в организме, в результате чего, падает уровень ферритина. При этом другие лабораторные показатели в анализе крови могут оставаться в пределах нормы. Организм старается компенсировать недостаток микроэлемента более активным всасыванием в кишечнике и выработкой транспортного белка. За счет этого, ЖДА на данном этапе еще не наступает, хотя предпосылки для нее уже присутствуют.
- Непосредственная железодефицитная анемиянаступает в тот момент, когда уровень эритроцитов снижается настолько, что они уже не могут в достаточной мере обеспечивать свои функции. На этой стадии начинают более явственно проявляться основные симптомы и характерные черты заболевания.
Классификация заболевания по причинам возникновения выделяет следующие виды:
- анемия, возникшая в результате обильной потери крови;
- железодефицитная анемия, появившаяся как следствие сбоев в работе эритроцитов;
- хроническая железодефицитная анемия;
- гемолитическая анемия (возвышает при высокой степени разрушения эритроцитов).
Классификация по уровню гемоглобина разделяет заболевание на виды в зависимости от тяжести:
- легкая степень тяжести (содержание гемоглобина более 90 г/л);
- средняя степень тяжести (70-90 г/л);
- высокая степень тяжести (ниже 70 г/л).
Степень ЖДА усиливается в организме постепенно и поначалу может практически не давать о себе знать. Латентный период заболевания характеризуется проявлением сидеропенического синдрома.
Позднее начинает проявляться общеанемический синдром, явственность которого определяется тяжестью анемии и способностью организма к сопротивлению. Наличие у пациента следующих признаков может свидетельствовать о заболевании железодефицитной анемией:
- быстрая утомляемость и хроническая усталость мышц. При дефиците железа в организме мышцы человека становятся более слабыми. На их повседневную работу затрачивается много энергии, которая перестает вырабатываться в нужном количестве из-за снижения уровня эритроцитов. В результате человек гораздо быстрее утомляется даже при небольших повседневных нагрузках. Железодефицитная анемия у детей может проявиться в стремлении ребенка к менее активным играм, вялом поведении и сонливости;
- появление одышки. При ЖДА затрудняется снабжение сердца кислородом из-за ухудшения циркуляции крови. По этой причине у пациента может наблюдаться учащение сердцебиения, появляется одышка и нехватка воздуха;
- ухудшение состояния кожи, ногтей и волос. Недостаток железа становится заметным внешне (см фото выше), когда кожные покровы становятся сухими и покрываются трещинами, появляется бледность. Ногти ослабевают, ломаются и покрываются специфичными поперечными трещинами. В некоторых случаях может наблюдаться выгибание ногтевой пластины в обратную сторону. Волосяной покров редеет. Волосы меняют свою структуру, раньше срока проявляется седина;
- поражение слизистых оболочек. Одним из ранних симптомов ЖДА является поражение слизистых покровов, потому как эти ткани наиболее остро ощущают недостаток железа из-за нарушения различных клеточных процессов:
- наиболее ярко поражение слизистых оболочек заметно в изменениях внешнего вида языка. Он становится гладким, покрытым трещинами и участками покраснений. Добавляются болевые ощущения, жжение. В некоторых случаях наблюдаются резкие нарушения во вкусовом восприятии;
- в полости рта появляется сухость и области атрофии. Появляется дискомфорт при употреблении пищи и боль при проглатывании. На губах образуются трещины;
- атрофия слизистой оболочки кишечника, вызванная железодефицитной анемией, сопровождается появлением болевых синдромов в животе, запорами, диареей. Ухудшается способность желудочно-кишечного тракта к всасыванию полезных веществ;
- поражение слизистых покровов мочеполовой системы характеризуется болями при мочеиспускании и недержанием мочи (как правило, в детском возрасте). Повышается риск заражения различными инфекциями;
- подверженность поражению различными инфекциями. Нехватка железа в организме отражается и на работе лейкоцитов – клеток крови, отвечающих за освобождение организма от возбудителей различных инфекций. В результате у больного наблюдается общее ослабление иммунитета, возрастает подверженность бактериальным и вирусным заражениям;
- затруднения интеллектуальной деятельности. Недостаточное обеспечение клеток головного мозга железом приводит к ухудшению памяти, рассеянности и ослаблению интеллекта в целом.
Железодефицитная анемия у детей и взрослых может быть установлена любым специалистом, однако детальная диагностика, направленная на выявление причин, и лечение данного заболевания должны проводиться врачом-гематологом. Обследования пациента включают в себя:
- визуальный осмотр пациента – первый этап диагностики ЖДА. Специалисту необходимо со слов пациента определить общую картину развития патологии и провести осмотр, который поможет сделать выводы о степени заболевания и выявить осложнения, если они присутствуют;
- общий анализ крови из пальца или из вены – обобщенная картина здоровья пациента, с помощью которой врач может однозначно установить наличие или отсутствие ЖДА у больного. Данный анализ проводится в лаборатории с использованием специального оборудования – гематологического анализатора. Диагноз железодефицитная анемия устанавливается у пациента, в случае:
- уменьшения количества эритроцитов (у мужчин – менее 4,0 х 1012/л, у женщин – менее 3,5 х 1012/л), когда количество тромбоцитов и лейкоцитов в норме или увеличено;
- преобладания в крови пациента эритроцитов, у которых величина меньше нормальной (отклонением считается размер менее 70 мкм3);
- цветовой показатель (ЦП) меньше 0,8;
- биохимический анализ крови позволяет более детально изучить состояние больного, принимая во внимание показатели, имеющие отношение к исследуемой области. О наличие железодефицитной анемии свидетельствуют следующие отклонения:
- сывороточное железо (СЖ): у мужчин – менее 17,9 мкмоль/л, у женщин – менее 14,3 мкмоль/л;
- общая железосвязывающая способность сыворотки (ОЖСС): значительно превышает уровень 77 мкмоль/л;
- ферритин (сложный белковый комплекс, выполняющий роль основного внутриклеточного депо железа у человека) ниже нормы: у мужчин – ниже 15 нг/мл, у женщин – менее 12 нг/мл;
- низкий уровень гемоглобина (менее 120 г/л);
Железодефицитная анемия у детей характеризуется следующими результатами анализа крови:
- сывороточное железо (СЖ) ниже 14 мкмоль/л;
- общая железосвязывающая способность сыворотки (ОЖСС) более 63 мкмоль/л;
- ферритин в крови ниже 12 нг/мл;
- уровень гемоглобина (менее 110 г/л).
- пункция костного мозга – метод диагностики, базирующийся на заборе образцов костного мозга путем его забора специальным инструментом из грудинной кости. При заболевании ЖДА наблюдается рост эритроидного ростка кроветворения;
- рентгенография проводится с целью определения патологий кишечника, которые могут вызывать хронические кровотечения, тем самым становясь причиной развития анемии;
- эндоскопические исследования слизистых покровов человека также проводятся для выявления различных патологий органов брюшной полости. Это могут быть:
- фиброэзофагогастродуоденоскопия (ФЭГДС);
- ректороманоскопия;
- колоноскопия;
- лапароскопия и другие.
По мнению врачей при лечении железодефицитной анемии у взрослых и детей нельзя ограничиваться только медикаментами. Восполнять дефицит важного микроэлемента лучше и проще всего при помощи здоровой пищи и правильно подобранной диеты.
Ежедневная норма железа, которую должен содержать рацион – не менее 20 мг. Следует отметить, что лечение этого заболевания будет неэффективным, если не принять мер по устранению первичной патологии, вызвавшей дефицит железа.
Для профилактики болезни каждому человеку следует каждый год проводить лабораторный анализ показателей крови, комплексно питаться и, при необходимости, вовремя устранять возможные причины значительной кровопотери.
Людям, имеющим предрасположенность к дефициту железа, следует обратиться к врачу за назначением курса лекарственных препаратов с высоким содержанием железа.
Сбалансированный рацион играет основную роль в профилактике и лечении ЖДА. При составлении диеты следует учитывать, что железо качественнее усваивается, если его прием осуществляется в совокупности с витамином C.
При этом этот микроэлемент лучше всего всасывается кишечником, если он содержится в продуктах животного происхождения (до 3 раз больше по сравнению с растительными продуктами).
Рейтинг продуктов, которые являются лидерами по количеству содержания железа, которые обязательно должны быть включены в лечебно-профилактическую диету при железодефицитной анемии:
- белая фасоль (72 мг);
- орехи всех видов (51 мг);
- гречневая крупа (31 мг);
- свиная печень (28 мг);
- патока (20 мг);
- пивные дрожжи (18 мг);
- морская капуста и водоросли (16 мг);
- семена тыквы (15 мг);
- чечевица (12 мг);
- ягоды черники (9 мг);
- говяжья печень (9 мг);
- сердце (6 мг);
- язык говяжий (5 мг);
- курага (4 мг).
Для более эффективного усвоения железа рекомендуется употреблять следующие препараты и витамины (в допустимых дозах):
- аскорбиновая кислота;
- янтарная кислота;
- фруктоза;
- никотинамид.
ДЛЯ СПРАВКИ! Морепродукты также богаты железом, но их не рекомендуется включать в рацион при дефиците этого микроэлемента. Дело в том, что в их состав помимо всего прочего входит большое количество фосфатов, которые затрудняют процесс усвоения железа в организме.
Несмотря на то, что железодефицитная анемия у детей грудного возраста развивается достаточно редко (за исключением случаев, когда у мамы присутствует это заболевание), следует отметить что в этом случае заболевание особенно опасно.
Нехватка железа у детей может обернуться серьезными нарушениями в физическом развитии, потому требует оперативного восполнения.
Лечение железодефицитной анемии в этом возрасте осуществляется путем строгой диеты и тщательного контроля над ежедневным рационом кормящей матери, а также пересмотром прикорма малыша, если он уже имеется.
Правильное питание является необходимым этапом в лечении и профилактике ЖДА, однако оно не может компенсировать недостаток нужного микроэлемента в организме самостоятельно, и потому врачи рекомендуют пациентам принимать медикаментозные препараты.
Чаще всего назначаются лекарства в виде таблеток, реже, в случаях сбоев в работе кишечника – парентеральное введение.
Лекарственные препараты при железодефицитной анемии должны употребляться длительным курсом (в течение нескольких недель или месяцев).
Все они предназначены для приведения в норму основных показателей при анализе крови и устранения симптомов болезни. Наиболее часто применяемые из них:
- Гемофер пролонгатум;
- Сорбифер Дурулес;
- Ферроцерон;
- Ферроплекс;
- Тардиферон.
Перед применением лекарственных средств необходимо проконсультироваться с врачом, неграмотное употребление может привести к переизбытку железа, что также чревато негативными последствиями и осложнениями.
В сложных случаях заболевания анемией может возникнуть необходимость в проведении операции по переливанию эритроцитов. Данная процедура может понадобиться при наличии серьезной угрозы жизни больного и должна быть проведена в минимально возможный промежуток времени. Показанием для назначения переливания эритроцитов может стать:
- значительная потеря крови;
- резкое уменьшение уровня гемоглобина;
- подготовка к хирургическому вмешательству или скорым родам.
Для успешного проведения этой процедуры и отсутствия осложнений очень важно, чтобы кровь донора идеально подходила пациенту по всем лабораторным показателям.
Степень сложности такого заболевания, как железодефицитная анемия на сегодняшний день является достаточно низкой.
При своевременном обнаружении симптомов и проведении качественно диагностики этот недуг может быть полностью устранен без каких-либо последствий.
В некоторых случаях развитие осложнений при лечении ЖДА может произойти. Причинами для этого могут послужить следующие факторы:
- неграмотное проведение диагностических процедур и, как следствие, установление ложного диагноза;
- не выявление первой причин;
- несвоевременное принятие мер по лечению;
- неправильная дозировка назначенных лекарств;
- несоблюдение регулярности лечения.
Возможные осложнения данного заболевания это:
- у детей – задержки роста и интеллектуального развития. Детский дефицит железа является очень опасным, так как в запущенных случаях заболевания сбои в организме ребенка могут стать необратимыми;
- анемическая кома, которая развивается на фоне некачественной циркуляции кислорода в организме, в частности, из-за недостаточного обеспечения кислородом мозга. Характерные признаки этого осложнения – обморочные состояния, ослабленные и замеленные рефлексы. При неоказании своевременной квалифицированной помощи врачей создается сильная угроза для жизни больного;
- появление сердечной недостаточности – частое явление при долгой нехватке железа в организме;
- инфекционные заболевания при анемии могут стать причиной для развития сепсиса.
Данные виды осложнений представляют наибольшую угрозу для пациентов детского и преклонного возраста.
источник