Врожденная микросфероцитарная анемия — гемолитическая анемия, в которой нарушается структура эритроцитов, то есть красных кровяных телец. Тахикардия и спленомегалия являются типичными симптомами наследственного гемолитического гепатита. У ребенка они обнаруживаются сразу после рождения. Также проводится диагностика заболевания в основном на результатах анализа крови с мазком, мочой. Болезнь нельзя вылечить, терапия уменьшает симптомы.
Микросфероцитарная анемия относится к группе гемолитической анемии. В классификации ICD-10 она упоминается как врожденная гемолитическая желтуха без выделения желчных мочевых путей, а также анемия Минковского-Шоффара. Она может быть унаследована, причем врожденная гемолитическая анемия диагностируется гораздо чаще.
Это наиболее распространенный вид наследственных анемий, возникающих с частотой 1 на 5000 человек. Из-за генетической мутации существует дефицит белков, которые создают мембраны эритроцитов — они принимают сферическую форму. Это приводит к их обширному разрушению в селезенке и в просвете кровеносных сосудов.
В 10-20% болезнь не наследуются, и мутация появляется спонтанно. Предварительно приобретенная анемия Минковского-Шоффара у детей может сопровождаться аутоиммунной гемолитической анемией, когда антитела разрушают эритроциты, неправильно признавая их чужеродными. Поэтому нельзя предотвратить развитие микросфероцитарной анемии и провести эффективную профилактику. Вот почему так важно диагностировать анемию Минковского-Шоффара как можно скорее, а затем осуществить соответствующее лечение.
Симптомы сфероцитарной анемии могут иметь разную степень тяжести, что является основой для классификации болезни при тяжелом, умеренном или легком течении. Этот тип гемолитической анемии может характеризоваться едва заметными симптомами, особенно в легкой форме заболевания. Если в семье присутствует врожденная микросфероцитарная анемия, симптомы не должны усиливаться.
Наиболее распространенными симптомами анемии Минковского-Шоффара являются:
- пожелтение кожи и слизистых оболочек (гемолитическая желтуха);
- увеличение селезенки (спленомегалия);
- холелитиаз как осложнение хронического гемолиза;
- общие симптомы гемолитической анемии: слабость, расстройства концентрации, головные боли и головокружение, плохая переносимость, ускоренный пульс.
Симптомы врожденной микросфероцитарной гемолитической анемии у детей появляются сразу после рождения или в раннем детстве. В крайних случаях болезнь приводит к смерти.
В дополнение к возникновению характерных симптомов и положительной семейной истории результаты лабораторных тестов имеют ключевое значение.
Исследования по наследственной микросфероцитарной анемии включают:
- Анализ крови с мазком, где можно заметить изменения, характерные для анемии: пониженные эритроциты (низкий уровень эритроцитов), сниженный гемоглобин; в мазке видны сфероциты, то есть сферические эритроциты и фрагменты дезинтегрированных клеток крови и повышенный ретикулоцитил.
- Биохимический анализ крови на увеличение билирубина, повышенную лактатдегидрогеназу, увеличение калия (гиперкалиемия) и гаптоглобина в крови.
- Анализ мочи, указывающий на присутствие уробилиногена, и определение стула стериколиногена.
Характерным исследованием, подтверждающим наследственную гемолитическую анемию, является тест на резистентность эритроцитов и тест с подкисленным глицерином. Эти тесты включают лечение крови пациента гипотоническим хлоридом натрия и глицерином, определение степени гемолиза эритроцитов.
Чтобы проверить, врожденная или приобретенная гемолитическая анемия, проводится прямой тест на антиглобулины Кумба, что дает положительный результат только в случае приобретенной анемии Минковского-Шоффара.
Кроме того, проводятся визуализационные обследования, такие как компьютерная томография или ультразвук брюшной полости и рентгенография грудной клетки.
В случае наследственной микросфероцитарной гемолитической анемии лечение невозможно, как и устранение ее причин. Если симптомы наследственной гемолитической желтухи усиливаются, используется лечение, типичное для каждой анемии: переливание концентрата эритроцитов, стероидная терапия, инъекция эритропоэтина, стимулирующего синтез эритроцитов.
Спленэктомия предназначена только для самых тяжелых случаев, особенно при холелитиазе (тогда фолликул также удаляется). Удаление селезенки не проводится у ребенка в возрасте до 7-8 лет.
Для профилактики послеоперационной инфекции все пациенты, получившие разрешение на спленэктомию, вакцинируются против пневмококков, менингококков и гемофилов.
источник
Микроцитарная гемолитическая анемия относится к наследственным заболеваниям. Наследуется по аутосомно-доминантному типу. Сущность патологического процесса заключается в дефекте структуры мембраны эритроцитов. В эксперименте на мышах показано, что при наследственном микросфероцитозе отсутствует белок мембраны эритроцитов спектрин. Костный мозг при этом продуцирует неполноценные эритроциты, отличающиеся от нормальных тем, что они меньшего диаметра и имеют форму не двояковогнутой, а двояковыпуклой линзы, вследствие чего и названы микросфероцитами. При этом объем эритроцитов остается в пределах нормальных колебаний, и анемия, являясь по существу сфероцитарной, микроцитарной не является. Название же «микросфероцитарная» отражает тот факт, что за счет изменения формы и уменьшения диаметра эритроцитов в мазке крови они выглядят аналогично микроцитам. Аппаратный же анализ показывает нормальные параметры красных клеток крови.
Мембрана таких эритроцитов обладает повышенной проницаемостью для ионов натрия. Это приводит к их набуханию. Сферическая форма и особенности структуры белка мембраны эритроцитов нарушают их способность проходить узкие места кровотока без повреждений и разрушения. Основным местом гемолиза является селезенка, исследования показали, что продолжительность жизни эритроцитов у таких больных составляет 8-15 дней вместо 90-120 у здоровых людей.
Первые признаки заболевания могут проявиться в детском возрасте, но чаще — в юношеском и зрелом. В течение длительного времени единственным признаком болезни является желтушное окрашивание склер и кожи. Течение волнообразное. Причиной усиления гемолиза и, соответственно, ухудшения состояния чаще всего являются инфекция, переохлаждение, беременность. Развивается слабость, появляются одышка и учащенное сердцебиение при физической нагрузке. Степень интенсивности желтухи может быть различной: от незначительной до резко выраженной. С каждым обострением желтушность усиливается. На фоне хронической интоксикации и гипоксии тканей могут наблюдаться отставание в росте и физическом развитии, снижение толерантности к физическим нагрузкам. У больных возможны скелетные аномалии в виде высоко стоящего твердого нёба («готическое нёбо») и др.
Следует иметь в виду, что течение этого вида гемолитической анемии может осложняться желчнокаменной болезнью вследствие образования желчных камней. В таких случаях возможно появление болевых приступов в правом подреберье. Интенсивность желтухи усиливается за счет присоединения обтурационного механизма. Характерным признаком заболевания является увеличение селезенки, а в дальнейшем и печени. Селезенка может увеличиваться до значительных размеров, что обусловлено усиленным гемолизом в ней эритроцитов.
В период обострения в моче повышается содержание уробилина, а в кале — стеркобилина. Содержание эритроцитов и уровень гемоглобина в период ремиссии может быть в норме, а в период усиления гемолиза развивается малокровие. Обращает на себя внимание наличие в периферической крови эритроцитов меньшего диаметра при сохранении или даже увеличении их объема. Сфероциты интенсивно окрашены и не имеют просветления в центре. Такие эритроциты обладают пониженной осмотической стойкостью. Гемолиз их может начинаться при концентрации натрия хлорида 0,60-0,70 % вместо 0,44-0,46 % в норме. Понижена и их резистентность. Как и для любой другой формы гемолитической анемии, характерно повышение количества ретикулоцитов, что свидетельствует об ускоренном их вымывании из костного мозга. Количество лейкоцитов как правило, не изменяется. В костном мозге наблюдается выраженная гиперплазия эритроидных клеток. Их количество может повышаться до 30-50% вместо 15-25% в норме.
Лечение. При стабильном течении, когда заболевание проявляется слабо выраженной желтушной окраской кожи, при хорошем самочувствии и отсутствии признаков анемии каких-либо особых методов лечения не требуется. При частых гемолитических кризах, сопровождающихся развитием анемии и осложнениями (желчнокаменная болезнь, инфаркт селезенки), показана спленэктомия. После спленэктомии исчезает желтуха, нормализуются уровень гемоглобина и количество эритроцитов, снижается количество ретикулоцитов, улучшается функция печени, содержание билирубина в сыворотке крови снижается до нормальных показателей. Однако характер эритропоэза не изменяется. Остаются микросфероцитоз и пониженная осмотическая стойкость эритроцитов. Улучшение состояния достигается лишь за счет удаления органа, где совершается наиболее интенсивный гемолиз эритроцитов, что приводит к увеличению продолжительности их жизни.
источник
Основные этапы патогенеза наследственного микросфероцитоза
Изменение белка в мембране эритроцита — первопричина дефекта красных кровяных клеток; нарушение транспорта катионов — вторично. Этой точки зрения в настоящее время придерживается преобладающее число исследователей. Существует мнение, что изменения белка вторичны, поскольку они обнаруживаются не только при наследственном сфероцитозе, но и при аутоиммунной гемолитической анемии. Обобщая данные литературы, основные патогенетические звенья наследственного микросфероцитоза можно представить в следующем виде. Наследственный дефект мембраны эритроцита приводит к повышенной проницаемости ее для ионов натрия, что, в свою очередь, содействует возрастанию интенсивности гликолиза, повышению интенсивности метаболизма липидов, потере поверхностных субстанций, изменению объема клетки, формированию стадии макроцита. Макроциты при движении на уровне селезенки начинают испытывать механическое затруднение, в связи с чем они длительно задерживаются в красной пульпе, подвергаясь всем видам неблагоприятных воздействий (гемоконцентрация, изменение рН, активная фагоцитарная система). Неблагоприятные условия обмена в селезенке способствуют повреждению мембраны, что еще более увеличивает сферичность клетки и содействует формированию стадии микроцитов. Уменьшенный внутриклеточный рН микросфероцитов способствует торможению их гликолитической активности в условиях недостаточного снабжения глюкозой в микрососудах селезенки, что сопровождается снижением активности транспорта ионов, повышением осмотического содержания клетки и осмотическим лизисом. Селезенка при данном заболевании, по мнению ряда авторов, активно наносит эритроцитам повреждение, содействуя еще большей фрагментации эритроцитарной мембраны и сферуляции. Этот факт нашел подтверждение в электронно-микроскопических исследованиях, которые обнаружили в эритроците ультраструктурные изменения, выражающиеся утолщением клеточной мембраны, ее разрывами и образованием вакуолей. Через 2—3 пассажа через селезенку микросфероцит подвергается лизису и фагоцитозу. Фагоцитарная гиперактивность селезенки, в свою очередь, вызывает прогрессирующую гиперплазию органа и дальнейшее повышение его фагоцитарной активности. Нормализация срока жизни эритроцитов после операции свидетельствует о том, что только фагоцитарная активность селезенки опасна для сфероцита, печень же в этом отношении остается интактной. То же самое подтверждается и исследованиями с радиоактивным хромом, выявляющими резкое повышение радиоактивности печени и селезенки при аутоиммунных гемолитических анемиях и только селезенки — при сфероцитозе. Следовательно, при сфероцитозе гемолиз зависит в основном от формы эритроцита. Селезенка является местом деформации и гибели эритроцитов. Гемолитический процесс при наследственном микросфероцитозе приводит к анемии и гипоксии, гиперцеллюлярной реакции костного мозга с выбросом в периферическую кровь эритроидных клеток, усиленному образованию и экскреции желчных пигментов. Большой интерес представляют работы, в которых было показано, что в эритроцитах больных наследственным микросфероцитозом, инкубируемых в среде без глюкозы, происходит прогрессивное снижение содержания липидов (преимущественно холестерола, сфингомиелина й лецитина), которое предшествовало уменьшению осмотической стойкости. Добавление глюкозы замедляло, но не предупреждало потери клеточных липидов сфероцитами. Фосфолипиды, как установлено, принимают участие в транспорте катионов через клеточную мембрану, и обмен их ускоряется при увеличении скорости вхождения натрия в клетку. Эти компоненты необходимы для поддержания постоянства структуры липопротеидного слоя мембраны, и ускоренный их метаболизм в сфероцитах, обусловленный повышенной скоростью транспорта натрия, приводит к потере мембранных компонентов клетки. В эритроцитах, утрачивающих как холестерин, так и фосфолипиды (что провоцируется нарушением гемостаза, в первую очередь в отношении глюкозы, и приводит к прогрессированию микросфероцитоза), нарушения мембраны необратимы, и такие клетки нежизнеспособны in vivo. Определенное значение в изменении формы эритроцитов имеет пониженное содержание в клетке АТФ, так как механические свойства эритроцитов (способность к деформации и фильтруемость) резко уменьшаются при падении уровня этого макроэрга в клетке, что сопровождается появлением микросфероцитоза. Эритроциты больных наследственным микросфероцитозом обладают, таким образом, следующими особенностями метаболизма: повышенным аутогемолизом, частично корригируемым глюкозой и АТФ, увеличенной скоростью гликолиза (последний аномально чувствителен к лишению глюкозы), повышенной скоростью прохождения натрия через клеточную мембрану, увеличенной потерей холестерина при инкубации в среде, содержащей глюкозу, и ускоренной и равномерной утратой липидов (холестерина и фракций фосфолипидов) при инкубации этих клеток в среде, лишенной глюкозы. Разрушение эритроцитов начинается в периферической крови и заканчивается в макрофагах, в которых из гемоглобина образуется билирубин и выделяется ими в периферическую кровь. Этот неконъюгированный (свободный) билирубин не выводится почками, поскольку содержит высокомолекулярное соединение глобин, задерживаемый внутренним слоем капсулы Шумлянского— Боумена. С током крови билирубин попадает в печень, там гепатоциты отщепляют глобин и образуют новое соединение, состоящее из порфириновой цепи. Это соединение выделяется желчью и называется конъюгированным билирубином. Являясь низкомолекулярным соединением, последний свободно проходит почечный фильтр. Неконъюгированный билирубин (дает «непрямую» реакцию с диазореактивом), нерастворимый в воде, в печеночной клетке соединяется с глюкуроновой кислотой, которая придает ему растворимость в воде, способность проходить через почечный фильтр и быструю (прямую) реакцию с диазореактивом. Неконъюгированный билирубин (гемобилирубин) в больших концентрациях токсичен, растворяется в жирах и легко проникает в нервные клетки коры головного мозга, расстраивая в них процессы окислительного фосфорилирования. Для проникновения неконъюгированного билирубина в печеночную клетку необходимо-наличие активного фермента глюкуронилтрансферазы. Таким образом, уровень гипербилирубинемии зависит как от количества внутриклеточно распадающихся эритроцитов, так и от функциональных способностей печеночной клетки «обезвреживать» этот билирубин, переводить его в водорастворимый билирубиндиглюкуронид. КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ. Первые признаки заболевания могут проявиться и в детском возрасте, но чаще — в юношеском и зрелом. При заболевании микросфероцитозом отмечают желтуху, анемию, спленомегалию, изменение скелета. В течение длительного времени единственным признаком заболевания является желтушное окрашивание склер и кожи. Течение волнообразное. Причиной усиления гемолиза и, соответственно, ухудшения состояния чаще всего является инфекция, переохлаждение, беременность. Развивается слабость, появляется одышка и учащенное сердцебиение при физической нагрузке. Степень интенсивности желтухи может быть различной: от незначительной до резки выраженной. С каждым обострением желтушность усиливается. У детей первых месяцев жизни с функциональной слабостью гепатоцитов гипербилирубинемия бывает особенно высокой с резко выраженной желтухой и поражением ядер головного мозга (ядерная желтуха). У детей старшего возраста проявление заболевания (кризов) нередко осложняется желчно-каменной болезнью, причем билирубиновые камни при рентгеноскопическом исследовании не обнаруживаются.
источник
При анемии в крови резко снижается уровень гемоглобина. С этим заболеванием в течение всей жизни приходится сталкиваться многим людям. Более того, не обходит оно стороной даже маленьких детей. Большинство разновидностей недуга обусловлены плохим питанием, дефицитом витаминов или приемом некоторых препаратов. После устранения провоцирующего фактора все симптомы купируются. Среди всего многообразия патологических процессов выделяется один сложный и весьма опасный. Это гемолитическая анемия Минковского-Шоффара. Именно о ней речь пойдет в сегодняшней статье.
Под анемией принято понимать состояние организма, характеризующееся резким снижением показателей эритроцитов и гемоглобина. Некоторые разновидности заболевания приводят к изменению формы красных кровяных клеток. С течением времени они утрачивают первоочередные функции.
Анемия часто сопровождает различные заболевания, но никогда не бывает первичной. Именно поэтому не стоит оставлять расстройство без внимания. Необходимо как можно быстрее найти его причину и постараться устранить.
Понятие «гемолитической анемии» включает в себя обширную группу заболеваний. Все они характеризуются общим патогенезом. Усиленное разрушение эритроцитов приводит к увеличению продуктов их распада и к нарастанию эритропоэза. Цикл формирования красных телец нарушается. Процессы их разрушения постепенно начинают превалировать над механизмами появления и вызревания.
Все гемолитические анемии условно подразделяются на две группы: наследственные и приобретенные. В этой статье мы более подробно остановимся на первом варианте. Если быть точнее, то рассмотрим, что представляет собой наследственная анемия Минковского-Шоффара.
В медицинских справочниках можно встретить несколько названий, описывающих патологический процесс. Это и микросфероцитарная анемия, и наследственный сфероцитоз, и болезнь Минковского-Шоффара. Чаще всего используется последнее наименование по фамилиям ученых-первооткрывателей.
Данное заболевание считается весьма распространенным (1 случай на каждые 5 тыс. населения). Диагностируется преимущественно у жителей Северной Европы. Первые признаки становятся заметны у детей в раннем возрасте. Если не приступить к лечению недуга своевременно, его течение негативно отразится на функционировании всего организма.
Анемия Минковского-Шоффара сопровождается нарушением структуры и функций клеточной мембраны эритроцитов. В результате происходящих процессов они меняют свою форму на круглую, становятся хрупкими. Появляются первые признаки гемолиза — разрушения красных кровяных клеток с одновременным выделением гемоглобина.
У здорового человека эритроциты по своей форме напоминают двояковогнутый диск, благодаря чему они беспрепятственно передвигаются по сосудам. При анемии в мембране этих элементов синтез белка нарушается. Это приводит к проникновению жидкости внутрь клеток. По этой причине они меняют свою форму. Проходя через сосуды, эритроциты сильно деформируются, а через некоторое время начинают разрушаться. На фоне происходящих процессов уровень красных кровяных элементов резко падает, развивается гемолитическая анемия.
Если у одного из родителей ранее уже был диагностирован этот недуг, он обязательно перейдет по наследству ребенку. Крайне редко больные дети рождаются у совершенно здоровых мам и пап. В этом случае анемия развивается на фоне изменений в ДНК. Первичная генная мутация происходит еще во время внутриутробного развития плода.
Обязательным условием развития болезни является воздействие на организм матери следующих факторов:
- радиация, рентгеновское излучение;
- интоксикация солями тяжелых металлов, наркотическими веществами, никотином;
- вирусная атака.
Клиническая картина во многом определяется степенью тяжести патологического процесса и количеством измененных эритроцитов. Первые его симптомы можно наблюдать у детей дошкольного и раннего школьного возраста. Течение анемии этого вида обычно волнообразное. Приступы гемолитического криза, когда происходит одновременное разрушение большого числа эритроцитов, сменяются периодами затишья. При этом симптомы могут чуть отличаться.
Например, межприступный период болезни проявляется признаками анемии. Среди них можно выделить бледность кожных покровов, слизистых и склер глаз. При гемолитическом кризе клиническая картина видоизменяется и сопровождается следующими симптомами:
- Повышение температуры до 38 градусов, головная боль, общее недомогание.
- Развитие желтухи.
- Боль в животе, отличающаяся спастическим характером.
- Дискомфорт в области печени из-за ее увеличения.
- Воспаление селезенки.
Наследственная гемолитическая анемия Минковского-Шоффара встречается и у взрослых. Наиболее частой причиной обращения к врачу в этом случае служит желтушность кожных покровов. Однако в большинстве случаев этот недуг протекает бессимптомно. Пациенты узнают о его существовании случайно и обычно во время профилактического осмотра.
Диагностика анемии Минковского-Шоффара достаточно проста. При подозрении на заболевание и появлении начальных его признаков следует обратиться за помощью к врачу. Патологии кроветворной системы находятся в компетенции гематолога. После изучения жалоб пациента и его семейного анамнеза специалист должен осмотреть кожные покровы и склеры, провести пальпацию живота. В обязательном порядке назначается УЗИ печени и селезенки, поскольку одним из симптомов недуга является увеличение в размерах этих органов.
Одновременно гематолог дает направление на ряд лабораторных анализов. Гемолитическая анемия Минковского-Шоффара подтверждается при наличии следующих изменений:
- Моча: гемоглобинурия, повышение показателей белка и уробилина.
- Биохимия крови: снижение холестерина, рост лактатдегидрогеназы, увеличение непрямого билирубина.
- Исследование эритроцитов: выраженный ретикулоцитоз, сокращение размеров клеток, понижение их осмотической устойчивости.
- Общий анализ крови: ускорение СОЭ, незначительное снижение тромбоцитов и лейкоцитов, сокращение цветового показателя.
Гемолитическая анемия Минковского-Шоффара у детей иногда вызывает трудности во время диагностики. Это заболевание имеет схожие с другими аутоиммунными патологиями симптомы. Поэтому врачи должны знать некоторые отличительные и характерные именно для данного вида анемии признаки.
В первую очередь речь идет о наследственной предрасположенности. Только в исключительных случаях оба родителя оказываются абсолютно здоровыми. С другой стороны, у больного ребенка прослеживаются явные изменения в костях черепа. В сомнительных случаях дополнительно назначается проба Кумбса. Если анализ отрицательный, у пациента подтверждается анемия Минковского-Шоффара. Диагностика на этом считается завершенной.
Терапия анемии подбирается с учетом ее тяжести. В период затишья, как правило, вмешательство не требуется. Во время очередного приступа больного сразу госпитализируют.
Консервативное лечение анемии Минковского-Шоффара включает в себя следующие меры воздействия:
- Заместительная терапия эритроцитарной массой, если уровень гемоглобина в крови падает до отметки 70 г/л.
- Лечение альбуминами назначается при высоких показателях билирубина.
- Для дезинтоксикации организма используется инфузионная терапия.
- В период отсутствия выраженного гемолитического криза показан прием желчегонных препаратов.
Продолжительность такой терапии, конкретные препараты и их дозировка — все эти вопросы решает врач в индивидуальном порядке.
Если микросфероцитарная гемолитическая анемия Минковского-Шоффара протекает в тяжелой форме, консервативное лечение не справляется с заявленными задачами, пациенту рекомендуется операция по удалению селезенки. Такой подход не позволяет полностью вылечить недуг. С другой стороны, после вмешательства заметно сокращается число разрушенных эритроцитов, а их жизненный цикл удлиняется.
Гемолитические кризы после операции не повторяются, но она имеет ряд противопоказаний. Например, удаление селезенки не рекомендуется детям младше 5 лет по причине высокого уровня смертности в послеоперационный период. Негативной стороной процедуры считается снижение сопротивляемости организма по отношению к вирусным и грибковым инфекциям.
Альтернативным вариантом удаления селезенки считается эндоваскулярная окклюзия. Это еще один метод лечения, к помощи которого часто прибегают при диагнозе «микросфероцитарная анемия Минковского-Шоффара». В ходе процедуры врач вводит в орган лекарство, которое провоцирует спазм и приводит к инфаркту селезенки. Некоторая ее часть после этого сохраняет полноценное кровоснабжение и не утрачивает способность сопротивляться инфекциям.
Гемолитическая анемия Минковского-Шоффара у детей дошкольного возраста часто приводит к отставанию в психическом и физическом развитии. Особенно если родители долго не обращались за медицинской помощью или игнорировали рекомендации врача.
У взрослых пациентов наиболее распространенным осложнением считается желчнокаменная болезнь на фоне нарушения билирубинового обмена. Все дело в том, что гемолитический криз часто воспринимают за начало развития механической желтухи, поэтому правильное лечение откладывается. При наличии камней в желчном пузыре рекомендуется проведение холецистэктомии вместе со спленэктомией.
При легком течении заболевания и своевременно проведенной операции по удалению селезенки прогноз благоприятный. Ремиссия обычно наступает сразу после гемолитического криза. Ее продолжительность может варьироваться, но в большинстве случаев составляет около двух лет.
Анемия Минковского-Шоффара носит наследственный характер. Поэтому предупредить возникновение заболевания не представляется возможным. В целях профилактики тяжелых форм недуга пациентам с выявленной формой анемии рекомендуется периодически проходить полное обследование у гематолога.
При планировании беременности следует понимать, что вероятность развития заболевания у будущего ребенка составляет 50%. Поэтому новорожденному также показано постоянное наблюдение у врача для выявления патологии на ранней стадии.
источник
Наследственный сфероцитоз – патология, при которой внутриклеточные дефекты провоцируют разрушение эритроцитов, вследствие чего и развивается анемия Минковского Шоффара. Согласно статистике, болезнь выявляется у 2 человек из 10 тыс. Чаще диагностируют патологию у грудных младенцев, но симптомы у детей будут проявляться позже, ближе к школьному возрасту. Большее количество случаев приходится на мальчиков. Чем в более раннем возрасте проявится болезнь, тем тяжелее будут симптомы.
Причиной развития патологии у детей становится наследственность. Болезнь в 50% случаев есть у близкого родственника. Наследование идет по аутосомно-доминантному признаку – ребенок получает дефектную мембрану эритроцита, через которую проходят ионы натрия.
Из-за указанного дефекта в к клетке скапливается жидкость, эритроцит набухает, его форма меняется на сферическую. Эритроцит по внешнему виду превращается в сфероцит.
Деформированная клетка крови теряет эластичность, в селезенке трансформируется из сфероцита в микросфероцит, утрачивая часть своей мембраны. Все перечисленные процессы значительно укорачивают жизнь кровяной клетки – вместо положенных 120 дней для здорового эритроцита поврежденный живет всего 10 суток.
Гибель кровяных телец сопровождается высвобождением непрямого билирубина, который выводится из организма кишечником и мочевым пузырем, поэтому нередко выявляются камни в желчевыводящих протоках и желчном пузыре.
Микросфероцитарная анемия может проявляться в любом возрасте, включая грудничковый, но признаки патологии приобретают выраженность ближе к начальной школе. У малышей гемолитическая анемия выявляется случайным образом, когда проводится плановое обследование и диагностика патологии.
Если болезнь начинает заявлять о себе у новорожденного, то ее течение будет тяжелым.
Насколько сильно будет проявляться малокровие, будет зависеть от того, как выражен гемолиз, а точнее – насколько сильно происходит процесс разрушение красных кровяных телец. Если на текущий момент обострение болезни отсутствует, то признаков никаких не будет. В период обострения повышается температура, возникает слабое состояние, кружится голова, наблюдается потеря аппетита, может болеть голова.
Основные признаки, которыми характеризуется болезнь Минковского-Шоффара:
- желтуха. Гемолитическая анемия всегда характеризуется желтухой, порой это единственный симптом, который выявляется на протяжении долгого времени у пациента. Выраженность желтухи зависит от того, насколько интенсивно распадаются красные кровяные тельца в организме, как печень соединяет глюкуроновую кислоту с билирубином;
- увеличенная селезенка. Орган начинает выступать за границы ребер примерно на 2-3 см, вызывая тяжесть с левой стороны ребер;
- каловые массы приобретают темно-коричневый цвет, поскольку в них содержится много пигмента стеркобилина;
- если болезнь уже протекает длительно, печень увеличивается в размерах. Если же человек страдает неосложненным гемолизом, габариты печени остаются без изменений;
- возможны приступы холецистита и желчнокаменной болезни, поскольку патология провоцирует формирование камней в желчном пузыре. В случае закупорки желчных протоков конкрементами может начаться механическая желтуха. При таком развитии событий уровень прямого билирубина резко повысится, из-за чего моча приобретает темный цвет. Пациент будет ощущать сильный зуд кожи, повысится температура, справа под ребрами появится боль;
- у детей ранний наследственный сфероцитоз проявляется нарушениями развития костей черепа и скелета лица. При такой болезни у ребенка глазницы сужены, нос седловидный, череп квадратный, зубы развиваются неправильно;
- у молодых людей и пациентов преклонного возраста анемия Минковского-Шоффара может спровоцировать трофические язвы на голени, что вызвано склейкой эритроцитов в мелких капиллярах нижних конечностей;
- анемия может вызвать нарушения в работе сердечно-сосудистой системы.
Выраженность симптомов при анемии бывает разной, патология до определенных сроков себя не выдает, постепенно снижается уровень гемоглобина в крови. Выраженные симптомы характерны для периода обострения. Наследственный сфероцитоз протекает волнообразно – периоды ремиссии чередуются с кризами, когда симптомы часто проявляются.
Гемолитический криз будет проявляться так:
- желтушность кожи и склер, пациент жалуется на сонливость и сильный зуд кожи;
- на фоне разрушения эритроцитов повышается температура;
- если появляются судороги, нужно обращаться в неотложку, симптом неблагоприятный;
- на фоне болей в животе наблюдается тошнота и рвота, учащаются позывы к опорожнению.
То, насколько часто проявляются кризы, сложно связать с какими-либо факторами. У некоторых пациентов, кроме желтухи, нет никаких обострений, и с этой единственной жалобой идут к врачу. Вызвать гемолитический криз может переохлаждение, беременность, присоединенные инфекции.
Иногда анемия настолько бессимптомно протекает, что патология выявляется случайным образом при плановом полном обследовании. Ремиссия может длиться от пары недель до месяцев и даже лет.
Если что-то из перечисленных выше симптомов начало беспокоить, лучше сразу обратиться к специалисту – гематологу. Врач проведет опрос, выяснит наличие болезней в роду, осмотрит пациента. Чтобы выявить точный диагноз, понадобится лабораторная диагностика. Врач даст направление на общий анализ крови, где определят показатель СОЭ, выявят вид и степень тяжести анемии, форму эритроцитов.
Также нужно пройти биохимическое исследование крови, чтобы уточнить уровень железа в крови и билирубина. Не менее важным будет исследование эритроцитной осмотической резистентности. В некоторых случаях может понадобиться костно-мозговая пункция. Такую процедуру назначают только, если врач затрудняется с точной постановкой диагноза, вернее, информации для диагностики анемии Минковского-Шоффара недостаточно.
В дополнение к перечисленному выше списку диагностики могут назначить УЗИ органов в брюшной полости, чтобы оценить размеры селезенки и печени, наличие камней в желчном пузыре.
После выявления диагноза врач может подобрать методику лечения. Терапия будет поэтапной и длительной. Пациенты должны настроиться, что выздоровление займет много времени, а сроки будут зависеть от возраста больного, степени тяжести патологии, показателей анализов.
Если болезнь протекает легко, основной упор делается на коррекцию диеты. Блюда должны содержать необходимые организму микроэлементы, особенно те, что богаты фолиевой кислотой и железом. В рационе должны быть такие продукты: капуста и спаржа, орехи и морковь, кукуруза и бобовые, помидоры и творог, арбузы и цитрусовые, греча и фрукты.
При тяжелом течении анемии пациента госпитализируют, назначают консервативное лечение. Тяжело поддается терапии анемия в преклонном возрасте, у таких пациентов велик риск развития гемолитического криза, а он может привести к смерти.
Спленэктомия или удаление селезенки – операция, которая проводится только в самых крайних случаях, когда консервативная терапия не может остановить заболевание. Если удалить селезенку, это позволит увеличить уровень эритроцитов и гемоглобина в крови. Уже спустя пару дней после операции кожа пациентов приобретает здоровый вид, утрачивая серость и желтушность.
Улучшения подтверждаются и лабораторными исследованиями. Детям спленэктомию делают с 4-6 лет. Желательно не откладывать операцию, если она необходима, поскольку это может привести к опасным изменениям в поджелудочной и печени.
В целях профилактики осложнений люди, склонные к анемии Минковского-Шоффара, должны находиться на учете у врача. Чтобы держать уровень эритроцитов, билирубина и гемоглобина в норме, пациент должен принимать определенные лекарства и витамины, сдавать анализы и контролировать состояние здоровья. Если результаты анализов покажут изменения, состояние начнет ухудшаться.
Тем, у кого анемия протекает в легкой форме, можно сдавать анализы каждые полгода, чтобы контролировать показатели крови. Раз в год такие люди проходят лечение. Около двух десятков лет тому назад лечили анемию гормонами, но сейчас врачи считают такой подход не результативным, поэтому не прибегают к такой практике. Прогноз благоприятный, если была проведена операция по удалению селезенки. В этом случае проявления гемолитической анемии не будут беспокоить и ухудшать состояние здоровья.
Если патология протекает в тяжелой форме, это может вызвать формирование камней в желчном пузыре и цирроз печени. При гемолитическом кризе есть риск отека мозга, в таком случае прогноз негативный.
Беременным назначают отличное от стандартного лечения, здесь важно обезопасить здоровье плода. Врачи рекомендуют применять иммуноглобулин. В крайних ситуациях делают переливание, вливая эритроцитную массу. В любом случае, беременная должна постоянно контролировать состояние, посещая лечащего врача.
Важным условием успешного лечения, как и при других недомоганиях, является своевременная диагностика и лечение. Самостоятельно этот вид анемии не проходит, лечиться по совету знакомых или интернет-друзей не следует, это чревато серьезным ухудшением здоровья.
источник
Наследственная микросфероцитарная гемолитическая анемия (болезнь Минковского-Шоффара) — наследственное заболевание, в основе которого лежит дефект белков мембраны эритроцитов — спектрина, анкирина, а также протеинов 4,2 и 3, что приводит к изменению формы (микросфероцитоз), укорочению продолжительности жизни эритроцитов и их разрушению.
Этиология. Заболевание носит обычно семейно-наследственный характер и передается по аутосомно-доминантному типу.
Эпидемиология. Болезнь распространена в средней и северной полосе России с частотой 2,2 случая на 10 000 населения.
Сводится к по вышенному внутриклеточному гемолизу, происходящему в органах ретикулоэндотелиальной системы, главным образом в селезенке и в меньшей степени в печени, костном мозге и лимфатических узлах. Непосредственная причина гемолиза — генетически обусловленная эритроцитопатия, связанная с дефектом белков цитоскелета эритроцитов. Это приводит к нарушению проницаемости для натрия и образованию сферичных эритроцитов, в силу чего продолжительность их жизни значительно укорачивается (до 7-14 дней вместо 120 в норме).
Клинические проявления
Первые симптомы болезни проявляются обычно в детском возрасте. Обращает внимание желтуха при отсутствии других признаков заболевания. В тяжелых случаях, сопровождающихся частыми гемолитическими кризами, рано появляются симптомы анемии: слабость, головокружение, сердцебиение, потеря аппетита.
Гемолитические кризы возникают под влиянием различных провоцирующих моментов (охлаждение, переутомление, травма, беременность, инфекции и др.) и характеризуются ознобами, повышением температуры, усилением желтухи, резким снижением количества эритроцитов и гемоглобина в крови, увеличением размеров селезенки.
При объективном исследовании отмечается лимонно-желтая окраска кожи и слизистых оболочек, обусловленная увеличенным содержанием в сыворотке крови непрямого билирубина. Значительная часть последнего после трансформации в прямой билирубин с желчью поступает в кишечник, последовательно превращаясь в уробилин и стеркобилин, в результате чего испражнения больных окрашиваются в темно-коричневый цвет. Часть уробилина, всасываясь в кишечнике, направляется по воротной вене в печень, но так как последняя в силу перегрузки не в состоянии перевести все количество уробилина в билирубин, то часть уробилина, минуя печень, поступает в кровь, а затем выделяется с мочой, придавая ей цвет пива или крепкого чая. Моча при гемолитической желтухе не содержит билирубина, так как он находится в крови не в свободном состоянии, а в соединении с белком.
Вторым признаком болезни является увеличение селезенки и в меньшей степени печени за счет резкой гиперплазии ретикулоэндотелиальной системы. При пальпации селезенка плотная, безболезненная и может достигать огромных размеров (1-2 кг).
Часто отмечается склонность к образованию камней в желчном пузыре и желчевыводящих путях с развитием клиники ЖКБ. Выпадению камней в желчном пузыре способствует сгущение желчи, богатой пигментами (плейохромия).
Нередко у больных наблюдаются аномалии развития скелета (башенный квадратный череп, седловидный нос, высокое стояние твердого нёба, отставание в росте, укорочение мизинцев, микрофтальмия и др.) и трофические язвы голени. Последние обусловлены нарушением кровоснабжения конечностей вследствие гемолиза эритроцитов и образования тромбов в капиллярах.
Гематологическая характеристика. Важным признаком заболевания является шарообразная форма эритроцитов без просветления в центре —сфероцитоз, а также микронитоз (диаметр эритроцитов менее 6,5 мкм). В легких случаях заболевания общее количество эритроцитов и гемоглобина не снижается, поскольку усиленная деятельность костного мозга обеспечивает компенсацию повышенного распада эритроцитов. При резко выраженном гемолизе, особенно во время кризов, анемия нарастает. Количество ретикулоцитов повышается до 50-100%о, а в отдельных случаях превышает даже 50%.
Существенно снижена осмотическая устойчивость эритроцитов к разведению — до 0,70-0,50 вместо нормы 0,48-0,32.
Течение болезни волнообразное, со сменой светлых промежутков периодами обострений, сопровождающихся гемолитическими кризами.
Прогноз болезни благоприятен. При отсутствии значительной анемии больные сохраняют трудоспособность в течение многих лет. Однако у некоторых лиц развивается калькулезный холецистит, сопровождающийся частыми приступами печеночной колики. В более редких случаях заболевание протекает с частыми гемолитическими кризами, что ведет к развитию анемии, физической и умственной отсталости, снижению трудоспособности больных.
Диагноз врожденной гемолитической анемии болезни (Минковского-Шоффара) ставится на основании характерной триады — гемолитической желтухи, спленомегалии и гиперрегенераторной анемии.
При дифференциальной диагностике следует иметь в виду приобретенную хроническую гемолитическую анемию типа Гайем-Видаля, а также острые гемолитические анемии, протекающие преимущественно с внутрисосудистым гемолизом.
В клинической картине врожденной и приобретенной гемолитических анемий имеется много общих черт: цикличность течения, наличие желтухи, увеличение содержания непрямого билирубина в сыворотке крови, анемия, ретикулоцитоз, эритробластическая реакция костного мозга и т. д. Приобретенная гемолитическая анемия, в отличие от болезни Минковского-Шоффара, характеризуется тяжелым течением и более выраженной анемией — количество эритроцитов снижается до 2х10 12/л , а НЬ — до 50 г/л. По образному выражению Шоффара, эти больные «более бледны, чем желтушны». В анамнезе у них отсутствуют указания на семейный характер заболевания. При этой форме анемии в крови нередко обнаруживаются антиэритроцитарные агглютинины (положительная проба Кумбса). При врожденной гемолитической анемии спленэктомия дает почти стопроцентный терапевтический эффект, а при приобретенной она обеспечивает неполное выздоровление, причем только в 50% случаев.
Дифференциальный диагноз более подробно представлен в таблице.
От острых гемолитических анемий болезнь Минковского-Шоффара отличается семейно-наследственным характером заболевания, цикличностью течения, наличием типичных гематологических признаков и отрицательной пробой Кумбса.
В отдельных случаях врожденную гемолитическую анемию приходится дифференцировать с билиарным циррозом печени. При этом помогают такие признаки, как повышение количества непрямого билирубина, а главное -наличие типичной гематологической триады (понижение осмотической резистентности эритроцитов, микросфероцитоз, высокий ретикулоцитоз). Кроме того, при болезни Минковского-Шоффара обычно отсутствуют симптомы поражения печени и портальной гипертензии.
источник
Что такое анемия Минковского-Шоффара, как она проявляется? Эти вопросы интересуют многих пациентов. При слове «анемия» возникает ассоциация с «малокровием». Той или иной формой заболевания страдают очень многие, причем нужно знать, что в самостоятельном виде оно не существует. Чаще всего это состояние организма, при котором в крови отмечаются низкие показатели эритроцитов и гемоглобина.
Чаще всего анемия развивается в виде осложнения патологии и бывает разных типов. Например, недостаток витаминов группы В, Е, или С также называют словом «анемия». Однако видов анемии намного больше. Некоторые из них имеют аутоиммунную природу происхождения, их называют гемолитическими.
Анемия Минковского-Шоффара имеет свои особенности. Существует несколько причин, которые способствуют развитию этого состояния организма. Кроме того, существуют некоторые виды гемолитической анемии, которые имеют похожие симптомы.
Это заболевание имеет наследственное происхождение, оно связано с повреждениями белков, которые находятся в мембране эритроцитов.
Их форма становится сферической, что постепенно разрушает селезенку.
Согласно статистике, чаще всего этот вид анемии встречается на европейском континенте, реже — в Африке, заболевание диагностируется и в России.
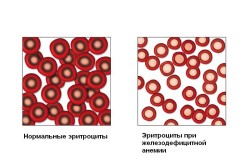
Как передается микросфероцитарная гемолитическая анемия?
- Механизм передачи по наследству этого заболевания лежит в аутосомно-доминантном типе.
- Нередко диагностируется заболевание, которое передается по гетерозиготному принципу.
При анемии этого типа в мембранах эритроцитов появляются дефекты, которые развиваются в результате того, что в клетки поступают ионы натрия в большом количестве.
В клетках появляется избыточное количество воды, в итоге эритроциты принимают сферическую форму. Процесс разрушения структуры мембраны происходит под воздействием макрофагов селезенки, что объясняется нарушением кровообращения.
Существует несколько форм гемолитической анемии, которые диагностируются у подростков и во взрослом возрасте.
Заболевание проявляется следующими симптомами:
- общая слабость;
- повышенная утомляемость;
- головокружение;
- шум в голове;
- одышка;
- тахикардия при физической работе;
- кожа и склеры становятся желтыми;
- образование камней в желчном пузыре;
- болит печень;
- моча становится темного цвета;
- на голенях начинают образовываться трофические язвы;
- может развиться тромбоз;
- пигментация на коже;
- экзема;
- гемангиомы.
Если анемия выявлена еще в детском возрасте, то она протекает с выраженной симптоматикой, которая выражается в деформации скелета и костей черепной коробки.
Нормохромный тип анемии выражен пониженным гемоглобином 90-100 г/л. В состоянии криза, который происходит часто, гемоглобин становится еще ниже — 40-50 г/л. В некоторых случаях заболевание протекает в скрытой форме и может не сопровождаться анемией. При этом отмечается незначительный ретикулоцитоз и возникает реакция костного мозга эритробластического типа.
Таким образом, анемия Минковского-Шоффара является наследственным заболеванием, которое также называется врожденной гемолитической желтухой. Болезнь сопровождается гемолизом печени и селезенки.

Нередко заболевание протекает в хронической форме, иногда даже состоянию глубокой анемии характерно бессимптомное течение. Очень часто появляется выраженная желтуха, при этом размеры селезенки и печени значительно увеличиваются. Для заболевания характерны регулярные обострения и фазы затухания.
Характерным признаком является появление мочи черного цвета. В зависимости от вида анемии, она может протекать в острой или в хронической форме. При холодовой гемагглютиновой анемии симптомы несколько иные: начинают синеть и белеть пальцы на руках и ногах, это приводит к нарушению периферического кровообращения, развивается тромбоз.
Для того чтобы определить развитие заболевания, врач назначает тесты и анализы крови. Для аутоиммунной анемии характерны макроцитоз и микросфероцитоз, нередко обнаруживаются нормобласты. Показатели СОЭ значительно увеличены. Если заболевание протекает в хронической форме, то лейкоциты образуются в пределах нормы. В период криза лейкоцитоз может быть на высоком уровне.
Полную ясность может внести только анализ крови. Очень часто заболевание протекает на фоне аутоиммунной тромбоцитопении. При этом нарушается и эритропоэз, чаще всего он усиливается. В кале появляется большое количество билирубина и стеркобилина. В том случае, если результат положительный, надо выявить, к какому классу относятся антитела.
Характерным признаком анемии данного типа является микросфероз эритроцитов.

- желтуха, которая продолжается длительное время;
- частые появления приступов желчекаменной болезни;
- частые обострения.
Единственным способом решить эти проблемы является спленэктомия.
На сегодняшний день этот способ является наиболее эффективным и применяется при лечении анемии, которая передается по наследству, или приобретенной. Однако при энзимопенической форме вмешательство не результативно или малоэффективно. Заболевание следует лечить, и подходить к этому вполне серьезно.
Чаще всего заболевание осложняется инфарктами и периспленитами, которые являются наиболее распространенным проявлением. Нередко они осложняются состоянием слабости и появлением анемичности. Характерными проявлениями являются трофические язвы в области голени.
Лечение трофических язв обычными способами не приносит никакого результата. Их образование происходит на фоне повышенного гемолиза. После проведения операции заживление язв происходит быстро. В легкой форме заболевание проявляется только незначительными косметическими дефектами. Если анемия протекает в тяжелой форме, то это может привести к инвалидности.
источник
Анемии, обусловленные эритроцитарными факторами
Мембрана эритроцитов в качестве структурной основы, как и другие биомембраны, имеет бислой фосфолипидов, в котором встроены белки. Внутренняя сторона мембраны эритроцитов связана с сетью миофиламентных белков, формирующих цитоскелет и придающий эритроциту в покое специфическую двояковогнутую форму (рис. 51).
При патологии белков и связей между элементами цитоскелета нарушается форма эритроцита. Дефекты цитоскелета сопровождаются развитием эллиптоцитоза (овалоцитоза), сфероцитоза, стоматоцитоза, акантоцитоза.
- Микросфероцитарная гемолитическая анемия (микросфероцитоз, болезнь Минковского-Шоффара)
Наследственно-семейное заболевание, чаще встречается гетерозиготная форма. Наследуется по аутосомно-доминантному типу. Распространенность заболевания составляет 1:5000 населения. Чаще всего болезнь проявляется в возрасте 3-15 лет, однако нередко клинические признаки выявляются в неонатальном периоде. Могут наблюдаться спорадические формы микросфероцитарной анемии.
Патогенез. При микросфероцитозе описаны разнообразные дефекты состава или функции белков мембраны эритроцитов. Наиболее распространена аутосомная доминантная форма, связанная с нарушением взаимодействия спектрина с актином и белком 4.1 или дефицитом белка 4.2, или с комбинированным дефицитом анкирина и спектрина. Кроме того, описана микросфероцитарная анемия из-за отсутствия спектрина, она наследуется как рецессивная аутосомная мутация. У всех больных отмечается дефицит спектрина. Слабое взаимодействие спектринактин может приводить к фрагментации мембраны, снижению площади поверхности мембраны, повышению ее проницаемости, увеличению содержания в клетке осмотически активных веществ. Наследственный дефект мембраны эритроцита способствует повышению проницаемости ее для ионов натрия, воды, что в конечном итоге изменяет объем клетки.
Формирующийся сфероцит при движении в селезенке испытывает механическое затруднение, длительно задерживается в красной пульпе, теряет способность деформироваться в узких участках кровотока в синусах селезенки. Снижение эластичности мембраны приводит к фрагментации при прохождении эритроцита через капилляры, что сопровождается уменьшением размеров эритроцита. Через 2-3 пассажа через селезенку сфероцит подвергается лизису и фагоцитозу (внутриклеточный гемолиз). Патология эритроцитов проявляется морфологической аномалией — микросфероцитозом, который, по данным одних авторов, выявляется в костном мозге на стадии эритробласта в период гемоглобинизации, по другим — форма эритроцита изменяется в периферической крови. Морфологическая аномалия эритроцитов остается на всю жизнь и в случае удаления селезенки. Микросфероциты имеют укороченные сроки пребывания в крови (до 12-14 дней), пониженную осмотическую и механическую резистентность.
Повышенное разрушение патологических эритроцитов происходит в органах РЭС, главным образом в селезенке. Селезенка задерживает и интенсивно гемолизирует неполноценные эритроциты. Развивается вторичная гиперспления, которая усугубляет гемолитический процесс. После спленэктомии срок пребывания сфероцитов в крови значительно возрастает, приближаясь к нормальным.
Клиника. Основной признак заболевания — гемолитический синдром, который проявляется желтухой, спленомегалией и анемией. В зависимости от формы наследования патологии (гомо- или гетерозиготная передача) болезнь может выявляться в раннем детском возрасте или в более поздние периоды жизни. Возникновение заболевания в детском возрасте нарушает нормальное развитие организма, в результате имеются выраженные клинические признаки: деформация скелета, особенно черепа, рано отмечается увеличение селезенки, общая отсталость развития (спленогенный инфантилизм). При гетерозиготной форме заболевания клинические признаки слабо выражены, но имеют место характерные морфологические изменения эритроцитов (микросфероцитоз). Гемолитический криз возникает под влиянием провоцирующих факторов (инфекция, переохлаждение, переутомление, беременность и др.).
Микросфероцитарная гемолитическая анемия имеет хроническое течение, сопровождается периодическими гемолитическими кризами и ремиссиями. В период криза может повышаться температура, появляется желтуха, увеличиваются размеры селезенки, нередко развивается анемия. В период ремиссии признаки заболевания незначительные. Высокий гемолиз и частые гемолитические кризы способствуют быстрому увеличению размеров селезенки, постоянному увеличению концентрации неконъюгированного билирубина в крови, иктеричности склер. Создаются условия застоя желчи в печени, который иногда приводит к осложнениям гемолитической болезни: образованию пигментных камней в желчном пузыре (желчекаменной болезни), ангиохолециститу и др.
Костный мозг гиперклеточный. Эритроидная гиперплазия наблюдается в плоских костях, диафизах и эпифизах трубчатых костей. Развиваются экстрамедуллярные очаги кроветворения в селезенке и других органах. Костномозговое кроветворение гипер- или регенераторное, следствием чего является увеличение количества миелокариоцитов. Преобладают эритробласты, число которых составляет 60-70% костномозговых клеток, соотношение лейко/эритро — 1:1 и более. Созревание эритробластов и выход эритроцитов на периферию идет ускоренными темпами. При интенсивном кроветворении после тяжелого гемолитического криза в костном мозге могут наблюдаться мегалобласты, очевидно, как следствие недостаточности витамина В12 или усиленного расхода фолиевой кислоты. Очень редко в стернальном пунктате обнаруживается эритробластопения — так называемый арегенераторный криз, который имеет обратимый характер.
Кровь. При выраженном некомпенсированном гемолизе анемия нормохромная. Вместе с тем, анемия долгое время может отсутствовать, однако в периферической крови обнаруживаются полихроматофилия и ретикулоцитоз — признаки активного костномозгового эритропоэза. Эритроциты (микросфероциты) характеризуются небольшим диаметром (в среднем 5 мкм), повышенной толщиной и нормальным объемом (МСV). Средняя толщина увеличена до 2,5-3,0 мкм. Сферический индекс (СФ) — отношение диаметра (d) эритроцита к его толщине (Т) -снижен в среднем до 2,7 (при норме 3,4-3,9). Содержание гемоглобина в эритроцитах в пределах нормы или несколько выше ее. Количество микросфероцитов в период ремиссии и при латентной форме болезни не бывает высоким, в то время как в период криза гемолиз может сопровождаться увеличением их до 30% и выше. Микросфероциты в мазках крови имеют небольшой размер, гиперхромные без центрального просветления (рис. 52).
Эритроцитарная гистограмма дает отклонение влево, в сторону микроцитов, RDW в норме или немного повышен.
Особенностью микросфероцитарной гемолитической анемии является постоянно повышенный гемолиз, который сопровождается ретикулоцитозом. В период гемолитического криза количество ретикулоцитов достигает 50-80% и больше, в ремиссии — не превышает 2-4%. Ретикулоциты обладают большим диаметром при нормальной толщине. Могут появляться эритрокариоциты. Гемолитический криз сопровождается небольшим нейтрофильным лейкоцитозом. Тромбоцитарный росток, как правило, не изменен. СОЭ в период криза повышена.
Одним из характерных признаков заболевания является снижение осмотической устойчивости эритроцитов. В норме начало гемолиза отмечается при концентрации NаСl 0,5-0,45%, а полный гемолиз при 0,4-0,35% NаСl. При сфероцитозе показатели резко снижены: гемолиз начинается при 0,7-0,6% NаСl (минимальная стойкость). Максимальная стойкость обычно повышена — полный гемолиз происходит при 0,3-0,4% NаСl. Среди больных микросфероцитарной гемолитической анемией встречаются лица, у которых, несмотря на явный сфероцитоз, осмотическая резистентность эритроцитов нормальная. В этих случаях необходимо исследовать резистентность эритроцитов по отношению к гипотоническим солевым растворам после предварительной их инкубации в течение двух суток. Спленэктомия не устраняет сниженной осмотической и механической устойчивости эритроцитов.
Развитию спленомегалии с синдромом гиперспленизма сопутствует лейкопения, нейтропения и нередко нерезко выраженная тромбоцитопения. Отмечается снижение гаптоглобина. Последствия высокого гемолиза: билирубинемия с преобладанием неконъюгированного билирубина, в моче увеличено содержание уробилиногена, моча имеет коричнево-красный оттенок, каловые массы резко окрашены из-за большого количества стеркобилиногена.
Овалоцитарная гемолитическая анемия (овалоклеточная, наследственный овалоцитоз, эллиптоцитоз)
Редкая форма болезни, наследуется по аутосомно-доминантному типу. Возникает, как правило, из-за молекулярного дефекта белков «скелета» мембраны, одним из которых является спектрин. Описано до 20 различных аномалий белков мембраны. В зависимости от гетеро- или гомозиготной передачи возможны различные клинические и гематологические проявления болезни.
Патогенез. В основе заболевания лежит патология мембраны эритроцитов. Продолжительность жизни овалоцитов в организме укорочена. Заболевание характеризуется внутриклеточным гемолизом с преимущественным разрушением эритроцитов в селезенке.
Клиника. Как аномалия овалоцитоз в большинстве случаев представляет собой бессимптомное носительство без клинических проявлений. При гомозиготной форме клинические признаки овалоцитарной анемии практически не отличаются от микросфероцитоза. Заболевание характеризуется хроническим нетяжелым течением с гемолитическими кризами, сопровождающимися компенсированным или декомпенсированным гемолизом, желтухой и анемией, уровень которой зависит от компенсаторных возможностей эритропоэза. Больным свойственны спленомегалия, конституциональные изменения скелета, в частности черепа, возможны трофические язвы голени и другие симптомы, которые могут наблюдаться при микросфероцитарной гемолитической анемии.
В костном мозге характерен регенераторный или гиперрегенераторный тип кроветворения с преобладанием эритробластов. Соотношение лейко/эритро составляет 1:3 и более за счет эритробластов в зависимости от активности гемолиза и костномозгового кроветворения.
Кровь. Анемия носит нормохромный характер с высоким ретикулоцитозом. Овалоциты имеют нормальный средний объем (МСV) и среднее содержание гемоглобина (МСН). Наибольший диаметр эритроцитов достигает 12 мкм, наименьший — 2 мкм (рис. 53, 54). Овалоцитоз эритроцитов может составлять от 10 до 40-50% клеток при гетерозиготном носительстве и до 96% эритроцитов при полном носительстве аномальных генов. Осмотическая резистентность овалоцитов понижена, повышен аутогемолиз, СОЭ ускорена.
Овалоцитоз как симптоматическая форма (с небольшим числом овалоцитов) может встречаться при различных патологических состояниях, главным образом при гемолитических анемиях, миелодиспластическом синдроме. Известно сочетание овалоцитоза с серповидноклеточной анемией, талассемией, пернициозной анемией. В таких случаях овалоцитоз носит временный характер и исчезает при эффективной терапии основного заболевания. Поэтому к истинному овалоцитозу следует относить лишь те случаи, при которых не менее 10% эритроцитов имеют овальную форму.
Стоматоцитарная гемолитическая анемия (стоматоцитоз)
Редкая форма заболевания, наследуется по аутосомно-доминантному типу.
Патогенез. В основе заболевания лежит нарушение структуры мембраны эритроцитов. Аномалия эритроцитов сопровождается повышенным их разрушением в РЭС (главным образом в селезенке) вследствие внутриклеточного гемолиза.
Клиника может быть с различными проявлениями: от полной компенсации у носителей патологического гена до тяжелой гемолитической анемии, напоминающей микросфероцитоз. Внутриклеточный гемолиз эритроцитов сопровождается увеличением селезенки, желтухой, имеет место склонность к образованию камней и изменениям скелета.
Костный мозг гиперклеточный за счет расширенного красного ростка. Показатели костномозгового кроветворения зависят от степени выраженности гемолиза и активности эритропоэза. Ремиссия может не сопровождаться анемией, в период криза анемия носит, как правило, регенераторный или гиперрегенераторный характер.
Кровь. Морфологическая особенность болезни — стоматоцитоз (рис. 55), который характеризуется наличием в центре клетки неокрашенного участка в виде вытянутой светлой полосы, напоминающей форму рта (Stoma — рот) или округлой формы. Объем эритроцитов и концентрация гемоглобина не отличаются от нормы, резистентность эритроцитов может быть понижена. В период тяжелых гемолитических кризов наблюдается низкий уровень гемоглобина и эритроцитов. Анемия сопровождается повышенным содержанием ретикулоцитов и неконъюгированного билирубина.
Гемолитические анемии, обусловленные нарушением структуры липидов мембраны эритроцитов (акантоцитоз)
Редкое заболевание, наследуется по аутосомно-рецессивному типу.
Патогенез. Заболевание связано с нарушением липидного обмена. Снижение содержания холестерина, триглицеридов, фосфолипидов в крови отражается на липидном составе мембраны эритроцитов, в них снижена концентрация лецитина, фосфатидилхолина, повышено содержание сфингомиелина; уровень холестерина нормальный, либо повышен, а содержание фосфолипидов нормальное или уменьшено. Все эти нарушения в эритроцитах способствуют снижению текучести мембраны и изменению их формы. Эритроциты приобретают зубчатый контур, похожий на листья аканта, поэтому их называют акантоцитами. Аномальные эритроциты разрушаются главным образом в селезенке вследствие внутриклеточного гемолиза.
В клинике имеют место признаки анемии, гемолиза эритроцитов, симптомы нарушения обмена липидов: пигментный ретинит, нистагм глаз, тремор рук, атаксическая походка.
Кровь. Анемия нормохромная нормоцитарная. Основным морфологическим признаком этой формы гемолитической анемии являются эритроциты с зубчатым контуром — акантоциты (рис. 56), которые могут составлять до 40-80% эритроцитов. Отмечается ретикулоцитоз. Осмотическая стойкость эритроцитов нормальная или сниженная. Количество лейкоцитов и тромбоцитов в пределах нормы.
В костном мозге — гиперплазия клеточных элементов эритропоэза.
Эритроциты такой же формы встречаются при циррозе печени, у пациентов, находящихся на АИК, космонавтов после приземления.
- Беркоу Р. Руководство по медицине The Merck manual. — М.: Мир, 1997.
- Руководство по гематологии / Под ред. А.И. Воробьева. — М.: Медицина, 1985.
- Долгов В.В., Луговская С.А., Почтарь М.Е., Шевченко Н.Г. Лабораторная диагностика нарушений обмена железа: Учебное пособие. — М., 1996.
- Козинец Г.И., Макаров В.А. Исследование системы крови в клинической практике. — М.: Триада-Х, 1997.
- Козинец Г.И. Физиологические системы организма человека, основные показатели. — М., Триада-Х, 2000.
- Козинец Г.И., Хакимова Я.Х., Быкова И.А. и др. Цитологические особенности эритрона при анемиях. — Ташкент: Медицина, 1988.
- Маршалл В.Дж. Клиническая биохимия. — М.-СПб., 1999.
- Мосягина Е.Н., Владимирская Е.Б., Торубарова Н.А., Мызина Н.В. Кинетика форменных элементов крови. — М.: Медицина, 1976.
- Рябое С.И., Шостка Г.Д. Молекулярно-генетические аспекты эритропоэза. — М.: Медицина, 1973.
- Наследственные анемии и гемоглобинопатии / Под ред. Ю.Н. Токарева, С.Р. Холлан, Ф. Корраля-Альмонте. — М.: Медицина, 1983.
- Троицкая О.В., Юшкова Н.М., Волкова Н.В. Гемоглобинопатии. — М.: Изд-во Российского университета дружбы народов, 1996.
- Шиффман Ф.Дж. Патофизиология крови. — М.-СПб., 2000.
- Baynes J., Dominiczak M.H. Medical Biochemistry. — L.: Mosby, 1999.
Источник: В.В.Долгов, С.А.Луговская, В.Т.Морозова, М.Е.Почтарь. Лабораторная диагностика анемий: Пособие для врачей. — Тверь: «Губернская медицина», 2001
источник



