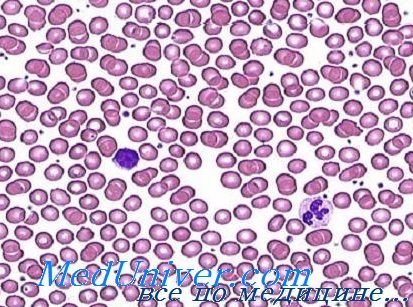
Периферическая кровь при железодефицитной анемии. Свойственные крови морфологические изменения заключаются в микроцитозе и гипохромии. Однако эти признаки отражают длительную недостаточность железа, сочетающуюся с тяжелой анемией. Исходно, когда в процессе гемоглобиногенеза отмечается отрицательное влияние недостаточного подвоза железа в костный мозг, кроветворение начинает приспосабливаться к новым условиям. По началу сокращается объем эритроцитов.
Микроцитоз и нормохромия обычное явление у женщин при показателе гемоглобина от 9 до 10 г на 100 мл. Гипохромия развивается, когда показатель уровня гемоглобина падает до меньших значений, причем вначале она умеренная, а затем становится все более выраженной. При тяжелой форме анемии эритроциты имеют кольчатый аспект (аннулоциты) или обретают вид клеток-мишень. Пойкилоцитоз наблюдается лишь при тяжелых формах анемии (Дачие и сотр.).
Показатели эритроцитов свидетельствуют о небольшом объеме (менее 80 мкг3), о количестве гемоглобина менее 27 пг и о средней концентрации гемоглобина на каждый эритроцит (менее 30 г/100/мл.). В принципе число ретикулоцитов в норме или немного больше; лишь е редких случаях их число занижено. Число эритроцитов обычно нормальное или немного меньшее нормы. Вот почему определение не дает точную справку о тяжести анемии. В отдельных случаях, особенно у детей, число эритроцитов превышает 5 млн/мм3. Следует отметить, что, при железодефицитной анемии увеличивается устойчивость эритроцитов к гипотонии.
Наиболее часто число лейкоцитов укладывается в норму. При длительной недостаточности железа развивается умеренная гранулоцитопения. В некоторых случаях выявляются гиперсегментированные нейтрофилы. Их появление при недостатке железа можно объяснить развитием вторичной недостаточности фолиевокислых солей или витамина В12 (Брукнер и сотр.).
В большинстве случаев показатель численности тромбоцитов высокий, однако еше не разработано четкое объяснение этому явлению. Высказана мысль о возможности появления тромбоцитоза в результате активной кровоточивости. В случаях тяжелой или длительной анемии отмечена умеренная тромбоцитопения, обратимая после проведения железотерапии.
У страдающих железодефицитной анемией количество клеточной массы в костном мозге выше нормы. Рост показателя костномозговых клеток объясняется увеличением числа эритробластов. Последние, в частности полихроматофильные и оксифильные меньших размеров, чем нормальные эритробласты в связи с сокращением количества цитоплазмы. Исследование мазка в условиях железодефицитной анемии выявляет не только малые размеры эритробластов, но также их нерегулярный, «изорванный» контур. В таких клетках были описаны аспекты дисэритропоэза и кариорексиса, почкования ядер, в некоторых случаях многоядерность и ядерные фрагменты.
Непосредственное исследование, без окраски, размозженных на стекле зерен костного мозга не выявляет наличие аггрегатов мелких, нерегулярных, золотистых, характерных гемосидерину частиц. Окраска по Перлсу выявляет отсутствие запасного железа в макрофагах и наличие менее 10% сидеробластов (Дачие и сотр.). В целях определения заболевания железодефицитной анемией этот тест представляет наибольшее диагностическое значение.
Сывороточное железо при железодефицитной анемии. Концентрация железа в сыворотке всегда меньше 50 мкг/100 мл., причем в отдельных случаях она не больше 10 мкг/100 мл. Общая связывающая способность железа (ОССЖ), отражающая количество находящегося в кровотоке трансферина, чаще завышена и лишь в редких случаях укладывается в норму или занижена. У больных с заниженной ОССЖ возможно вмешательство и других факторов, например гипопротеинемии (McGibbon и Mollin5). Насыщение трансферином (железо сыворотки/ОССЖ х 100) в любом случае меньше 16%, однако встречаются и случаи 1%-ой насыщенности.
Следует обратить особое внимание на интерпретацию насыщения трансферином у женщин на последнем квартале беременности. У последних насыщение трансферином менее 16% не всегда указывает на наличие недостатка железа. Объяснение такому явлению следует искать в повышении количества трансферина, что характерно беременным независимо от возможного дефицита железа.
Показатель свободного протопорфирина эритроцитов (СПЭ) в принципе характеризуется высокими значениями — более 70 мкг/100 мл. а в отдельных случаях даже больше 300 мкг/мл. При этом следует обратить внимание на тот факт, что на повышение уровня СПЭ влияет больше продолжительность железо дефицита, чем его интенсивность (Dameshek).
Показатель феритина в сыворотке — растворимой формы находящегося в запасе железа—составляет менее 12 мкг/л. у женщин и детей раннего возраста и менее 35 мкг/л. у мужчин. Существует четкая взаимосвясь сывороточного феритина и количеством железа выявляемого в костном мозге и печени путем окраски по Перлсу.
Кинетика железа. В процессе выявления недостатка железа кинетика последнего не применяется как текущий метод. При использовании этого метода обнаруживается весьма быстрый клиренс железа плазмы, перенос железа в костный мозг и его расход нормальными или увеличенными эритроцитами, при этом интенсивность и скорость метаболизма железа эритроцитов больше нормы. Эти данные свидетельствуют о наличии неэффективного кроветворения в условиях недостатка железа:
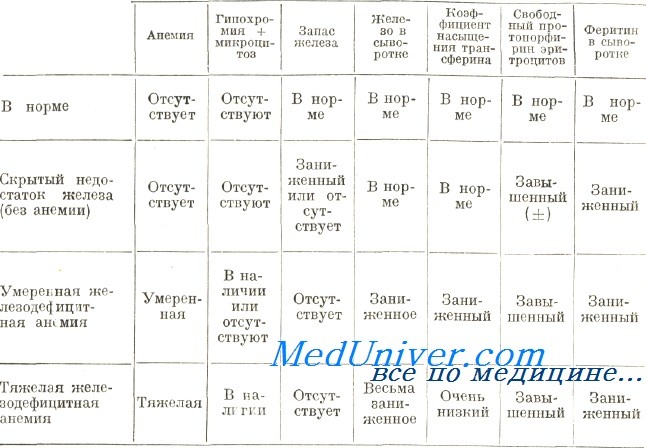
Диагностирование тяжелой железодефицитной анемии по клиническим и лабораторным данным дело несложное, при этом сделанное определение подтверждается терапевтическим испытанием. Осложнения появляются при мало выраженной форме анемии и нечетких клинических и лабораторных признаках. Ниже в таблице приведены морфологические, биохимические и цитохимические данные, на основе которых дифференцируются этапы недостатка железа.
Элементы лабораторного диагноза стадий железной недостаточности
Железодефицитную анемию следует отличать от остальных видов гипохромной анемии. Среди последних, на втором месте по частоте после железодефицитной анемии, находится бета-талассемия (по данным приема для страдающих болезнями крови при Центре гематологии). Учитывая тяжесть заболевания, ранный возраст страдающего и характерную клиническую картину тяжелая бета-талассемия (анемия Кули) распознается без затруднений.
В противоположность этому легкая форма бета-талассемии в отдельных случаях не различима от железодефицитной анемии по клиническим признакам и результатам морфологического исследования крови. Возможные кровоточивость в анамнезе, наблюдаемые в слизистых оболочках и роговых образованиях изменения, равно как и бледность сыворотки подсказывают диагноз железодефицитной анемии. Гипохромия и микроцитоз общее, для обеих групп явление, однако при талассемии они выделяются более ярко.
Отмечаем, что, при талассемии, более характерной чертой микроцитоза это не сокращенный диаметр эритроцитов, а их значительно уменьшенная толщина (микроплатициты). Вот почему выраженная гипохромия с показателем гемоглобина примерно 10 г/100 мл или более подсказывает диагноз талассемии. Также, при железодефицитной анемии с более 8 г/100 мл гемоглобина пойкилоцитоз единичное явление, в то время как при талассемии наблюдается часто. В условиях талассемии выраженный микроцитоз отражается ростом численности эритроцитов, по сравнению с железодефицитной анемией.
Что касается остальных лабораторных данных следует не забывать, что при талассемии чаще наблюдаются такие признаки, как повышенное число ретикулоцитов, полихроматофильных эритроцитов и наличие точечно-базофильных красных кровяных клеток, к тому же осмотическая устойчивость последних больше.
В связи со сказанным для различения этих двух заболеваний наибольшую ценность представляют тесты метаболизма железа. В принципе, при талассемии показатель железа в крови характеризуется нормальными или завышенными значениями. Редко, у больных с хронической кровоточивостью развивается гипосидеремия. В таких случаях ОССТЖ, показатель которой при талассемии отличается низкими значениями (обычно менее 250 мкг/100 мл), увеличивается до нормы и даже более.
За исключением случаев, осложненных недостатком железа, костномозговые запасы железа при талассемии укладываются в норму или несколько больше. В отдельных случаях количество железа в митохондриях нормобластов очень велико, что создает аспект кольчатых сидеробластов.
Анемия с многонедельным течением, развивающаяся при инфекциях и хронических воспалениях, в принципе носит нормоцитный и нормохромный характер, причем эта характеристика действительна и в отношение анемий, наблюдаемых при свежих новообразованиях. Но после длительного течения в условиях этих заболеваний анемия становится микроцитной и гииохромной. В подобном случае различение этой анемии от железодефицитной возможна путем выявления первичного заболевания, в частности посредством лабораторных исследований. Морфологическое исследование крови не представляет данные, способствующие дифференциальному диагнозу.
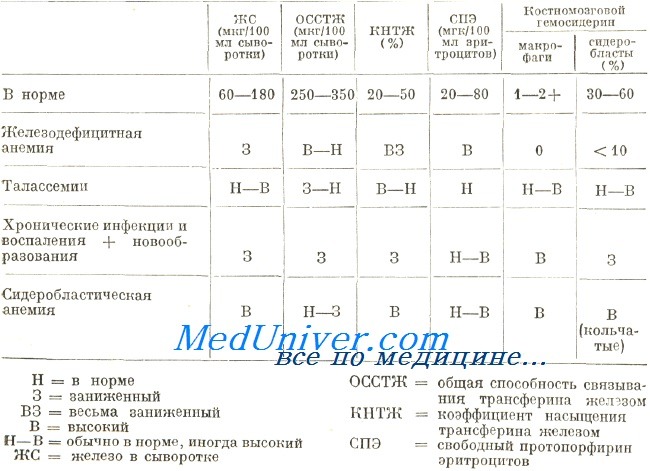
Элементы дифференциальной диагностики при гипохромной анемии
Концентрация железа в сыворотке невелика в обеих группах заболеваний, в то время как показатель ОССТЖ в принципе высокий при железодефицитной анемии и низкий при хронических воспалениях и новообразованиях. По этой причине коэффициент насыщенности трансферина меньше у страдающих железодефицитной анемией. Обследование дополняется определением гемосидерина на костномозговом мазке. В костном мозге страдающих хроническим воспалением и новообразованием содержатся макрофаги, загруженные гемосидерином, который всегда отсутствует в условиях железодефицитной анемии. При обоих заболеваниях сидеробласты обнаруживаются в малом количестве или совсем отсутствуют.
В процессе, диагностирования возникают затруднения и в случае сидеробластической анемии. Тем не менее, в условиях сидеробластической анемии, эритроциты отличаются частным видом. На мазге различаются две популяции эритроцитов, из них одна микроцитная и гипохромная) другая — макроцитная и нормохромная («частичная гипохромия»). Дифференциальная диагностика основывается на определении метаболизма железа, который, при сидеробластической анемии, отражает нормальную или завышенную сидеремию, нормальную или низкую ОССТЖ и высокий показатель гемосидерина в костном мозге с наличием кольчатых сидеробластов.
Из гемолитических анемий наличие гипохромии отмечается при гемоглобинопатиях К, КС, Е, Кёлн. В отдельных случаях наблюдаются клетки мишень. Высокие показатели сидеремии и гемосидерина в костном мозге исключают возможность наличия железодефицитной анемии. Гемолитическая анемия с хроническим внутрисосудистым гемолизом, в частности ночной пароксизмальной гемоглобинурией сочетается с характерной для железодефицитной анемии картиной. Дифференциация возможна по признакам гемолиза и данным лабораторных анализов специфических ночной пароксизмальной гемоглобинурии.
После проведения курса лечения витамином В12 или фолиевой кислотой сидеремия и запасы железа быстро сокращаются под влиянием ускоренного эритропоэза. Это сокращение четко выражено у женщины с небольшим запасом железа. Дифференциальная диагностика представляет трудности, поскольку признаки мегалобластоза в костном мозге исчезают после проведения специфической терапии. В таком случае наиболее важным представляется исследование мазка крови, выявляющее наличие макроцитоза с нормохромией и гиперсегментирование нейтрофилов.
Нередко исследование мазка крови страдающего недостатком железа указывает на наличие нормохромии. Вот почему представляется важной постановка дифференциального диагноза по сравнению с группой нормохромных анемий. Отсутствие костномозгового гемосидерина характеризует железодефицитную анемию, даже при ее умеренной форме.
Необходимо отметить, что в условиях истинной полицитемии, эритроциты нередко гипохромные уже при первом обследовании врача, до вскрытия вен. К тому же обнаруживается невысокая сидеремия и отсутствие костномозгового запаса железа. Тем не менее истинная полицитемия отличается характерной клинической и лабораторной симптоматологией.
источник
Причинами их возникновения является длительное не поступление железа и соответственно уменьшение его запасов в организме. При недостаточном поступлении железа происходит нарушение формирования гемоглобина в эритроците. В этой ситуации образуются эритроциты небольшого размера, они называются микроциты. В микроцитах содержание гемоглобина снижено. При микроскопии препаратов периферической крови в мазке обнаруживаются уменьшение размеров клеток и снижение интенсивности окрашивания (гипохромия) эритроцитов из-за недостатка гемоглобина. Поэтому железодефицитная анемия по морфологическим признакам относится к гипохромной микроцитарной анемии.
К анемии также приводит недостаточное количест во витамина В12 (цианкобаламин) и В9 (фолиевой кислоты), которые необходимы для их нормального созревания и роста кровяных клеток — эритроцитов. Их дефицит сопровождается появлением клеток, которые не способны нормально дифференцироваться в зрелые эритроциты. Появляются аномально крупные клетки – мегалобласты, которые в последствие разрушаются.
Другая часто встречающаяся причина развития анемии – хроническая кровопотеря. Длительные кровопотери приводят к развитию железодефицитных анемий. Они возникают при маточных кровотечениях в период менструаций у женщин. При нормальных менструациях, достаточном питании и при нормальном поступлении железа анемия не развивается. Другой частой причиной развития железодефицитной анемии может быть наличие хронических кровотечений при поражении желудочно-кишечного тракта. К основным причинам относят: язвы желудка и 12-перстной кишки, рак пищевода, наличие полипов, варикозное расширение вен пищевода. Возможны кровопотери при заболевании легких – туберкулез, в запущенных случаях, рак легкого.
К физиологическим причинам, при которых возможно возникновение железодефицитной анемии, относится период беременности и лактации.
Основными клиническими симптомами при железодефицитной анемии (как впрочем, и при других видах анемии) являются: общее недомогание, слабость, снижение работоспособности, аппетита, появление мышечной слабости, атрофии сосочков языка. В запущенных случаях наблюдается одышка и сердцебиение, возможно нарушение обоняния и вкуса. Повышается восприимчивость к вирусным инфекциям. Железодефицитная анемия сопровождается изменениями ногтей, кожи, волос. Ногти становятся ломкими, кожа и волосы сухими.
Диагностика железодефицитных состояний строится на комплексной оценке показателей обмена железа. Диагностика, основанная только на определении содержания железа, может привести при лечении к перегрузке препаратами железа при их назначении и развитию гемосидероза. Диагностика железодефицитной анемии строится на изучении клеточного состава крови при помощи гематологических анализаторов и мазка периферической крови: определения гемоглобина, количества эритроцитов, ретикулоцитов, тромбоцитов, лейкоцитов, эритроцитарных индексов. Изучаются морфологические характеристики эритроцитов. Биохимические показатели включают: определение содержания железа сыворотки, трансферрина, трансферритина, растворимый рецептор трансферрина (sTfR). Измеряют ненасыщенную железосвязывающую способность сыворотки крови/латентную железосвязывающую способность сыворотки (НЖСС, ЛЖСС), общую железосвязывающую способность (ОЖСС), билирубин. В некоторых случаях для проведения дифференциальной диагностики, возможно, необходимо изучение пунктата костного мозга.
Михаил Голубев, д.м.н., эксперт Medaboutme
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
В соответствии с рекомендациями ВОЗ, стандартизованы следующие критерии диагностики железодефицитных анемий у детей:
- снижение уровня СЖ менее 12 мкмоль/л;
- повышение ОЖСС более 69 мкмоль/л;
- насыщение трансферрина железом менее 17%;
- содержание гемоглобина ниже 110 г/л в возрасте до 6 лет и ниже 120 г/л — в возрасте старше 6 лет.
Таким образом, ВОЗ рекомендует достаточно точные критерии для диагностики железодефицитной анемии, однако методы диагностики требуют забора крови из вены и проведения достаточно дорогих биохимических исследований, что не всегда возможно в украинских лечебных учреждениях. Имеются попытки минимизации критериев диагностики железо-дефицитной анемии.
Федеральная служба по заболеваемости, эпидемиологии и образованию (United States Federal Government Centers for Disease Control — CDC) со штаб-квартирой в Атланте (Джорджия, США) рекомендует использовать для диагностики железо-дефицитной анемии 2 доступных критерия: снижение концентрации гемоглобина и гематокрита (Ht) при отсутствии у больного других заболеваний. Устанавливают предположительный диагноз железодефицитной анемии и назначают лечение препаратами железа на 4 нед из расчёта 3 мг элементарного железа на 1 кг массы тела больного в сутки. Достоинство данных рекомендаций — регистрация ответа на терапию препаратами железа по строго фиксированным критериям. К концу 4-й нед лечения концентрация гемоглобина должна повыситься на 10 г/л по отношению к исходной, a Ht — на 3%. Такой ответ подтверждает диагноз «железодефицитная анемия», и лечение продолжают в течение нескольких месяцев. Если ответ не получен, рекомендуют остановить лечение препаратами железа и пересмотреть данный случай с точки зрения диагностики процесса. Перегрузка железом организма за 4 нед при приёме препаратов железа внутрь маловероятна.

Лабораторную диагностику железодефицитной анемии осуществляют с помощью:
- общего анализа крови, выполненного «ручным» методом;
- анализа крови, выполненного на автоматическом анализаторе крови;
- биохимических исследований.
При диагностике любой анемии обязательно выполнение общего анализа крови с определением количества ретикулоцитов. Врач ориентируется на гипохромный и микроцитарный характер анемии. В общем анализе крови, выполненном «ручным» методом, выявляют:
- снижение концентрации гемоглобина ( 12 /л) количество эритроцитов;
- снижение цветового показателя ( 12-16 мм/ч);
- анизоцитоз (характерны микроциты) и пойкилоцитоз эритроцитов.
Ошибка определения параметров может достигать 5% и более. Стоимость одного общего анализа крови составляет около 5 долларов США.
Точным и удобным методом диагностики и дифференциальной диагностики служит метод определения эритроцитарных показателей на автоматических анализаторах крови. Исследование проводят как в венозной, так и в капиллярной крови. Ошибка в определении параметров значительно ниже, чем при «ручном» методе, и составляет менее 1%. При развитии дефицита железараньше всего повышается показатель выраженности анизоцитоза эритроцитов — RDW (норма
Портал iLive не предоставляет медицинские консультации, диагностику или лечение.
Информация, опубликованная на портале, предназначена только для ознакомления и не должна использоваться без консультации со специалистом.
Внимательно ознакомьтесь с правилами и политикой сайта. Вы также можете связаться с нами!
Copyright © 2011 — 2019 iLive. Все права защищены.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Железодефицитная анемия (ЖДА) составляет 70–90% всех случаев анемий [1]. Наиболее предрасположены к развитию ЖДА женщины репродуктивного возраста, беременные, дети раннего возраста (особенно до 1 года), а также пациенты старше 65 лет, нередко страдающие хроническими заболеваниями ЖКТ, почек, алиментарной недостаточностью. ЖДА наблюдается не менее чем у 10–15% взрослого населения России, достигая в отдельных регионах 25–30% среди женщин детородного возраста [2].
Важно помнить, что латентный (скрытый) дефицит железа, при котором ЖДА до определенного времени отсутствует, но транспортные и органные запасы железа уже истощены, наблюдается еще чаще – не менее чем у трети населения, обусловливая многочисленные проявления так называемого сидеропенического синдрома.
В целом, по данным ВОЗ, во всем мире насчитывается сегодня 1,6 млрд больных ЖДА и 3,6 млрд пациентов со скрытым дефицитом железа [3], что подчеркивает медико-социальное значение своевременной диагностики и лечения ЖДА и профилактики дефицита железа.
В норме в организме поддерживается баланс между поступлением и потерями железа. Суточная потребность в железе у взрослого здорового человека составляет примерно 15–20 мг. Около 90% железа, поступающего в костный мозг и другие органы, – это эндогенное железо, освобождающееся при распаде эритроцитов в макрофагах ретикулоэндотелиальной системы селезенки и печени. Экзогенное железо поступает в организм с пищей обычно в количестве 10–15 мг, хотя всасывается не более 10% от этого количества (1,0–1,5 мг). Кстати, обычные потери железа составляют примерно 1 мг/сут. В пище железо в основном находится в окисленном состоянии (Fe3+) и входит в состав белков или солей органических кислот. В желудке под действием соляной кислоты происходит частичная ионизация железа (Fe2+) с образованием его закисной 2-валентной формы. Только в этой форме железо всасывается в кишечнике, преимущественно в двенадцатиперстной кишке. Железо 3-валентное экзогенное (Fe3+), не всосавшееся в кишечнике, выводится из организма в виде окисных соединений.
Абсорбированное 2-валентное железо может быть либо сохранено в пределах клетки в форме ферритина, либо перенесено через базолатеральную мембрану энтероцита в кровь при помощи еще одного белка – ферропортина. Здесь под действием медьсодержащего фермента ферроксидазы (церулоплазмина) железо окисляется до Fe3+ и связывается с трансферрином – гликопротеином, который является основной транспортной формой Fe3+. В составе трансферрина железо доставляется по системе воротной вены в печень и далее в костный мозг и другие органы, где оно используется для синтеза железосодержащих белков (гемоглобина (Hb), миоглобина, цитохромов, Fe-содержащих ферментов и др.) или депонируется в ферритине, который содержится почти во всех тканях и органах, особенно в большом количестве – в печени, селезенке и костном мозге [4].
1. Хронические кровопотери: маточные (меноррагии, миома матки, эндометриоз, внутриматочные контрацептивы); пищеводно-желудочные (язвенная болезнь желудка и двенадцатиперстной кишки, эрозивный гастрит, цирроз печени, злокачественные опухоли); кишечные (болезнь Крона, язвенный колит, дивертикулез кишечника, геморрой, опухоли кишечника); почечные (геморрагический цистит, опухоли почек и мочевого пузыря); геморрагический синдром при нарушениях свертывания крови, заболеваниях печени, системных васкулитах, передозировке антикоагулянтов и т. д.
2. Нарушения всасывания пищевого железа и пристеночного (мембранного) пищеварения в тонком кишечнике и развитие синдрома мальабсорбции: хронические энтериты (инфекционные, болезнь Крона, болезнь Уиппла); дисахаридазная недостаточность, глютеновая энтеропатия (целиакия); опухоли тонкой кишки (лимфомы); пострезекционные синдромы (синдром короткой кишки, синдром слепой кишки); паразитарные инвазии; дивертикулез тонкой кишки; эндокринные заболевания (диабетическая энтеропатия, болезнь Аддисона, гиперпаратиреоидизм, гипертиреоз, гастринома, карциноид с метастазами); внешнесекреторная недостаточность поджелудочной железы; гастрогенная недостаточность всасывания железа (хронический атрофический гастрит, рак желудка, резекция желудка, гастрэктомия).
3. Повышенная потребность в железе: беременность, лактация, интенсивный рост (у детей), заместительная терапия рекомбинантным эритропоэтином больных с хронической почечной недостаточностью, пациентов с миелодиспластическим синдромом и др.
4. Алиментарная недостаточность железа: недостаточное питание, анорексии различного происхождения, вегетарианство.
Важно подчеркнуть, что при перечисленных выше поражениях ЖКТ, являющихся причиной развития ЖДА, как правило, наблюдается также нарушение всасывания витамина В12, фолиевой кислоты и микроэлементов, которые стимулируют процессы нормального созревания эритроцитов в костном мозге [4].
Следует помнить еще об одной важной причине развития гипохромной анемии, особенно у лиц пожилого и старческого возраста, связанной с низким содержанием железа в сыворотке крови. Этот вариант анемии нередко возникает при тяжелых хронических или острых воспалительных и онкологических заболеваниях внутренних органов (сепсис, тяжелые пневмонии, системные заболевания соединительной ткани, злокачественные опухоли различной локализации и др.), при которых развивается анемия, сопровождающаяся снижением содержания сывороточного железа и рефрактерная к лечению пероральными препаратами железа. В патогенезе этой анемии, которая получила название «анемия хронических заболеваний» (АХЗ), или «анемия воспаления», ведущую роль играет нарушение функции белков, регулирующих метаболизм железа в организме, – гепсидина и ферропортинов.
Гепсидин – пептид, синтезируемый печенью. Свою основную функцию обеспечивает, взаимодействуя с рецепторами транспортировки железа из клеток – ферропортинами, ограничивая их функцию и снижая или прекращая транспортировку железа из энтероцитов и макрофагов в плазму крови [5].
При тяжелых хронических и острых заболеваниях внутренних органов, как известно, повышается уровень провоспалительных цитокинов (фактор некроза опухоли-α, интерлейкин (ИЛ) -6, ИЛ-10), стимулирующих образование гепсидина [6, 7], чрезмерная концентрация которого приводит к прекращению функции ферропортинов. В результате железо не поступает в кровь ни из энтероцитов, ни из макрофагов, оказываясь как бы в «клеточной ловушке». Содержание сывороточного железа снижается, что сопровождается развитием анемии, тогда как паренхиматозные органы перегружены железом.
Клиническая картина ЖДА складывается из 2-х основных синдромов: анемического и сидеропенического. Неспецифический анемический синдром, обусловленный гемической гипоксией органов и тканей, характеризуется появлением немотивированной слабости, быстрой утомляемости, головокружений, синкопальных и предсинкопальных состояний, одышки и сердцебиений при небольшой физической нагрузке, повышенной раздражительности, плаксивости. При объективном исследовании у больных выявляются бледность кожных покровов и видимых слизистых, тенденция к снижению АД, тахикардия, функциональный систолический шум над сердцем. О тяжести течения болезни судят обычно по уровню Hb. Легкая степень анемии характеризуется снижением Hb до 120–90 г/л; средняя степень – от 89 до 70 г/л; тяжелая – 69 г/л и ниже.
Сидеропенический синдром, обусловленный тканевым дефицитом железа, нередко выявляемый даже при нормальном уровне Hb, приводит к снижению активности многих ферментов, в состав которых входит железо (цитохромоксидазы, пероксидазы, сукцинат-дегидрогеназы и др.). Это приводит к весьма характерным симптомам – извращению вкуса (pica chlorotica) и обоняния. У лиц с дефицитом железа возникает желание употреблять в пищу мел, уголь, глину, песок, сырое тесто, фарш, крупу, лед, а также пристрастие к неприятным запахам (бензин, ацетон, запах лаков, красок, гуталина и т. д.). Кроме того, у пациентов с дефицитом железа появляются выраженная мышечная слабость и утомляемость, атрофия мышц и снижение мышечной силы в связи с дефицитом миоглобина и ферментов тканевого дыхания. При объективном исследовании определяются сухость кожи, истончение, ломкость и поперечная исчерченность ногтей, койлонихии, ангулярный стоматит, глоссит («лакированный» язык), а также атрофические изменения слизистой оболочки пищевода (сидеропеническая дисфагия), желудка и кишечника (атрофический гастрит, энтерит). Возможно повышение температуры тела до субфебрильных цифр («сидеропенический субфебрилитет»).
Диагностическими критериями анемий считают снижение уровня Hb Литература
- Дворецкий Л. И. Железодефицитные анемии // Русский медицинский журнал. 1997. № 19. С. 1234–1242.
- Цветкова О.А. Медико-социальные аспекты железодефицитной анемии // Русский медицинский журнал. 2009. № 5. С. 387–391.
- WHO/NHD. Iron Deficiency Anaemia. Assessment, Prevention and Control: A guide for programme managers, 2001.
- Ройтберг Г.Е., Струтынский А.В. Внутренние болезни. Лабораторная и инструментальная диагностика. М.: МЕДпресс-информ, 2011. 800 с.
- Kaushansky K., Lichtman M., Beutler E. et al. // Williams Hematology. Anemia of Chronic Disease, 2010.
- Дворецкий Л.И., Дятлов Н.В. Анемия у больных ХСН // Фарматека. 2011. № 14. С. 24–29.
- Бирюкова Л.С. Оптимальная терапия железом и средствами, стимулирующими эритропоэз, у пациентов с ХБП // Лечебное дело. 2012. № 1. С. 44–48.
- Андреичев Н.А., Балеева Л.В. Железодефицитные состояния и железодефицитная анемия // Вестник современной клинической медицины, 2009. № 3. С. 60–65.
- Демидова А.В. Анемии // М.: МЕДпресс-информ, 2005. 64 с.
- Weiss G., Goodnough L.T. Anemia of Chronic Disease // N. Engl. J. Med. 2005. Vol. 352 Р. 1011–1023.
- Сельчук В.Ю., Чистяков С.С., Толокнов Б.О. и др. Железодефицитная анемия: современное состояние проблемы // Русский медицинский журнал. 2012. № 1. С. 1–8.
- Идельсон Л.И. Гипохромные анемии. М.: Медицина, 1981. 192 с.
- Alleyne M., Horne M.K., Miller J.L. Individualized treatment for iron deficiency anemia in adults // Am. J. Med. 2008. Vol. 121 (11). Р. 943–948.
- Коноводова Е.Н., Бурлев В.А. Эффективность применения препарата Ферро-Фольгамма у беременных и родильниц с железодефицитной анемией // Русский медицинский журнал. 2003. Т. 11. № 16. С. 899–901.
- Верткин А.Л., Городецкий В.В., Годулян О.В. Сравнительная эффективность и переносимость различных железосодержащих препаратов у больных железодефицитной анемией // Русский медицинский журнал. 2004. № 5. С. 309–313.
- Мурашко Л.Е. Коноводова Е.Н, Бурлев В.А., Сопоева Ж.А. Объемный транспорт кислорода у беременных с анемией и гестозом при лечении Ферро-Фольгаммой // Русский медицинский журнал. 2002. Т. 10. № 7. С. 364–367.
- Петрухин В.А., Гришин В.Л. Лечение анемии беременных с использованием препарата Ферро-Фольгамма // Проблемы репродукции. 2002. № 6. С. 28–33.
- Серов В.Н., Шаповаленко С.А., Флакс Г.А. Диагностика и лечение железодефицитных состояний у женщин в различные периоды жизни // Кардиология. 2008. № 2. С. 17–20.
- Лебедев В.А., Пашков В.М. Принципы терапии железодефицитной анемии у беременных // Трудный пациент. 2010. № 8. С. 28–31.
- Сопоева Ж.А. Коррекция железодефицитных анемий у беременных с гестозом: Автореф. дис. … канд. мед. наук. М., 2002.
- Бурлев В.А., Коноводова Е.Н., Мурашко Л.Е. и др. Коррекция железодефицитных состояний у беременных с гестозом // Проблемы репродукции. 2002. № 6. С. 30–34.
- Коколина В.Ф. Опыт применения препарата Ферро-Фольгамма в лечении железо-дефицитных анемий у больных с ювенильными маточными кровотечениями // Справочник педиатра. 2005. № 6. С. 13.
- Шилов А.М., Мельник М.В., Ким И.Р. и др. Особенности течения ИБС на фоне анемического синдрома различной этиологии // Фарматека. 2006. № 11. С. 32–36.
- Городецкий В.В., Годулян О.В. Железодефицитные состояния и железодефицитная анемия: лечение и диагностика. М.: Медпрактика, 2004. Т. 3. 28 с.
- Никитин Е.Н., Красноперова О.В., Никитин Ю.Е. Опыт лечения железодефицитной анемии препаратом Ферро-Фольгамма // Клиническая медицина. 2009. № 3. С. 64–67.
Только для зарегистрированных пользователей
источник
И. В. Маев, Д. Т. Дичева, Д. Н. Андреев, Ю. С. Субботина
ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А. И. Евдокимова» Минздрава России, Москва, Российская Федерация
Цель представления клинического наблюдения.
Проиллюстрировать трудности выявления источников желудочно-кишечного кровотечения (ЖКК) при обследовании пациентки, страдающей хронической железодефицитной анемией тяжелой степени.
Основные положения.
На момент поступления в стационар явного источника ЖКК у пациентки выявлено не было. В результате проведенного комплексного обследования в качестве потенциальных источников ЖКК обнаружены: грыжа пищеводного отверстия диафрагмы (ГПОД) и дивертикулы толстой кишки. Данные патологии в ряде случаев осложняются как клинически-манифестными ЖКК, так и микропотерями. Описываемый случай иллюстрирует чрезвычайно высокие адаптивные возможности женского организма к хронической кровопотере — пациентка продолжала работать вплоть до момента госпитализации. Безусловной особенностью представленного наблюдения является диссоциация между тяжестью анемии и отсутствием клинических проявлений ГПОД и дивертикулярной болезни.
Заключение.
Рассматриваемый случай подчеркивает исключительную важность контроля клинического анализа крови у женщин в постменопаузальном периоде и целесообразность диспансеризации пациентов.
Ключевые слова:
железодефицитная анемия, грыжа пищеводного отверстия диафрагмы, дивертикулярная болезнь, препараты железа.
I. V. Maev, D. T. Dicheva, D. N. Andreyev, Yu. S. Subbotina
State educational government-financed institution of higher professional education «Yevdokimov Moscow State University of Medicine and Dentistry», Ministry of Healthcare of Russia, Moscow, Russian Federation
The aim of clinical case presentation.
To illustrate difficulties of detection of sources of gastro-intestinal bleeding (GIB) at investigation of patient with severe chronic iron-deficiency anemia.
Key points.
At the moment of hospital admission in obvious cause of GIB has not been revealed. At complex investigation potential sources of blood loss were found out: hiatal hernia (HH) and diverticula of the large intestine. Pathology data in some cases are complicated both by overt clinical GIB, and microlosses. Presented case illustrates extremely high adaptive potential of female body to chronic blood loss — patient continued to work down to the moment of hospital admission. Definite feature of presented case is the dissociation between severity of anemia and absence of clinical symptoms of HH and diverticular disease.
Conclusion.
Presented case emphasizes exclusive importance of control of total blood count in women in postmenopausal period and necessity in prophylactic medical examination of patients.
Key words:
iron-deficiency anemia, hiatal hernia, diverticular disease, iron supplements.
Анемия относится к наиболее часто встречающейся патологии системы крови в практике врача вне зависимости от специальности. По данным ВОЗ, анемией страдают 1 987 300 000 жителей Земли, причем доля железодефицитной анемии (ЖДА) составляет 80—90%, и ею страдают 1 788 600 000 человек [1, 3]. В развитых странах распространенность ЖДА ниже, чем в развивающихся. Это связано с достаточным рационом питания, высоким потреблением мясных продуктов, а также с малым числом беременностей. ЖДА чаще встречается среди женщин детородного возраста и составляет 14—20% [3]. К редким формам анемии относят гемолитическую аутоиммунную, серповидно-клеточную, талассемии. В последние годы наблюдается рост анемии хронических заболеваний, которая может доминировать в клинической картине при опухолевых поражениях, нефрологической или гепатологической патологии.
Число больных анемией увеличивается с возрастом. У лиц старше 85 лет частота встречаемости колеблется от 27 до 40% среди мужчин и от 16 до 21% среди женщин. В12-дефицитная анемия практически не наблюдается в детском и юношеском возрасте, ее распространенность нарастает к 50—70 годам [1].
Общепринятой классификации анемии не существует. В клинической практике анемии по содержанию гемоглобина в эритроцитах подразделяют на гипохромные, гиперхромные и нормохромные. Эта классификация основывается на оценке насыщенности эритроцитов при микроскопии и расчете цветового показателя [1]. Анемии подразделяют также по величине эритроцитов (расчет среднего объема отдельного эритроцита) на нормоцитарные (встречаются при острых кровотечениях, некоторых гемолитических анемиях, апластических анемиях), мегалоцитарные (развиваются при отсутствии антианемического фактора — витамина В12), макро-цитарные (при токсических формах — уремии, циррозе печени, при некоторых приобретенных гемолитических анемиях), микроцитарные (при дефиците железа, серповидно-клеточной анемии и некоторых других гемолитических формах) [14].
На основании патогенетического варианта выделяют анемии:
— обусловленные нарушением синтеза гемма (сидероахристические, дефект немсинтетазы);
— связанные с нарушением синтеза ДНК — мегалобластные (В12-дефицитная и фолиеводефицитная анемии);
— обусловленные нарушением транспорта железа (атрансферринемия);
— гемолитические;
— связанные с нарушением регуляции эритропоэза;
— обусловленные костномозговой недостаточностью.
Перед практикующим врачом, как правило, стоит задача поиска источника кровопотери у пациента с впервые выявленной или хронической ЖДА.
Различают кровотечения из верхних (пищевод, желудок, двенадцатиперстная кишка — ДПК) и нижних (дистальнее связки Трейтца) отделов желудочно-кишечного тракта (ЖКТ). На долю нижних отделов приходится не более 20% всех острых, не менее 50% хронических и большинство скрытых, в том числе наиболее сложных для топической диагностики, кровотечений. Причиной профузных кровотечений в преобладающем большинстве случаев являются патологические процессы в верхних отделах ЖКТ [8]. К ним относятся язвы ДПК (35—40%), язвы желудка (15—20%), эрозивно-геморрагический гастрит и эзофагит (15-20%) [6, 7].
Бывает достаточно сложно установить источник кровотечения. Сбор анамнеза может помочь в этом. Необходимо установить: продолжительность кровотечения, когда оно началось, возникло впервые или повторно, оценить цвет крови (алый, темно-бордовый, черный), покрывает ли кровь кал или смешана с ним, имеются ли сгустки крови. Если колоноскопия с полипэктомией выполнены менее 30 сут назад, можно предполагать кровотечение из участка проведения полипэктомии. Кровь из прямой кишки после дефекации капает или выделяется струей чаще всего свидетельствует о кровотечении из внутренних геморроидальных узлов.
Следует определить, беспокоят ли пациента боли в животе или в перианальной области. Интенсивные боли в перианальной области или спазмы в сочетании с выделением алой крови и оформленного стула обычно возникают при трещинах заднего прохода.
Необходимо выявить наличие в анамнезе сопутствующих заболеваний, оперативных вмешательств (например, по поводу язвенной болезни). Собирается лекарственный анамнез, особенно в отношении приема антикоагулянтов, аспирина и других нестероидных противовоспалительных препаратов, средств и витаминных добавок народной медицины (часто содержащих салицилаты) — все эти вещества могут повреждать слизистую оболочку органов ЖКТ с развитием кровотечения.
Наиболее часто кровотечение из верхних отделов ЖКТ обусловлено язвенной болезнью ДПК (30%), реже — эрозивным гастритом (27%), язвенной болезнью желудка (22%), эзофагитом (11%), дуоденитом (10%), варикозным расширением вен пищевода и желудка (5%), синдромом Мэллори-Вейса (5%); кроме того, причиной могут быть скользящая грыжа пищеводного отверстия диафрагмы (ГПОД), дивертикулез двенадцатиперстной или тощей кишки, эктазия сосудов антрального отдела желудка, опухоли желудка и тонкой кишки, ангиодисплазия, аортокишечный свищ, рак поджелудочной железы [4, 7, 10]. Скользящая ГПОД может вызывать также хроническую кровопотерю. При этом заболевании вследствие разности давлений между грудной полостью и желудком происходит смещение слизистой желудка относительно лежащих глубже слоев и в ней возникают линейные надрывы. Основные причины кровотечения из нижних отделов ЖКТ (в порядке убывания частоты):
2) в возрасте более 55 лет:
Внутренний геморрой на амбулаторном приеме является наиболее частой причиной кровотечения из нижних отделов ЖКТ. Он развивается в 13-16% у взрослого населения РФ. В развивающихся странах заболеваемость геморроем значительно ниже — менее 5% [7]. Дивертикулярная болезнь толстой кишки часто протекает бессимптомно, нередко ее выявляют случайно при ирригоскопии.
Высокая распространенность дивертикулеза в промышленно развитых странах обусловлена употреблением в пищу продуктов с низким содержанием клетчатки. Это приводит к образованию менее оформленного кала, увеличению времени его прохождения по кишке, повышает нагрузку на мышечные волокна кишечной стенки и внутрипросветное давление, следствием чего является формирование дивертикулов. При дивертикулезе обычно наблюдается острый, обильный, безболезненный кровавый стул. В 75-95% случаев кровотечение прекращается самостоятельно или на фоне консервативной терапии.
Кровотечение из дивертикулов толстой кишки не бывает хроническим и не вызывает скрытой кровопотери. Интересна сосудистая анатомия кровоточащих дивертикулов: прямые сосуды, отходящие от ветвей брыжеечной артерии, пенетрируют стенку толстой кишки от серозной до подслизистой оболочки, проходя над куполом дивертикула. Прямые сосуды отделены от просвета дивертикула только слизистой оболочкой и небольшим количеством мышечных волокон. Дефект артерии обычно формируется именно со стороны просвета дивертикула. Со временем стенка сосуда ослабевает и разрывается в просвет дивертикула, вызывая артериальное кровотечение. Ишемический колит также может являться причиной кровотечения. Как правило, заболевание начинается остро, со схваткообразных болей в левом нижнем квадранте живота, позывов на дефекацию, кровянистой диареи. Ишемия чаще развивается на границе отделов ободочной кишки, в которых недостаточно развито коллатеральное кровообращение, например в селезеночном изгибе, сигмовидной ободочной кишке.
Таким образом, можно заметить, что желудочно-кишечные кровотечения нередко представляют большие сложности как для диагностики, так и для лечения и требуют четкой совместной работы персонала приемного покоя, отделения реанимации, терапевтов, эндоскопистов, рентгенологов и хирургов, а в большинстве случаев и длительного амбулаторного наблюдения [5, 6].
Клинический пример.
Больная К., 57 лет, поступила в апреле 2013 г. с жалобами на общую слабость, головокружение, усталость, сердцебиение, ощущение перебоев в работе сердца, слабость в нижних конечностях в положении стоя и при ходьбе.
Ухудшение состояния отметила в течение последнего месяца, когда возросла общая слабость, появилось головокружение, усилилась тахикардия, снизилась толерантность к привычной физической нагрузке, что послужило поводом в апреле 2013 г. обратиться за медицинской помощью. При прицельном расспросе жалуется на ухудшение общего самочувствия в последние три года, периодически возникающую усталость, вялость, перебои в работе сердца, эпизодическую тахикардию как в покое, так и при незначительном физическом напряжении. Самостоятельно принимала поливитамины и биологически активные добавки, за медицинской помощью не обращалась.
При осмотре: выраженная бледность кожных покровов и видимых слизистых, умеренная пастозность лица. В приемном отделении по cito выполнен клинический анализ крови (впервые выявлена анемия со снижением уровня гемоглобина до 28 г/л, эр. 2,19*10 12 /л, СОЭ 60 мм/ч), после консультации хирурга данных за кровотечение не получено. Пациентка госпитализирована в реанимационное отделение, где проводились коррекция водно-электролитных нарушений, заместительная терапия препаратами крови, железозамещающая, антибактериальная терапия. На фоне лечения отмечен отчетливый положительный эффект, уровень гемоглобина повысился до 69 г/л. Для дальнейшего обследования переведена в гастроэнтерологическое отделение.
Состояние на момент поступления средней тяжести. Гиперстенического телосложения, повышенного питания. Масса тела 82 кг, рост 164 см. Индекс массы тела 31. Кожные покровы и видимые слизистые бледные, нормальной влажности. Периферические лимфоузлы не увеличены. Периферических отеков нет. Частота дыхания —17 в минуту. Дыхание везикулярное, хрипы не выслушиваются. Тоны сердца приглушены, ритм правильный. Число сердечных сокращений 90 в минуту, АД 130/80 мм рт. ст. Язык влажный, чистый, сосочки сглажены. Живот при пальпации мягкий, безболезненный во всех отделах. Печень у края реберной дуги, безболезненна при пальпации, селезенка не пальпируется. Стул регулярный, оформленный, обычного цвета, без патологических макропримесей.
В клиническом анализе крови отмечается гипохромная анемия (Hb 69 г/л, цветовой показатель 0,52, эр. 2,82*10 12 /л), анизоцитоз. В биохимическом анализе снижение уровня сывороточного железа — 3,9 мкмоль/л (норма 9—27), трансферрин 3,70 г/л (норма 2,35—3,7), общая железосвязывающая способность крови 46,8 мкмоль/л (норма 44,8—80,6). Таким образом, выявлена ЖДА тяжелой степени. Креатинин, общий билирубин, прямой билирубин, общий белок, альбумин, глюкоза, гамма-глутамилтранспептидаза, аспартатаминотрансфераза, аланинаминотрансфераза, щелочная фосфатаза в норме.
Результаты клинического анализа крови пациентки в динамике за время госпитализации приведены в таблице.
Данные клинического анализа крови больной К.
| Показатели крови | Дата | |||||
| 26.04.13 | 27.04.13 | 28.04.13 | 29.04.13 | 06.05.13 | 13.05.13 | |
| Лейкоциты, х10 9 /л | 5,54 | 6,20 | 8,10 | 12,00 | 6,06 | 5,14 |
| Эритроциты, х10 12 /л | 2,19 | 2,82 | 2,90 | 3,35 | 4,53 | 4,88 |
| Гемоглобин, г/л | 28 | 49 | 52 | 68 | 104 | 118 |
| Гематокрит | 12,4 | — | 19,4 | 24,6 | 36,9 | 40,2 |
| Цветовой показатель | — | 0,52 | — | — | — | — |
| Тромбоциты, х10 9 /л | 455 | 272 | 256 | 343 | 345 | 490 |
| Нейтрофилы, % | 64,6 | 65,0 | 72,0 | 78,3 | 66,5 | 53,2 |
| Лимфоциты, % | 21,0 | 23,0 | 15,0 | 8,7 | 23,0 | 33,3 |
| Моноциты, % | 10,4 | 10,0 | 8,0 | 9,4 | 6,2 | 5,9 |
| Эозинофилы, % | 0,5 | 2,0 | 5,0 | 1,7 | 2,2 | 3,3 |
| Базофилы, % | 1,1 | 0,8 | 0,5 | 1,8 | ||
| Ретикулоциты, % | 14,20 | 20,00 | 6,78 | |||
| СОЭ, мм/ч | 60 | 39 | 40 | 30 | 23 | 19 |
| Палочкоядерные, % | 1 | 2 | 2 | 3 | ||
Анализ крови на онкомаркёры: рака яичника СА 125, ЖКТ СА 19—9, СА 15—3, кишечника СЕА, гепатоцеллюлярной карциномы, альфа-фетопротеин — в пределах допустимых значений.
Анализ кала на скрытую кровь — отрицательный.
Прямая проба Кумбса — отрицательная.
Реакция пассивной гемагглютинации (РПГА) с сальмонеллезным О комплексным агглютинином (АГ) — отрицательная, реакция непрямой гемагглютинации (РНГА) с иерсиниозным О3 АГ — отрицательная, О9 АГ — отрицательная, РПГА с шигеллезным Зонне АГ — отрицательная, Флекснера АГ — отрицательная, РПГА с псевдотуберкулезным АГ — отрицательная.
Анализ крови на гормоны щитовидной железы в норме, на коагулограмме незначительное повышение фибриногена — 3,8 г/л (норма 1,75—3,5).
В общем анализе мочи существенных изменений не наблюдалось.
С целью уточнения источника кровопотери выполнены следующие инструментальные исследования.
ЭГДС: пищевод свободно проходим, стенки эластичные, слизистая оболочка бледная, гладкая, блестящая. Признаки небольшой неосложненной ГПОД. Розетка кардии смыкается. В желудке содержимого нет. Складки эластичные, рельефные, расправляются воздухом. Слизистая бледная, гладкая, блестящая. Стигм кровотечения, дефектов не выявлено. Перистальтика обычная. Привратник проходим. Луковица ДПК средних размеров, округлой формы, слизистая бледная, гладкая, блестящая. Постбульбарные отделы без особенностей, содержат небольшое количество светлой, прозрачной желчи. Заключение: неосложненная ГПОД, анемизация слизистой, органической патологии осмотренных отделов ЖКТ нет.
Рентгенологическое исследование желудка с барием: акт глотания не нарушен. Пищевод свободно проходим, часть тела желудка расположена в заднем средостении. Стенки желудка эластичные, перистальтика симметричная. Эвакуация не нарушена. Тонкая кишка на всем протяжении не изменена. Заключение: фиксированная грыжа пищеводного отверстия диафрагмы.
Ирригоскопия: контрастная масса свободно заполняет все отделы толстой кишки — положение отделов обычное. Гаустрация симметричная. В левой половине толстой кишки — мелкие дивертикулы. Заключение: дивертикулез левой половины толстой кишки без признаков дивертикулита.
Колоноскопия: множественные неосложненные дивертикулы с узкими устьями в ободочной и сигмовидной кишке, других патологических изменений не выявлено.
При УЗИ органов брюшной полости, почек, малого таза, эхокардиографии, рентгенографии органов грудной клетки диагностически-значимой патологии не обнаружено.
Консультация гематолога: данных за гематологическое заболевание не найдено. Консультация гинеколога: гиперплазия эндометрия в постменопаузе, тяжелая анемия с гинекологической патологией не связана.
Пациентке было проведено комплексное лечение препаратами фолиевой кислоты и препаратами железа с положительной динамикой (содержание Hb повысилось до 118 г/л).
Представленный клинический случай демонстрирует трудности поиска источника кровотечения при ЖДА. Выявленная при обследовании патология (ГПОД, дивертикулярная болезнь) может приводить как к клиническим проявлениям желудочно-кишечных кровотечений, так и к микропотере, что длительно ускользает от внимания больного. Так, глубокая анемия со снижением уровня Hb до 26 г/л не нарушала общее состояние настолько, чтобы искать медицинской помощи. Испытывая слабость, пациентка тем не менее полностью себя обслуживала, интенсивно работала (5-дневная «полная» рабочая неделя). Это лишний раз иллюстрирует степень адаптации организма к кровопотере. Угасание менструальной функции также не способствовало более ранней диагностике анемии. Малая выраженность симптоматики в данном случае объясняется еще и тем, что анемия носила хронический характер, нарастала постепенно, была обусловлена микропотерями в течение длительного времени. Рентгенологическое обследование при ГПОД и дивертикулярной болезни информативно и должно дополнять эндоскопические методы.
Рациональная терапия ЖДА.
Патогенетической основой терапии ЖДА являются препараты железа [1, 10, 13]. В человеческом организме биологические функции железа могут тормозиться при отсутствии ряда микронутриентов, в частности цинка, магния, меди, хрома, молибдена и витаминов С и группы В. Особую роль в процессах усваивания железа играют также медь и марганец. Медь служит незаменимым элементом, который входит в состав ферментов, участвующих в процессе эритропоэза и гранулоцитопоэза. Она необходима для созревания и стимуляции ретикулоцитов и других гемопоэтических клеток путем активации цитохромоксидазы, а также является составляющей электронпереносящих белков, участвующих в реакциях окисления органических веществ молекулярным кислородом. Количество меди в организме тесно связано с обменом железа. На фоне ЖДА неизбежно изменяется плазменная концентрация церулоплазмина и меди [13].
Марганец выступает в качестве кофактора различных систем ферментного обмена, в том числе он детерминирует важные биохимические и физиологические процессы — синтез нуклеиновых кислот, метаболизм гормонов. Участвует в метаболизме форменных элементов крови, а также в синтезе молекул гемоглобина. В комбинации с железом отмечается улучшение усвоения обоих элементов по сравнению с раздельным их применением.
Железо является жизненно важным микроэлементом, так как стимулирует процессы дыхания на клеточном уровне, участвует в формировании гемма. Оно входит и в другие комплексы, в частности в фермент рибонуклеотид-редуктазу, который участвует в синтезе ДНК. Суточная потребность организма человека в железе колеблется от 4 до 33 мг, при этом у женщин она выше, чем у мужчин.
Обычно соли железа плохо абсорбируются, в силу чего предпочтение в терапевтической практике отдается комплексным препаратам. С учетом приведенных выше данных целесообразным представляется применение мультиэлементного препарата — Тотемы (Innothera Chouzy, Франция), восполняющего дефицит железа, а также усиливающего антиоксидантную защиту. В состав Тотемы входит легко усвояемое двухвалентное железо в дозе 50 мг, а также медь 0,7 мг и марганец 1,33 мг: медь и марганец улучшают метаболизм железа, что позволяет снизить эффективную лечебную или профилактическую дозу препарата, и улучшают транспорт железа к тканям за счет достаточного количества церулоплазмина и гефестина. Важным представляется эффект блокирования образования свободных радикалов как путем быстрой элиминации двухвалентных ионов железа с помощью церулоплазмина (медь-зависимая фероксидаза), так и за счет активации антиоксидантной защиты в составе супероксиддисмутазы [2].
Как известно, при применении препаратов железа возможно развитие аллергических реакций (зуд, кожные высыпания, крапивница), редко анафилактических реакций. По мнению ряда авторов [2, 9], Тотема обладает значительно лучшей переносимостью в сравнении с препаратами трехвалентного железа, однако у пациентов с патологией ЖКТ желательно принимать указанное средство в перерывах между едой (т. е. не натощак), разбавлять содержимое ампулы как минимум в 100 мл воды. При наличии диспептических проявлений или болевого абдоминального синдрома начинать с минимальных количеств (50 мг для взрослых) в течение 2-3 дней, увеличивая до терапевтической дозы в 200 мг и добиваясь достижения нормализации уровня гемоглобина; продолжать прием в профилактической дозировке до нормализации показателей депо железа. Пациентам, страдающим заболеваниями ЖКТ, разовую дозу лучше разделять на 2-3 приема, что улучшает переносимость препарата [9]. Вследствие того, что препараты железа окрашивают эмаль зубов, их рекомендуют принимать через трубочку, а затем споласкивать ротовую полость или чистить зубы сразу после приема.
Заключение
Рассматриваемый клинический случай подчеркивает исключительную важность контроля клинического анализа крови у женщин в постменопаузальном периоде и целесообразность диспансеризации пациентов. Мультиэлементные препараты двухвалентного железа обладают высокой клинической эффективностью, позволяя скорректировать ЖДА при минимизации возможных побочных эффектов.
Маев Игорь Вениаминович — доктор медицинских наук, профессор, член-корреспондент РАН, заведующий кафедрой пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А. И. Евдокимова»
Maev Igor V — MD, PhD, professor, corresponding member of the Russian Academy of Science, head of Chair of internal diseases propedeutics and gastroenterology, State educational government-financed institution of higher professional education «Yevdokimov Moscow State University of Medicine and Dentistry»
Дичева Диана Тодоровна — кандидат медицинских наук, доцент кафедры пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А. И. Евдокимова»
Dicheva Diana T — MD, senior lecturer, Chair of internal diseases propedeutics and gastroenterology, State educational government-financed institution of higher professional education «Yevdokimov Moscow State University of Medicine and Dentistry»
Андреев Дмитрий Николаевич — ассистент кафедры пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А. И. Евдокимова».
Andreyev Dmitry N — assistant-professor, Chair of internal diseases propedeutics and gastroenterology, State educational government-financed institution of higher professional education «Yevdokimov Moscow State University of Medicine and Dentistry».
1. Воробьев ПА. Анемический синдром в клинической практике. М.: Ньюдиамед; 2001. 165 с.
1. Vorobyev PA. Anemic syndrome in clinical practice. M.: Nyudiamed; 2001.165 p.
2. Громова ОА, Торшин ИЮ, Хаджидис АК. Анализ молекулярных механизмов воздействия железа (II), меди, марганца в патогенезе железодефицитной анемии. Клин фармакол фармакоэкономика 2010; 1: 1-8.
2. Gromova OA, Torshin IYu, Hadzhidis AK. Analysis of molecular mechanisms of influence of iron (II), copper, manganese in pathogenesis of an iron-deficiency anemia. Klin farmakol farmakoekonomika 2010; 1:1-8.
3. Комаров ФИ. Дифференциальная диагностика и лечение внутренних болезней. В 4-х т. М.: Медицина; 2003.
3. Komarov FI. Differential diagnostics and treatment of internal diseases. In 4 т. M.: Medicine; 2003.
4. Маев ИВ, Андреев ДН, Дичева ДТ. Гастроэзофагеальная рефлюксная болезнь: от патогенеза к терапевтическим аспектам. Consilium Medicum 2013; 15(8):30-4.
4. Mayev IV, Andreev DN, Dicheva DT. Gastroesophageal reflux disease: from a pathogenesis to therapeutic aspects. Consilium Medicum 2013; 15(8):30-4.
5. Маев ИВ, Гончаренко АЮ, Дичева ДТ, Андреев ДН, Швыдко ВС, Бурагина ТА. Лечение язвенных кровотечений и профилактика их рецидивов: взгляд терапевта. Медицинский совет 2013; 10: 22-6.
5. Mayer IV, Goncharenko AYu, Dicheva DT, Andreyev DN, Shvydko VS, Buragina TA. Treatment of ulcerative bleeding and prevention of relapse: view of the physician. Meditsinsky sovet 2013; 10:22-6.
6. Маев ИВ, Самсонов АА, Андреев НГ, Андреев ДН. Важные практические результаты и современные тенденции в изучении заболеваний желудка и двенадцатиперстной кишки. Рос журн гастроэнтерол гепатол колопроктол 2012; 4: 17-26.
6. Mayer IV, Samsonov AA, Andreyev NG, Andreyev DN. The important practical results and modern trends in studying stomach and duodenum diseases. Ros zhurn gastroenterol gepatol koloproktol 2012; 4:17-26.
7. МакНелли ПР. Секреты гастроэнтерологии. М.: БИНОМ; 2005. 907 с.
7. MakNelli PR. Secrets of gastroenterology. M.: the BINOMIAL; 2005. 907 p.
8. Парфенов АИ. Энтерология. — М.: Медицинское информационное агентство; 2009. 875 с.
8. Parfenov AI. Enterology. — M.: Medical news agency; 2009. 875 p.
9. Стуклов НИ. Мета-анализ данных переносимости питьевой формы глюконата железа (II), меди и марганца (препарат Тотема) при лечении железодефицитной анемии у детей и взрослых. Земский врач 2012; 4:18-27.
9. Stuklov NI. Metaanalysis of data of tolerability of the oral form of ferrous gluconate (II), copper and manganese (Totema) at iron-deficiency anemia at children and adults. Zemsky vrach 2012; 4:18-27.
10. Тинсли Р. Харрисон. Внутренние болезни. М.: Практика; 2005. 433 с.
10. Tinsli R. Harrison. Internal diseases. M.: Practice; 2005. 433 p.
11. Халиф ИЛ, Маев ИВ, Дичева ДТ, Березутская ОЕ, Андреев ДН. Фульминантная форма язвенного колита. Эксперим клин гастроэнтерол 2011; 9:136-9.
11. Khalif IL, Mayer IV, Dicheva DT, Berezutskaya OE, Andreyev DN. The fulminant form of ulcerative colitis. Eksperim klin gastroenterol 2011; 9:136-9.
12. Халиф ИЛ, Маев ИВ, Дичева ДТ, Березутская ОЕ, Андреев ДН, Головкина НЛ. Трудности терапии язвенного колита. Мед вестн МВД 2011; 4: 30-2.
12. Khalif IL, Mayer IV, Dicheva DT, Berezutskaya OE, Andreyev DN, Golovkina NL. Difficulties of treatment of ulcerative colitis. Med vestn of the Ministry of Internal Affairs 2011; 4 : 30-2.
13. Broadway-Duren JB, Klaassen H Anemias. Crit Care Nurs Clin North Am 2013; 25(4): 411-26.
14. Means RT. Iron deficiency anemia. Hematology. 2013; 18(5): 305-6.
источник