Ф.Ю.Копылов, Д.Ю.Щекочихин
Первый МГМУ им. И.М. Сеченова Кафедра профилактической и неотложной кардиологии ФППОВ, Москва
Анемия с давних времен является спутником человечества. Выдающийся немецкий врач Йоханнес Ланге (Johannes Lange) уже в 1554 г. дал название анемии как «болезни девственниц (morbus virgineus)». Он считал эту болезнь специфичной для целомудренных девушек, а причиной указывал задержку менструальной крови [1], ссылаясь на описание Гиппократа, представленное в сочинении «О болезнях девушек».
За последующие несколько столетий мы существенно продвинулись в понимании патофизиологии анемии, и в настоящий момент крупные исследования посвящаются оценки роли анемии в развитии и течении различных заболеваний на популяционном уровне. Касательно сердечно-сосудистых заболеваний (ССЗ) доказано, что анемия является независимым фактором риска неблагоприятных исходов ССЗ у пациентов с хронической сердечной недостаточностью (ХСН) и хронической почечной недостаточностью (ХПН). Для общей популяции больных ССЗ большинство данных свидетельствует о том, что анемия является и здесь независимым фактором риска, однако данных для включения в официальные рекомендации пока недостаточно [2].
Определение понятия и распространенность
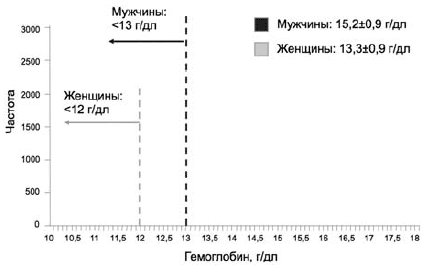
Согласно определению ВОЗ, анемия регистрируется у взрослых женщин при снижении концентрации гемоглобина ниже 12 г/дл, а у мужчин ниже 13 г/дл [3]. На рис. 1 проиллюстрировано применение данных критериев на примере крупной выборки исследования NHANES III (n=40 000) [4]. Применение критерия 12 г/дл для женщин позволяет включить в число страдающих анемией существенно большее число лиц, по сравнению с мужчинами. Этот факт находит свое отражение и в других исследованиях, в которых распространенность анемии у женщин почти в 3 раза превышает таковую у мужчин: 13 и 4,8% соответственно [5], и должен быть принят во внимание при оценке результатов различных исследований.
Рис 1. Применение критериев ВОЗ для определения анемии на популяционном уровне [4]
Распространенность анемии среди пациентов с сердечно-сосудистыми заболеваниями относительно хорошо изучена. Среди пациентов с ишемической болезни сердца (ИБС) составляет от 10 до 30% [6, 7], а на примере ХСН — варьирует в широком диапазоне от 4 до 61% (в среднем 18%) в зависимости от тяжести основного заболевания и применяемых критериев анемии [8].
Этиология и патогенез
Причинами анемии у пациента кардиологического профиля могут быть все факторы характерные для общей популяции. Однако если рассматривать группу больных с прогрессирующими ССЗ и в первую очередь с ХСН, то основными этиопатогенетическими факторами анемии можно считать следующие:
1. Анемия хронических заболеваний.
2. Анемия за счет гемодилюции (псевдоанемия).
3. Анемия за счет недостатка железа/витаминов.
4. Нарушение функции почек — снижение продукции эритропоэтина.
5. Действие лекарств.
Анемия хронических заболеваний
Анемия, возникающая у пациентов с инфекцией, воспалением, неоплазиями, хронической почечной недостаточностью и продолжающаяся более 1-2 мес, обозначается как анемия хронических заболеваний (АХЗ) — «анемия воспаления», «цитокинопосредованная анемия». Характерной чертой этого типа анемии является сочетание пониженного уровня железа сыворотки с достаточными его запасами в ретикулоэндотелиальной системе (РЭС). АХЗ по распространенности занимает 2-е место среди анемий (после железодефицитной — ЖДА) [9]. В случае наличия ХСН данный вид анемии является самым распространенным и отмечается у 58% пациентов [10].
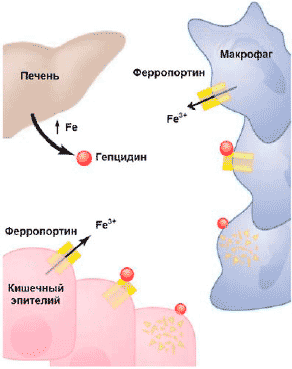
В настоящее время считается, что в основе АХЗ лежит иммуноопосредованный механизм: цитокины и клетки РЭС вызывают изменения в гомеостазе железа, пролиферации эритроидных предшественников, продукции эритропоэтина и продолжительности жизни эритроцитов [11]. Открытие гепсидина (hepcidin) — железорегулирующего острофазового белка — позволило во многом прояснить связь между иммунным механизмом нарушения гомеостаза железа и развитием АХЗ: именно через усиление синтеза в печени гепсидина под влиянием воспалительных стимулов, (главным образом интерлейкина-6), происходят снижение абсорбции железа в кишечнике и блокирование высвобождения железа из макрофагов (рис. 2). Дизрегуляция гомеостаза железа ведет к последующей недостаточности доступного для эритроидных предшественников железа, ослаблению пролиферации этих клеток вследствие негативного влияния на них нарушения биосинтеза гема.
Рис 2. Механизм действия гепцидина: угнетение всасывание железа в кишечнике, замедление мобилизации железа из депо, способствуя его накоплению в макрофагах
Анемия вследствие гемодилюции (псевдоанемия)
Данная причина анемии связана с избыточным «разбавлением» крови и характерна для пациентов с повышенным объемом плазмы (ХСН, ХПН, беременность). Предполагается, что у многих больных ХСН анемия может быть вызвана гемодилюцией [12]. Однако, несмотря на увеличение общего объема плазмы у всех пациентов с систолической и у 71% с диастолической ХСН, истинный дефицит эритроцитов имеется у 88% больных анемией при диастолической ХСН и у 59% при систолической ХСН [13].
Анемия вследствие недостатка железа/витаминов
Еще 50 лет назад было показано непосредственное влияние железодефицита на ферментативные процессы, даже в отсутствии анемии [14]. Экспериментальные исследования на животных показали возможность непосредственного влияния железодефицита на диастолическую функцию, провоцирование сердечной недостаточности, фиброза миокарда, уменьшение уровня циркулирующего эритропоэтина, влияние на молекулярные сигнальные пути и активацию воспаления [15].
Железодефицитная анемия является самой распространенной формой в популяции, однако у пациентов кардиологического профиля уступает первенство АХЗ и составляет до 21% [16].
Распространенность железодефицитного состояния при ХСН во многом зависит от критериев определения. Если учитывать лишь снижение насыщения трансферина менее 16%, то его можно обнаружить у 78% анемичных и 61% неанемиченых больных ХСН, если к критериям добавить уровень ферритина 30-100 мг/л, то распространенность снизится до 20 и 15% соответственно [17]. В другом исследовании, где критериями железодефицита были значения ферритина менее 100 мг/л при насыщении трансферина менее 16%, нарушения выявлены у 61% анемичных и 43% неанемичных пациентов ХСН [18].
Таким образом, можно говорить о высоком распространении у больных ХСН как абсолютного (определяемого как уровень ферритина 100 мг/л и процента сатурации трансферина 200 мкг/л.
Разграничение АХЗ и ЖДА имеет важное практическое значение: некорректная трактовка пациента с АХЗ как имеющего дефицит железа влечет за собой неэффективную терапию железом с риском развития осложнений (перегрузки железом, особенно при внутривенном введении). Показатели дифференциальной диагностики при АХЗ, ЖДА и их сочетаниях представлены в таблице.
Показатели дифференциальной диагностики при АХЗ и ЖДА
| Показатели | ЖДА | АХЗ |
| Сывороточное железо | Снижено | Снижено |
| ОЖСС | Повышена | Снижена или N |
| Средний корпускулярный объём | Снижен | Снижен (30%) |
| Насыщение трансферрина | Снижено | N или снижено |
| Сывороточный ферритин | Снижен | N |
| Железо костного мозга | Снижено или отсутствует | N |
| Тест с пероральным железом | Подъем hb | Нет подъема Hb |
Анемия при почечной недостаточности
У больных с хроническими заболеваниями почек наиболее важный вклад в развитие анемии вносят снижение продукции эритропоэтина вследствие уменьшения массы функциональных тканей почек и антипролиферативное действие уремических токсинов. Кроме того, развитие анемии может быть вызвано сокращением продолжительности жизни эритроцитов со 120 дней до 70-80 дней, а также потерей крови, ингибированием эритропоэза в результате хронического воспаления, недостатком свободного железа в организме и дефицитом нутриентов, побочным действием лекарств. По современным представлениям, в случае ХПН можно говорить о едином патогенетическом механизме с АХЗ [20].
У большинства пациентов с ХСН и анемией имеется хроническая болезнь почек (ХБП) различной степени, то есть снижение скорости клубочковой фильтрации (СКФ) 2 . Такое сочетание анемии, ХБП и ХСН D.S.Silverberg и соавт. предложили называть кардиоренальным анемическим синдромом, каждое из трех составляющих которого ухудшает течение остальных двух (рис. 3) [21].
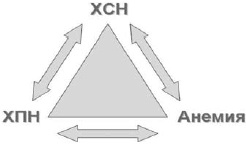
Рис 3. Взаимосвязь при кардиоренальном анемическом синдроме (модифицированна по [21])
Действие лекарств
Применительно к кардиологической практике можно выделить три основных лекарственных воздействия, которые могут провоцировать возникновение и поддержание анемии:
1. Непосредственное подавление костного мозга (вплоть до апластической анемии) могут вызывать следующие лекарственные препараты: НПВС, цитостатики, мерказолил, метамизол (анальгин).
2. Невозможность восстановления присутствующего в пище трехвалентного железа до двухвалентного (всасывающегося во много раз быстрее, нежели трехвалентное) в связи с относительной гипоацидностью (обусловленной сопутствующим применением антисекреторных или антацидных препаратов).
3. Ингибиторы ангиотензинпревращающего фермента и антагонисты к рецепторам ангиотензина могут уменьшать продукцию эритропоэтина и чувствительность к нему костного мозга, так как ангиотензин является мощным стимулятором синтеза эритропоэтина и эритропоэза [22].
Кроме того, необходимо помнить, что нитраты способны вызывать метгемоглобинемию и привести к снижению кислородной емкости крови, однако этот эффект наблюдается в основном при использовании очень высоких доз [23].
Анемия — фактор риска ССЗ
Наличие анемии у пациентов само по себе ассоциировано с пожилым возрастом, нарушением функции почек, сахарным диабетом, тяжелой сердечной недостаточностью, снижением переносимости физических нагрузок и низкими показателями качества жизни [24]. В этой связи наибольшую ценность представляют исследования, выполненные на больших выборках, позволяющие при анализе провести коррекцию на другие факторы риска.
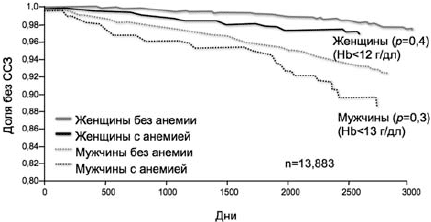
Из исследований, проведенных на популяционном уровне, по данному вопросу можно выделить ARIC-study (Atherosclerosis Risk in Communities), в котором проводилось наблюдение более 6 лет за почти 14 000 пациентов без ССЗ [25]. При оценке анемии как фактора риска ССЗ оказалось, что пациенты со сниженным уровнем гемоглобина имели риск развития указанных заболеваний почти в 1,5 раза выше вне зависимости от всех остальных факторов риска ССЗ (рис. 4).
Рис 4. Кривые Каплана-Мейера для ССЗ у мужчин и женщин, стратифицированных по наличию или отсутствию анемии [25]
Анализ других работ по оценке популяционного риска анемии дал противоречивые результаты. Исследователи пришли к выводу о необходимости дополнительных изысканий для определенных рекомендаций в этой области [2].
Анемия и ИБС
Широко известно, что ряд некоронарных заболеваний, в патогенезе которых имеет место гемическая или тканевая гипоксия, может инициировать клинические проявления ИБС, оказывать отягчающее влияние на характер течения основного заболевания. Возможным механизмом представляется усиление симпатической активности и сердечного выброса за счет длительной индуцированной гипоксией вазодилятации, что приводит к гипертрофии левого желудочка и увеличению размеров сердца и, соответственно, к повышению потребления кислорода [26]. Также у пациентов с ИБС по сравнению со здоровыми отмечена сниженная толерантность миокарда к низким уровням гемоглобина [27].
Вопросы сочетания ИБС и анемий представлены в научной литературе немногочисленными источниками. При рассмотрении вопроса влияния анемии на исходы ИБС можно выделить три основных направления исследований:
Наличие анемии перед проведением чрескожного коронарного вмешательства у пациентов с инфарктом миокарда (ИМ) с подъемом сегмента ST достоверно увеличивает риск большого кровотечения как на протяжении 30 сут после ИМ, так и в течение 1 года [28]. Анализ более чем 45 000 случаев чрескожного коронарного вмешательства при ОКС и стабильной ИБС показал, что анемия является независимым фактором риска госпитальной летальности у мужчин и серьезных сердечно-сосудистых осложнений и у мужчин, и у женщин [7]. Повышенный риск неблагоприятных исходов также отмечается у пациентов со сниженным уровнем гемоглобина перед аортокоронарным шунтированием [29].
Сходные результаты показывают исследования, посвященные исходам ОКС в зависимости от наличия анемии, в которых снижение уровня гемоглобина признается значительным фактором риска прогрессирования ИБС, развития ХСН и нарушений ритма, а также смертности [30]. N.C.Meneveau и соавт., помимо признания анемии как независимого фактора риска смерти при ОКС, предлагают включить ее наравне с другими факторами в шкалу риска GRACE (Global Registry of Acute Coronary Events) для более точного прогноза [31].
Исследования, проведенные на популяционном уровне [32] и у больных ИБС [33], подтверждают наличие U-образной зависимости между уровнем гемоглобина и сердечно-сосудистой заболеваемостью и смертностью, т. е. высокий уровень гемоглобина (>13 г/дл) ассоциирован с плохим прогнозом, наряду с низким уровнем.
Анемия и ХСН
Факт увеличения общей и сердечно-сосудистой смертности при наличии анемии у больных с ХСН подтвержден в большом количестве исследований. Так, в ретроспективном исследовании SOLVD показано, что снижение гематокрита на 1% увеличивает общую смертность больных ХСН на 2,7% [34]. Исследование OPTIME продемонстрировало увеличение риска смерти или повторной госпитализации на 12% при уровне гемоглобина менее 12 г/дл [35]. При этом более тяжелый функциональный класс СН по NYHA ассоциировался с более низким уровнем гемоглобина и высоким уровнем креатинина. Имеются данные о наиболее худшем прогнозе относительно сердечно-сосудистой смертности при ЖДА по сравнению другими видами анемии [36].
Анемия при ХСН также является независимым фактором риска более тяжелого течения заболевания: высокого функционального класса, сниженной переносимости физических нагрузок, когнитивных нарушений, низкого качества жизни [37].
Анемия и гипертоническая болезнь
Данные о соотношениях анемии с гипертонической болезнью, несмотря на их широкое распространение, достаточно немногочисленны. Имеются указания на связь анемии с повышением артериального давления в ночные часы и среднего артериального давления (сумма диастолического давления плюс 1/3 пульсового) по данным суточного мониторирования [38], а также на достоверно более широкую распространенность нормоцитарной анемии у пациентов с неконтролируемым уровнем артериального давления — 20%, по сравнению с пациентами поддерживающих нормотонию — 16% (р=0,03) [39].
Лечение
Терапевтические мероприятия, направленные на устранение анемии, должны быть обращены, в первую очередь, на устранение этиологического фактора. В соответствие с этим пациенты должны проходить полноценное обследование для выяснения причины анемии. В рамках данного обзора мы остановимся на АХЗ и ЖДА, составляющих по отдельности или в сочетании подавляющее большинство анемий в кардиологической практике. В данных ситуациях в качестве основной терапии применяются пероральные и внутривенные препараты железа, а также препараты эритропоэтина.
Препараты железа
В случаях выявления устранимой причины ЖДА лечение должно быть направлено на устранение этиологического фактора (эрозивно-язвенные и опухолевые поражения ЖКТ, миома матки, энтериты, алиментарная недостаточность и др.). В этом случае, а также при наличии неустранимой причины непроходимо проводить патогенетическую терапию препаратами железа (ПЖ).
Необходимо отметить ошибочность мнения о возможности коррекции дефицита железа с помощью пищевых продуктов с высоким содержанием железа. Предвидя установление данного факта, врач Мелампас (Melampus) в Греции за 1500 лет до н. э. для избавления принца Ификласа Тезалия (Iphyclus of Thesaly) от полового бессилия, возникшего у него на почве постгеморрагической анемии, давал ему вино с ржавчиной, соскобленной с лезвия старого ножа [40].
В настоящее время мы имеем широкий выбор препаратов железа (ПЖ) для приема внутрь, которые назначаются в большинстве случаев (при отсутствии специальных показаний). Основные ПЖ в виде солей представлены сульфатом, глюконатом, хлоридом, фумаратом, глицинсульфатом. Среди ПЖ в виде железосодержащих комплексов, обладающих большей степенью абсорбции, имеются железо-полимальтозный комплекс, железо-сорбитоловый комплекс, протеин сукцинилат железа, железо-сахаратный комплекс.
Необходимо учитывать, что всасывание железа может уменьшаться под влиянием содержащихся в некоторых пищевых продуктах веществ — фитинов (рис, соя), фосфатов (рыба, морепродукты), танин (чай, кофе). Препараты железосодержащих комплексов (в частности, гидрокси-полимальтозный комплекс) лишены подобных недостатков, поскольку пищевые продукты и медикаменты не оказывают влияния на всасываемость железа в виде трехвалентной формы.
Оптимальная тактика ведения больных ЖДА предполагает насыщающую и поддерживающую терапию ПЖ. Длительность насыщающей терапии зависит от темпов прироста и сроков нормализации показателей гемоглобина, составляя в среднем 3-4 нед, при этом минимальная суточная доза свободного железа должна составлять не менее 100 мг (оптимальная 150-200 мг). Поддерживающая терапия показана в тех ситуациях, когда сохраняется или трудно устранима причина дефицита железа (меноррагии, беременность, патология кишечника).
Оценка результатов лечения:
1. Изменение содержания ретикулоцитов. Считается, что ретикулоцитарный криз появляется на 3-7 сут от начала лечения препаратами железа. Содержание ретикулоцитов может при этом возрастать до 10-20 промилле. Максимальная ретикулоцитарная реакция наступает на 7-10 сут от начала лечения.
2. Прирост гемоглобина начинается с 5 сут при правильном лечении. Если в течение этого периода прироста гемоглобина нет, то это говорит о плохом усвоении препаратов железа. Нормальным считается прирост гемоглобина 1% в сутки или на 0,15 г/сут.
3. Восстановление числа эритроцитов и цветного показателя.
В большинстве случаев для коррекции дефицита железа при отсутствии специальных показаний ПЖ следует назначать внутрь. Показания для внутривенного введения ПЖ у больных ЖДА определяется конкретной клинической ситуацией, в частности, основными являются: состоянием кишечного всасывания и переносимостью пероральных ПЖ.
При переводе на парентеральный прием обязательно надо контролировать уровень сывороточного железа. Без этого показателя вводить внутривенно препараты железа противопоказано (кроме массивной кровопотери). При переводе с перорального на парентеральный прием, пероральное железо должно быть отменено за 2-3 дня.
Несколько другой взгляд относительно пути введения препаратов железа при ХСН представлен в обзоре D.S.Silverberg и соавт. [41]. При сравнении применения пероральных и внутривенных форм ПЖ оказалось, что при отдельном применении, а также в сочетании с эритропоэтином пероральных форм у больных с ХСН не удается достичь того положительного эффекта, получаемого при внутривенном введении, вероятно, за счет блокирования всасывания железа гепсидином. Данное заключение стало возможно после ряда исследований в этой области, которые начались с в некотором смысле революционного подхода в лечении пациентов с ХСН и дефицитом железа, предложенного английскими исследователями, по аналогии с лечением у больных с почечной патологией — внутривенного введения препаратов железа вне зависимости от наличия анемии без эритропоэтина [42]. В данном исследовании, а также в двух других[43, 44] показано достоверное увеличение уровня гемоглобина, фракции выброса левого желудочка, функционального класса ХСН, качества жизни, функции почек, снижение натрийуретических пептидов, С-реактивного белка, а также уменьшение частоты госпитализаций.
В другом исследовании терапии внутривенным железом при ХСН у больных с дефицитом железа вне зависимости от наличия анемии показано улучшение функционального класса ХСН, потребления кислорода и общего состояния даже при отсутствии повышения гемоглобина [45]. Эти данные подтверждают возможность непосредственного влияния железа на митохондриальные процессы окисления. Учитывая существенные различия по клинико-фармакологическим параметрам между препаратами железа необходимо отметить, что в данных исследованиях применялось железо в форме гидроксидсахарозного комплекса (венофер), по применению которого у больных ХСН накоплена в настоящий момент наибольшая доказательная база.
На этом фоне интересным представляется появление в распоряжении врачей нового препарата железа в виде карбоксимальтозатного комплекса (феринъект), обладающего существенно более удобным режимом введения (1 раз в неделю) и лучшим профилем безопасности по отношению к другим препаратам железа. Данная форма железа изучалась в одном из недавних крупных исследований, аналогичном упомянутым выше, у пациентов с ХСН и дефицитом железа вне зависимости от наличия анемии -FAIR-HF, показавшем при 6-месячном наблюдении достоверный переход в более низкий функциональный класс ХСН и улучшение показателей качества жизни при применении внутривенного препарата железа вне зависимости от снижения уровня гемоглобина [46]. Результаты данной работы позволяют частично ответить на вопрос о первичной роли железодефицита по сравнению с наличием анемии в патогенезе ХСН и необходимости его максимально безопасной коррекции.
В настоящий момент отсутствуют полноценные данные о влиянии монотерапии внутривенными препаратами железа на смертность и другие неблагоприятные исходы ХСН при долговременном наблюдении, для окончательного решения этого вопроса необходимы длительные крупные исследования, по результатам которых будут внесены изменения в соответствующие рекомендации.
Эритропоэтины
Применение рекомбинантного эритропоэтина и его в 3 раза более длительно действующего деривата дарбепоэтина в кардиологии наиболее всего изучено у пациентов с ХСН. В нескольких небольших исследованиях применения эритропоэтина в качестве монотерапии или в сочетании с парентеральными препаратами железа было показано снижение смертности и частоты госпитализаций [47]. Наряду с этим показан положительный эффект от данной терапии на различные клинические и функциональные показатели: систолическую и диастолическую функцию правого и левого желудочка, дилатацию камер сердца, гипертрофию левого желудочка, функциональный класс сердечной недостаточности, переносимость физических нагрузок, потребление кислорода, калорийность потребляемой пищи, качество жизни, активность эндотелиальных прогениторных клеток [47]. Данные эффекты не могут полностью объяснены воздействием на эритропоэз и связываются с плеотропными эффектами эритропоэтина, в частности активацией эндотелиальной NO синтетазы и AKT (протеинкиназа В), которая медиирует фосфорилирование, приводя к длительной NO-зависимой вазодилатации [48].
Эритропоэтины, позволяющие увеличить уровень гемоглобина в среднем на 2 г/дл, считаются основными препаратами для коррекции выраженной анемии, в том числе из-за редкости возникновения побочных реакций. Однако данные полученные в онкологических исследованиях свидетельствуют о повышенной частоте сердечно-сосудистых неблагоприятных исходов (в основном за счет тромботических осложнений) при превышении уровня гемоглобина более 12 г/дл [49]. При этом стоит отметить, что дозы эритропоэтинов в данных исследованиях в несколько раз превышали, используемые при ХСН. С другой стороны, у пациентов с ХСН и ХПН не выявлено дополнительного преимущества повышения уровня гемоглобина выше 11-12 г/дл, более того отмечено повышенное количество неблагоприятных исходов при повышении уровня гемоглобина выше 13 г/дл, так называемая U-образная зависимость уровня гемоглобина и смертности [50]. В настоящий момент, в отсутствии официальных рекомендаций по целевому уровню гемоглобина при ХСН, большинство исследователей сходятся на значении 12 г/дл [47].
Заключение
В настоящее время существуют достоверные данные о необходимости активного выявления и коррекции анемии у пациентов кардиологического профиля. Особый интерес вызывает вопрос терапии анемии при длительно протекающей сердечно-сосудистой патологии, в частности ХСН. Накопленная доказательная база у данных больных по лечению анемии эритропоэтинами и/или препаратами внутривенного железа не позволяет однозначно определить целесообразность и безопасность такого подхода. Данные исследований по применению внутривенных препаратов железа в качестве монотерапии у больных ХСН и железодефицитом вне зависимости от наличия анемии могут существенно расширить показания для их применения при данной патологии. Этот и некоторые другие вопросы, как например, наличие универсального маркера ответа при терапии препаратами железа, целевых уровнях гемоглобина при различных заболеваниях и многие другие требуют своего разрешения в научных работах.
До получения результатов крупных исследований лучшим подходом остается считать применение пероральных препаратов железа у пациентов с умеренной ЖДА, а у больных с тяжелой анемией возможна комбинация внутривенного железа и препаратов эритропоэтина, что позволит уменьшить дозы и снизить частоту побочных эффектов. При ХСН даже только с дефицитом железа без анемии можно рассмотреть назначение внутривенных препаратов железа.
источник
Слово «анемия» знакомо практически всем. Это заболевание, которое характеризуется сниженным количеством белка гемоглобина в крови. Его существует несколько видов, и далее рассмотрим, что такое вторичная анемия, причины, симптомы и способы лечения данной патологии.
Анемии, которые возникают на фоне сопутствующих болезней называют вторичными
Гемоглобин – это один из важнейших белков в человеческом организме. Он находится в эритроцитах, кровяных телах и отвечает за транспорт кислорода. То есть, при вдохе, кислород попадает в легкие и в крови, а белок его «разбирает» на молекулы и «доставляет» во все органы. Этим и обусловлена ценность гемоглобина. Без него, кислород не распространится по всему организму, что приводит к сбоям всех органов и систем.
Анемия не является самостоятельным заболеванием. Это последствие от той или иной болезни. Именно поэтому данную форму патологии называют вторичной или симптоматической. В связи с этим, когда обнаруживается низкий гемоглобин, необходимо пройти диагностику организма полностью, чтобы выявить истинную ее причину и назначить лечение.
Белок гемоглобин вырабатывается в эритроцитах, а они напрямую зависят от количества железа в организме.
Таким образом, когда железо падает, под воздействием определенных факторов, падает и гемоглобин. Если анемия первичная, тогда назначается курс железа и определенная диета. Спустя пару недель все показатели восстанавливаются. При вторичной анемии необходимо разобраться, из-за чего она возникла, а потом начинать лечение. При этом одним железом не получится восстановить уровень белка, так как изначально нужно побороть основную причину снижения гемоглобина.
Бледность кожи, головные боли, одышка и тахикардия – признаки заболевания
Для вторичной анемии существует множество причин, которые являются основным заболеванием, на фоне которых снизился гемоглобин.
Рассмотрим самые распространенные случаи:
- Анемия, возникшая при воспалительных процессах, связанных с заболеваниями, спровоцированными болезнетворными микроорганизмами. Часто снижается количество белка в крови из-за гнойных ран и при всех инфекциях (вирусах, бактериях, грибах), включая ВИЧ. Как правило, если болезнь длиться более месяца, но гемоглобин «падает» до 90. Основными факторами, которые провоцируют анемию, являются следующие: уменьшения количества железа в организме в результате лихорадки; из-за воздействия инфекции сокращается продолжительность жизни эритроцитов — тел, в который и вырабатывается гемоглобин; нарушение всасывания железа. В этом случае от анемии удастся избавиться только после лечения основного заболевания. Например, если гемоглобин снизился в результате пневмонии, то и лечить нужно пневмонию.
- Анемия при печеночных патологиях. Когда возникают заболевания печени, развивается анемия из-за недостатка железа. При циррозе могут возникать внутренние кровотечения в желудке, в конечностях из-за варикозного расширения вен. В результате заболевания Вильсона-Коновалова (нарушение обмена меди), чаще всего анемия бывает хронической. Данная болезнь характеризуется накоплением меди в эритроцитах, из-за чего и нарушается выработок белка.
- При онкологических заболеваниях анемия возникает по многим причинам: гемолиз, геморрагический статус, дефицит железа, последствие от лечения цитостатическими препаратами. В этом случае лечение дается сложно, так как при некоторых болезнях анемия не поддается терапии. Доказано, что при лимфомах, употребление железа не помогает от анемии. Это связано с тем, что оно просто не всасывается в кровь.
- Вторичная анемия нередко возникает у пациентов с патологиями соединительных тканей. Она развивается из-за нарушения секреции эритропоэтина и, конечно, из-за недостатка железа.
Из видео можно узнать основные симптомы анемии:
Кроме этого, существует еще множество причин, которые провоцируют анемию. Для точного определения и назначения лечения необходимо пройти дополнительную диагностику.
Что касается симптоматики, то развитие анемии можно определить по следующим факторам:
- быстрая утомляемость
- усталость после сна
- бледный цвет кожи
- вялость, сонливость
- боль в ногах и спине, желание прилечь
- выпадение волос, ломкость ногтей
- учащенное сердцебиение
- у некоторых – нарушение работы желудочно-кишечного тракта
- нарушение концентрации
- смена вкусовых качеств (желание есть мел, землю)
- чрезмерная раздражительность
Анемия негативно влияет на работу сердечно-сосудистая система
Если своевременно не оказать нормальное лечение, могут начаться осложнения. Выше уже писалось о том, какую роль выполняет гемоглобин в организме. То есть, если он разносит кислород, то при его недостатке может начаться кислородное голодание. В результате все жизненные процессы нарушатся и возникнут сбои практически во всех системах.
Особенно нельзя допускать осложнения при наличии хронических сердечно сосудистых заболеваний. Если своевременно не начать лечение анемия будет развиваться, а гемоглобин становиться все ниже и ниже. В результате это может привести к анемической коме – потеря сознания, которая возникает из-за недостаточного количества кислорода, приливаемого к головному мозгу.
Анемия плотно связана с сердечно-сосудистой системой. По статистике почти 50% пациентов с сердечной недостаточностью страдают от нехватки гемоглобина. Это связано с нарушением кровообращения и кислородной недостаточностью, возникающей из-за неполноценной работы сердца.
В результате кровь становится гуще, возникают проблемы с сосудами и развиваются сопутствующие заболевания – анемия, варикоз, тромбоз, атеросклероз и другие. Большая часть таких случаев заканчивается инсультом или инфарктом миокарда.
Диагностировать патологию можно с помощью анализа крови
Чтобы диагностировать вторичную анемию существует несколько способов:
- осмотр и опрос. Врач предварительно изучает анамнез, спрашивает у пациента о симптомах, самочувствии и болезнях, которые были в ближайшее время. Потом проводит осмотр визуальный, что даст возможность оценить состояние волос, кожи, слизистых
- общий анализ крови (из пальца) – это один из основных анализов, позволяющих оценить состояние здоровья пациента. Данный анализ позволяет определить количество кровяных тел и их соотношение, уровень гемоглобина, ретикулоциты, объем эритроцитов, соотношение белка и эритроцитов
- биохимический анализ крови (из вены), который укажет на уровень сывороточного железа и железосвязывающую способность крови.
Также необходимо провести диагностику, в соответствии с тем заболеванием, которое могло послужить причиной для развития вторичной анемии.
Как правило, это следующие исследования:
- компьютерная томография
- рентген легких, почек, печени, селезенки
- УЗИ половых органов, почек, печени
После того, как готовы все результаты, врач сможет сделать заключение. То есть определить степень тяжести вторичной анемии и причину ее развития. А уже после этого составляется курс лечения.
Если в процессе диагностики определиться, что причиной могло стать новообразование, тогда пациент направляется на дополнительный осмотр в онкологический диспансер, где врачи также проведут ряд анализов и определят состояние здоровья пациента.
Терапия зависит от тяжести болезни
Лечение вторичной анемии происходит в несколько этапов:
- Самый первый и важный – это воздействие на причину, которая спровоцировала развитие анемии. То есть, это лечение либо воспаления, либо воздействие болезнетворных микроорганизмов, некоторые патологии внутренних органов или, возможно, онкологическое заболевание.
- Прием медикаментозных средств, повышающих гемоглобин – железо, витамин В12.
- Соблюдение диетического питания, добавление в рацион продуктов, содержащих железо.
- Восполнение количества эритроцитов (тел, в которых образуется гемоглобин). Оно производится методом переливания или очищения крови.
В процессе лечения несколько раз берется анализ, чтобы контролировать изменение показателей. Если спустя некоторое время нет эффективности (то есть гемоглобин не повышается), тогда врач назначает дополнительные препараты.
Анемию очень сложно предугадать и провести методы профилактики, потому что это не самостоятельное заболевание, и возникает из-за любых патологических процессах в организме. Самый верный и эффективный способ предупредить вторичную анемию – это контроль. Специалисты рекомендуют регулярно контролировать уровень гемоглобина. Для этого нужно не реже, чем два раза в год сдавать кровь, чтобы контролировать показатели.
Кроме этого, удерживать гемоглобин в норме позволит правильное питание и здоровый образ жизни.
Важно отказаться от курения, или хотя бы свести к минимуму количество выкуриваемых сигарет. Также рекомендуется убрать из рациона питания продукты, которые затрудняют выработку эритроцитов и негативно влияют на качество крови – сладкое, соленое, острое, жирное, копченое. Для повышения гемоглобина используется гранатовый сок (натуральный) и печень – эти продукты содержат в себе рекордное количество железа, необходимого для поддержания нормального уровня гемоглобина.
Заметили ошибку? Выделите ее и нажмите Ctrl+Enter, чтобы сообщить нам.
источник
Следствием и проявлением сердечной недостаточност является уменьшение или увеличение кровенаполнения, кровотока или (и) давления в тех или иных центральных и периферических звеньях кровообращения. Эти изменения возникают не только как прямое механическое следствие нарушения насосной функции сердца, но и как результат неадекватности адаптационных реакций. К таким реакциям относятся тахи- и брадикардия, изменения сосудистого периферического и легочного сопротивления, «централизация» кровообращения и другие формы перераспределения кровенаполнения, задержка жидкости, натрия, гипертрофия и расширение отдельных камер сердца и пр. Нарушения гемодинамики в свою очередь ведут к патологическим изменениям как в самом сердце и сосудах, так и в других органах и системах и сопровождаются расстройствами, ограничивающими жизненную активность больного и, в конечном счете, угрожающими его жизни.
Симптомы, течение неодинаковы для различных форм и стадий сердечной недостаточности.
- Застойная левожелудочковая недостаточность характерна для митрального порока, для тяжелых форм ИБС — особенно у больных с артериальной гипертензией. Повышенное давление в легочных венах способствует наполнению левого желудочка и сохранению достаточного минутного объема сердца. В то же время застойные изменения в легких нарушают функцию внешнего дыхания и являются основным фактором, отягощающим состояние больного при этой форме СН. Проявления: одышка, ортопноэ, признаки застоя в легких аускультативные (сухие хрипы ниже уровня лопаток, мигрирующие влажные хрипы) и рентгенологические, сердечная астма и отек легких, вторичная легочная гипертензия, тахикардия. Левожелудочковая недостаточность выброса характерна для аортального порока, ИБС, артериальной гипертензии. Проявления: недостаточность мозгового кровообращения (головокружение, потемнение в глазах, обмороки), коронарная недостаточность, сфигмографические и эхокардиографические гризнаки низкого выброса. В тяжелых случаях возможны дыхание Чейна — Стокса, альтернирующий пульс (редко), пресистолический ритм галопа (патологический IV тон), клинические проявления застойной левожелудочковой недостаточности. В терминальной стадии может присоединиться правожелудочковая недостаточность. Застойная правожелудочковая нвдостаточность характерна для митрального и трикуспидального порока, констриктивного перикардита. Обычно присоединяется к застойной левожелудочковой недостаточности. Проявления: набухание шейных вен, высокое венозное давление, акроцианоз, увеличение печени, субиктеричность, отеки — полостные и периферические. Правожелудочковая недостаточность выброса характерна для стеноза легочной артерии, легочной гипертензии. Диагностируется и основном рентгенологически (обедненный периферический легочный сосудистый рисунок). Могут обнаруживаться другие признаки этой формы: одышка при строго определенном пороговом уровне физической нагрузки, гипертрофия правого желудочка — пальпаторные, затем и ЭКГ-признаки по типу «нагрузки давлением» (высокий зубец Я и снижение зубца Т в правых грудных отведениях). В особо тяжелых случаях серая окраска кожных покровов. Дистрофическая форма. Как правило, терминальная стадия правожелудочковой недостаточности. Варианты: а) кахектический; б) отечно-дистрофический с дистрофическими изменениями кожи (истончение, блеск, сглаженность рисунка, дряблость), отеками — распространенными или ограниченными подвижными, гипоальбуминвмией, в наиболее выраженных случаях — анасарка; в) некорригируемое солевое истощение.
В ряде случаев на первый план выступают изменения самого сердца (кардиомегалия, атриомегалия, мерцательная аритмия), что позволяет говорить о «центральной» форме сердечной недостаточности. В качестве особых форм со специфическими механизмами нарушения кровообращения и проявлениями рассматривают СН при «синих» врожденных пороках с недостаточным кровотоком в малом круге и несниженным или избыточным — в большом, при легочном сердце, тиреотоксикозе, анемии, артериовенозном соустье, циррозе печени, а также аритмогенную сердечную недостаточность. У больных с детства может развиться «пассивная адаптация» (малые масса тела и рост, плохое физическое развитие, резко сниженная физическая активность, инфантилизм). Перечисленные формы сердечной недостаточности встречаются в различных сочетаниях, часто удается выделить лишь ведущую форму.
Из многочисленных признаков СН. перечисляемых при описании той или иной стадии, необходимо выделить немногие, каждый из которых достаточен для определения конкретной стадии.
Стадия I. субъективные симптомы СН при умеренных или более значительных нагрузках. Стадия IIА.
- выраженные субъективные симптомы СН при незначительных нагрузках; ортопноэ; приступы удушья; рентгенографические, в части случаев — и электрокардиографические признаки вторичной легочной гипертензии; повторное появление отеков; повторное увеличение печени ; кардиомегалия без других признаков этой стадии; мерцательная аритмия без других признаков этой стадии.
- повторные приступы сердечной астмы; постоянные периферическив отеки; существенные полостные отеки — постоянные или появляющиеся повторно; стойкое увеличение печени, которая в ходе лечения может сократиться, но остается увеличенной; атриомегалия; кардиомегалия в сочетании хотя бы с одним из признаков предыдущей стадии; мерцательная аритмия в сочетании хотя бы с одним из признаков предыдущей стадии.
- тяжелые субъективные расстройства при минимальных нагрузках или в покое; неоднократные в течение недели эпизоды сердечной астмы; дистрофические изменения органов и тканей.
Если имеется хотя бы один «достаточный» признак более тяжелой стадии, то должна быть установлена именно эта стадия. Приоритет отдается клиническим критериям. Отрицательные результаты инструментальных исследований часто оказываются непоказательными. Такие наиболее очевидные конечные проявления СН, как снижение минутного объема, недостаточное кровоснабжение органов и тканей и недостаточное обеспечение их кислородом могут отсутствовать не только в покое, но и при доступной больному нагрузке. Подобно артериальному давлению соответствующие показатели могут не выходить за широкие пределы вариантов нормы и при тяжелой СН — вплоть до последних дней и часов жизни больного («компенсация на патологическом уровне»).
Наиболее существенные «прямые» проявления СН, определяющие качество жизни больного, оцениваются по шкале, принятой в международной практике модифицированной классификации Нью-Йоркской кардиологической ассоциации. Функциональные классы (ФК) определяются появлением тягостной одышки, сердцебиения, чрезмерного утомления или ангинозной боли — хотя бы одного из этих субъективных проявлений СН. Эти проявления отсутствуют при «ФК О». При классах I — IV они возникают при нагрузках той или иной интенсивности;
ФК I — при нагрузках выше ординарных (при быстрой ходьбе по ровному месту или при подъеме по отлогому склону); ФК II — при ординарных, сопровождающих повседневную жизнедеятельность, умеренных нагрузках (появляются, когда больной идет наравне с другими людьми своего возраста по ровному месту); ФК III — при незначительных, менее ординарных нагрузках, которые заставляют останавливаться при ходьбе по ровному месту в обычном темпе, при небыстром подъеме на один этаж; ФК IV — при минимальных нагрузках (несколько шагов по комнате, надевание халата, рубашки) или в покое.
Для оценки толерантности к физической активности проводятся пробы с дозированной физической нагрузкой (велоэргометр, тредмил). При острых и подострых формах ИБС, аортальном и субаортальном стенозе, высокой артериальной гипертензии, выраженной СН они противопоказаны.
В развернутом диагнозе должны фигурировать форма и степень (стадия) СН, а также ее основные проявления: мерцательная аритмия. сердечная астма (редкие, частные эпизоды), отек легких, вторичная легочная гипертензия, гепатомегалия, асцит гидроперикард, анасарка, кахексия, кардиомегалия, атриомегалия.
Следует объективно оценивать субъективные симптомы и убедиться, что они обусловлены именно СН, а не другой причиной — такой, например, как заболевание легких или невротическая реакция. В сомнительных случаях необходимо исключить легочную, почечную недостаточность, цирроз печени, микседему.
Распространенность и причины анемии у пациентов с хронической сердечной недостаточностью
Несмотря на значительные успехи, достигнутые в лечении больных, хроническая сердечная недостаточность (ХСН) ассоциируется с высокими показателями заболеваемости и смертности. Кроме того, в настоящее время ХСН уже не являются исключительно “кардиологической” проблемой и приобретает ряд междисциплинарных аспектов для специалистов различных областей клинической медицины. Все большее внимание исследователей привлекает сочетание ХСН и анемии, которая зачастую лечится неадекватно или вообще не корригируется, а порой даже не выносится в диагноз. Между тем анемия вносит потенциальный вклад в развитие и прогрессирование ХСН [1].
Распространенность анемии среди пациентов c ХСН, по разным данным, составляет от 10 до 50 %. Такой большой разброс показателей можно объяснить отсутствием единого подхода к диагностике анемий, различиями в возрастном и половом составе пациентов [2], наличием сопутствующей патологии, в частности хронической почечной недостаточности, артериальной гипертензии [3] и степенью тяжести ХСН [4]
Причины и патогенетические механизмы анемии при ХСН неоднозначны. По данным J. Ezekowitz, у 58 % пациентов встречается анемия хронических заболеваний (АХЗ), у 21 % – железодефицитная анемия (ЖДА) [3]. Согласно сведениям J.N. Nanas, ЖДА диагностирована в 73 % случаев, АХЗ – в 18,9 %, у 5,7 % пациентов выявлена гемодилюция, а у 2,4 % – анемия трактовалась как следствие приема лекарств [5].
Дефицит витамина В12 и фолиевой кислоты встречается у пациентов с ХСН довольно редко [6]. Дефицит железа среди больных ХСН диагностировался, по разным данным, в 5–21 % случаев [3, 5, 7, 8]. ЖДА у больных ХСН может развиваться в результате синдрома мальабсорбции и скрытых желудочно-кишечных кровотечений, вызванных приемом ацетилсалициловой кислоты. В исследовании R. de Silva и соавт. показано, что в 43 % случаев встречается снижение концентрации либо сывороточного железа, либо ферритина, однако микроцитарная анемия обнаруживается лишь в 6 % случаев [9]. В то же время, согласно данным J.N. Nanas и соавт. снижение запаса железа в костном мозге обнаруживается у 73 % пациентов. При этом уровень сывороточного железа, ферритина и эритропоэтина (ЭПО) в сыворотке оставался в пределах нормы, а средний объем эритроцита соответствовал нижней границе нормы, что не укладывалось в микроцитарный характер анемии [5]. Эти данные свидетельствуют скорее о возможном “перераспределении” железа при ХСН из костного мозга в другие макрофагальные депо, где оно оказывается недоступным для эритропоэза даже при нормальном уровне сывороточного железа и ферритина, как это происходит при АХЗ [10].
Таким образом, абсолютный или относительный дефицит железа довольно часто встречается среди пациентов с ХСН и приводит к развитию анемического синдрома.
У больных ХСН нередко имеет место дисфункция почек с нарушением выработки ЭПО. Последний синтезируется преимущественно специализированными фибробластами, расположенными внутри коркового и мозгового слоев почек [11]. Основным сигналом для повышения выработки ЭПО служит снижение парциального давления кислорода. Как известно, почка весьма чувствительна к гипоксии, несмотря на то что получает около 25 % от сердечного выброса, а использует менее 10 % полученного кислорода. Согласно данным ряда авторов, уровень эндогенного ЭПО в крови у пациентов с ХСН достоверно выше, чем у здоровых людей, причем чем тяжелее степень ХСН, тем выше концентрация ЭПО [12, 13]. В то же время у пациентов с ХСН и наличием анемии чаще встречается низкая концентрация ЭПО. По-видимому, усиление выработки этого гормона почками в ответ на снижение перфузии при застойной ХСН непродолжительно [14]. При снижении фракции выброса на фоне застойной ХСН происходит уменьшение почечного кровотока [15], что в конечном итоге приводит к почечной дисфункции, которая обусловливает снижение выработки ЭПО с последующим развитием анемии [16].
Анемия при ХСН может развиваться из-за нарушения в ренин-ангиотензиновой системе, а также вследствие приема ингибиторов ангиотензинпревращающего фермента (АПФ). Ренин-ангиотензиновая система играет важную роль в регуляции объема плазмы и числа эритроцитов. Увеличение концентрации ангиотензина II (АТ-II) в плазме приводит к изменению перитубулярного парциального давления кислорода [17]. Снижение парциального давления кислорода в перитубулярных фибробластах коркового вещества приводит к повышению концентрации активных форм кислорода внутри клетки, которые активируют фактор гипоксии HIF-1, увеличивая экспрессию гена ЭПО [18], т. е. АТ-II увеличивает секрецию ЭПО за счет эффектов снижения почечного кровотока и усиления реабсорбции в проксимальных канальцах. Имеются данные о том, что АТ-II оказывает прямое стимулирующее воздействие на эритроидный росток костного мозга [19]. Таким образом, применение ингибиторов АПФ и антагонистов рецепторов AT-II вызывает анемию путем снижения выработки ЭПО [20, 21]. В оригинальном исследовании А. Ishani и соавт. показано, что у пациентов с ХСН с нормальными показателями гематокрита на фоне приема эналаприла увеличивается частота выявления анемий в течение года. Тем не менее у пациентов, получавших эналаприл, выживаемость была выше по сравнению с пациентами, не получавшими данный препарат, даже при развитии анемического синдрома [20]. Это свидетельствует о том, что, несмотря на способность ингибиторов АПФ вызывать анемию, они остаются препаратами первого ряда при лечении ХСН.
При развитии ХСН отмечено нарастание концентрации фактора некроза опухоли α (ФНО-α), интерлейкина-6 (ИЛ-6) и других провоспалительных цитокинов [22], а также С-реактивного белка [23], что может приводить к уменьшению концентрации гемоглобина (Hb) [24]. Показано, что ИЛ-6 и ФНО-α ингибируют синтез ЭПО в почках путем активации гена GATA II и нуклеарного фактора В [25]. Это объясняет, почему у пациентов с ХСН снижается выработка эндогенного ЭПО после кратковременной стимуляции его синтеза. Кроме того, интерлейкины способны напрямую ингибировать эритроидный росток костного мозга [26], усугубляя анемию, хотя механизмы их действия остаются невыясненными. В экспериментах на крысах с индуцированной ХСН показано уменьшение числа клеток-предшественников эритроидного ростка и клеток, синтезирующих ЭПО [25].
В клиническом исследовании С. Opasich и соавт. причина анемии среди 148 пациентов с ХСН была выявлена лишь у 43 %, причем только у 5 % больных была диагностирована ЖДА. У остальных 57 % пациентов верифицировать генез анемии не удалось. Следует подчеркнуть, что именно у данной категории больных были выявлены нарушения синтеза гема, а также низкий уровень эндогенного ЭПО и высокая активность провоспалительных цитокинов, несмотря на адекватные депо железа в организме [8]. Еще одним механизмом развития анемии в условиях высокой концентрации ИЛ-6 является увеличение синтеза гепсидина печенью, который в свою очередь уменьшает всасывание железа в кишечнике. Кроме того, ИЛ-6 ингибирует экспрессию белка ферропортина на мембране клеток-депо железа (энтероцитов, гепатоцитов, макрофагов). Этот белок отвечает за транспорт железа из клетки наружу, т. е. снижение его количества приводит к нарушению высвобождения железа из депо [10]. Аналогичный механизм развития анемии наблюдается у онкологических пациентов [27]. Таким образом, активация провоспалительных цитокинов – основной механизм развития АХЗ – во многом обусловливает развитие анемии у пациентов с ХСН. На рис. 1 представлены основные патогенетические механизмы анемии при ХСН.
Большинство исследователей приходят к заключению о неблагоприятном влиянии анемического синдрома на прогноз у больных ХСН. Так, у пациентов с тяжелой ХСН снижение содержания Hb оказалось независимым предиктором смертности (относительный риск – 1,131, 95 % доверительный интервал – 1,045–1,224 для снижения уровня Hb на 1 г/дл) [28].
источник
Чаще всего нехватка гемоглобина в крови возникает по таким причинам:
- Неправильное питание.
- Частые кровопотери, в том числе и донорство.
- Инфекции: туберкулез и другие поражения легких, эндокардит, пиелонефрит , остеомиелит, микозы так далее.
- Системные заболевание соединительной ткани: ревматоидный артрит, волчанка и другие.
- Поражение глистами.
- Нарушения в системе распада эритроцитов – у больных малокровием это происходит быстрее.
Сама по себе анемия при сердечно-сосудистых заболеваниях может не давать специфических симптомов, или вообще протекать на первых этапах бессимптомно. Поэтому к некоторым состояниям при их частом и беспричинном повторении следует отнестись очень серьезно. Признаками анемии могут быть:
- Усталость, общая слабость.
- Бледность.
- Ломкость ногтей и выпадение волос.
- Сухость слизистых.
- Усложненное дыхание.
- Головные боли.
- Низкая концентрация внимания.
- Шум в ушах.
- Ощущение холода в конечностях.
- Раздражительность.
- Изменение вкуса. Например, человек начинает есть несъедобные вещи – мел, песок, глину и другое.
Плохое состояние сердечно-сосудистой системы при анемии доказано: приблизительно 48% пациентов с сердечной недостаточностью страдают от дефицита гемоглобина. Кроме этого, такая особенность состава крови повышает риск развития инфаркта миокарда.
Болезни ССС в принципе тяжелее переносятся пациентами с малокровием, но хуже всего оно сочетается с сердечно-сосудистой недостаточностью, лечение которой при наличии сопутствующего диагноза осложняется.
Заболевания крови не редкость среди населения, но безусловным лидером конечно же является анемия, которую с легкостью можно отнести к полиэтиологичным заболеванием, появляющиеся в результате патогенного воздействия внешних и внутренних факторов на состав и состояние крови.
Что такое анемия и чем опасна, каковы симптомы болезни, виды и стадии, как лечить анемию и не допустить ее развития? В данной статье попробуем разобраться!
Клинические признаки анемии заметны на второй и третей стадии болезни. Общими симптомами анемии являются следующие состояния:
- повышенная утомляемость;
- хроническая усталость;
- дрожание конечностей;
- головокружение;
- обморочные состояния;
- сухость и бледность кожных покровов;
- постоянная одышка, даже при отсутствии физических нагрузок;
- сердцебиение;
- рассеянное внимание;
- снижение памяти;
- шум в ушах;
- плохой аппетит;
- круги под глазами;
- «мушки» перед глазами.
Бледность и сухость кожи при анемии
Симптомы анемии достаточно выраженные, но они также могут присутствовать и при других заболеваниях или нарушениях. Поэтому если у Вас присутствуют признаки анемии, не нужно ставить себе диагноз. Единственным правильным решением станет посещение врача, который после результатов лабораторных исследований сможет подтвердить или опровергнуть Ваши предположения.
Лечить анемию нужно комплексно, только тогда можно добиться желаемого результата. Легкая стадия анемии зачастую не требует медикаментозного лечения. Врач рекомендует побольше употреблять продуктов, которые содержат железо, белки и другие витамины и минералы.
Медикаментозная терапия назначается врачом только когда ясен вид анемии, причина и степень тяжести. Не редко анемия не требует медикаментозной коррекции, особенно тогда, когда устранена причина, на фоне которой появилась анемия.
Если все же болезнь требует медикаментозного лечения, тогда врач назначает препараты, которые позволят костному мозгу быстрее восполнить дефицит эритроцитов и гемоглобина в крови. К таким лекарствам относятся:
- Препараты железа: Фенюльс, Тотетема, Сорбифер, Актиферрин;
- Витаминные средства: вит. В12, фолиевая кислота, комплексы витаминов группы В.
Медикаментозное лечение анемии
В более тяжелых случаях, когда препараты железа не дают положительный результат, врач может назначить глюкокортикоидные гормоны, эритропоэтины, анаболические стероиды, химиотерапевтические средства и другие лекарства, лечение которыми проводят в стационаре.
Рецепт 1 . Для приготовления понадобится 150 мл свежего сока алоэ 250 г меда и 350 мл вина «Кагор». Все хорошо перемешать и принимать по 1 ложке 3 раза в день, на протяжении 1 месяца.
Рецепт 2. Хороший эффект можно получить от следующего настоя. Понадобятся: плоды шиповника, плоды земляники лесной в равных частях по 10 гр. Плоди нужно залить кипятком, поставить на водяную баню на 15 минут, затем охладить, отжать и принимать по 1/2 стакана 2 раза вдень.
Рецепт 3 . Листы земляники (2 ст. л.) нужно залить кипятком, отцедить и принимать 3 раза в день по 2 столовых ложки.
Лечение анемии народными средствами может служить только как вспомогательная терапия к основному лечению.
Препараты железа: фенюльс, тотетема, сорбифер, актиферрин;Витаминные средства: цианокобаламин (витамин В12), фолиевая кислота, комплексы витаминов группы В (мильгама, неуробекс), аскорбиновая кислота, витамин Е.
Глюкокортикоидные гормоны: дексаметазон, метилпреднизолон, солу-кортеф, кортинеф;Препараты крови: отмытые эритроциты, эритроцитарная масса;Эритропоэтины: эпоэтин, эпокомб, эпрекс, анаболические стероиды (местеролон, надролон);Химиотерапевтические средства: цитостатитки (имуран).
Любые виды медикаментозной коррекции обязательно должны сочетаться с коррекцией образа жизни и правильным питанием. Рацион обогащается говядиной, субпродуктами, рыбой и морепродуктами, свежими овощами и фруктами.
Лечение анемии зависит от ее степени и вида
Наиболее часто анемия отражается на сердечно-сосудистой системе и работе головного мозга, однако если болезнь не лечится, то в результате дефицит гемоглобина сказывается на всех органах. Для сердца тотальное кислородное голодание из-за недостаточно насыщенной крови означает повышенную работу – для того чтобы обеспечить организм, ему приходится сокращаться чаще.
Поэтому состояние сердечно-сосудистой системы при анемии быстро ухудшается, могут проявляться аритмии, сильное сердцебиение, скачки артериального давления и сердечная недостаточность. Большая перекачка крови может влиять и на состояние сосудов, которые быстрее изнашиваются, становятся менее эластичными.
Уменьшение количества гемоглобина;Снижение количества эритроцитов (возникает в большинстве случаев);Признаки нарушения кровоснабжения тканей и их гипоксия (кислородное голодание).
При этом происходит снижение интенсивности метаболических процессов и функционирования всех систем организма, утяжеляется течение имеющихся заболеваний.
Важно помнить! Поскольку кровь взаимодействует с каждой клеткой, патологические процессы любой локализации способны повлиять на ее состояние и состав. Это делает анемию полиэтиологичным заболеванием, которое возникает в результате патогенного действия множества факторов на красный росток крови!
Существует не мало причин, которые способны привести к развитию анемии. Как самостоятельное заболевание, анемия развивается редко. Чаще всего спусковым механизмом для появления данного синдрома становятся различные заболевания внутренних органов или неблагоприятные факторы, которые повлияли на состав крови.
Анемия — причины могут становится приобретенные или генетические заболевания: ревматоидный артрит, системная красная волчанка, почечная недостаточность, хронические инфекций. Дефицит железа в организме может произойти при неправильном образе жизни, некачественном питании, при больших кровопотерях, чрезмерных физических и психологических нагрузках.
Дефицит вит B12 – причина анемии
Железодефицитная анемия – наиболее распространенный вид анемии, поскольку диагностируется у 90% больных. Данный вид анемии может резвится при неблагоприятных условиях жизни, после операции или травмах, в которых произошла большая потеря крови.
Пернициозная анемия — развивается на фоне дефицита витамина В12. Причиной чаще становится врожденная неспособность кишечника усваивать вит. B12. У взрослых болезнь развивается при атрофии желудка.
Гемолитическая анемия – проявляется в результате неспособности головного мозга в достаточном количестве вырабатывать клетки. Среди причин анемии можно выделить: наследственность, инфекционные заболевания, постоянные стрессы, депрессивные состояния.
Серповидноклеточная анемия – характеризуется гибелью эритроцитов. Причиной такого состояния являются генетические дефекты.
Талассемия — наиболее тяжелая форма анемии, которая относится к наследственным анемиям, возникающие на фоне генетических нарушений.
Несмотря на достаточное количество причин анемии, ее виды, в любом из случаев болезнь не должна оставаться без должного внимания. Кроме того, каждый вид анемии ведет к кислородному голоданию внутренних органов, что значительно ухудшает их функциональность и может привести к необратимым последствиям.
- потеря крови (острые или хронические кровотечения);
- повышенное разрушение эритроцитов (гемолиз);
- уменьшенное производство эритроцитов.
Также следует заметить, что в зависимости от вида анемии причины ее возникновения могут отличаться.
Факторы, влияющие на развитие анемии
- гемоглобинопатии ( изменение строения гемоглобина наблюдается при талассемии, серповидноклеточной анемии );
- анемия Фанкони ( развивается вследствие имеющегося дефекта в кластере белков, которые отвечают за восстановление ДНК );
- ферментативные дефекты в эритроцитах;
- дефекты цитоскелета ( клеточный каркас, располагающийся в цитоплазме клетки ) эритроцита;
- врожденная дизэритропоэтическая анемия ( характеризуется нарушением образования эритроцитов );
- абеталипопротеинемия или синдром Бассена-Корнцвейга ( характеризуется нехваткой бета-липопротеина в клетках кишечника, что ведет к нарушению всасываемости питательных веществ );
- наследственный сфероцитоз или болезнь Минковского-Шоффара ( вследствие нарушения клеточной мембраны эритроциты принимают шарообразную форму ).
- дефицит железа;
- дефицит витамина B12;
- дефицит фолиевой кислоты;
- дефицит аскорбиновой кислоты ( витамин С );
- голодание и недоедание.
Хронические заболевания и новообразования
- почечные заболевания ( например, туберкулез печени, гломерулонефрит );
- заболевания печени ( например, гепатит, цирроз );
- заболевания желудочно-кишечного тракта ( например, язва желудка и двенадцатиперстной кишки, атрофический гастрит, неспецифический язвенный колит, болезнь Крона );
- коллагеновые сосудистые болезни ( например, системная красная волчанка, ревматоидный артрит );
- доброкачественные и злокачественные опухоли ( например, миома матки, полипы в кишечнике, рак почек, легких, кишечника ).
- вирусные заболевания ( гепатит, инфекционный мононуклеоз, цитомегаловирус );
- бактериальные заболевания ( туберкулез легких или почек, лептоспироз, обструктивный бронхит );
- протозойные заболевания ( малярия, лейшманиоз, токсоплазмоз ).
Ядохимикаты и медикаментозные средства
- неорганический мышьяк, бензол;
- радиация;
- цитостатики ( химиотерапевтические препараты, используемые для лечения опухолевых заболеваний );
- антибиотики;
- нестероидные противовоспалительные средства;
- антитиреоидные препараты ( снижают синтез гормонов щитовидной железы );
- противоэпилептические препараты.
Анемия, как и любое другое заболевание может нанести серьезный вред нашему здоровью. При несвоевременном или некачественном лечении любого вида анемии, развивается риск развития кислородного голодания внутренних органов и систем, которые не только не получают кислород, но и питательные вещества.
Самым грозным осложнением анемии является гипоксическая кома, в 80% случаях ведет к смерти человека. Кроме того, люди, страдающие анемией входят в группу риска к развитию сердечно – сосудистых патологий, также дыхательной недостаточности.
Нарушения в работе сердечно – сосудистой системы при анемии
Анемия имеет свои стадии развития:
- Легкая или анемия 1 степени характеризуется снижением гемоглобина дог/л. На данном этапе симптомы отсутствуют. Для повышения гемоглобина достаточно правильно питаться, употреблять как можно больше железосодержащих продуктов.
Коррекции в питании при 1 степени анемии
- Средняя или 2 стадия анемии сопровождается снижением гемоглобина дог/л. В этот период симптомы анемии достаточно выраженные. Человек ощущает общую слабость, частые головные боли, головокружение. Повысить гемоглобин помогут лекарственные препараты и правильное питание.
Хроническая усталость – как признак анемии
- Тяжелая, или 3 стадия – опасна для жизни. Количество гемоглобина в крови ниже 70 г/л. На данном этапе, больной ощущает нарушения в работе сердца, значительно ухудшается общее состояние человека.
Изменения в сердечно-сосудистой системе закономерно обнаруживаются при достаточно выраженной анемии. Уменьшение насыщения крови кислородом компенсируется увеличением минутного объема сердца, в частности увеличением коронарного кровотока.
Одновременно увеличивается поглощение миокардом кислорода в крови. В механизме увеличения сердечного выброса при анемии играет роль ряд факторов. При этом в отличие от других гипердинамических состояний увеличение функции надпочечников или симпатической нервной системы, по-видимому, не имеет решающего значения, так как блокада β-адренергических рецепторов не предупреждает усиления функции левого желудочка.
Существенное значение придают следующим факторам: расширению периферических артерий, образованию артериовенозных шунтов и особенно снижению вязкости крови. Увеличение сердечного выброса достаточно отчетливо выявляется при снижении уровня гемоглобина приблизительно вдвое, т. е.
ниже 70 г/л (7 г%), при гематокрите ниже 25%. Приступы стенокардии, а на более позднем этапе — сердечная недостаточность с застойными явлениями могут развиваться при анемии, однако чаще всего у лиц с предшествующим поражением сердца другой природы.
Декомпенсация может возникнуть как следствие очень тяжелой анемии самой по себе, особенно у лиц ослабленных с недостаточным белковым питанием, что встречается в слаборазвитых странах. Обычно это больные талассемией и серповидноклеточной анемией, у которых имеет место гемолиз.
Постгеморрагическая анемия может приводить к поражению миокарда с увеличением размеров сердца и даже к развитию сердечной недостаточности при снижении уровня гемоглобина ниже 40 г/л (4 г%). Увеличение сердечного выброса при анемии происходит как за счет тахикардии, так и в результате повышенного ударного объема, в связи с чем у многих больных отмечают повышение пульсового давления.
Больные анемией обычно бледны. Помимо указанных изменений пульса и артериального давления, иногда виден так называемый капиллярный пульс на ногтевом ложе. На обеих сонных артериях закономерно выслушивается систолический шум, который на ФКГ занимает несколько больше первой половины систолы.
Характерен систолический шум изгнания на легочной артерии, что отражает усиление кровотока в этой области. При тяжелой анемии, протекающей с дилатацией сердца, выслушиваются шумы, обусловленные недостаточностью митрального и трехстворчатого клапанов. У таких больных описаны также Шумы, типичные для аортальной недостаточности.
Мы наблюдали больного, у которого наличие быстро прогрессирующей анемии при появлении лихорадки, шумов в сердце, в том числе диастолического на аорте, большой амплитуды артериального давления, позволило подозревать затяжной септический эндокардит с поражением аортальных клапанов.
Однако отсутствие спленомегалии, почечного синдрома, отрицательная формоловая проба вызывали сомнение в этом диагнозе. Изменение крови укладывалось в картину апластической анемии, что подтвердилось дальнейшим течением болезни клинически и было подтверждено на вскрытии.
При патологическом исследовании обнаружены апластическая анемия с геморрагическим диатезом, множественные кровоизлияния во все внутренние органы, в том числе в ткань миокарда. Сердце было увеличенным, клапаны эластичными.
Мышца сердца на разрезе имела вид вареного мяса со множеством очагов кровоизлияния под эпикардом. Возможно появление при анемии других шумов в сердце, в том числе диастолического шума на верхушке, который вызывает подозрение на митральный стеноз.
Особенно часто этот шум возникает при серповидноклеточной анемии. Рентгенологически конфигурация сердца при выраженной, достаточно длительно существующей анемии часто приближается к митральной из-за раннего увеличения правого желудочка.
Встречающееся иногда закругление дуг свидетельствует о миогенной дилатации. В отличие от митрального порока при анемии редко увеличивается левое предсердие, а при расширении последнего контрастированный пищевод отклоняется кзади по пологой дуге.
При анемиях возможны и другие, в первую очередь аускультативные, симптомы, которые позволяют подозревать порок сердца. Так, иногда имеют место тенденция к увеличению расщепления II тона на выдохе и аускультативные признаки дефекта межпредсердной перегородки.
Время кровотока при анемии обычно нормальное или уменьшенное и мало уменьшается даже при развитии сердечной недостаточности. Исследование гемодинамики даже при нерезко выраженной анемии (гемоглобин в среднем 95 г/л) показало, что при этом в покое сердечный выброс близок к нормальному, но после нагрузки он увеличивается значительно больше, чем у здоровых лиц.
При развитии признаков сердечной недостаточности минутный объем несколько уменьшается, оставаясь выше нормы. На ЭКГ, помимо синусовой тахикардии, может быть снижение амплитуды зубца Т и сегмента ST в левых грудных отведениях.
Лечение анемии зависит от основного заболевания, вызвавшего ее (дефицит железа, пернициозная анемия, гемолиз, кровопотеря). Если в связи с анемией развивается сердечная недостаточность, то лечение анемии является обязательным условием ее коррекции и эффективной терапии.
Обычно раннее применение препаратов наперстянки у таких больных считается малоперспективным. Однако теперь анемия сама по себе (без сопутствующего поражения сердца иной природы) не приводит к нарушению кровообращения, поэтому применение дигиталиса в таких случаях следует считать обоснованным.
Это подтверждают и исследования гемодинамики: под влиянием строфантина у больных анемией уменьшается повышенное давление в предсердиях и увеличивается сердечный выброс. Целесообразно рекомендовать постельный режим, ограничить прием натрия и назначить мочегонные средства.
Пополнение красной крови при этом следует проводить постепенно. Переливание цельной крови таким больным может спровоцировать развитие острой сердечной недостаточности. С целью быстрого улучшения показателей красной крови медленно переливают эритроцитную массу.
Заболевания системы крови занимают одни из первых позиций по распространенности в общей структуре заболеваемости. Среди них безусловным лидером является анемия крови. Но, несмотря на свою частую встречаемость, особенно среди женского населения и у детей, ее исходы не такие печальные, как у других гематологических болезней.
Все зависит от причин и механизмов возникновения, степени выраженности, устойчивости к медикаментозной коррекции и общего состояния организма. Тонкостям анемии, как самостоятельной проблемы, посвящена данная статья.
По патогенезу анемия может развиться вследствие кровопотери, нарушения образования эритроцитов или из-за их выраженного разрушения.
По механизму развития выделяют:
- анемии вследствие острой или хронической кровопотери;
- анемии вследствие нарушения кровообразования ( например, железодефицитная, апластическая, ренальная анемия, а также B12 – и фолиеводефицитная анемия );
- анемии вследствие усиленного разрушения эритроцитов ( например, наследственная или аутоиммунная анемия ).
В зависимости от уровня снижения гемоглобина различают три степени тяжести течения анемии. В норме уровень гемоглобина у мужчин составляет 130 – 160 г/л, а у женщин 120 – 140 г/л.
Существуют следующие степени тяжести анемии:
- легкая степень, при которой наблюдается снижение уровня гемоглобина относительно нормы до 90 г/л;
- средняя степень, при которой уровень гемоглобина составляет 90 – 70 г/л;
- тяжелая степень, при которой уровень гемоглобина ниже 70 г/л.
Цветовой показатель — это степень насыщения эритроцитов гемоглобином. Рассчитывается он на основе результатов анализа крови следующим образом. Цифру три необходимо умножить на показатель гемоглобина и поделить на показатель эритроцитов (запятая убирается).
Классификация анемий по цветному показателю:
- гипохромная анемия ( ослабленная окраска эритроцитов ) цветовой показатель менее 0,8;
- нормохромная анемия цветовой показатель равен 0,80 – 1,05;
- гиперхромная анемия ( эритроциты чрезмерно окрашены ) цветовой показатель более 1,05.
По морфологическому признаку
При анемиях во время исследования крови могут наблюдаться эритроциты различные по размеру. В норме диаметр эритроцитов должен составлять от 7,2 до 8,0 мкм (микрометр). Меньший размер эритроцитов (микроцитоз) может наблюдаться при железодефицитной анемии.
Классификация анемий по морфологическому признаку:
- микроцитарная анемия, при которой диаметр эритроцитов менее 7,0 мкм;
- нормоцитарная анемия, при которой диаметр эритроцитов варьирует от 7,2 до 8,0 мкм;
- макроцитарная анемия, при которой диаметр эритроцитов более 8,0 мкм;
- мегалоцитарная анемия, при которой размер эритроцитов составляет более 11 мкм.
По способности костного мозга к регенерации
Так как формирование эритроцитов происходит в красном костном мозге, то основным признаком регенерации костного мозга является увеличение уровня ретикулоцитов (предшественники эритроцитов) в крови. Также их уровень указывает на то, как активно протекает образование эритроцитов (эритропоэз). В норме в крови человека число ретикулоцитов не должно превышать 1,2% всех эритроцитов.
По способности костного мозга к регенерации различают следующие формы:
- регенераторная форма характеризуется нормальной регенерацией костного мозга ( количество ретикулоцитов составляет 0,5 – 2% );
- гипорегенераторная форма характеризуется сниженной способностью костного мозга к регенерации ( количество ретикулоцитов составляет ниже 0,5% );
- гиперрегенераторная форма характеризуется выраженной способностью к регенерации ( количество ретикулоцитов составляет более двух процентов );
- апластическая форма характеризуется резким подавлением процессов регенерации ( количество ретикулоцитов менее 0,2%, или наблюдается их отсутствие ).
Снижение уровня гемоглобина до 90 г/л;Снижение уровня гемоглобина от 70 до 90 г/л;Снижение гемоглобина менее 70 г/л.
Данная рубрика классификации также важна, как и этиологическая, так как влияет на лечебную тактику в отношении анемии. Особенно опасно снижение гемоглобина, возникающее при острой кровопотере, так как организм не успевает адаптироваться к таким условиям.
Беременность – один из факторов риска по возникновению железодефицитной анемии
Нарушение поступления железа в организм
- вегетарианство вследствие неупотребления белков животного происхождения ( мясо, рыба, яйца, молочные продукты );
- социально-экономическая составляющая ( например, недостаточно денег для полноценного питания ).
Нарушение усвоения железа
Всасывание железа происходит на уровне слизистых желудка, поэтому такие заболевания желудка как гастриты, язвенная болезнь или резекция желудка приводят к нарушению всасывания железа.
Повышенная потребность организма в железе
- беременность, в том числе многоплодная беременность;
- период лактации;
- подростковый возраст ( за счет быстрого роста );
- хронические заболевания, сопровождающиеся гипоксией ( например, хронический бронхит, пороки сердца );
- хронические нагноительные заболевания ( например, хронические абсцессы, бронхоэктатическая болезнь, сепсис ).
Потери железа из организма
- легочные кровотечения ( например, при раке легких, туберкулезе );
- желудочно-кишечные кровотечения ( например, язва желудка и двенадцатиперстной кишки, рак желудка, рак кишечника, варикозное расширение вен пищевода и прямой кишки, неспецифический язвенный колит, глистные инвазии );
- маточные кровотечения ( например, преждевременная отслойка плаценты, разрыв матки, рак матки или шейки матки, прервавшаяся внематочная беременность, миома матки );
- почечные кровотечения ( например, рак почек, туберкулез почек ).
- анемический синдром;
- сидеропенический синдром.
Анемический синдром характеризуется следующими симптомами:
- выраженная общая слабость;
- повышенная утомляемость;
- дефицит внимания;
- недомогание;
- головная боль и головокружение;
- сонливость;
- стул черного цвета (при желудочно-кишечном кровотечении);
- сердцебиение;
- одышка.
Сидеропенический синдром характеризуется следующими симптомами:
- извращение вкуса (например, больные едят мел, сырое мясо);
- извращение обоняния (например, больные нюхают ацетон, бензин, краски);
- волосы ломкие, тусклые, секущиеся;
- на ногтях появляются белые пятна;
- кожные покровы бледные, кожа шелушится;
- в углах рта могут появляться хейлиты (заеды).
Также больной может жаловаться на развитие судорог в ногах, например, при подъеме вверх по лестнице.
- бледность кожных покровов и слизистых;
- трещины в углах рта;
- «глянцевый» язык;
- в тяжелых случаях увеличение размеров селезенки.
В общем анализе крови наблюдаются следующие изменения:
- снижение уровня эритроцитов и гемоглобина;
- микроцитоз (эритроциты малого размера);
- гипохромия эритроцитов (слабая окраска эритроцитов);
- пойкилоцитоз (эритроциты разных форм).
В биохимическом анализе крови наблюдаются следующие изменения:
- снижение уровня ферритина;
- сывороточное железо снижено;
- железосвязывающая способность сыворотки повышена.
Инструментальные методы исследования
Для выявления причины, которая привела к развитию анемии, больному могут быть назначены следующие инструментальные исследования:
- фиброгастродуоденоскопия (для исследования пищевода, желудка и двенадцатиперстной кишки);
- УЗИ (для исследования почек, печени, женских половых органов);
- колоноскопия (для исследования толстого кишечника);
- компьютерная томография (например, для исследования легких, почек);
- рентген легких.
В питании железо делится на:
- гемовое, которое поступает в организм с продуктами животного происхождения;
- негемовое, которое поступает в организм с продуктами растительного происхождения.
Следует заметить, что гемовое железо усваивается в организме значительно лучше, нежели негемовое.
Количество железа на сто миллиграмм
Продукты питания растительного происхождения
- сушеные грибы;
- свежий горох;
- гречка;
- геркулес;
- свежие грибы;
- абрикосы;
- груша;
- яблоки;
- сливы;
- черешня;
- свекла.
- 35 мг;
- 11,5 мг;
- 7,8 мг;
- 7,8 мг;
- 5,2 мг;
- 4,1 мг;
- 2,3 мг;
- 2,2 мг;
- 2,1 мг;
- 1,8 мг;
- 1,4 мг.
При соблюдении диеты также следует увеличить потребление продуктов, содержащих витамин C, а также белок мяса (они повышают усвояемость железа в организме) и снизить потребление яиц, соли, кофеина и кальция (они уменьшают всасываемость железа).
При лечении железодефицитной анемии больному параллельно с диетой назначается прием препаратов железа. Данные лекарственные средства предназначены для восполнения дефицита железа в организме. Они выпускаются в виде капсул, драже, инъекций, сиропов и таблеток.
- возраста пациента;
- степени тяжести заболевания;
- причины, вызвавшей железодефицитную анемию;
- на основе результатов анализов.
Препараты железа принимаются за один час до еды или через два часа после приема пищи. Данные лекарственные средства нельзя запивать чаем или кофе, так как снижается всасываемость железа, поэтому их рекомендуется запивать водой или соком.
Принимать внутрь по одному грамму три – четыре раза в сутки.
Принимать по одной таблетке в день, с утра за тридцать минут до приема пищи.
Принимать по одной таблетке один – два раза в день.
Данные препараты рекомендуется назначать совместно с витамином C (по одной таблетке один раз в день), так как последний увеличивает всасываемость железа.
- при тяжелой степени анемии;
- если анемия прогрессирует, несмотря на принимаемые дозы железа в виде таблеток, капсул или сиропа;
- если у больного имеются заболевания желудочно-кишечного тракта (например, язва желудка и двенадцатиперстной кишки, неспецифический язвенный колит, болезнь Крона), так как принимаемый препарат железа может усугубить имеющееся заболевание;
- перед оперативными вмешательствами с целью ускоренного насыщения организма железом;
- если у пациента имеется непереносимость препаратов железа при их приеме внутрь.
Хирургическое лечение
Хирургическое вмешательство производится при наличии у больного острого или хронического кровотечения. Так, например, при желудочно-кишечном кровотечении может применяться фиброгастродуоденоскопия или колоноскопия с выявлением области кровотечения и последующей его остановкой (например, удаляется кровоточащий полип, коагулируется язва желудка и двенадцатиперстной кишки).
источник