Серповидно-клеточная анемия – это наследственное заболевание крови. Попробуем разобраться, в чем же оно заключается. Эритроциты крови содержат гемоглобин – белок, который переносит кислород в крови. В норме эритроциты имеют круглую форму и они гибкие, что позволяет им двигаться через мелкие кровеносные сосуды, чтобы доставить кислород ко всем частям тела.
Серповидно-клеточная анемия заставляет клетки крови принимать форму полумесяца, или серпа. В такой форме клеток крови эритроциты очень легко распадаются, что вызывает анемию. Серповидные красные клетки живут всего 10-20 дней вместо 120 дней, как бывает в норме у здоровых клеток. Кроме того, поврежденные эритроциты слипаются и прилипают к стенкам кровеносных сосудов, блокируя поток крови. Это может стать причиной сильных болей и постоянного повреждения мозга, сердца, легких, почек, печени, костей и селезенки.
Серповидно-клеточная анемия человека вызывается генетической аномалией в гене гемоглобина. Эта аномалия приводит к появлению серповидного гемоглобина. Когда кислород высвобождается от серповидного гемоглобина, он склеивается и образует длинные стержни, которые повреждают эритроцит и изменяют его форму. Серповидные эритроциты и вызывают симптомы серповидно-клеточной анемии.
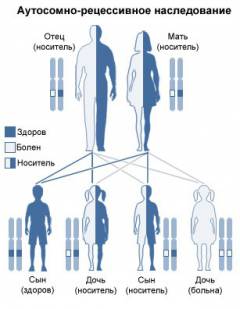
Серповидно-клеточная анемия человека не заразна. Это генетическое заболевание, с которым рождается человек. Заболевание развивается, когда ребенок наследует два аномальных гена гемоглобина, по одному от каждого из родителей. Люди, которые унаследовали только один аномальный ген гемоглобина, являются его носителями, но у них не будет анемии и симптомов этого заболевания.
Симптомами серповидно-клеточной анемии могут быть:
- Сильные боли;
- Анемия;
- Боль в груди и затрудненное дыхание;
- Боль в суставах, артрит;
- Закупорка кровотока в селезенке или печени;
- Тяжелые инфекции.
У больных серповидно-клеточной анемией развивается тяжелая боль в груди, спине, руках, ногах и животе. Кроме того, боль может возникать в любой части тела. Серповидные красные кровяные клетки в легких могут вызвать серьезные заболевания с такими симптомами, как боль в груди, лихорадка и затрудненное дыхание. Серповидно-клеточная анемия может привести и к необратимым повреждениям мозга, сердца, почек, печени, селезенки и костей. Ососбенность этого заболевания в том, что тяжесть и симптомы болезни могут сильно отличаться у разных людей, даже если они являются кровными родственниками.
Серповидные эритроциты можно увидеть, когда образец крови исследуется под микроскопом. Но для диагностики серповидно-клеточной анемии человека используется специальный анализ крови – гемоглобин-электрофорез, который позволяет измерить количество аномального гемоглобина. В зависимости от установленного количества серповидного гемоглобина можно определить, является ли человек носителем гена или имеет заболевание серповидно-клеточную анемию.
Есть и быстрые скрининг-тесты, которые помогают выявить серповидные эритроциты или сгустки аномального гемоглобина, когда кислород выходит из крови. Но эти тесты применяются редко, потому что они не позволяют отличить заболевание и простое наличие гена болезни.
Перинатальная диагностика серповидно-клеточной анемии проводится путем изучения ДНК клеток плода, полученных при биопсии хориона или амниоцентеза.
Для лечения серповидно-клеточной анемии человека применяются:
- Опиоидные обезболивающие (например, морфин);
- Противовоспалительные препараты (например, ибупрофен);
- Антибиотики для лечения инфекций;
- Кислород;
- Внутривенное или пероральное введение специальных жидкостей.
Переливание эритроцитов может понадобиться в случае тяжелой анемии, для профилактики приступов стенокардии или перед операцией. Иногда обменное переливание осуществляется с помощью специального аппарата, который удаляет серповидные красные кровяные клетки и заменяет их на здоровые.
Для лечения серповидно-клеточной анемии может назначаться специальный препарат – гидроксимочевина. Он помогает предотвратить приступы боли. Исследования показали, что при регулярном приеме гидроксимочевины у больных серповидно-клеточной анемией уменьшается частота и тяжесть приступов боли, а также сокращается количество необходимых переливаний крови и госпитализаций.
Единственным способом действительно вылечить серповидно-клеточную анемию человека является пересадка стволовых клеток. Это достаточно новый метод лечения. Он сопряжен с серьезными рисками (около 5-10% риск смертельного исхода), но те пациенты, трансплантация стволовых клеток у которых прошла успешно, полностью вылечились от серповидно-клеточной анемии.
Пересадка стволовых клеток обычно делается молодым пациентам с тяжелой серповидно- клеточной анемией, для которых удается подобрать подходящего донора. Иногда для трансплантации стволовых клеток используется пуповинная кровь от донора-родственника.
Важно и то, что ученые постоянно изучают возможность лечения серповидно-клеточной анемии человека с помощью новых препаратов, которые предотвращают выработку серповидно- клеточных эритроцитов красных кровяных клеток и улучшают кровоток и доставку кислорода к органам и тканям. И эти новые методы лечения уже довольно успешно проходят тестовые испытания.
Вообще люди с серповидно-клеточной анемией, как правило, имеют меньшую продолжительность жизни. Но современная медицина показывает неплохие результаты. Современные методики лечения позволяют существенно продлить жизнь таким пациентам.В 1973 году средняя продолжительность жизни людей с серповидно-клеточной анемией была 14 лет, а сегодня цифра 40-50 лет является вполне реальной. Бывает, что пациенты живут 60 лет и дольше. Постоянное лечение гидроксимочевиной может продлить жизнь.
источник
Серповидно-клеточная анемия – заболевание, которое развивается на фоне генной мутации. Наследственное заболевание приводит к изменению формы и структуры эритроцитов. Видоизмененные клетки крови приводят к анемии и множеству других отрицательных последствий. Пациент страдает от неправильного развития скелета, кислородного голодания мозга, кризов. Заболевание не поддается лечению, однако существуют меры его профилактики. Терапия назначается симптоматическая.
Что происходит в организме больного серповидной клеточной анемией? Нарушается структура эритроцитов, в результате генной мутации они меняют форму. Видоизмененные клетки приводят к закупориванию сосудов и анемии. Виноваты в этих явлениях серповидные клетки – эритроциты типа S. Медицинское обозначение – HbS.
Серповидную анемию относят к хроническим неизлечимым заболеваниям. Эта болезнь поддается симптоматическому лечению: при начале приступа срочно проводится терапия с использованием питательных веществ, аппаратов для насыщения тканей кислородом.
У болезни есть несколько форм. Самая опасная – гомозиготная. Пациенты с такой формой в основном умирают в возрасте до 10 лет. Носители другой формы – гетерозиготной – могут прожить полноценную жизнь, но страдают от побочных симптомов и более подвержены кризам, выкидышам, инфекционным и вирусным заболеваниям; у них часто развивается тромбоцитоз.
Серповидноклеточная анемия – генетическое заболевание. Оно появляется у детей, чьи родители – носители гена эритроцита S. Болезнь считается рецессивной, то есть подавляется при наличии здоровыми генами. Если только один из родителей является носителем гена, а второй здоров, то вероятность заболевания ребенка – 25%. При наличии генов у обоих родителей малыш будет страдать от гетерозиготной анемии. Это анемия, при которой больной ген – лишь один, и концентрация мутировавших эритроцитов сниженная.
Если же генный тип ребенка в направлении эритроцитов полностью состоит из мутировавших генов, то он страдает от гомозиготной формы заболевания. Эта форма не поддается лечению, пациенты с такой серповидноклеточной анемией в основном умирают еще в детстве.
Опасаться болезни стоит в основном семьям, где один или оба супруга – выходцы из Индии, Средней Азии, прилежащих территорий. Заболевание пошло именно из этих районов. Появление S типа эритроцитов можно связать с большим риском заражения малярией в рассмотренных местах. Пациенты с серповидными клетками крови не подвержены этому заболеванию, так как возбудитель не может встроиться в длинный изогнутый эритроцит.
Носителем может оказаться и человек европейской внешности.
Причины серповидноклеточной анемии могут быть и вторичными. Это те факторы, которые вызывают не появление заболевания, а его развитие. Носители гена могут не проявлять симптомов отклонения до тех пор, пока они не подвергнутся:
- обезвоживанию;
- гипоксии;
- серьезной инфекции;
- стрессам;
- физической перегрузке.
Это провоцирующие факторы, которых для профилактики отклонения нужно избегать.
Тип наследования серповидноклеточной анемии – рецессивный. Рассмотреть его можно на примере: «AA+Aa=Aa/AA». Здесь ген анемии – a, то есть рецессивный, который проявит себя полностью только при наличии второго такого же гена. Однако в представленном примере у полностью здорового родителя и носителя заболевания рождается ребенок с неполным обладанием вредоносным геном. Это случай гетерозиготного заболевания. Подробнее о нем можно узнать в разделе ниже.
При рецессивном типе наследования риск передачи заболевания не стопроцентный. Оно может передаться в приведенных ниже случаях.
- Оба родителя – обладатели генов aa (вероятность 100%).
- Один из родителей носитель генов aa, другой – Aa (вероятность гетерозиготной формы – 100%, гомозиготной – 75%).
- Оба родителя – носители генов Aa (вероятность гетерозиготной формы – 50%, гомозиготной – 25%, рождения здорового ребенка – 25%).
- Один из родителей обладает генотипом AA, другой Aa (гомозиготная форма невозможна, вероятность гетерозиготной – 25%).
Эти данные используются для прогнозирования передачи серповидноклеточной анемии от родителей к ребенку при планировании беременности. Единственный способ снижения риска болезни – найти другого партнера, не являющегося носителем гена.
Наследование серповидноклеточной анемии может быть гетерозиготным. Чем отличается такая форма недуга? Больной обладает и стандартными эритроцитами, и мутировавшими. При этом концентрация каждых клеток разнится. В основном мутировавших клеток меньше, и человек не замечает свой недуг до момента сильного физического напряжения или гипоксии: 2 из 3 новорожденных ребенка не будут проявлять симптомы серповидноклеточной анемии, характерные для детей, вплоть до полового созревания.
Гетерозиготная форма серповидной клеточной анемии развивается при наследовании только половины вредоносного гена. Пациенты с такой формой склонны к следующим проблемам:
- поздним менструациям;
- выкидышам;
- ранним родам;
- болезням сердца и печени, селезенки;
- сниженным иммунитетом.
Для предотвращения кризов такие больные должны соблюдать меры профилактики.
Как проходит патогенез серповидной клеточной анемии.
- В полилипидной бета-цепи эритроцита глутаминовая кислота заменяется валином.
- В результате изменения структуры эритроцит становится в 100 раз менее растворяемым; человек страдает повышенным разрушением эритроцитов.
- Пониженная растворяемость вкупе с постоянной циркуляцией эритроцитов по сосудам приводит к формированию особой формы клеток. Они становятся серповидными.
- Эритроциты, несущие гемоглобин s, плохо проходят по сосудистым путям в связи с изменением формы. Они вызывают тромбы и кризы. Часть больных не может предотвратить тромбообразование.
- В результате постоянного закупоривания сосудов страдают ткани организма. Развиваются некрозы, нарушения костной структуры. Вероятна умственная отсталость на фоне ослабленного питания мозга и недостатка кислорода.
Нормальных эритроцитов (с типом гемоглобина а) у пациентов с гомозиготной формой болезни нет. Поэтому они страдают от хронического типа недуга. Мозг таких больных обычно остается на уровне 2-3 летнего ребенка, не развиваются речевые центры.
Результатом постоянного голодания клеток из-за серповидной клеточной анемии организм подвергается необратимым структурным изменениям. Итогом таких нарушений становится смерть больного (при гомозиготах). Гетерозиготные пациенты серповидно клеточной анемии страдают от нарушения всю жизнь, но могут поддерживать нормальную жизнедеятельность.
Диагностировать серповидную клеточную анемию можно на любой стадии развития: до рождения ребенка, в неонатальный период, в детстве или взрослом возрасте. Основной метод диагностики – исследования крови:
- мазок крови с периферии;
- биохимический анализ – биохимия при серповидноклеточной анемии позволяет определить растворимость эритроцитов;
- электрофорез гемоглобина;
- пренатальная диагностика.
Потомку носителя болезни диагностика назначается обязательно как при рождении, так и при планировании ребенка.
Предотвратить серповидно-клеточную анемию можно еще на стадии планирования ребенка. Будущим родителям, являющимся носителями гена серповидных эритроцитов, необходимо пройти генетический тест. Он выявит вероятность рождения больного ребенка. Далее необходимо консультироваться со специалистами по планированию беременности. Диагностика серповидно клеточной болезни в пренатальный период проводится путем взятия цепей ДНК из ворсин хориона.
Повсеместным становится использованием тестов на анемию у новорожденных. Они уже включены в обязательную программу скрининг-тестов в западных странах. Чтобы определить форму эритроцита, проводится электрофорез. Он позволяет дифференцировать клетки HbS, A, B,C. Растворимость эритроцитов в сосудах в раннем возрасте проверить еще нельзя.
При периоде разгара заболевания ярко выражены симптомы кислородного голодания. Человек страдает от головокружений, потерей сознания, снижения чувствительности нервной системы. Но есть и более специфичные признаки анемии:
- боли в печени, сердце, почках и селезенке;
- рубцевание и некроз органов;
- человек становится более подвержен тромбозам сосудов;
- снижается иммунитет;
- кризис селезненки;
- неправильно растут кости;
- различные кризы;
- кожа приобретает желтоватый оттенок;
- видны признаки истощения, хотя человек питается нормально.
Состояние больного постоянно ухудшается, так как даже при купировании главной проблемы болезни (закупорки сосудов) ткани все равно успевают подвергнуться голоданию и некрозам.
Во время кризов при серповидноклеточной анемии может происходить временное прекращение кровообращения в некоторых частях организма. Это особенно сказывается на селезенке и печени. Эти органы начинают рубцеваться и увеличиваться. Сильное увеличение селезенки на фоне недостаточного питания или другой хронической проблемы и называется кризисом.
Проявления кризиса следующие:
- частая икота;
- проблемы при приеме пищи (орган не позволяет сильно растягиваться желудку, в результате чего съесть получается лишь небольшую порцию);
- боли с левой стороны живота.
Явление имеет медицинское обозначение – спленомегалия.
При серповидноклеточной анемии у детей и взрослых происходят периодические обострения – кризы. Они характеризуются специфичными признаками. Симптомы обострения серповидной клеточной анемии.
- При вазоокклизивном кризе – сильные боли в костях и тахикардия. Развивается лихорадка, повышенная потливость. Это самый распространенный вид обострения.
- При секвестрационных кризах страдают печень и селезенка. Появляются боли в этих органах, высок риск коллапса клапанов или инфаркта.
- При серповидном грудном синдроме (следствии вазоокклизивного криза) развивается инфаркт костного мозга и дыхательная недостаточность. Это главная причина смертности взрослых больных.
- При аппластическом кризе резко снижается гемоглобин. Это состояние купируется силами организма.
При кризах необходимо срочно обращаться за врачебной помощью из-за высокой вероятности летального исхода.
Осложнения серповидно клеточной болезни происходят на фоне недостатка питания костей и тканей. Основные последствия:
- нарушение зрения;
- учащенные респираторные заболевания;
- нерегулярные менструации;
- нарушения умственного и речевого развития;
- инфекции;
- острые боли в животе;
- тахикардия;
- постоянное увеличение селезенки.
Острые формы осложнений могут привести к смерти.
Лечение серповидноклеточной анемии проводится только в рамках устранения симптома. Генетическая болезнь является неизлечимой, поэтому полностью избавиться от нее невозможно. В будущем будет вероятно излечение благодаря генной терапии, но сейчас это лечение только на стадии разработки. При тяжелых формах для сохранения жизни пациента могут предложить пересадку стволовых клеток, однако это действие сопряжено с большим риском смерти (5-10%).
В основном меры терапии следующие:
- гемотрансфузии;
- общеукрепляющее лечение;
- использование симптоматической медикаментозной терапии.
Больные серповидно клеточной анемией могут принимать симптоматические препараты для борьбы с признаками болезни. Основным видом лечения считаются анальгетики опиоидного типа. Они вводятся внутривенно в амбулаторных условиях. Подходят такие медикаменты, как морфин. Следует избегать ввода меперидина. В домашних условиях допустимы только слабые анальгетики.
При серповидной клеточной анемии, особенно при кризах, резко падает гемоглобин. Для предотвращения этого явления и восстановления уровня гемоглобина назначаются гемотрансфузии. Их эффективность еще полностью не доказана. Процедура назначается при содержании в крови гемоглобина менее 5 г на литр.
Пациентам, страдающим легкой формой серповидноклеточной анемии или подверженным ее началу, назначается общее укрепление организма. Оно включает комплексные процедуры по укреплению иммунитета, улучшению питания и сосудистой системы тела. Назначаются физические упражнения, способствующие насыщению крови кислородом. Прописываются профилактические курсы антибиотиков и уколов фолиевой кислоты. С любой инфекцией борются антибиотиками. Остальные укрепляющие действия можно отнести к профилактике, подробнее о которой написано ниже.
Профилактика болезни включает меры, направленные на предотвращение кризов. У больных с гомозиготной формы данные процедуры бесполезны: закупоривание сосудов и неблагоприятные последствия происходят в любом случае, так как концентрация серповидных эритроцитов преимущественна перед стандартными. Профилактические меры направлены на снижение риска возникновения кризов у больных с гетерозиготной формой.
- избегание повышенных физических нагрузок;
- ограничение в высотности проживания (не в горах);
- ограничения в местах пребывания (запрещены экскурсии в гору, посещения аттракционов-башен с резким падением, бейсджампинг и др.);
- избегание авиаперелетов.
Эти действия направлены на предотвращение гипоксии – синдрома, возникающего при перепадах давления. Другие меры связаны с иммунными, физиологическими нагрузками на сердце:
- нужно избегать инфекций: тщательно мыть руки, соблюдать гигиену;
- в период обострения респираторных заболеваний, эпидемий обязательно необходимо принимать препараты для улучшения иммунитета;
- детям назначаются дополнительные прививки: от менингита и пневомококковой инфекции;
- необходимо соблюдать питьевой режим во избежание развития обезвоживания.
При правильном образе жизни и полноценном питании прогноз для гетерозиготных носителей положительный.
Прогноз для больных гомозиготной формой отрицательный. В качестве профилактики используются периодические сеансы спленэктомии, обязательны регулярные посещения гематолога.
источник

Серповидноклеточная анемия (СКА) является наиболее тяжелой формой наследственных гемоглобинопатий (генетически обусловленных нарушений строения гемоглобина). Серповидные эритроциты быстро разрушаются в организме, а также закупоривают множество сосудов по всему организму, что может стать причиной тяжелых осложнений и даже смерти.
Данное заболевание крови широко распространено в странах Африки и является частой причиной смерти лиц негроидной расы. Это связано с широким распространением малярии в данном регионе (инфекционного заболевания, поражающего эритроциты человека). Ввиду миграции населения и смешивания этнических групп сегодня данный вид анемии может встречаться у людей любой расы в самых различных регионах мира. Мужчины и женщины болеют одинаково часто.
Интересные факты
- Первое документированное упоминание о серповидноклеточной анемии датируется 1846 годом.
- Около 0,5% населения Земли являются здоровыми носителями гена серповидноклеточной анемии.
- Как больные серповидноклеточной анемией, так и бессимптомные носители мутантного гена практически невосприимчивы к малярии. Это связано с тем, что возбудитель малярии (малярийный плазмодий) способен поражать только нормальные эритроциты.
- На сегодняшний день серповидноклеточная анемия считается неизлечимым заболеванием, однако при адекватном лечении больные люди могут доживать до глубокой старости и иметь детей.
Внутреннее пространство эритроцита почти полностью заполнено гемоглобином – особым белково-пигментным комплексом, состоящим из белка глобина и железосодержащего элемента – гема. Именно гемоглобин играет главную роль в транспорте газов в организме.
Каждый эритроцит содержит, в среднем, 30 пикограмм (пг) гемоглобина, что соответствует 300 миллионам молекул данного вещества. Молекула гемоглобина состоит из двух альфа (а1 и а2) и двух бета (b1 и b2) белковых цепей глобина, которые образуются путем соединения множества аминокислот (структурных компонентов белков) в строго определенной последовательности. В каждой цепи глобина находится молекула гема, включающая в себя атом железа.
Образование глобиновых цепей запрограммировано генетически и контролируется генами, расположенными в различных хромосомах. Всего в организме человека 23 пары хромосом, каждая из которых представляет собой длинную и компактную молекулу ДНК (дезоксирибонуклеиновой кислоты), которая включает в себя огромное число генов. Избирательная активация того или иного гена приводит к синтезу определенных внутриклеточных белков, которые в конечном итоге и определяют структуру и функцию каждой клетки организма.
За синтез а-цепей глобина ответственны четыре гена с 16 пары хромосом (ребенок получает по 2 гена от каждого из родителей, а синтез каждой цепи контролируется двумя генами). В то же время синтез b-цепей контролируется только двумя генами, расположенными в 11 паре хромосом (каждый ген отвечает за синтез одной цепи). К каждой образовавшейся цепи глобина присоединяется гем, в результате чего формируется полноценная молекула гемоглобина.
Важно отметить, что кроме альфа-цепей и бета-цепей, в эритроцитах могут образовываться и другие цепи глобина (дельта, гамма, сигма). Их комбинации приводят к образованию различных видов гемоглобина, что характерно для определенных периодов развития человека.
В организме человека определяется:
- HbA. Нормальный гемоглобин, состоящий из двух альфа и двух бета-цепей. В норме данная форма составляет более 95% гемоглобина взрослого человека.
- HbA2. Малая фракция, в норме составляющая не более 2% всего гемоглобина взрослого человека. Состоит из двух альфа и двух сигма-цепей глобина.
- HbF (фетальный гемоглобин). Данная форма состоит из двух альфа и двух гамма-цепей и преобладает в период внутриутробного развития плода. Она обладает большим сродством к кислороду, что обеспечивает тканевое дыхание ребенка в период рождения (когда доступ кислорода из организма матери ограничен). У взрослого человека доля HbF не превышает 1 – 1,5% и встречается в 1 – 5% эритроцитов.
- HbU (эмбриональный гемоглобин). Начинает образовываться в эритроцитах со 2 недели после зачатия и полностью замещается фетальным гемоглобином после начала кроветворения в печени.
Транспортная функция эритроцитов обусловлена наличием атомов железа в составе гемоглобина. При прохождении через легочные капилляры железо присоединяет к себе молекулы кислорода и транспортирует их ко всем тканям организма, где происходит отделение кислорода от гемоглобина и переход его в клетки различных органов. В живых клетках кислород принимает участие в клеточном дыхании, а побочным продуктом данного процесса является углекислый газ, который выделяется из клеток и также связывается с гемоглобином.
При повторном прохождении через легочные капилляры углекислый газ отсоединяется от гемоглобина и выделяется из организма с выдыхаемым воздухом, а к освободившемуся железу присоединяются новые молекулы кислорода.
Образование эритроцитов (эритропоэз) впервые отмечается на 19 день эмбрионального развития в желточном мешке (особом структурном компоненте эмбриона). По мере роста и развития человеческого организма кроветворение происходит в различных органах. Начиная с 6 недели внутриутробного развития основным местом образования эритроцитов являются печень и селезенка, а на 4 месяце появляются первые очаги кроветворения в красном костном мозге (ККМ).
Красный костный мозг представляет собой совокупность стволовых кроветворных клеток, расположенных в полостях костей организма. Больше всего вещества ККМ находится в губчатых костях (костях таза, черепа, тел позвонков), а также в длинных трубчатых костях (плеча и предплечья, бедра и голени). Постепенно доля кроветворения в ККМ увеличивается. После рождения ребенка кроветворная функция печени и селезенки угнетается, и костный мозг становится единственным местом образования эритроцитов и других клеток крови – тромбоцитов, обеспечивающих свертываемость крови, и лейкоцитов, выполняющих защитную функцию.
Все клетки крови образуются из так называемых стволовых клеток, которые появляются в организме плода на раннем этапе эмбрионального развития в небольшом количестве. Данные клетки считаются практически бессмертными и уникальными. Они содержат ядро, в котором располагается ДНК, а также множество других структурных компонентов (органоидов), необходимых для роста и размножения.
В скором времени после образования стволовая клетка начинает делиться (размножаться), в результате чего появляется множество ее клонов, которые дают начало другим клеткам крови.
Из стволовой клетки образуется:
- Клетка-предшественница миелопоэза. Эта клетка схожа со стволовой, но обладает меньшим потенциалом к дифференцировке (приобретению специфических функций). Под влиянием различных регуляторных факторов она может начать делиться, при этом происходит постепенная утрата ядра и большинства органоидов, а результатом описанных процессов является образование эритроцитов, тромбоцитов или лейкоцитов.
- Клетка-предшественница лимфопоэза. Данная клетка обладает еще меньшей способностью к дифференцировке. Из нее образуются лимфоциты (разновидность лейкоцитов).
Процесс дифференцировки (превращения) клетки-предшественницы миелопоэза в эритроцит стимулируется особым биологическим веществом – эритропоэтином. Он выделяется почками, если ткани организма начинают испытывать недостаток в кислороде. Эритропоэтин усиливает образование эритроцитов в красном костном мозге, их количество в крови повышается, что увеличивает доставку кислорода к тканям и органам.
Эритропоэз в красном костном мозге длится около 4 – 6 дней, после чего в кровоток выделяются ретикулоциты (молодые формы эритроцитов), которые в течение суток окончательно созревают, превращаясь в нормальные эритроциты, способные выполнять транспортную функцию.
Средняя продолжительность жизни нормального эритроцита оставляет 100 – 120 дней. Все это время они циркулируют в крови, постоянно изменяясь и деформируясь при прохождении через капилляры органов и тканей. С возрастом происходит уменьшение пластических свойств эритроцитов, они становятся более округлыми и утрачивают способность к деформации.
В норме небольшая доля красных клеток крови разрушается в красном костном мозге, в печени или непосредственно в сосудистом русле, однако абсолютное большинство стареющих эритроцитов разрушается в селезенке. Ткань данного органа представлена множеством синусоидных капилляров, имеющих в своих стенках узкие щели. Нормальные эритроциты без труда проходят через них, после чего возвращаются в кровоток. Старые эритроциты менее пластичны, в результате чего они застревают в синусоидах селезенки и разрушаются специальными клетками данного органа (макрофагами). Кроме того, изъятию из кровообращения и разрушению подвергаются эритроциты с нарушенной структурой (как при серповидноклеточной анемии) либо зараженные различными вирусами или микроорганизмами.
В результате разрушения эритроцитов, образуется и выделяется в кровоток пигмент желтого цвета – билирубин (непрямой, несвязанный). Это вещество плохо растворяется в воде. С током крови оно переносится в клетки печени, где связывается с глюкуроновой кислотой – образуется связанный, или прямой, билирубин, который включается в состав желчи и выделяется с калом. Часть его всасывается в кишечнике и выделяется с мочой, придавая ей желтоватый оттенок.
Железо, входящее в состав гема, также выделяется в кровоток при разрушении эритроцитов. В свободной форме железо токсично для организма, поэтому оно быстро связывается со специальным белком плазмы – трансферрином. Трансферрин переносит железо в красный костный мозг, где оно вновь используется для синтеза эритроцитов.
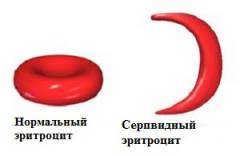
Артериальная кровь, оттекающая от легких, насыщена кислородом, поэтому никаких изменений в структуре гемоглобина не происходит. На тканевом уровне молекулы кислорода переходят в клетки различных органов, что приводит к полимеризации гемоглобина и образованию серповидных эритроцитов.
На начальных этапах заболевания данный процесс обратим — при повторном прохождении через легочные капилляры кровь насыщается кислородом, и эритроциты приобретают свою нормальную форму. Однако такие изменения повторяются каждый раз, когда эритроциты проходят через различные ткани и отдают им кислород (сотни или даже тысячи раз в день). В результате этого строение мембраны эритроцитов нарушается, повышается ее проницаемость для различных ионов (из клетки выходит калий и вода), что привод к необратимому изменению формы эритроцитов.
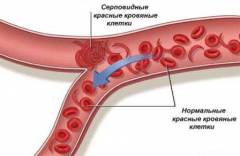
Пластические способности серповидного эритроцита значительно снижены, он не способен обратимо деформироваться при прохождении через капилляры и может закупоривать их. Нарушение кровоснабжения различных тканей и органов обуславливает развитие тканевой гипоксии (недостатка кислорода на тканевом уровне), что приводит к образованию еще большего количества серповидных эритроцитов (образуется так называемый порочный круг).
Мембрана серповидных эритроцитов отличается повышенной ломкостью, в результате чего продолжительность их жизни значительно укорачивается. Уменьшение общего количества эритроцитов в крови, а также местные нарушение кровообращения на уровне различных органов (в результате закупорки сосудов) стимулирует образование эритропоэтина в почках. Это усиливает эритропоэз в красном костном мозге и может частично или полностью компенсировать проявления анемии.
Важной отметить, что HbF (состоящий из альфа-цепей и гамма-цепей), концентрация которого в некоторых эритроцитах достигает 5 – 10%, не подвергается полимеризации и предотвращает серповидную трансформацию эритроцитов. Клетки с малым содержанием HbF подвергаются изменениям в первую очередь.
Половые клетки мужчины и женщины содержат в себе по 23 хромосомы. В процессе оплодотворения происходит их слияние, в результате чего образуется качественно новая клетка (зигота), из которой и начинает развиваться плод. Ядра мужских и женских половых клеток также сливаются между собой, восстанавливая, таким образом, полноценный набор хромосом (23 пары), присущий клеткам человеческого организма. При этом ребенок наследует генетический материал от обоих родителей.
Серповидноклеточная анемия наследуется по аутосомно-рецессивному типу, то есть, чтобы родился больной ребенок, он должен унаследовать мутантные гены от обоих родителей.
В зависимости от набора генов, полученных от родителей, может родиться:
- Ребенок, больной серповидноклеточной анемией. Такой вариант возможен в том и только в том случае, если и отец, и мать ребенка больны данным заболеванием либо являются его бессимптомными носителями. При этом ребенок должен унаследовать по одному дефектному гену от обоих родителей (гомозиготная форма заболевания).
- Бессимптомный носитель. Данный вариант развивается в том случае, если ребенок наследует один дефектный и один нормальный ген, который кодирует образование нормальных цепей глобина (гетерозиготная форма заболевания). В результате в эритроците будет примерно одинаковое количество как гемоглобина S, так и гемоглобина А, которого достаточно для поддержания нормальной формы и функции эритроцита в обычных условиях.
На сегодняшний день не удалось установить точную причину возникновения генных мутаций, приводящих к возникновению серповидноклеточной анемии. Однако исследованиями последних лет выявлен ряд факторов (мутагенов), воздействие которых на организм может приводить к повреждению генетического аппарата клеток, вызывая целый ряд хромосомных заболеваний.
Причиной генетических мутаций может быть:
- Малярийная инфекция. Данное заболевание вызывается малярийными плазмодиями, которые при попадании в организм человека поражают эритроциты, вызывая их массовую гибель. Это может приводить к мутациям на уровне генетического аппарата красных клеток крови, обуславливая появление различных заболеваний, в том числе серповидноклеточной анемии и других гемоглобинопатий. Некоторые исследователи склонны считать, что хромосомные мутации в эритроцитах являются своего рода защитной реакцией организма против малярии, так как серповидные эритроциты практически не поражаются малярийным плазмодием.
- Вирусная инфекция. Вирус представляет собой неклеточную форму жизни, состоящую из нуклеиновых кислот РНК (рибонуклеиновой кислоты) или ДНК (дезоксирибонуклеиновой кислоты). Данный инфекционный агент способен размножаться только внутри клеток живого организма. Поражая клетку, вирус встраивается в ее генетический аппарат, изменяя его таким образом, что клетка начинает продуцировать новые фрагменты вируса. Данный процесс может вызывать возникновение различных хромосомных мутаций. В качестве мутагена могут выступать цитомегаловирусы, вирусы краснухи и кори, гепатита и многие другие.
- Ионизирующее излучение. Представляет собой поток невидимых невооруженным глазом частиц, которые способны воздействовать на генетический аппарат абсолютно всех живых клеток, приводя к возникновению множества мутаций. Количество и выраженность мутаций зависит от дозы и длительность облучения. Помимо естественного радиационного фона Земли дополнительными источниками радиации могут стать аварии на АЭС (атомных электростанциях) и взрывы атомных бомб, частные рентгенологические исследования.
- Вредные факторы окружающей среды. В данную группу входят различные химические вещества, с которыми сталкивается человек в процессе своей жизнедеятельности. Сильнейшими мутагенами являются эпихлоргидрин, используемый в производстве множества медикаментов, стирол, использующийся при изготовлении пластмасс, соединения тяжелых металлов (свинца, цинка, ртути, хрома), табачный дым и множество других химических соединений. Все они обладают высокой мутагенной и канцерогенной (вызывающей рак) активностью.
- Лекарственные препараты. Действие некоторых медикаментов обусловлено их влиянием на генетический аппарат клеток, что связано с риском возникновения различных мутаций. Наиболее опасными лекарственными мутагенами являются большинство противоопухолевых препаратов (цитостатиков), препараты ртути, иммунодепрессанты (угнетающие деятельность иммунной системы).
На тяжесть клинического течения серповидноклеточной анемии влияют:
- Наличие гемоглобина F. Чем его больше, тем менее выражена симптоматика заболевания. Этим объясняется отсутствие симптомов СКА у новорожденных – большая часть HbF замещается на HbA к шестому месяцу жизни ребенка.
- Климатические и географические условия. Давление кислорода во вдыхаемом воздухе обратно пропорционально высоте над уровнем моря. Другими словами, чем выше находится человек, тем меньше кислорода поступает в его легкие при каждом вдохе. Симптомы серповидноклеточной анемии могут проявляться и ухудшаться уже через несколько часов после поднятия на высоту более 2000 метров над уровнем моря (даже у людей с гетерозиготной формой заболевания). Больным СКА абсолютно противопоказано проживание в условиях высокогорья (некоторые города Америки и Европы располагаются на высоте в несколько километров).
- Социально-экономические факторы. Доступность и своевременность лечения осложнений серповидноклеточной анемии также влияет на выраженность клинических проявлений заболевания.
Внешние проявления серповидноклеточной анемии обусловлены, в первую очередь, скоростью разрушения (гемолиза) серповидных эритроцитов (срок жизни которых укорачивается до 10 – 15 дней), а также различными осложнениями, возникающими в результате закупорки серповидными эритроцитами капилляров по всему организму.
Среди симптомов серповидноклеточной анемии выделяют:
- симптомы, связанные с разрушением эритроцитов;
- гемолитические кризы;
- симптомы, обусловленные закупоркой мелких сосудов;
- увеличение селезенки;
- склонность к тяжелым инфекциям.
Данная группа симптомов обычно начинает проявляться через полгода жизни ребенка, когда уменьшается количество гемоглобина F (в тяжелых случаях гомозиготной формы заболевания) либо в более поздние сроки.
Наиболее ранними проявлениями серповидноклеточной анемии являются:
- Бледность. Развивается из-за уменьшения количества красных клеток в крови. Кожа и видимые слизистые оболочки (полости рта, конъюнктивы глаза и другие) становятся бледными и сухими, кожа становится менее эластичной.
- Повышенная утомляемость. Дети с серповидноклеточной анемией характеризуются вялым и малоподвижным образом жизни. При любой физической нагрузке увеличивается потребность организма в кислороде, то есть развивается гипоксия. Это приводит к тому, что большее число эритроцитов приобретают серповидную форму и разрушается. Транспортная функция крови снижается, в результате чего быстро появляется чувство усталости.
- Частые головокружения. Обусловлены недостатком кислорода на уровне головного мозга, что является опасным для жизни состоянием.
- Одышка. Данный термин подразумевает увеличение частоты и глубины дыхательных движений, возникающее в результате ощущения нехватки воздуха. У больных серповидноклеточной анемией этот симптом обычно возникает в периоды физической активности, однако возможно его появление и в покое (при тяжелых формах заболевания, в условиях высокогорья).
- Отставание в росте и развитии. Ввиду того, что транспортная функция крови значительно снижена, ткани и органы не получают достаточного количества кислорода, необходимого для нормального роста и развития организма. Следствием этого является отставание в физическом и умственном развитии — дети позже, чем их сверстники, начинают ходить, говорить, им хуже дается школьная программа. Также отмечается задержка в половом созревании ребенка.
- Желтушность кожи. Пигмент билирубин, выделяющийся в кровоток при разрушении эритроцитов, придает коже и видимым слизистым оболочкам желтоватую окраску. В норме данное вещество довольно быстро нейтрализуется в печени и выводится из организма, однако при серповидноклеточной анемии количество разрушающихся эритроцитов настолько велико, что печень оказывается не в состоянии обезвредить весь образующийся билирубин.
- Темная моча. Цвет мочи изменяется из-за увеличения концентрации билирубина в ней.
- Избыток железа в организме. Данное состояние может развиться в результате тяжелых, часто повторяющихся гемолитических кризов, когда в кровоток выделяется слишком много свободного железа. Это может привести к возникновению гемосидероза – патологического состояния, характеризующегося отложением оксида железа в различных тканях (в ткани печени, селезенки, почек, легких и так далее), что приведет к нарушению функции пораженных органов.
Гемолитические кризы могут возникать в различные периоды жизни. Длительность ремиссии (периода без кризов) может исчисляться месяцами или годами, после чего может наступить целый ряд приступов.
Развитию гемолитического криза может предшествовать:
- тяжелая генерализованная инфекция;
- тяжелая физическая работа;
- подъем на большую высоту (более 2000 метров над уровнем моря);
- воздействие чрезмерно высоких или низких температур;
- обезвоживание (истощение запасов жидкости в организме).
Для гемолитического криза характерно быстрое образование большого числа серповидных эритроцитов, которые закупоривают мелкие сосуды и разрушаются в селезенке, печени, красном костном мозге и других органах, а также непосредственно в сосудистом русле. Это приводит к резкому уменьшению количества красных клеток крови в организме, что проявляется нарастанием одышки, частыми головокружениями (вплоть до потери сознания) и другими симптомами, описанными ранее.
Как уже говорилось, серповидные эритроциты не способны проходить через мелкие сосуды, поэтому застревают в них, что приводит к нарушению кровообращения практически в любых органах.
Симптомами серповидноклеточной анемии являются:
- Болевые кризы. Возникают в результате закупорки сосудов, питающих определенные органы. Это приводит к развитию недостатка кислорода на тканевом уровне, что сопровождается приступами сильной острой боли, которые могут длиться от нескольких часов до нескольких дней. Результатом описанных процессов является гибель участка ткани или органа, доставка кислорода к которому нарушена. Болевые кризы могут возникать внезапно на фоне полного благополучия, однако чаще всего им предшествуют вирусные и бактериальные инфекции, выраженная физическая нагрузка или другие состояния, сопровождающиеся развитием гипоксии.
- Кожные язвы. Развиваются в результате закупорки мелких сосудов и нарушения кровообращения в различных участках кожных покровов. Пораженный участок изъязвляется и довольно часто инфицируется, что может стать причиной развития тяжелых инфекционных заболеваний. Наиболее характерным расположением язв является кожа верхних и нижних конечностей, однако возможно поражение кожи туловища, шеи и головы.
- Нарушения зрения. Развиваются в результате закупорки артерии, питающей сетчатку глаза. В зависимости от диаметра пораженного сосуда могут появляться различные нарушения, начиная от снижения остроты зрения и заканчивая отслойкой сетчатки и развитием слепоты.
- Сердечная недостаточность. Причиной поражения сердца может быть закупорка серповидными эритроцитами коронарных артерий (сосудов, доставляющих кровь к сердечной мышце) и развитие острого инфаркта миокарда (гибели части сердечной мышцы, вызванной нарушением доставки кислорода). Кроме того, длительная анемия и гипоксия рефлекторно вызывают увеличение частоты сердечных сокращений. Это может привести к гипертрофии (увеличению в размерах) сердечной мышцы с последующим истощением компенсаторных механизмов и развитием сердечной недостаточности.
- Гематурия (кровь в моче). Данный симптом может появляться в результате тромбоза почечных вен и поражения нефронов (функциональных единиц почечной ткани, в которых происходит образование мочи), в результате чего они становятся проницаемыми для эритроцитов. При длительном течении заболевания может наступить гибель более 75% нефронов и развитие почечной недостаточности, что является неблагоприятным прогностическим признаком.
- Приапизм. Данный термин подразумевает спонтанное возникновение длительной и болезненной эрекции полового члена у мужчин. Этот симптом обусловлен закупоркой мелких капилляров и вен, через которые происходит отток крови от органа, что иногда может привести к развитию импотенции.
- Изменение структуры костей. Для серповидноклеточной анемии характерны частые инфаркты костной ткани, что приводит к изменению структуры костей, они становятся менее прочными. Кроме того длительная гипоксия стимулирует выделение большого количества эритропоэтина почками, что приводит к разрастанию эритроидного ростка кроветворения в красном костном мозге и деформации костей черепа позвонков, ребер.
- Поражение суставов. Отмечаются припухлость и болезненность суставов конечностей (стоп, голеней, кистей, пальцев тук и ног).
- Неврологические проявления. Являются результатом закупорки артерий, питающих различные участки головного и спинного мозга. Неврологическая симптоматика у больных серповидноклеточной анемией может проявляться нарушениями чувствительности, парезами (нарушением двигательных функции), плегиями (полной утратой двигательных функций в конечностях), а также острым ишемическим инсультом (возникающим в результате закупорки артерии головного мозга), что может привести к смерти человека.
Увеличение селезенки происходит в результате задерживания и разрушения в ней большого числа серповидных эритроцитов. Кроме того, могут развиваться инфаркты селезенки, в результате чего значительно снижаются ее функциональные способности.
На начальных этапах серповидноклеточной анемии в селезенке задерживаются и разрушаются только серповидные эритроциты. По мере прогрессирования заболевания происходит закупорка синусоидов органа, что нарушает прохождение (фильтрацию) всех остальных клеток крови и обуславливает увеличение органа в размерах (спленомегалию).
В результате застоя крови в увеличенной селезенке может развиться состояние, называемое гиперспленизмом. Оно характеризуется разрушением не только поврежденных, но и нормальных клеточных элементов (тромбоцитов, лейкоцитов, неизмененных эритроцитов). Это сопровождается быстрым уменьшением количества данных клеток в периферической крови и развитием соответствующих симптомов (частых кровотечений, нарушения защитных свойств организма). Развитие гиперспленизма особенно опасно в раннем детском возрасте, когда в увеличенной селезенке может произойти быстрое разрушение большинства эритроцитов крови, что приведет к смерти ребенка.

В диагностике серповидноклеточной анемии применяется:
- общий анализ крови;
- биохимический анализ крови;
- электрофорез гемоглобина;
- ультразвуковое исследование (УЗИ);
- рентгенологическое исследование.
Один из первых анализов, назначаемых всем пациентам при подозрении на заболевание крови. Он позволяет оценить клеточный состав периферической крови, что дает информацию о функциональном состоянии различных внутренних органов, а также о кроветворении в красном костном мозге, наличии инфекции в организме. Для общего анализа могут брать как капиллярную кровь (из пальца), так и венозную.
Техника взятия капиллярной крови
Кровь берут утром, натощак. Накануне перед сдачей анализа не рекомендуется употреблять алкогольные напитки, курить или принимать наркотические препараты. Непосредственно перед взятием крови следует согреть пальцы левой руки, что улучшит микроциркуляцию и облегчит процедуру.
Забор материала для анализа производится медицинской сестрой в процедурном кабинете поликлиники. Кожу кончика пальца обрабатывают ватным тампоном, который предварительно смачивают 70% раствором спирта (с целью предотвращения занесения инфекции). После этого специальной иглой-скарификатором производят прокол кожи на боковой поверхности пальца (обычно используется 4 палец левой руки, однако это не принципиально). Первая появившаяся капля крови удаляется ватным тампоном, после чего медсестра начинает поочередно сдавливать и отпускать кончик пальца, набирая в стерильную градуированную трубку несколько миллилитров крови.
При подозрении на серповидноклеточную анемию палец, из которого будет браться кровь, предварительно перевязывают веревкой или жгутом (на 2 – 3 минуты). Это создает условия гипоксии, в результате чего образуется большее число серповидных эритроцитов, что облегчит постановку диагноза.
Техника взятия венозной крови
Забор крови также производится медицинской сестрой. Правила подготовки к анализу такие же, как при взятии крови из пальца. Обычно кровь берут из подкожных вен локтевой области, расположение которых довольно легко определить.
Пациент присаживается и кладет руку на спинку стула, максимально разгибая ее в локтевом суставе. Медсестра накладывает резиновый жгут в плечевой области (сдавливание подкожных вен приводит к переполнению их кровью и выбуханию над поверхностью кожи) и просит пациента несколько секунд «поработать кулаком» (сжимать и разжимать кулак), что также способствует наполнению вен кровью и облегчает их определение под кожей.
Определив расположение вены, медсестра дважды обрабатывает локтевую область ватным тампоном, предварительно пропитанным 70% спиртовым раствором. После этого стерильным одноразовым шприцем прокалывается кожа и стенка вены и производится забор необходимого количества крови (обычно нескольких миллилитров). К месту прокола прижимается чистый ватный тампон (также смоченный в спирте), и игла извлекается. Пациенту рекомендуют подождать в коридоре 10 – 15 минут, так как возможно возникновение определенных побочных реакций (головокружения, потери сознания).
Микроскопическое исследование крови
Несколько капель полученной крови переносится на предметное стекло, окрашивается специальными красителями (обычно метиленовым синим) и исследуется в световом микроскопе. Данный метод позволяет примерно определить количество клеточных элементов крови, оценить их размеры и строение.
При серповидноклеточной анемии возможно выявление серповидных эритроцитов (при исследовании венозной крови), однако их отсутствие не исключает диагноза. Обычное микроскопическое исследование не всегда позволяет выявить серповидные эритроциты, поэтому применяется исследование «влажного мазка» крови. Суть исследования заключается в следующем — каплю крови переносят на предметное стекло и обрабатывают особым веществом – пиросульфитом натрия. Он «вытягивает» кислород из эритроцитов, в результате чего они приобретают серповидную форму (если человек действительно болен серповидноклеточной анемией), что обнаруживается при исследовании в обычном световом микроскопе. Данное исследование является высокоспецифичным и позволяет подтвердить диагноз в большинстве случаев.
Исследование крови в гематологическом анализаторе
Большинство современных лабораторий оборудованы гематологическими анализаторами – аппаратами, позволяющими быстро и точно определить количественный состав всех клеточных элементов, а также многие другие параметры крови.
| Исследуемый показатель | Что обозначает? | Норма | Возможные изменения при серповидноклеточной анемии |
| Концентрация эритроцитов (RBC) | При серповидноклеточной анемии отмечается выраженное разрушение эритроцитов (гемолиз), в результате чего их концентрация в крови будет снижена. Данное состояние особенно характерно для гемолитических кризов, когда может разрушаться более половины циркулирующих в крови эритроцитов. | Мужчины (М): 4,0 – 5,0 х 10 12 /л. | Менее 4,0 х 10 12 /л. |
| Женщины (Ж): 3,5 – 4,7 х 10 12 /л. | Менее 3,5 х 10 12 /л. | ||
| Общий уровень гемоглобина (HGB) | В результате разрушения эритроцитов снижается и общий уровень гемоглобина в крови. | М: 130 – 170 г/л. | Менее 130 г/л. |
| Ж: 120 – 150 г/л. | Менее 120 г/л. | ||
| Концентрация лейкоцитов (WBC) | Лейкоциты защищают организм от различных инфекционных агентов. При серповидноклеточной анемии отмечается предрасположенность к инфекционным заболеваниям, ввиду чего данный показатель может повышаться. | 4,0 – 9,0 х 10 9 /л. | Повышение уровня лейкоцитов выше 9,0 х 10 9 /л говорит о наличии инфекционного процесса в организме. |
| Концентрация тромбоцитов (PLT) | В случае развития гиперспленизма в увеличенной селезенке разрушаются не только серповидные эритроциты, но и нормальные клетки крови. | 180 – 320 х 10 9 /л. | В норме или снижена. |
| Концентрация ретикулоцитов (RET) | Уменьшение концентрации эритроцитов стимулирует выделение эритропоэтина почками, что усиливает процессы кроветворения в красном костном мозге. Результатом этого является выделение в периферический кровоток большого количества ретикулоцитов. | М: 0,24 – 1,7%. | Повышена, особенно после гемолитических кризов. |
| Ж: 0,12 – 2,05%. | |||
| Гематокрит (Hct) | Гематокрит – лабораторный показатель, отражающий количественное соотношение между клеточными элементами крови и объемом плазмы. Выраженный гемолиз приводит к уменьшению общего количества эритроцитов и, следовательно, к уменьшению гематокрита. | М: 42 – 50%. | Ниже нормы, вплоть до 15 – 20% в периоды гемолитических кризов. |
| Ж: 38 – 47%. | |||
| Скорость оседания эритроцитов (СОЭ) | Определяется время, в течение которого произойдет оседание эритроцитов на дно пробирки. В нормальных условиях наружная поверхность мембран эритроцитов несет отрицательный заряд, в результате чего клетки отталкиваются друг от друга. Уменьшение концентрации эритроцитов, а также различные инфекционные процессы в организме способствуют более быстрому оседанию эритроцитов. | М: 3 – 10 мм/час. | Более 10 мм/час. |
| Ж: 5 – 15 мм/час. | Более 15 мм/час. |
| Исследуемый показатель | Что обозначает? | Норма | Возможные изменения при серповидноклеточной анемии |
| Уровень билирубина (несвязанная фракция) | Данный показатель отображает интенсивность процессов разрушения эритроцитов как в селезенке, так и непосредственно в сосудистом русле. | 4,5 – 17,1 мкмоль/л. | Значительно выше нормы. |
| Свободный гемоглобин плазмы | Данный показатель отображает интенсивность процесса разрушения эритроцитов непосредственно внутри сосудов (внутрисосудистого гемолиза), при котором в кровь выделяется большое количество свободного гемоглобина. | Менее 220 мг/л. | Значительно выше нормы, особенно в период гемолитического криза. |
| Уровень гаптоглобина в плазме | Гаптоглобин – это белок плазмы крови, образующийся в печени. Одной из основных его функций является связывание свободного гемоглобина в крови и транспортировка его в селезенку, где он подвергается разрушению. При гемолизе эритроцитов в сосудистом русле количество выделяемого в кровь гемоглобина настолько велико, что весь гаптоглобин находится в связанном с ним состоянии, поэтому его количество уменьшается. | 0,8 – 2,7 г/л. | Значительно ниже нормы, особенно в период гемолитических кризов. |
| Концентрация свободного железа в крови | Повышение количества свободного железа в плазме крови обычно характерно для гемолитического криза. Белок трансферрин не успевает связать все железо, поступающее в кровь в результате разрушения большого количества эритроцитов, поэтому его концентрация повышается. | М: 17,9 – 22,5 мкмоль/л. | В период гемолитического криза данный показатель может быть в несколько раз выше нормы. |
| Ж: 14,3 – 17,9 мкмоль/л. | |||
| Уровень аланинаминотрансферазы (АлАТ) и аспартатаминотрансферазы (АсАТ) | Данные вещества являются внутриклеточными ферментами, содержащимися в клетках печени в больших количествах. Увеличение их концентрации в крови является маркером разрушения ткани печени, что может быть следствием микроинфарктов (в результате закупорки печеночных сосудов серповидными эритроцитами). | М: до 41 Ед/л. | При тяжелом течении заболевания значительно превышает норму. |
| Ж: до 31 Ед/л. |
Широко распространенный научный метод исследования, позволяющий определить качественный состав гемоглобина в крови. Суть метода заключается в следующем — на бумагу, расположенную в стационарном электрическом поле между двумя электродами, помещают раствор, содержащий различные белки, которые начинают перемещаться от катода (отрицательно заряженного электрода) к аноду (положительно заряженному электроду).
Скорость перемещения белковых молекул зависит от их молекулярной массы, пространственной конфигурации и электрического заряда. Данные параметры строго специфичны для каждой отдельной цепи глобина (как нормальной, так и патологической), в результате чего их электрофоретическая подвижность будет различной. На основании контрольных маркеров определяют виды гемоглобина в исследуемой крови и количество каждого из них.
| Вид гемоглобина | Нормальные значения | Возможные изменения при серповидноклеточной анемии |
| HbA | Более 95%. | Менее 50%. |
| HbA2 | Менее 2%. | В норме или снижено. |
| HbF | 1 – 1,5 %. | В норме или слегка повышено. |
| HbS | Отсутствует. | 50% и более. |
Современный метод исследования внутренних органов, основанный на принципе эхолокации, позволяющий определить расположение и структуру объекта по скорости возвращения звуковой волны, отраженной от его поверхности.
УЗИ является одним из наиболее простых и безвредных диагностических методов. За несколько часов перед исследованием пациенту необходимо исключить прием пищи и больших объемов жидкости. Сама процедура может проводиться как в специально оборудованном кабинете, так и непосредственно у постели больного. На кожу исследуемой области наносится специальный гель (это предотвращает попадание воздуха между датчиком и кожей пациента, что могло бы исказить результаты исследования). После этого врач прикладывает к коже пациента специальный датчик, излучающий ультразвуковые волны, и начинает перемещать его над исследуемой областью. Звуковые волны отражаются от поверхностей различных органов и структур, находящихся на их пути, и улавливаются специальным приемником. После компьютерной обработки на мониторе появляется примерное изображение исследуемых тканей и органов.
Разновидностью ультразвукового исследования является допплерография – метод, позволяющий оценить характер кровотока в сосудах.
При серповидноклеточной анемии метод УЗИ может выявить:
- увеличение селезенки и печени;
- наличие инфарктов во внутренних органах (в селезенке, печени, почках и других);
- нарушение кровообращения во внутренних органах;
- нарушение кровотока в конечностях.
Это исследование основано на способности рентгеновских лучей проходить через организм человека. При этом они частично поглощаются различными тканевыми структурами, в результате чего на специальной пленке формируется теневое отображение всех органов и тканей, оказавшихся на их пути.
Наибольшей поглощающей способностью в организме человека обладает костная ткань, что позволяет использовать данный метод для определения наличия и выраженности поражений костей при серповидноклеточной анемии.
Рентгенологическое исследование позволяет выявить:
- деформацию и расширение тел позвонков (из-за множественных инфарктов);
- деформацию и истончение костей скелета (из-за избыточного разрастания костномозговой ткани);
- наличие остеомиелита (гнойного инфекционного процесса в костной ткани).
Эффективного лечения серповидноклеточной анемии, позволяющего раз и навсегда избавиться от данного недуга, на сегодняшний день не существует. Помощь больным заключаются в предотвращении образования большого количества серповидных эритроцитов, а также в устранении симптомов заболевания.
Принципами лечения серповидноклеточной анемии являются:
- правильный образ жизни;
- повышение количества эритроцитов и гемоглобина;
- кислородотерапия;
- устранение болевого синдрома;
- устранение избытка железа в организме;
- профилактика и лечение инфекционных заболеваний.
Если у человека диагностирована серповидноклеточная анемия, ему следует соблюдать определенные рекомендации, которые позволят облегчить течение заболевания и минимизировать риск развития осложнений.
Пациентам с серповидноклеточной анемией рекомендуется:
- проживать на высоте не более 1500 метров над уровнем моря;
- проживать в зоне с умеренным климатом (исключающим воздействие экстремально низких или высоких температур);
- употреблять не менее 1,5 литров жидкости ежедневно;
- исключить прием алкогольных напитков и наркотиков;
- отказаться от курения (как самому больному человеку, так и членам его семьи);
- избегать тяжелых физических нагрузок;
- выбирать профессию, не связанную с тяжелой физической работой или воздействием высоких/низких температур.
| Название препарата | Механизм леченого действия | Способ применения и дозы | Оценка эффективности лечения | |
| Немедикаментозные методы | ||||
| Эритроцитарная масса | Перелитые донорские эритроциты в течение некоторого времени (обычно не более 100 дней) могут транспортировать дыхательные газы в организме больного. Данный метод используется крайне редко, ввиду возможности развития тяжелых побочных реакций. | Основным показанием для переливания донорских эритроцитов является резкое снижение уровня гемоглобина ниже 70 г/л (например, при гемолитическом кризе). В таком случае устанавливается катетер в одну или сразу в несколько центральных вен (в яремные, расположенные на шее или в подключичные), и производится переливание эритроцитарной массы. Целевой уровень гемоглобина при этом составляет не менее 100 г/л. | ||
Перед началом переливания проводится целый ряд тестов, направленных на определение совместимости крови донора и реципиента.
- повышение уровня гемоглобина (определенное лабораторно);
- исчезновение одышки;
- нормализация цвета кожи.
Применение гидроксимочевины в лечении серповидноклеточной анемии считается экспериментальной методикой. Широкомасштабных исследований, оценивающих эффективность препарата и возможные побочные реакции, еще не проводилось.
Частота и выраженность гемолитических кризов определяет тяжесть клинического течения серповидноклеточной анемии. Как уже говорилось, развитию гемолитического криза предшествуют различные состояния, сопровождающиеся гипоксией. Применение кислорода в первые минуты или часы после начала гемолиза предотвращает образование и последующее разрушение серповидных эритроцитов. Это облегчает течение заболевания, уменьшает риск развития осложнений и улучшает качество жизни пациента.
Пациент с развивающимся гемолитическим кризом должен быть госпитализирован как можно скорее. Непосредственно в машине скорой помощи ему дается кислородная маска, которая обеспечивает подачу кислорода со скоростью 4 – 6 литров в минуту. После поступления в стационар кислородотерапия продолжается на протяжении нескольких часов или дней.
| Название медикамента | Механизм лечебного действия | Способ применения и дозы | Оценка эффективности лечения |
| Трамадол | Синтетическое наркотическое обезболивающее средство, действующее на уровне головного и спинного мозга. Активирует опиоидные рецепторы в организме, что уменьшает интенсивность болевого синдрома. | Внутривенно или внутрь, в дозе 50 – 100 мг. Максимальная суточная доза – 400 мг. Не рекомендуется принимать детям младше 1 года. | Обезболивающий эффект развивается примерно через 15 минут после приема внутрь (при внутривенном введении – через 5 – 10 минут) и длится до 6 часов. |
| Промедол | Активирует опиоидные рецепторы и нарушает передачу болевых импульсов в центральной нервной системе, чем и обусловлено его обезболивающее, противошоковое и легкое снотворное действие. | Внутрь, 3 – 4 раза в день. |
Рекомендуемые дозы:
- детям старше 2 лет – 0,1 – 0,5 мг/кг;
- взрослым – 25 – 50 мг.
Рекомендуемые дозы:
- детям – 0,2 – 0,8 мг/кг;
- взрослым – 10 – 20 мг.
| Название медикамента | Механизм лечебного действия | Способ применения и дозы | Оценка эффективности лечения |
| Десферал (Дефероксамин) | Комплексообразующий препарат, который обладает способностью связывать и выводить свободное железо из организма. | Данный медикамент назначается после гемолитических кризов, при повышении уровня сывороточного железа. Вводится внутривенно. Начальная доза составляет 20 мг/кг. При повторном возникновении кризов доза может быть увеличена до 40 мг/кг. | Лечение проводится до нормализации уровня железа в крови, подтвержденной лабораторно. |
| Эксиджад | Препарат для приема внутрь, обладающий железосвязывающей способностью. Усиливает выведение железа из организма преимущественно с калом. | Внутрь, 1 раз в день, в дозе 10 – 30 мг/кг. | Лечение проводится до нормализации уровня железа в крови. |
| Название медикамента | Механизм лечебного действия | Способ применения и дозы |
| Амоксициллин | Полусинтетический антибиотик, подавляющий образование клеточной стенки различных видов бактерий (стафилококков, стрептококков, пневмококков и других), что приводит к их гибели. | Может назначаться с профилактической целью, начиная с шестимесячного возраста (при тяжелом течении гомозиготной формы серповидноклеточной анемии). Принимается внутрь, 2 – 3 раза в сутки. |
Рекомендуемые дозы:
- детям младше 2 лет – 20 мг/кг;
- детям от 2 до 5 лет – 125 мг;
- детям от 5 до 10 лет – 250 мг;
- детям старше 10 лет и взрослым – 500 мг.
Рекомендуемые дозы:
- детям – 10 – 30 мг/кг, 3 раза в сутки;
- взрослым – 750 мг 3 раза в сутки.
Рекомендуемые дозы:
- детям – 10 – 15 мг/кг, 2 – 3 раза в сутки;
- взрослым – 250 – 500 мг 3 – 4 раза в сутки.
Если один или оба родителя больны серповидноклеточной анемией, то их ребенок также может унаследовать данный недуг. Одним из методов, позволяющим определить вероятность наследования гена, ответственного за развитие данного заболевания, является полимеразная цепная реакция (ПЦР). Суть метода заключается в исследовании генетического материала обоих родителей и выявлении мутантных генов. При этом определяется как их наличие (или отсутствие), так и форма заболевания (гомозиготная или гетерозиготная).
Результаты генетического исследования могут быть следующими:
- Оба родителя больны. Это подразумевает, что у обоих родителей имеется по 2 мутантных гена, кодирующих образование b-цепей глобина. Рождение здорового ребенка в таком случае практически невозможно.
- Оба родителя являются бессимптомными носителями. В данном случае вероятность рождения здорового ребенка составляет 25%, вероятность рождения больного ребенка (с гомозиготной формой заболевания) – 25%, и вероятность рождения бессимптомного носителя (с гетерозиготной формой заболевания) – 50%.
- Один из родителей болен, а второй является бессимптомным носителем. У таких родителей с одинаковой долей вероятности может родиться либо больной ребенок, либо бессимптомный носитель. Рождение абсолютно здорового ребенка в данном случае невозможно.
- Один из родителей болен, а второй здоров. В данном случае ребенок унаследует один мутантный ген от больного родителя и один нормальный ген от здорового родителя, то есть он будет бессимптомным носителем гена серповидноклеточной анемии.
С помощью ПЦР возможно выявить наличие мутантных генов у плода на ранних этапах внутриутробного развития и определить форму заболевания. Это позволяет своевременно поднять вопрос о прерывании беременности.
источник