Врожденная гемолитическая анемия — хроническое заболевание, обусловленное особенностями организма, передаваемыми по наследству. Она характеризуется желтухой на почве повышенного гемолиза, увеличением селезенки, понижением осмотической стойкости эритроцитов, микроцитозом, приближением формы эритроцитов к шаровидной и часто анемией. Основным ее симптомом является усиленный обмен крови.
История изучения. В 1900 г. Минковский сообщил о 8 случаях заболевания, наблюдавшегося им в трех поколениях одной и той же семьи, характеризовавшегося «наследственной хронической желтухой, протекавшей с уробилинурией, спленомегалией и почечным сидерозом».
В 1907 г. Шоффар установил, что при гемолитической желтухе имеется пониженная осмотическая стойкость эритроцитов. Негели доказал, что при семейной гемолитической желтухе форма эритроцитов приближается к сферической (сфероцитоз).
В 1908 г. Видаль описал случай приобретенной гемолитической желтухи.
Этиология и патогенез. Заболевание может носить семейный характер. Уже первые описанные случаи касаются людей с конституциональными недостатками. По данным Генслена, у таких больных встречается «башенный» череп, седловидный нос, увеличение числа пальцев (полидактилия), инфантилизм и пр.
Интересны отдельные наблюдения. Мать страдала гемолитической желтухой. У нее была удалена селезенка по поводу этой болезни с хорошим результатом. Через 9 лет она родила ребенка, болеющего этой же болезнью в тяжелой форме.
Описываются случаи приобретенной гемолитической желтухи, по общей клинической картине сходные с врожденной желтухой. Но между той и другой формой заболевания имеются и существенные различия.
Патогенез гемолитической болезни, основным симптомом которой является усиленная и ускоренная гибель эритроцитов, ускоренный обмен крови, возбуждал много споров. Имеются основные факты: микроцитоз и сфероцитоз (малая величина и своеобразная форма красных кровяных телец), осмотическая стойкость которых постоянно и значительно понижена. Кроме того, всегда увеличена селезенка, пульпа селезенки переполнена кровью.
Указывают, что сферическая форма эритроцитов при этом заболевании вызывает уменьшение их поверхности по отношению к объему клетки (по сравнению с нормальным эритроцитом). Благодаря этому предел возможности набухания эритроцитов (в данном случае в гипотонических растворах) ограничен, они скорее разрушаются. Сфероциты обладают «повышенной ломкостью при механической травме».
Увеличение селезенки, набухание и болезненность ее во время обострения заболевания (кризы гемолитической болезни) направили мысль исследователей в сторону признания ведущей роли селезенки как основной причины усиленного гемолиза («гиперспленизм»). В связи с этим была предложена операция спленэктомии. Результаты ее были блестящи. Но позже у некоторых оперированных больных возобновлялись симптомы повышенного гемолиза, видимо, в связи с тем, что другие части ретикуло-эндотелиальной системы стали усиленно функционировать.
После спленэктомии характерные признаки со стороны эритроцитов (микроцитоз, сфероцитоз, ретикулоцитоз) остаются. Можно говорить «о клиническом выздоровлении, а не о полном излечении».
Интересно указание, что спленэктомия дает это клиническое выздоровление при наследственной гемолитической желтухе и реже — при приобретенной.
Эппингер считал, что при этом заболевании имеется нарушение функционального состояния ретикуло-эндотелиальной системы.
Д. Н. Яновскому кажется наиболее вероятным, что развитие синдрома хронической гемолитической желтухи находится в тесной зависимости от повышения функциональной способности и раздраженности ретикуло-эндотелиальной системы. Д. Н. Яновский и Дамешек говорят об участии аутогемолизинов в разрушении эритроцитов.
Вопрос о том, где причина усиленного гемолиза при гемолитической болезни: в эритроцитах — сфероцитах или в селезенке, следует считать решенным, в частности, опытами Дейси, Моллисона. Эритроциты здорового донора, перелитые страдающему гемолитической болезнью, живут нормальный срок. Наоборот, эритроциты такого больного (сфероциты), перелитые здоровому человеку, быстро разрушаются. Значит ускоренный гемолиз у данных больных зависит не от усиленной функции селезенки («гиперспленизм»), а от структурной и функциональной неполноценности сфероцитов.
По Дейси, эритроцит больного гемолитической болезнью имеет короткую жизнь — 8-15 дней. Спленэктомия не влияет на этот симптом.
Шрумпф получил иные данные. Он переливал кровь страдающего «наследственным сфероцитозом» людям с удаленной селезенкой как с нормальной характеристикой эритроцитов, так и больным, подвергшимся спленэктомии по поводу гемолитической болезни. В том и другом случае сфероциты жили нормальный промежуток времени (около 100 дней).
Последние данные позволяют считать установленным, что роль селезенки сводится лишь к секвестрации и разрушению эритроцитов с пониженной осмотической и механической стойкостью.
Гемолиз при гемолитической желтухе происходит не внутри сосудов, как полагали Шоффар, Мейленграхт, а внесосудисто в клетках ретикулоэндотелия селезенки и печени.
Усиленный распад эритроцитов, несмотря на повышенную работу костного мозга, вызывает то более, то менее выраженную анемию.
Патологическая анатомия. На секции находят активный красный костный мозг в состоянии резкой гиперплазии, территория его увеличена. Костный мозг длинных костей — бедренной, костей голени — становится красным. Среди клеток костномозговой ткани резко преобладают эритробласты. В случае Вейнера и Кацнельсона среди ядерных клеток костного мозга эритробласты составляли 63,8% (вместо 20% в нормальном костном мозгу). Кроме того, имелось 10% свободных ядер эритробластов.
Селезенка велика, мягка, переполнена кровью. Вес ее от 500 до 12 000 г. Количество соединительной ткани в ней не увеличено.
Сращений с соседними органами, в частности с диафрагмой (явлений периспленита), нет. Имеется гиперплазия всего органа. Увеличено количество специфических элементов селезенки: эндотелиальных клеток синусов, клеток пульпы. Пульпа наводнена кровью, синусы, наоборот, сдавлены, пусты. Имеются наблюдения, что при этом заболевании химическим путем обнаруживается увеличенное количество железа в тканях.
Печень не представляет специфических изменений. При гистологическом ее исследовании многие авторы отмечают увеличение числа клеток Купфера, увеличение размеров отдельных клеток, наличие в них фагоцитированных эритроцитов. При химическом исследовании печеночной ткани Эппингер нашел увеличенное количество железа. Кроме того, Мейленграхт не обнаружил изменений как в печеночных клетках, так и в клетках Купфера.
Желчный пузырь полон темной, богатой пигментом желчи. Очень часто в нем имеются пигментные камни.
Симптомы. Течение гемолитической желтухи волнообразно. Ее симптомы то ослабевают, то резко усиливаются. Иногда ухудшения бывают связаны с той или иной инфекцией. Первые проявления гемолитической желтухи также могут быть связаны с интеркуррентным заболеванием. Особое влияние могут иметь инфекции, связанные с раздражением ретикуло-эндотелиального аппарата и протекающие с увеличением селезенки, например малярия. Заболевание может проявиться и в раннем детстве.
В периоды обострения больные умеренно лихорадят. Появляется желтушность. Однако она мало беспокоит больного. По выражению Шоффара, они «более желтушны, чем больны». Желчь густа, насыщена пигментами. Испражнения интенсивно окрашены. Моча темна, богата уробилином. В испражнениях количество стеркобилина превышает норму иногда в 25 раз (3000 мг в сутки вместо нормальных 60-120 мг по Тервену). Сыворотка крови насыщенно желта, дает непрямую реакцию ван ден Берга, количество билирубина в ней увеличено: 2-3 мг%, иногда до 6 мг% и больше.
Кожного зуда, как правило, не бывает. Наступающий в редких случаях после криза зуд объясняется осложнением гемолитической желтухи обтурационной желтухой на почве присоединившейся желчнокаменной болезни.
В периоды усиления гемолиза, а вместе с тем и желтухи печень увеличивается и становится чувствительной, но остается мягкой. Одновременно иногда наблюдаются приступы болей, сходные с желчной коликой, зависящие от усиленного поступления в желчные ходы и желчный пузырь богатой пигментом и поэтому очень густой желчи. Возможны и приступы истинной желчнокаменной болезни на почве образования пигментных камней. Шоффар находил в этих камнях до 52% билирубина. В клинике Мэйо в 68% случаев гемолитической желтухи отмечены симптомы, характерные для желчнокаменной болезни.
Нередки показания к холецистэктомии. Встречаются случаи, при которых удаление желчного пузыря было произведено до постановки диагноза гемолитической желтухи. Часто наблюдаются сращения желчного пузыря с окружающими органами.
Селезенка в большинстве случаев увеличена и прощупывается, выступая на несколько пальцев из-под края ребер. На ощупь она плотна, часто чувствительна. Она может доходить до подвздошной кости, заходить за среднюю линию. В отдельных случаях она не пальпируется. Необходимо пользоваться не только ощупыванием, но и перкуссией. Чем более увеличена селезенка, тем тяжелее протекает заболевание. Во время обострений гемолитического процесса она заметно увеличивается, становится более чувствительной.
Увеличение селезенки объясняется тем, что в разрушении эритроцитов, происходящем в ретикуло-эндотелиальной системе, особенно большое участие принимает именно селезенка.
Лимфатические узлы не увеличены.
Плоские кости (грудина) обычно болезненны при давлении и постукивании.
Чрезвычайно интересны изменения скелета у больных гемолитической болезнью. Они особенно подробно и систематически изучены Генсленом. Наиболее часто встречается при этом заболевании так называемый «башенный» череп, седлообразный нос, широко расставленные глаза. Нередко имеется высокое небо. Часто отмечают неправильный рост зубов. Генслен обращал внимание на своеобразное строение костей черепной коробки и свода черепа, на расширение пространств между костными перекладинами. Он связывал это с резко выраженной гиперплазией костного мозга, повышенной его активностью в отношении эритропоэза.
Примерно в половине случаев наблюдаются подобные изменения черепа. Они бывают выражены, если заболевание проявилось в детском возрасте. Кости фаланг пальцев рук иногда короткие — брадидактилия.
Нередки стойкие, плохо поддающиеся лечению язвы голени. Патогенез их появления не выяснен. После операции удаления селезенки эти язвы исчезают. Они не связаны с узловатыми расширениями вен.
Со стороны других органов имеются только явления, наблюдающиеся при всяком малокровии.
Желудочная секреция не понижена. Иногда отмечается повышенная кислотность.
В случаях, когда заболевание проявилось в детстве, отмечается отставание в развитии. Может отставать рост, больные инфантильны. У девушек запаздывает появление менструаций. Они могут, начавшись, протекать неправильно.
Со стороны крови имеется уменьшение количества эритроцитов и гемоглобина. Число эритроцитов может упасть до 2-1 млн. в 1 мм3, количество гемоглобина — до 30-15%. Такие низкие цифры гемоглобина и эритроцитов наблюдаются во время так называемых гемолитических кризов.
Цветной показатель Очень близок к единице. Вскоре после криза число эритроцитов нарастает быстрее количества гемоглобина и соответственно этому цветной показатель становится низким. При явлениях истощения костного мозга цветной показатель ниже единицы, обычно же вне криза он несколько выше единицы (гиперхромная анемия). Следует подчеркнуть, что малокровие, по крайней мере в известные периоды болезни, не является обязательным для конституциональной гемолитической анемии. Костный мозг при достаточной активности может покрывать расход эритроцитов, вызываемый усиленным гемолизом. Наблюдаются случаи с длительным нормальным количеством эритроцитов и гемоглобина. Описываются даже случаи с полицитемическим составом крови — 6 млн. и больше эритроцитов в 1 мм3. Эти наблюдения вполне оправдывают предложенное Дебрэ название заболевания — morbus haemolyticus — гемолитическая болезнь.
Это название подчеркивает существо болезни, а не тот или иной симптом (анемия, желтуха).
Хорошая сравнительно регенерация эритроцитов в костном мозгу объясняется, по всей вероятности, тем, что при разрушении эритроцитов в организме эритробластическая ткань широко использует продукты распада эритроцитов, специально гемоглобина, для выработки нового гемоглобина и новых эритроцитов.
Характерна микроскопическая картина мазка крови. Бросается в глаза малый размер эритроцитов.
При гемолитической болезни диаметр эритроцитов уменьшается. Особый характер им придает отсутствие центрального побледнения, характерного для нормального эритроцита. Несмотря на малые линейные размеры, объем каждого эритроцита увеличен. Встречаются в периферической крови эритробласты. Количество эритроцитов с суправитальной зернистостью чрезвычайно велико и вместо 0,3-0,8% в нормальной крови достигает громадной величины — 20-30- 50% и даже 90%. Ни при каком другом заболевании не наблюдается такого ретикулоцитоза. Как и остальные признаки заболевания, ретикулоцитоз волнообразно меняется в своей интенсивности.
Стойкость эритроцитов по отношению к гипотоническим растворам хлористого натрия понижена. Вместо нормальной минимальной стойкости 0,42-0,46 она достигает 0,60-0,70, т. е. уже в 0,7% растворе NaCl часть эритроцитов теряет свой гемоглобин. Понижена также и максимальная резистентность; она достигает 0,40-0,44 вместо нормальных 0,30-0,32, т. е. уже в 0,4% растворе все эритроциты подвергаются гемолизу.
Число лейкоцитов нормально или несколько увеличено главным образом за счет нейтрофилов. Много моноцитов, до 10% и выше. В увеличении их числа нельзя не видеть выражения усиленной деятельности ретикулоэндотелия.
Число кровяных пластинок нормально или несколько увеличено. Следует отметить, что среди них преобладают молодые формы.
Территория активного костного мозга увеличена. При пункции грудины он легко насасывается, имеет темно-красный цвет.
Пункция костного мозга показывает наличие усиленного эритропоэза с большим количеством эритробластов разного возраста. Много эритробластов с базофильной протоплазмой, многие в состоянии кариокинеза. Часто число эритробластов больше числа клеток — родоначальниц лейкоцитов.
Количество полихроматофильных и оксифильных эритробластов значительно увеличено. Из 15 больных, наблюдавшихся М. И. Аринкиным, у 10 оно достигало 30-45% (вместо 12-14% нормы) и только у 3 процент соответствовал нормальным цифрам. Повышен процент проэритробластов. По данным М. И. Аринкина, он был увеличен у 14 больных из 15 (достигая 15% вместо 1,2%). Таким образом, количество эритробластов увеличено и имеется значительный «сдвиг влево», значительное преобладание числа более молодых клеток. Увеличено количество митозов.
Важно наблюдение М. И. Аринкина, что процент ретикулоцитов в пунктате бывает меньше, чем в периферической крови. Это подтверждено и другими исследователями. Указывается, что подобное явление встречается только при этом заболевании.
Во всяком случае количество ретикулоцитов и в костном мозгу чрезвычайно велико, достигая 25-40%. Среди них имеются как молодые клетки — ретикулоциты, так и более старые с одним-двумя зернышками в протоплазме эритроцита.
Несколько увеличено в костном мозгу количество ретикуло-эндотелиальных клеток. Наблюдается эритрофагоцитоз клетками ретикулоэндотелия и мегакариоцитами. Встречается зеленый пигмент, фагоцитированный и свободный (дериват гемоглобина).
Моча, как правило, содержит большое число уратов. Часто в осадке имеются кристаллы мочевой кислоты. Благодаря этому моча часто имеет характерный желтовато-бурый цвет. После спленэктомии выделение уратов значительно сокращается. Большое количество мочевой кислоты в моче связывают с усиленным разрушением клеток крови.
Отдельные клинические формы. Заболевание может протекать скрыто, почти бессимптомно.
Генслен в 10% наблюдавшихся им случаев гемолитической болезни отметил отсутствие пониженной стойкости эритроцитов, в 35% — отсутствие анемии, в 30% — отсутствие спленомегалии. В 40% не было выраженной желтухи.
В обычной клинической практике чаще наблюдаются случаи со всеми характерными чертами. Наряду с этим описываются случаи, когда имеется налицо или по крайней мере резко, выделяется то тот, то другой симптом («моносимптомные» случаи). Иногда преобладают явления малокровия без резкой и постоянной желтухи (вследствие недостаточной регенераторной способности эритробластической ткани), в других случаях преобладает увеличение селезенки без выраженной желтухи и малокровия (здесь можно предположить усиленный гемолиз в прошлом и спленомегалию вследствие реактивной гиперплазии ткани селезенки). Наконец, наблюдаются случаи с преобладанием желтухи (в результате недостаточности в данном случае выделительной способности печеночного эпителия в отношении билирубина).
Подробное обследование членов семей лиц, страдающих гемолитической болезнью, давало возможность установить, что у отдельных членов этих семей имеются только характерные изменения эритроцитов (микросфероцитоз без других объективных и субъективных признаков заболевания).
Течение. Течение болезни продолжительно. Болезнь хроническая, в принципе неизлечимая. Наступает то ухудшение общего состояния, то более или менее продолжительные ремиссии (несколько месяцев и даже лет).
Гемолитическая болезнь протекает волнообразно. Без лечения она может привести к истощению костного мозга с его аплазией (вторичная апластическая анемия). Интересно наблюдение, что тяжесть течения болезни в данной семье нарастает из поколения в поколение.
Нередко развивается уплотнение печени, ее увеличение и присоединяются признаки нарушения ее функции (усиленная уробилинурия), возникает хронический гепатит, иногда цирроз печени.
Волнообразность течения гемолитической болезни проявляется и в так называемых кризах. Они состоят в резком, остром усилении всех основных признаков гемолитической болезни: остро нарастает желтуха, резко увеличивается селезенка. Это может сопровождаться появлением боли в левом подреберье. Увеличивается ретикулоцитоз, еще более резко возрастает количество эритробластов в костном мозгу.
Различные влияния, например душевные переживания, могут вызвать подобные обострения.
Кризы обычно связывают и с заболеванием той или иной острой инфекционной формой. Так, описывают случай, когда у трех членов одной и той же семьи возник криз при одновременном заболевании их гриппом.
В. В. Свирчевская наблюдала усиление гемолитического процесса во время беременности (у одной больной) и через некоторое время после родов (у 2 больных). Некоторые из ее больных указывали на усиление желтухи в предменструальном периоде.
Если, с одной стороны, периоды обострения болезни могут быть вызваны различными ослабляющими моментами, то, с другой — больные гемолитической болезнью легче заболевают различными инфекционными болезнями.
Диагноз. Распознавание основывается на клинической картине (желтуха, малокровие, увеличение селезенки), типичном анамнезе (семейный характер заболевания, длительность течения с обострениями) и исследовании крови (анемия гиперхромного типа, микроцитоз, сфероцитоз, пониженная стойкость эритроцитов, ретикулоцитоз).
Дифференцировать приходится с болезнью Аддисон-Бирмера. При гемолитической болезни нет изменений со стороны языка, ахилии, явлений со стороны нервной системы. При исследовании крови, не отмечается мегалоцитоза и мегалобластоза. Нет лейкопении и сдвига ядерной формулы нейтрофилов вправо. Лечение печенкой результата не дает или дает эффект небольшой и лишь временный.
При гипертрофическом циррозе, за который можно ошибочно принять те случаи гемолитической анемии, при которых развилось уже увеличение и уплотнение печени, нет характерных для гемолитической желтухи изменений крови.
При желчнокаменной болезни не наблюдается изменений со стороны селезенки, анемии. Желтуха обтурационного типа.
Дифференциальный диагноз между врожденной и приобретенной гемолитической анемией не всегда легок. В настоящее время большое подсобное значение получила реакция Кумбса, которая обычно бывает отрицательной.
Прогноз. Прогноз относительно благоприятен. Больные могут дожить до глубокой старости. Трудоспособность сохраняется, если нет большого малокровия. Они не должны быть заняты на производствах, где возможно вредное действие на кроветворную систему (действие свинца, бензола, бензина, рентгеновых лучей).
Прогноз зависит от степени малокровия. Как выше уже было упомянуто, процесс может привести к истощению костного мозга и смерти от малокровия. Смерть может наступить от осложнений, чаще всего со стороны печени и желчных путей.
Лечение. Легко протекающие случаи особого лечения не требуют. При явлениях нерезкой анемии рекомендуют мышьяк. У тяжелобольных лечение железом и мышьяком не дает осязательных и стойких результатов. Лечение печенкой тоже существенного успеха не приносит. Переливание крови при этом заболевании является обычно бесполезным, а нередко и вредным вмешательством вследствие усиления гемолиза. Однако допустимы и даже в ряде случаев показаны переливания плазмы до 100-150 мл 1-2 раза в неделю.
Значительное малокровие, частые обострения, прогрессирующее ухудшение состояния представляют собой прямые показания к единственно эффективному способу лечения при данной болезни — к удалению селезенки. С каждым годом статистика при этой операции дает все лучшие результаты. Смертность от операции около 5%. Большие статистики последних лет дают 3,3% смертности (на 166 операций 5 случаев смерти). Этот процент продолжает падать.
Впервые спленэктомия при гемолитической болезни была произведена с благоприятным результатом Микели.
Результаты спленэктомии при врожденной гемолитической желтухе бесспорны и в большинстве случаев «поистине изумительны», «чудесны», «блестящи». Так же прекрасны результаты спленэктомии и по данным советских гематологов и хирургов.
Все основные симптомы болезни очень быстро, буквально на глазах, смягчаются или исчезают. Во время операции поражает легкость удаления сравнительно большой, но свободной от сращений селезенки. Отсутствует сколько-нибудь значительное кровотечение. Имевшееся малокровие быстро и стойко снижается. В течение нескольких месяцев, а иногда и недель количество эритроцитов и гемоглобина может достигнуть нормальных цифр.
Иногда наблюдались случаи, когда тот и другой показатели вслед за удалением селезенки превышали нормальные, становились характерными для полицитемии (6,5-7,5 млн. эритроцитов, 120-135% гемоглобина). Обычно падает число (процент) ретикулоцитов. Буквально сразу после операции изменяется обмен крови. Если до операции он был резко ускорен, показателем чего был резкий ретикулоцитоз, то вслед за операцией он становится замедленным — приход даже может превысить расход эритроцитов. В результате содержание гемоглобина и эритроцитов временно может достигать, как указано, полицитемического уровня. Исчезает желтуха. По Негели, уже на следующий день после операции исчезает желтушная окраска сыворотки крови и повышенное количество уробилина в моче. В течение нескольких недель исчезает желтушное окрашивание кожи и слизистых. Желчь при дуоденальном исследовании становится менее насыщенного цвета, испражнения — менее темными.
Несколько увеличивается осмотическая стойкость эритроцитов, однако сфероцитоз остается.
После операции довольно часто наблюдается кратковременное повышение температуры до высоких цифр (39,5-40-41°). Увеличивается лейкоцитоз. В крови, как обычно после удаления селезенки, появляются на долгое время тельца Жолли.
В костном мозгу (данные пункции) количество и процентное содержание эритробластов снижаются до нормы или приближаются к ней. Костный мозг в диафизах длинных костей из красного становится желтым, т. е. приобретает свойства нормального.
С течением времени больные могут стать снова желтушными, но желтуха никогда не достигает прежней степени. Могут наблюдаться и гемолитические кризы, опять-таки слабые. Анемия не развивается.
Костный мозг работает более спокойно. В этом отношении интересны наблюдения Т. В. Кенигсон и А. А. Коровина. Как указано выше, они находили при гемолитической болезни омоложение кровяных пластинок. Сразу после спленэктомии в крови встречаются по преимуществу старые пластинки. Через 1-2 года имеется снова сдвиг к более молодым формам.
С течением времени обмен крови становится опять более усиленным. Функция других отделов ретикуло-эндотелиальной системы повышается, но не достигает прежних величин.
Операция удаления селезенки при гемолитической болезни себя оправдала. Она показана при этом заболевании. Чем раньше, чем в более молодом возрасте ее делать, тем лучше.
При гемолитической болезни, как указано выше, часто наблюдается образование пигментных камней в желчном пузыре, нередки припадки желчнокаменной болезни. Может потребоваться оперативное вмешательство.
В отличие от приобретенной гемолитической анемии лечение адренокортикотропным гормоном обычно бесполезно.
источник
- Наследственная форма гемолитической анемии, обусловленная нарушением мембраны эритроцитов
- Наследственная форма гемолитической анемии, обусловленная нарушением активности ферментов эритроцитов
- Наследственная форма гемолитической анемии, обусловленная нарушением синтеза или структуры гемоглобина
- Анемия, обусловленная влиянием антител
- Анемия, обусловленная изменением структуры мембраны, вызванной соматической мутацией
- Анемия, обусловленная механическим повреждением оболочки эритроцитов
- Анемия, вызванная химическим повреждением эритроцитов
- Анемия, вызванная дефицитом витаминов (фолиевой кислоты и цианокобаламина)
- Анемия, вызванная разрушением эритроцитов паразитами
Болезнь Минковского-Шоффара (наследственный микросфероцитоз) – группа наследственных гемолитических анемий, характеризующихся образованием микросфероцитов (шаровидных эритроцитов) и обусловленных дефектом протеинов цитоскелета эритроцитов. При этом эритроциты теряют часть мембраны, уменьшается соотношение площади поверхности к объему, в результате чего эритроцит превращается в микросфероцит. Как правило, патология наследуется по аутосомно-доминантному признаку. Распространенность наследственного микросфероцитоза составляет примерно 1 случай на 1000-4500 человек.
При наследственном микросфероцитозе генетические нарушения влияют на протеины цитоскелета, преимущественно на те, которые объединяют цитоскелет с мембраной эритроцита. У большинства больных отмечается значительный дефицит спектрина, и только в некоторых случаях этот дефицит обусловлен генетическими дефектами самого спектрина.
Главные признаки наследственного микросфероцитоза – анемия, желтуха, спленомегалия (увеличенная селезенка). Анемия возникает из-за внутриклеточного распада эритроцитов. Желтуха развивается посредством непрямой гипербилирубинемии, может быть непостоянной и, как правило, слабо выражена у детей раннего возраста. Повышенное содержание билирубина в желчи часто является причиной образования пигментных желчных камней (даже у детей). Увеличение селезенки (спленомегалия) отмечается практически во всех случаях. При системных инфекционных патологиях интенсивность гемолиза может увеличиваться, в результате чего развивается спленомегалия.
Тяжелые формы наследственного микросфероцитоза характеризуются деформацией скелета: изменение расположения зубов, акрокефалия (башенный череп), высокое верхнее небо, микрофтальмия (уменьшение глазного яблока). В некоторых случаях отмечаются укороченные мизинцы. Могут образовываться трофические язвы на ногах.
Наследственный микросфероцитоз сопровождается апластическими кризами, которые провоцируются инфекцией (особенно парвовирусной).
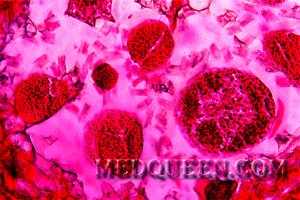
Микросфероцитоз – характерное изменение формы эритроцитов при этой патологии. При анализе мазка крови в биологическом материале наблюдаются микросфероциты в виде мелких клеток без центрального просветления (см рисунок 1). Отметим, что обнаружение микросфероцитов в мазках не всегда является признаком наследственного сфероцитоза.
Рисунок 1. Наследственный микросфероцитоз. Микросфероциты в мазке периферической крови (окр. по Романовскому-Гимзе, ув. ×100)
Такой признак обнаруживается при аутоиммунной гемолитической анемии с неполными тепловыми агглютинами, при наследственных дизэритропоэтической анемии. Средний объем эритроцитов, как правило, остается в норме или незначительно снижен. Показатель среднего содержания гемоглобина в эритроцитах в норме или незначительно повышен. Средняя концентрация гемоглобина в эритроцитах повышена почти у 50% пациентов.
Количественным показателем сферичности эритроцитов является осмотическая устойчивость (она снижена). Уровень ретикулоцитов в крови при гемолитическом кризе может значительно повышаться. Миелограмма показывает резкое раздражение красного ростка. Дифференциальный диагноз проводят с аутоиммунной гемолитической анемией, для которой характерна положительная проба Кумбса, отсутствие этой патологии среди родственников пациента и отсутствие данных о начале заболевания в детском возрасте.
Основной метод лечения анемии при наследственном микросфероцитозе – спленэктомия, с помощью которой устраняется анемия; при этом нельзя устранить морфологический дефект эритроцитов.
Наследственная гемолитическая анемия, обусловленная дефицитом глюкозо-6-фосфат дегидрогеназы эритроцитов – наиболее распространенная ферментопатия эритроцитов из группы ферментопатий пентозофосфатного пути метаболизма глюкозы. Глюкозо-6-фосфатдегидрогеназа эритроцитов – олигомер (в зависимости от условий может быть димер или тетрамер), который состоит из субъединиц с молекулярной массой 56 000 D. По данным ВОЗ (Всемирной организации здравоохранения) во всем мире количество людей, страдающих этой патологией, составляет более 200 млн. Наиболее широкое распространение этого заболевания характерно для Средиземноморского региона (Сицилия, Греция, Сардиния), негроидной расы, жителей Ближнего и Дальнего востока.
Клиническая картина при наследственной форме гемолитической анемии полиморфна: степень тяжести патологии может колебаться от гемолитической анемии, возникающей спонтанно после рождения, до гемолитических кризов. Гемолитический криз, который может провоцироваться метаболическим ацидозом или гипогликемией, развивается за несколько часов. В тяжелых случаях у больного развивается гемоглобинурия и шок. Также наблюдаются желтуха, моча приобретает бурый или черный цвет, одышка, диарея, рвота, снижение артериального давления, развивается тяжелая анемия, увеличиваются печень (гепатомегалия) и селезенка (спленомегалия).
Тяжелый гемолитический криз может спровоцировать развитие ДВС-синдрома (диссеминированного внутрисосудистого свертывания крови). Некоторые пациенты не переносят конские бобы (Viciafaba), после употребления которых происходит молниеносное развитие гемолитического криза (это явление также известно, как фовизм или примахиновая анемия).
Дефицит глюкозо-6-фосфат дегидрогеназы эритроцитов необходимо подозревать во всех случаях острого гемолиза, особенно у лиц негроидной расы и жителей средиземноморского региона. Диагноз подтверждается путем проведения лабораторных анализов. Острый гемолиз характеризуется быстрым снижением гематокрита с одновременным повышением уровня гемоглобина и непрямого гемоглобина, а также снижением уровня гаптоглобина. Анализ мазка крови показывает наличие фрагментов эритроцитов. Основой диагностики считается качественное (при необходимости – количественное) определение активности глюкозо-6-фосфат дегидрогеназы эритроцитов. У пациентов с вариантом «А-» явление аномального гемолиза проходит, как правило, самостоятельно – такие больные не нуждаются в специальном лечении. В случае развития тяжелого гемолитического криза необходимо проводить форсированный диурез, профилактику ДВС-синдрома, плазмаферез (с целью удаления продуктов гемолиза).
В случае возникновения качественной гемоглобинопатии происходит изменение аминокислотной последовательности цепей глобина. Талассемия (количественная гемоглобинопатия) характеризуется снижением образования цепей глобина без изменения их цепей. Нужно отметить, что разница между качественной и количественной гемоглобинопатиями не абсолютна.
Талассемия (анемия Кули) – группа патологий, обусловленных генетическим нарушением синтеза одной из цепей глобина. В норме процесс синтеза глобиновых цепей сбалансирован, поэтому свободных цепей глобина нет. В случае нарушения синтеза одной из цепей глобина баланс нарушается, образуются лишние цепи, которые агрегируют и откладываются в эритрокариоцитах. Среди жителей Средиземноморья наиболее распространена β-талассемия.
«Большая талассемия» (болезнь Кули, β-талассемия) – наследственная гемолитическая анемия, впервые описанная американскими педиатрами-гематологами Томасом Бентоном Кули (Thomas Benton Cooley) и Ли (P. Lee) в статье «Серия случаев спленомегалии у детей с анемией и необычными изменениями костей» («A Series of Cases of Splenomegaly in Children, with Anemia and Peculiar Bone Changes»), где были приведены случаи у выходцев из стран Средиземноморья. Для анемии Кули характерна тяжелая степень течения с самого детства, задержка роста и изменения костей в результате увеличения объема костного мозга, возникающие в случае отсутствия соответствующего лечения). Также при этой патологии у больного наблюдаются гепатомегалия, спленомегалия, гиперспленизм, деформации черепа (монголоидное лицо, башенный череп); желтуха, бледность и отложение меланина придают коже особый медный оттенок. Кроме этого, наблюдается перегрузка железом сердца, легких, печени, поджелудочной железы и других органов эндокринной системы, переломы костей, сдавления периферических нервов, разного рода инфекционные осложнения.
Результаты лабораторных исследований периферической крови показывают гипохромную анемию, ретикулоцитоз, мишеневидные эритроциты (см рис 2-4).
Рисунок 02. Анемия Кули (большая талассемия). Периферическая кровь. Микроцитоз, выраженная гипохромия, мишеневидные нормобласты и эритроциты (окр. по Романовскому-Гимзе, ув. ×100)
Рисунок 03. Анемия Кули (большая талассемия). Периферическая кровь (окр. по Романовскому-Гимзе, ув. ×50)
Рисунок 04. Анемия Кули (большая талассемия). Периферическая кровь. Множественные мишеневидные эритроциты (окр. по Романовскому-Гимзе, ув. ×100)
Миелограмма демонстрирует раздражение «красного ростка» и повышение количества сидеробластов. Также наблюдается повышение осмотической резистентности эритроцитов и количества билирубина за счет непрямой фракции. В крови повышается содержание железа и ферритина, развивается гемосидероз (чрезмерное отложение гемосидерина в тканях) внутренних органов. При гомозиготной β-талассемии необходимо проводить пренатальную диагностику – забор клеток плода из амниотической жидкости на предмет выявления мутации генов, отвечающих за кодирование β-цепи глобина, с применением метода полимеразной цепной реакции.
Без соответствующего лечения больные анемией Кули умирают в детском возрасте. Продлить жизнь, предупредить деформации костей и задержку роста можно путем регулярных трансфузий эритроцитарной массы (лучше переливать отмытые или размороженные эритроциты) при условии поддержания достаточно высокого уровня гемоглобина. В случае значительной спленомегалии и явлениях гиперспленизма больному показана спленэктомия (удаление селезенки). С целью предотвращения развития гемосидероза пациентам периодически назначают Деферазирокс (Эксиджад) или Дефероксамин (Десферал). Излечение возможно при аллогенной трансплантации костного мозга.
Серповидноклеточная анемия обусловлена носительством гемоглобина, который меняет свою структуру в условиях гипоксии. Самой распространенной аномалией структуры гемоглобина является гемоглобинопатия Sα2β26 глу+вал. При гомозиготном носительстве можно говорить о серповидноклеточной анемии; при гетерозиготном носительстве – серповидноклеточная аномалия. Патология наследуется по аутосомно-доминантному признаку. При серповидноклеточной анемии наблюдается мутация, в результате которой в цепи глобина глутаминовая кислота заменяется валином. В результате растворимость гемоглобина S при отдаче кислорода снижается, что приводит к образованию геля.
Серповидноклеточная анемия наиболее распространена среди населения Центральной Африки, Турции, Индии, Кубы. У больных диагностируется анемия, тромботические осложнения, поражения костей и суставов (отмечаются некрозы плечевой и бедренной костей). Кроме этого, тромбозы осложняются инфарктами (сердца, легких, почек, селезенки, головного мозга), приступами сильной боли в области живота. У детей отмечаются нарушения физического (отставание в росте) и полового развития, ночное недержание мочи, нарушение зрения (тромбозы сосудов сетчатки). Также могут развиваться гемолитический, апластический и секвестрационные кризы, при этом в селезенке происходит резкое накопление эритроцитов, что вызывает гиповолемический шок и резкое снижение уровня гемоглобина.
Для анализов крови при апластической анемии характерны низкий уровень гемоглобина, наличие серповидных эритроцитов (рисунок 5), базофильная пунктация эритроцитов, их мишеневидность, повышение уровня ретикулоцитов и непрямого билирубина. Миелограмма демонстрирует раздражение «красного ростка».
Рисунок 5. Серповидноклеточная анемия. Периферическая кровь. Серповидные и мишеневидные эритроциты. выраженная гипохромия эритроцитов (окр. по Романовскому-Гимзе, ув. ×100)
В качестве лечения применяют адекватную инфузионную терапию, переливания эритроцитарной массы, оксигенотерапии.
К приобретенным гемолитическим анемиям относится группа заболеваний разного патогенеза, которые объединяет внутрисосудистый гемолиз (гемолиз эритроцитов в периферической крови). В зависимости от механизма эритролиза приобретенная гемолитическая анемия может носить иммунный и неиммунный характер. Но, несмотря на разные патогенетические механизмы, клинические признаки этих анемий часто совпадают.
Гемолитическая анемия у пациентов с протезированными клапанами сердца и сосудами развивается примерно в 10% случаев при протезированном аортальном клапане. При использовании стеллитовых запирательных элементов частота гемолиза незначительно увеличивается (по сравнению с селиконовыми). Также некоторое увеличение частоты гемолиза отмечается при наличии околоклапанной регургитации и при малом диаметре клапана. Биопротезы (свиные клапаны) в редких случаях являются причиной механического гемолиза. Гораздо реже причиной гемолиза может быть также протезированный митральный клапан, так как трансклапанный градиент давления в этом случае ниже.
Гемолиз протезированными клапанами происходит в результате одновременного действия сразу нескольких факторов:
- Значительная сила сдвига, которая при турбулентном токе крови действует на мембрану эритроцитов, особенно когда под высоким давлением кровь проходит через маленькое отверстие (например, при околоклапанной регургитации)
- Отложения фибрина на участках неплотного прилегания кольца клапана к тканям сердца
- Прямое механическое повреждение эритроцитов при закрытии запирательного элемента
Значительное разрушение эритроцитов может наблюдаться после закрытия дефекта межпредсердной перегородки типа ostium primum заплатой из синтетического материала. Умеренное сокращение жизни эритроцитов с легкой анемией или без нее может наблюдаться при значительном обызвествлении аортального клапана. Механический гемолиз обнаруживается также у пациентов, перенесших аортокоронарное и аортобедренное шунтирование.
Тяжелые случаи механического гемолиза сопровождаются тяжелой анемией, ретикулоцитозом, обнаруживаются фрагментированные эритроциты (шизоциты), гемоглобинемия и гемоглобинурия, повышается активность лактатдегидрогеназы, снижается уровень гаптоглобина. Выведение железа из организма с мочой в виде гемосидерина или гемоглобина может вызвать дефицит железа в организме. В случае развития дефицита железа пациенту назначается пероральный прием препаратов железа. Терапия препаратами железа способствует повышению уровня гемоглобина и способствует снижению сердечного выброса и снижению интенсивности гемолиза. Отметим, что ограничение физической активности также способствуют снижению интенсивности распада эритроцитов. Если предпринимаемые меры не приводят к желаемому результату, нужно полностью устранить околоклапанную регургитацию или заменить протез.
источник
Наследственный микросфероцитоз (болезнь Минковского-Шоффара)
Это анемия, связанная с генетическим дефектом мембраны эритроцитов, что обусловливает их микросфероцитарную форму и гемолиз.
Тип наследования — аутосомно-доминантный.
Нарушение структурного белка (спектрина) ведет к изменению клеточной мембраны, изменению формы эритроцитов.
При данном заболевании наблюдается повышение проницаемости эритроцита для натрия, что приводит к проникновению избытка натрия и воды в клетку. Эритроциты приобретают сферическую форму, что нарушает их способность деформироваться в узких участках кровотока, например, при переходе из межсинусных пространств селезенки в синусы. Здесь эритроциты повреждаются и разрушаются макрофагами селезенки. Таким образом, тип гемолиза при наследственном микросфероцитозе — внутриклеточный. В крови нарастает анемия и билирубинемия. Длительно существующий гемолиз ведет к стимуляции эритропоэза, у больных нарушается костеобразование: «башенный череп», «готическое небо», монголоидный тип лица.
Клиника
1. Первые клинические симптомы анемии чаще проявляются в детском возрасте.
2. Желтуха, увеличение селезенки, боли в левом подреберье, иногда увеличение печени, склонность к образованию камней в желчном пузыре (желчная колика), изредка симметричные язвы голеней.
3. Деформации скелета («башенный череп», «готическое небо», деформация челюстей с неправильным расположением зубов, полидактилия), микрофтальмия.
4. Периодически возникают гемолитические кризы (часто провоцируются инфекцией): боли в области печени, селезенки и их увеличение, озноб, потемнение мочи, повышение температуры тела до 39—40 ºС, рвота, усиление желтухи и анемии, лейкоцитоз со сдвигом влево, в крови появляются нормоциты или нормобласты.
5. Иногда могут возникать апластические кризы, вызванные инфицированием парвовирусом (PV) — быстро нарастает арегенераторная анемия, иногда ведущая к летальному исходу. Если же происходит выживание, возникает пожизненный иммунитет, обеспечиваемый противовирусным IgG.
Лабораторные данные
1. В крови — нормохромная, микросфероцитарная, гиперрегенераторная анемия, возможны признаки гиперспленизма (тромбоцитопения), например: эр. — 2,1 • 10 12 /л, Hb — 68 г/л, ЦП — 1,0, ретик. — 56 ‰, тромб. — 190 • 10 9 /л, лейк. — 6,1 • 10 9 /л: э — 1, п — 4, с — 60, л — 30, м — 5, СОЭ — 12 мм/ч, анизоцитоз +++, Ht — 30 %, микросфероциты.
2. Снижение осмотической резистентности эритроцитов (в норме минимальный гемолиз 0,48—0,46 % NaCl, максимальный гемолиз — 0,34—0,32 % NaCl). Например, min — 0,64 %, max — 0,42 % NaCl.
3. Костный мозг: раздражение красного ростка (преобладание эритробластов и нормоцитов).
4. В крови — повышение билирубина за счет свободного, увеличение активности ЛДГ.
5. В моче много уробилина, в кале — стеркобилина (плейохромия).
6. Специальный метод исследования: определение продолжительности жизни эритроцитов с помощью радиоактивного хрома (время полувыведения 5—6 дней при норме 22—30).
7. Рентгенологически: изменение костей («волосатый череп»).
Дифференциальная диагностика проводится с АИГА, при апластическом кризе с АА.
1. Наиболее эффективным методом лечения является спленэктомия (при наличии конкрементов в ЖВП — их удаление), приводящая к клиническому выздоровлению.
Показания к спленэктомии (рекомендуется проводить в возрасте 7—8 лет и старше):
— выраженная анемия с частыми гемолитическими кризами, гиперспленизмом и спленомегалией (может быть показанием к операции в любом возрасте);
— вторичная желчнокаменная болезнь (при ее наличии одновременно проводится холецистоэктомия);
— упорная желтуха.
2. Переливание эритроцитарной массы производится только по жизненным показаниям — при крайне тяжелой степени анемии, в период тяжелых гемолитических кризов, а также при выраженной анемии и отказе от спленэктомии. Фолиевая кислота курсами.
3. При апластическом кризе Ig человека для в/в введения в дозе 1—2 г/сут. в течение 5 дней.
4. Дезагреганты и антикоагулянты для профилактики тромбозов (Флебодиа).
источник
Гемолитические анемии — группа заболеваний, в основе которых лежит уменьшение продолжительности жизни эритроцитов в результате их повышенного разрушения — гемолиза.
Распространенность гемолитических анемий значительно варьирует в различных географических зонах, в различных возрастных периодах и зависит от конкретной нозологической формы.
Причинами гемолиза могут быть наследственные факторы:
• аномалии самого эритроцита — биохимические дефекты мембраны, ферментных систем эритроцитов, структуры гемоглобина или его синтеза;
• внешние факторы, воздействующие на эритроциты, — сывороточные антитела, инфекционные агенты, механическая травма при циркуляции крови.
Заболевания, в основе которых имеет место наследственный дефект эритроцитов, группируются следующим образом: гемолитические анемии, обусловленные изменениями мембраны эритроцитов, — наследственный сфсроцитоз (болезнь Минковского—Шоффара), наследственный овалицитоз (эллиптоцитоз); гемолитические анемии, обусловленные изменениями активности ферментов, — дефицит глюкозо-6-фосфатдегидрогеназы; гемолитические анемии, обусловленные нарушением синтеза гемоглобина, — серповидно-клеточная анемия, та- лассемии.
Приобретенная гемолитическая анемия возникает в результате воздействия химических веществ (мышьяк, свинец, фенол, толуол, фосфор, анилин, сероводород, уксусная и другие кислоты, медь, змеиный или грибной яд, нафталин, пестициды), лекарственных препаратов (хинин, сульфаниламиды, пирамидон, фенацетин, некоторые антибиотики), бактериальных токсинов (с1о$(псИит регГппёепз, а- и Р-гемолитические стрептококки, пневмококки, сальмонеллы, менингококки), паразитарной инфекции (р1а$тос)шт Га1с1рагит), вирусной инфекции, физических факторов (охлаждения, ожоги).
Гемолиз может быть обусловлен иммунными факторами в результате действия антиэритроцитарных антител:
• образующихся в процессе иммунизации реципиента эритроцитарны- ми антигенами донора или изоиммунного конфликта в результате антигенных различий эритроцитов матери и плода;
• реагирующих при температуре тела и направленных против собственных эритроцитов;
• реагирующих при низких температурах и также направленных против собственных эритроцитов.
Травматические гемолитические анемии возникают при механическом повреждении эритроцитов. Источник травмирования может находиться внутри сердца при стенозе аортального клапана, при протезировании клапанов аорты; в сосудах стоп при длительном беге или ходьбе по твердой почве («маршевая» гемоглобинурия); в артериолах при злокачественной гипертензии и некоторых опухолях; в концевых артериолах при тромбоцитопенической пурпуре или при диссеминированном внутрисосудистом свертывании.
Патогенез. Нормальный эритропоэз состоит из нескольких этапов диф- ференцировки клеток, начиная с полипотентной стволовой клетки. В процессе созревания морфологически различимые клетки эритроидного ряда проходят следующие этапы: эритробласт -*■ пронормобласт (пронормоцит) — базофильный, полихроматофильный, оксифильный нормоцит— костномозговой ретикулоцит. В периферической крови определяются зрелые эритроциты. У здоровых лиц можно обнаружить молодые формы эритроцитов — ретикулоциты, количество которых колеблется от 2 до 12%.
По мере созревания эритроидные клетки синтезируют гемоглобин, который состоит из активной части гема и белковой структуры — глобина. Образование гемоглобина происходит при участии клеточных структур — ядра и митохондрий. По мере созревания эритроцита происходит разрушение орга- нелл и выталкивание ядра. Нормальная молекула гемоглобина взрослых (НЬА) состоит из двух полипептидных цепей — а и (3.
Гемоглобин А неоднороден и состоит из НЬА, и НЬА^ Тип цепей и химическая структура отдельных полипептидов определены генетически. Возможен синтез аномального гемоглобина с нарушением физических и химических свойств, что ведет к развитию анемий, более тяжелых у гомозигот и более легких у гетерозигот. У человеческого плода преобладает НЬР, включающий две а-цепи и две у-цепи, но его количество постепенно уменьшается уже в первые месяцы жизни, а у взрослых он составляет менее 2% всего гемоглобина. В результате несбалансированного синтеза гемоглобина из-за нарушения скоростей образования нормальных полипептидных цепей глобина возникает патология с гемолизом различной тяжести — талассемия. На основе генетического картирования с использованием рекомбинантной ДНК удалось установить две пары генов, которые кодируют синтез цепей глобина. В зависимости от делеции одного или двух генов из пары генов может быть гомозиготное или гетерозиготное носительство этой патологии и различная клиническая симптоматика.
Для изучения характеристик и различий гемоглобинов используется метод электрофореза, с помощью которого был выделен НЬ$. Отличие НЬ$ от НЬА состоит в том, что вместо одной из аминокислот (глютаминовой кислоты) в цепочке из четырех аминокислот в гемоглобине 5 присутствует другая аминокислота — валин. Эритроциты, содержащие такой гемоглобин, приобретают форму серпа и выявляются у больных с гемолитической анемией, которая называется серповидно-клеточная анемия.
Энергозатраты эритроцитов обеспечиваются за счет гликолиза — ферментативного расщепления глюкозы. После проникновения в клетку она превращается в лактат либо путем анаэробного гликолиза, либо через гексозомоно- фосфатный шунт. В ферментных системах этих метаболических путей у некоторых больных обнаружен наследственный дефект, связанный с дефицитом глюкозо-6-фосфатдегидрогеназы. Этот дефицит наследуется как аутосом- но-рецессивный признак и вызывает гемолитическую анемию, которая клинически чаще всего проявляется повышенной чувствительностью к лекарственным препаратам и при употреблении в пищу бобов.
Эритроцит ограничен белково-липидной мембраной, состоящей из двух слоев белка. Исследования цитоскелета эритроцитов показали, что врожденные структурные аномалии обусловлены изменениями белков клеточной мембраны. Врожденные мембранопатии характеризуются изменением формы эритроцитов. В клинической практике встречается микросфероцитарная гемолитическая анемия (болезнь Минковского-Шоффара). Сферическая форма эритроцитов и особенности структуры белка их мембраны нарушают пластичность и способность изменять свою форму в узких местах кровотока, поэтому они не могут своевременно пройти через микроциркуляторное русло селезенки, что приводит к их повреждению и разрушению.
В физиологических условиях длительность жизни эритроцитов человека составляет в среднем 120 дней. Эритропоэтическая функция находится в тесной взаимосвязи с процессами разрушения эритроцитов, которые осуществляются внутриклеточно в ретикулоэндотелиальной системе, главным образом — в селезенке. Небольшая часть эритроцитов разрушается внутри сосудистого русла (внутрисосудистый гемолиз).
При гемолитических анемиях возможен внутриклеточный (внесосудис- тый) и внутрисосудистый гемолиз.
Внутриклеточный гемолиз происходит, как и в норме, в клетках фагоцитарной системы — костном мозге, печени, селезенке. Стареющие, патологически малоизмененные эритроциты с тепловыми антителами на поверхности захватываются и разрушаются в селезенке — секвестрационный гемолиз. Эритроциты с выраженной патологией, а также адсорбировавшие холодовые антитела или комплемент разрушаются в печени. Костный мозг более активен в отношении эритрокариоцитов — незрелых ядросодержащих клеток красного ростка.
При внутриклеточном гемолизе, наряду с эритроцитами, разрушается гемоглобин. Основным производным окислительного катаболизма гема является несвязанный или непрямой билирубин, который находится в плазме в транспортируемой форме и из клеток фагоцитарной системы поступает в печень, где соединяется с глюкуроновой кислотой. Количество непрямого билирубина отражает, таким образом, интенсивность процессов гемолиза. Уровень связанного или прямого билирубина остается в пределах нормы. Так как циркулирующий в плазме непрямой билирубин связан с белком, он не может проходить через почечные клубочки. Следовательно, у больных с внутриклеточным гемолизом развивается желтуха с повышением уровня непрямого билирубина, при хроническом течении уровень уробилиногена в моче нормальный или незначительно повышен.
Внутрисосудистый гемолиз развивается редко и обусловлен грубыми повреждениями эритроцитов. При внутрисосудистом разрушении эритроцитов гемоглобин оказывается в сосудистом русле. В плазме или сыворотке крови находится гаптоглобин, который прочно связывается с белковой частью гемоглобина. Если уровень гемоглобина превышает порог гемоглобинсвязыва- ющей способности гаптоглобина, свободный гемоглобин плазмы проходит через почечные клубочки. Клетки проксимального нефрона реабсорбируют гемоглобин и превращают его в гемосидерин и ферритин, часть этих веществ реутилизируется, а часть выводится с мочой. При нарушении абсорбирующей способности канальцевых клеток наступает гемоглобинурия, при этом моча окрашивается в бурый или почти черный цвет. Таким образом, обнаружение гемосидерина и гемоглобина в моче свидетельствует о внутрисосудистом гемолизе.
Симптоматика гемолитических анемий зависит от типа скорости гемолиза и количества разрушенных эритроцитов. Степень анемии определяется соотношением между скоростью распада эритроцитов и активностью эритро- поэза. Анемия появляется при длительном гемолизе с укорочением срока жизни эритроцитов менее 20 дней.
Для гемолитических анемий, обусловленных внутриклеточным гемолизом, характерна клиническая триада: анемия, желтуха и спленомегалия.
Анемия проявляется общей слабостью, утомляемостью, снижением трудоспособности, одышкой и циркуляторными расстройствами.
Важным симптомом гемолитических анемий является желтуха, характеризующаяся лимонной окраской кожи. В сыворотке крови определяется увеличение содержания непрямого билирубина, уробилиноген в моче может быть нормальным. Возрастает выделение стеркобилиногена с калом, который окрашен в темно-коричневый цвет. При хроническом гемолизе желчь становится густой и интенсивно окрашенной — плейохолия, что способствует образованию пигментных желчных камней желчного пузыря и желчных протоков. Желчнокаменная болезнь с приступами печеночной колики является частым спутником гемолитических анемий. Присоединяется механическая желтуха, что усугубляет клиническое течение основного заболевания. Длительный застой желчи приводит к развитию билиарного гепатита и цирроза печени.
Спленомегалия — характерный симптом гемолитических анемий, объясняется гиперплазией системы фагоцитирующих клеток. Селезенка увеличивается обычно умеренно.
Клинически различают три формы гемолитической анемии с внутриклеточным гемолизом: латентную, хроническую и подострую.
Латентная (компенсированная) форма характеризуется уменьшением продолжительности жизни эритроцитов и усилением гемолиза, однако сохранена и даже увеличена регенерационная способность эритропоэза, в с связи с этим количество эритроцитов нормальное или незначительно снижено. У больных не отмечается выраженной желтухи, однако может быть желчнокаменная болезнь.
У больных с хронической формой выявляется умеренная желтуха, анемия с ретикулоцитозом.
Подострая форма проявляется острым гемолитическим кризом с выраженной желтухой, уробилинурией, резким снижением количества эритроцитов.
Для гемолитических анемий с внутрисосудистым гемолизом специфическим клиническим проявлением считается гемолитический криз, для которого характерно острое начало, нередко — высокая температура, резкая слабость, тошнота, рвота и боли в животе. В рвотных массах находится много желчи. Состояние тяжелое, вплоть до развития комы. Обращает внимание резкая бледность, с желтушным оттенком кожных покровов и слизистых, геморрагические кожные высыпания. Выслушивается систолический шум на верхушке, тахикардия, определяется резкое снижение артериального давления. При пальпации обнаруживается гепатоспленомегалия.
В связи с массивным гемолизом эритроцитов выделяется большое количество эритроцитарного тромбопластического фактора, который приводит к возникновению синдрома диссеминированного внутрисосудистого свертывания крови. Этот синдром может завершиться острой почечной недостаточностью или геморрагическим синдромом. Типичным признаком гемолитического криза является гемоглобинурия.
Наиболее информативным методом, который используется для установления компенсаторных возможностей костного мозга при анемиях, является подсчет ретикулоцитов. Гемолиз подтверждается обнаружением увеличения продукции молодых эритроцитов — ретикулоцитов.
В мазке периферической крови у больных гемолитической анемией обнаруживаются морфологически аномальные эритроциты, которые имеют определенное значение для диагностики конкретной формы гемолитической анемии. Эритроциты меньшего диаметра, шаровидной формы, без центрального просветления специфичны для наследственного сфероцитоза (болезни Минков- ского—Шоффара), в основе которого лежит дефект белка спектрина мембраны эритроцитов. Сфероциты также обнаруживаются в крови при приобретенных гемолитических анемиях после гемотрансфузий, при иммуногемолитических состояниях, связанных с тепловыми антигенами. Эритроциты в форме мишени (кодоциты) определяются у больных талассемией, наследственной гемолитической анемией, обусловленной нарушением синтеза гемоглобина. При гемоглобинопатии НЬР в эритроцитах при использовании специальной окраски обнаруживаются включения — тельца Гетца. Постоянное присутствие в крови эритроцитов в форме серпа или полумесяца (дрепаноциты) характерно для гемоглобинопатии — серповидно-клеточной анемии. При обнаружении в одном и том же мазке дрепаноцитов и мишеневидных клеток предполагается, что больной является гетерозиготным носителем гена талассемии и гена гемоглобинопатии 5. Измененной формы эритроциты в виде шлема, шпоры, так называемые шизоциты, появляются при кризе с внутрисосудис- тым гемолизом как результат травматического повреждения эритроцитов протезами клапанов и сосудов, а также при ДВС-синдроме, тромбоцитопеничес- кой пурпуре.
Для прогностических и научных целей используется метод определения продолжительности жизни эритроцитов с помощью радиоактивного хрома ( 51 Сг). Согласно этим исследованиям выделяют умеренный гемолиз (продолжительность жизни эритроцитов 20—40 дней) и выраженный гемолиз (продолжительность жизни эритроцитов 5—20 дней). Этот метод позволяет не только подтвердить наличие гемолиза, но и определить места секвестрации эритроцитов.
Среди биохимических показателей в диагностике гемолитических анемий важное значение имеет определение в сыворотке крови билирубина, гапто- глобина, лактатдегидрогеназы. Индикаторами гемолиза служат следующие данные: увеличение количества непрямого билирубина, уменьшение или отсутствие гаптоглобина, увеличение активности лактатдегидрогеназы. В моче при внутриклеточном гемолизе билирубин отсутствует, уробилиноген вариабелен. При внутрисосудистом гемолизе в моче определяется гемоглобин и гемо- сидерин.
Для выяснения наличия и типа аномального гемоглобина проводится электрофоретическое исследование. Анемии, связанные с иммунными нарушениями, распознают по наличию антител к эритроцитам. Эти антитела выявляются на эритроцитах с помощью прямого антиглобулинового теста — проба Кумбса. При этой пробе антиглобулиновые антитела вступают в реакцию с иммуноглобулинами, а компоненты комплемента — с эритроцитами больного (прямая реакция Кумбса). Существует модификация этой пробы — непрямая реакция Кумбса для выявления свободных антител в плазме крови боль-
ного, при смешивании его плазмы с нормальными эритроцитами. Около 90% больных с аутоиммунной гемолитической анемией имеют положительную прямую пробу Кумбса.
КЛАССИФИКАЦИЯ (А. Ф. Романов и соавт., 1997)
— наследственный сфероцитоз (болезнь Минковского—Шоффара);
— наследственный овалицитоз (эллиптоцитоз).
источник