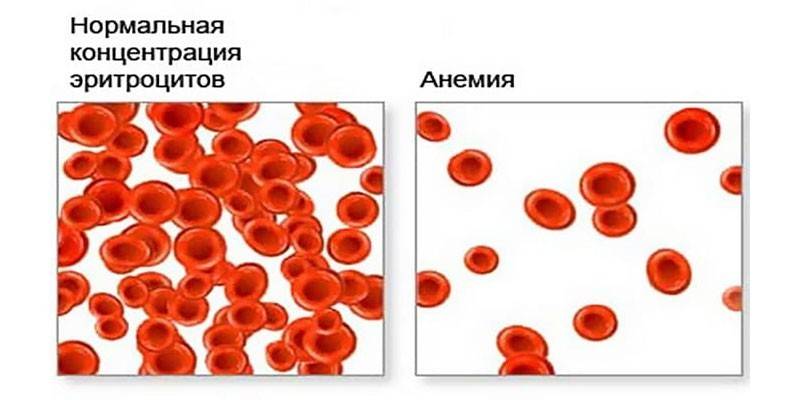
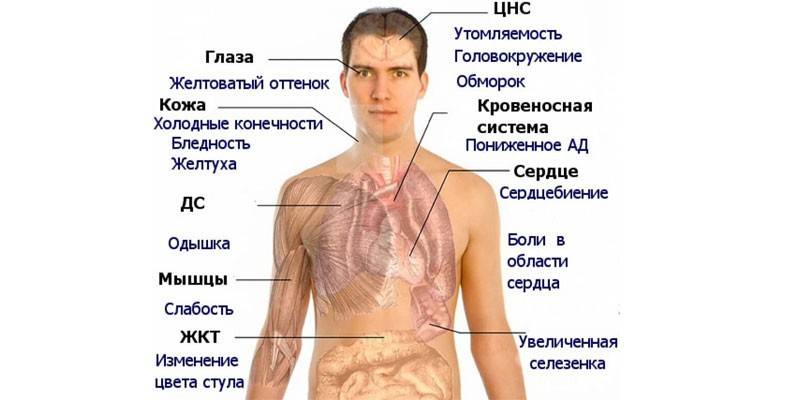
Витамин B12 и фолиевая кислота участвуют в реакциях синтеза нуклеиновых кислот, поэтому без их участия невозможно эффективное кроветворение.
Ежесуточная потребность организма в витамине B12 составляет 1-5 мкг, но, поскольку в ЖКТ всасывается только пятая часть поступившего с пищей витамина B12, то для возмещения физиологической потери необходимо поступление 25 мкг витамина в сутки, чего без труда можно достичь при сбалансированном питании, включающем животную пищу. Организм здорового взрослого человека содержит порядка 4 мг депонированного цианкобаламина, что дает возможность восполнять потери витамина B12 на протяжении почти 3 лет, без поступления его извне.
Ежесуточная потребность в фолиевой кислоте составляет 50 мкг. При рациональном сбалансированном питании организма человека получает до 1000 мкг фолатов. Несмотря на то, что запасы фолатов в организме человека составляют 5-10 мг, дефицит фолиевой кислоты при ее недостаточности будет ощущаться уже через несколько месяцев.
Наиболее распространенной причиной развития витаминодефицитных анемий является нарушение их всасывания в пищеварительном тракте. Также ряд лекарственных препаратов, алкоголь и другие химические соединения блокируют механизмы всасывания и транспорта витаминов. Витаминодефицит может возникать при возрастании физиологических потребностей и усилении расходования в периоды усиленного роста, развития, беременности.
Патогенез клинических проявлений при дефиците витамина B12 и фолиевой кислоты:
- Нарушается синтез ДНК, в результате замедляются процессы созревания клеток, что приводит к макроцитозу и мегацитозу (увеличению размеров клетки) — формируется мегалобластический тип кроветворения.
- Увеличивается до 50% доля неэффективного эритропоэза (в норме до 20%), вследствие повышения уровня внутрикостномозгового разрушения клеток эритроидного ряда.
- Укорачивается в 3-4 раза продолжительность жизни макроцитов, циркулирующих в крови.
- Недостаток витамина B12 приводит к нарушению пролиферации эпителия пищеварительного тракта (глоссит Хантера — сглаженный болезненный язык без сосочков, имеющий малиновый цвет).
- При выраженном дефиците витамина B12 развиваются неврологические нарушения, ведущие к повреждению нервной ткани, развитию периферической невропатии, фуникулярному миелозу.
- Наряду с дефицитными анемиями существуют ахрестические анемии, связанные с нарушением утилизации костным мозгом витамина B12. При ахрестических анемиях прием витамина B12 противопоказан.
- Менее 5% анемий не связана с дефицитом витамина B12 и фолатов, а является следствием других факторов, нарушающих синтез ДНК.
Для B12 и фолиеводефицитных анемий характерны следующие гематологические проявления:
- количество эритроцитов снижается в большей степени, чем количество гемоглобина (гиперхромная анемия);
- количество ретикулоцитов может быть снижено, но может быть и в норме;
- наличие в крови мегалобластов;
- повышается цветовой показатель (гиперхромная анемия);
- эритроциты увеличены, в мазках крови обнаруживается макроциты, мегалоциты, пойкилоциты, анизоцитоз;
- обнаруживаются эритроциты с патологическими включениями;
- наблюдается тромбоцитопения и лейкопения, также характерно наличие гигантских тромбоцитов и нейтрофилов с гиперсегментированным ядром.
Пример гемограммы больного мегалобластической гипохромной анемией
- эритроциты — 1,8·10 12 /л;
- гемоглобин — 78 г/л;
- цветовой показатель — 1,30;
- ретикулоциты — 0,1%;
- гематокрит — 0,25 л/л;
- в мазке:
- присутствуют макроциты и мегалоциты;
- анизоцитоз +++;
- пойкилоцитоз +
- СОЭ — 31 мм/ч;
- тромбоциты — 135·10 9 /л;
- лейкоциты — 3,2·10 9 /л;
- эозинофилы — 0%;
- базофилы — 0%;
- нейтрофилы:
- юные — 0%;
- палочкоядерные — 1%;
- сегментоядерные — 40%
- лимфоциты — 47%;
- моноциты — 12%
источник
Кандидат медицинских наук, доцент В.А. Ткачев
В12-дефицитная анемия – это тяжелая прогрессирующая анемия, возникающая при нарушении усвоения витамина В12, поступающего с пищей, вследствие пониженной (или при отсутствии) секреции внутреннего желудочного фактора.
Номенклатура названия этого заболевания разная, и оно нередко обозначается в литературе как пернициозная анемия (perniciosa – гибельная), злокачественная болезнь Аддисона–Бирмера (по фамилии авторов), а также мегалобластная анемия (по типу кроветворения).
Болеют лица старше 40 лет. Женщины подвержены этому заболеванию в два раза чаще, чем мужчины и, прежде всего, в возрасте старше 50–60 лет. Известны случаи В12-дефицитной анемии у детей, вскармливаемых козьим молоком или сухими молочными смесями. Заболеваемость составляет от 20 до 60 случаев на 10 000 населения.
Историческая справка. Первое описание этого заболевания сделал Кумбс в 1822 г. и назвал его тяжелым первичным малокровием. В 1855 г. врач Аддисон описал это страдание под названием «идиопатическая анемия». В 1872 г. Бирмер опубликовал результаты наблюдения за группой больных, страдавших прогрессирующей пернициозной анемией. Однако возможность излечения этого заболевания появилась только в 1926 г., когда Майнот и Мерфи обнаружили выраженный лечебный эффект от назначения сырой печени.
Через три года американский физиолог Кастл показал, что сырое мясо, печень, дрожжи, обработанные желудочным соком здорового человека, обладают свойством вызывать ремиссию у больного пернициозной анемией. Исследования Кастла легли в основу концепции, согласно которой в результате взаимодействия двух факторов – внешнего, содержащегося в сыром мясе, сырой печени, дрожжах, и внутреннего, вырабатываемого слизистой оболочкой желудка, создается антианемическое соединение, которое обеспечивает физиологическое вызревание костномозговых клеток.
Природа внешнего фактора была установлена – им является цианкобаламин (витамин В12). Витамин В12 по потребности организма используется не только для гемопоэза в костном мозге, но и для нормального функционирования нервной ткани и органов пищеварения.
Комплексное соединение, состоящее из пептидов (появляющихся в процессе превращения пепсиногена в пепсин) и мукоидов (выделяемых добавочными клетками слизистой оболочки желудка) было названо гастромукопротеидом или внутренним фактором Кастла. Роль внутреннего фактора (гастромукопротеида) заключается в образовании с витамином В12 комплекса, обеспечивающего транспорт цианкобаламина по кишечнику и препятствующего его распаду и инактивации. Резорбция (всасывание) витамина В12 происходит в подвздошной кишке. Дальнейшее поступление его в портальный кровоток осуществляется при помощи белковых переносчиков: транскобаламина-1 (-глобулина) и транскобаламина-2 (-глобулина), которые образуют белково-В12-витаминный комплекс, способный депонироваться в печени.
Этиология. Ведущим фактором в этиологии заболевания является эндогеннная недостаточность витамина В12, возникающая вследствие нарушения его всасывания из-за прекращения секреции внутреннего фактора (гастромукопротеида).
Нарушение всасывания В12 может возникнуть в результате поражения желудочно-кишечного тракта воспалительным или злокачественным процессом, после субтотального или тотального удаления желудка, после обширной резекции части тонкого кишечника. В редких случаях пернициозная анемия развивается при нормальной секреции внутреннего желудочного фактора и обусловлена врожденным отсутствием транскобаламина-2, с которым витамин В12 связывается и доставляется в печень, либо в результате отсутствия в кишечнике белкового акцептора (воспринимающего) витамина В12, необходимого для поступления цианкобаламина из кишечника в кровеносное русло. В отдельных случаях имеет место генетический фактор развития В12-дефицитной анемии вследствие врожденного нарушения выработки желудочного фактора или наличия антител против париетальных клеток.
К возникновению В12-дефицитной анемии могут привести и следующие факторы:
нарушение всасывания В12 в тонком кишечнике в результате хронического энтерита или глютеновой энтеропатии;
конкурентное поглощение витамина В12 в тонком кишечнике широким лентецом или микроорганизмами;
полное исключение пищи животного происхождения;
длительное снижение внешнесекреторной активности поджелудочной железы, следствием чего является нарушение расщепления протеина R, без которого витамин В12 не может связаться с мукополисахаридом;
длительное назначение некоторых лекарственных препаратов: метотрексат, сульфасалазин, триамтерен, 6-меркаптопурин, азатиоприн, ацикловир, фторурацил, цитозар, фенобарбитал и др.
Патогенез. Нарушение кроветворения при В12-дефицитной анемии характеризуется мегалобластическим типом для всех трех ростков крови: эритроидного, гранулоцитарного и мегакариоцитарного. Отмечается неэффективность красного кроветворения: нарушение дифференцировки эритроидных клеток и появление аномальных клеток типа промегалобластов, мегалобластов (большого размера клеток с базофильной цитоплазмой и ядром, содержащим ядрышки).
В результате дефектного метаболизма фолиевой кислоты (из-за дефицита В12), которая участвует в образовании ДНК, нарушается клеточное деление. Следствием этого является выраженная интрамедуллярная гибель эритроидных элементов и снижение количества эритроцитов на периферии.
Из-за несостоятельности клеточных элементов крови усилен гемолиз, который проявляется гипербилирубинемией, уробилинурией, увеличением стеркобилина в кале.
Патологоанатомические изменения характеризуются общим малокровием, желтушностью кожи и слизистых, жировой дистрофией миокарда, печени, почек. Костный мозг сочный, малинового цвета из-за гиперплазии.
Со стороны органов пищеварения выявляются атрофические изменения сосочков языка (их сглаженность), воспалительные его изменения (глоссит), афтозные высыпания, трещины (Гунтеровский глоссит), а также атрофия слизистой оболочки щек, неба, глотки, пищевода. Наибольшая атрофия регистрируется в желудке, которая характеризуется истончением его стенок, формированием полипов. Слизистая оболочка кишечника также атрофирована. Селезенка, как правило, нормальных размеров или увеличена.
Гепатомегалия невыраженная. Выявляется гемосидероз в печени, селезенке, почках (ржавый оттенок на разрезе) в результате гемолиза эритроцитов.
В нервных волокнах языка (нервных сплетениях Мейснера и Ауэрбаха), а также в задних столбах спинного мозга (очаговое набухание с распадом миелиновых нервных волокон) отмечаются дистрофические изменения.
Клинические проявления В12-дефицитной анемии чаще развиваются постепенно: нарастает слабость, недомогание, головокружение, диспепсические расстройства, шум в ушах, склонность к ожирению. Редко заболевание начинается остро, с подъема температуры тела до 38 С, выраженной слабости.
Анемический синдром характеризуется вялостью, бледностью кожных покровов с лимонно-желтым оттенком, иногда (у 12% больных) субиктеричностью склер. В периферической крови регистрируется анемия, чаще (58%) тяжелая, с увеличением цветного показателя до 1,4, снижением ретикулоцитов до 0,5 – 1,0% (у трети больных – ретикулоцитоз), пойкилоцитозом и наличием телец Жолли и колец Кэбота в эритроцитах. Часто выявляется лейкопения, лимфоцитоз, но тромбоцитопения.
В костном мозге определяются признаки мегалобластического типа кроветворения.
Синдром желудочной диспепсии (37,% наблюдений) проявляется отрыжкой, тошнотой, потерей вкусовых ощущений, снижением аппетита вплоть до отвращения к пище, тяжестью в эпигастрии, иногда дисфагией, чувством жжения языка, слизистой оболочки рта. На ЭГДС выявляются атрофические изменения в слизистой оболочки пищевода и желудка.
Синдром кишечной диспепсии характеризуется неустойчивым стулом, похуданием.
Глоссит проявляется наличием «ошпаренного» (красного) или «лакированного» с трещинами языка. Боли в языке отмечаются у 30% больных с В12-дефицитной анемией.
Синдром желтухи бывает у 50% больных и проявляется субиктеричностью склер и гипербилирубинемией.
Синдром фуникулярного миелоза (сенсорная атаксия – нарушение координации движений) отмечается у больных с В12-дефицитной анемией в 11% случаев и развивается в результате нарушения проприорецептивной чувствительности из-за атрофических процессов в задних рогах спинного мозга. Могут быть и другие симптомы поражения нервной системы: парестезии, расстройства функции тазовых органов, снижение рефлексов.
Синдром межреберной невралгии встречается существенно чаще (до 30% случаев), чем признаки фуникулярного миелоза, проявляется невралгическими болями по ходу межреберий и также обусловлен функциональной недостаточностью нервной ткани проводников.
У части больных отмечается поражение черепномозговых нервов (зрительного, слухового, обонятельного), наличие симптомов спинального паралича (спастический парапарез с повышенными рефлексами и клонусами) Может обнаруживаться центральная скотома (дефект поля зрения) с потерей зрения.
Изменения со стороны центральной нервной системы могут проявляться синдромом психомоторного возбуждения (маниакальное состояние с эйфорией или синдромом депрессии с нарушением памяти и критики — мегалобластное слабоумие).
Кардиальный синдром (в 15–20% наблюдений) характеризуется одышкой, сердцебиением, болями в области сердца, миокардиодистрофией. При аускультации сердца выслушивается функциональный анемический шум. На ЭКГ определяется снижение ST, расширение желудочкового комплекса.
Отечный синдром встречается при В12-дефицитной анемии в 80% случаев и проявляется периферическими отеками, могущими достигать степени анасарки, как результат недостаточности кровообращения.
Увеличение печени (синдром гепатомегалии) встречается у 22% больных, увеличение селезенки (синдром спленомегалии) в 10% случаях.
При нелеченной В12-дефицитной анемии может развиться синдром пернициозной комы, проявляющийся ишемией головного мозга, потерей сознания, арефлексией, падением температуры тела, снижением АД, рвотой, непроизвольным мочеиспусканием.
С целью диагностики заболевания проводится тщательное гематологическое исследование, включающее изучение картины периферической крови, стернального пунктата и сывороточных факторов, участвующих в гемопоэзе. Точный диагноз очень важен, т.к. эти больные в ряде случаев нуждаются в пожизненном лечении.
Гиперсегментация нейтрофилов (более пяти ядерных долей) периферической крови является первой гематологической патологией при мегалобластном статусе. У здорового человека могут циркулировать в крови до 2% гиперсегментированных нейтрофилов. У больных мегалобластной анемией количество гиперсегментированных нейтрофилов превышает 5%.
Для костномозгового кроветворения характерен мегалобластический тип, для которого типично раздражение красного ростка и появление мегалобластов. Костный мозг гиперклеточный за счет увеличения количества ядросодержащих клеток красного ряда. В результате нарушения клеточного деления эритроидные клетки становятся очень крупными (мегалобласты). Они характеризуются большой величиной, нежной структурой и необычным расположением хроматина в ядре, асинхронной дифференцировкой ядра и цитоплазмы.
В сыворотке крови у больных с В12-дефицитной анемией повышена концентрация билирубина, железа, ферритина (железосодержащий белок печени). Активность сывороточной лактатдегидрогеназы (ЛДГ) значительно повышена и увеличивается по мере прогрессирования заболевания. Уровень сывороточного цианкобаламина обычно низкий, но может быть нормальным.
Дифференциальная диагностика проводится с фолиево-дефицитной анемией. Дефицит фолиевой кислоты наблюдается обычно в более молодом возрасте, не сопровождается атрофическими изменениями слизистой оболочки желудка и неврологической симптоматикой.
Для исключения фолиево-дефицитной анемии проводится тест Шиллинга: вводят витамин В12 парентерально, который определяется в моче в минимальных количествах при В12-дефицитной анемии и в больших количествах — при фолиево-дефицитной. Важно учитывать, что назначение больным с В12-дефицитной анемией фолиевой кислоты быстро способствует развитию фуникулярного миелоза.
Следует помнить, что симптоматическую мегалобластную анемию вызывают опухоли желудка, тонкой и слепой кишки, а также глистная инвазия (глистная В12-дефицитная анемия), что необходимо исключить при верификации диагноза.
Дифференцировать следует и с эритромиелозами (начальные формы проявления лейкоза), которые сопровождаются анемией, протекающей с повышенным содержанием в крови витамина В12 и резистентной к лечению цианкобаламином.
При проведении дифференциальной диагностики В12-дефицитной анемии необходимо установить ее причины.
Лечение В12-дефицитной анемии включает парентеральное введение витамина В12 или гидрооксикобаламина (метаболит цианкобаламина) в дозах, обеспечивающих удовлетворение дневной потребности и удвоение запасов депо. Витамин В12 вводят по 1000 мкг внутримышечно ежедневно в течение двух недель, затем один раз в неделю до нормализации уровня гемоглобина, после чего переходят на введение 1 раз в месяц в течение всей жизни.
Оксикобаламин по фармакологическим свойствам близок к цианкобаламину, но сравнительно с последним быстрее превращается в организме в активную коферментную форму и дольше сохраняется в крови. Вводится оксикобаламин в дозе 500–1000 мкг через день или ежедневно. При наличии неврологической симптоматики необходимо введение препарата в дозе 1000 мкг каждые две недели в течение шести месяцев.
При фуникулярном миелозе назначаются массивные дозы цианкобаламина по 1000 мкг ежедневно в течение 7–10 дней, далее два раза в неделю до исчезновения неврологических признаков.
Начало терапии кобаламином быстро улучшает самочувствие больных. Костномозговой эритропоэз превращается из мегалобластного в нормобластный уже через 12 часов после введения витамина В12. Поэтому назначение витамина В12 при коматозном состоянии относится к неотложным мероприятиям. Ретикулоцитоз появляется на 3–5 день, пик его (ретикулоцитарный криз) наиболее выражен на 4–10 день. Концентрация гемоглобина нормализуется через 1–2 месяца. Гиперсегментация нейтрофилов сохраняется до 10–14 дней.
Трансфузии эритроцитарной массы показаны для срочной ликвидации симптомов гипоксии.
После терапии кобаламином может развиться тяжелая гипокалиемия. Поэтому в процессе лечения витамином В12 необходимо тщательно контролировать содержание калия в крови и при необходимости проводить заместительную терапию.
Лечение кобаламином следует назначать всем больным после тотальной гастрэктомии. Для предупреждения обострения витамин В12 вводится один раз в две недели по 100 – 200 мкг.
Диспансеризация. Больные В12-дефицитной анемией подлежат диспансерному наблюдению, в ходе которого проводится мониторинг состояния периферической крови 1-2 раза в год, а также лечение заболеваний и состояний, приведших к развитию данного вида анемии.
Существуют разные схемы поддерживающей терапии кобаламинами. При назначении цианкобаламина рекомендуются пожизненно ежегодные профилактические трехнедельные курсы по 400-500 мкг через день либо ежемесячное введение 500-1000 мкг препарата. Гидроксикобаламин рекомендуется ежегодными профилактическими курсами по одной инъекции в неделю (1 мг) в течение 2-х месяцев.
источник
При мегалобластной анемии в костном мозге определяются клетки с характерными морфологическими признаками: крупные, незрелые по внешнему виду ядра, окруженные относительно более зрелой цитоплазмой. С точки зрения биохимии основной причиной этого состояния является нарушение синтеза ДНК: в S-фазе клеточного цикла клетки прекращают развиваться (при частичной репликации ДНК клетка не может завершить процесс деления). При этом синтез РНК не нарушен. Происходит нарушение дифференцировки ядра. Учитывая, что синтез цитоплазматических компонентов очень интенсивный (особенно гемоглобина), площадь клеток-эритроидных предшественников очень расширена – это способствует образованию макроцитов (гиперхромных эритроцитов крупных размеров) или мегалоцитов. Такие изменения также характерны для гранулоцитарных предшественников и мегакароцитов.
Впервые мегалобласная анемия была описана английским ученым Аддисоном (Addison) в 1849 году. Аддисон обозначил ее как злокачественную (пернициозную). Врач Фенвик (Fenwick) из Лондона в 1870 году при вскрытии больного с пернициозной анемией обнаружил атрофию слизистой оболочки желудка. Немецкий врач Биермер (Biermer, Цюрих) в 1872 году в отношении этой патологии применил термин «прогрессирующая пернициозная анемия». А в 1880 ученый Эрлих (Ehrich) в костном мозге больных пернициозной анемией обнаружил крупные клетки со специфической структурой – мегалобласты. В начале XX века пернициозная анемия была одной из самых распространенных патологий крови и считалась неизлечимой.
Специалистам, которые изучали эту патологию и методы ее лечения, было присвоено пять Нобелевских премий. В 1930 году Касл (Castle) предполагал, что в мясе животных содержится «внешний фактор», который связывается с «внутренним фактором», в результате чего образуется так называемое гемопоэтическое вещество, способное усваиваться и депонироваться в печени. Ученые Минот (Minot), Марфи (Murphy) и Випл (Whipple) получили Нобелевскую премию в области медицины и физиологии за новый метод лечения пернициозной анемии сырой печенью. В 1948 году сразу две группы ученых (в США под руководством Фолкерса (Folkers) и в Великобритании под руководством Лестера-Смита (Lester-Smith)) выделили внешний фактор, витамин B12. Также Нобелевскую премию получила Дороти Кроуфут-Хоткин (Dorothy Crowfoot-Hodgkin) за изучение структуры пенициллина и витамина B12.
Витамин B12 (цианокобаламин) обладает структурой корриноида, в основе которой находится углеродная структура коррина, схожего по строению с порфирином. Цианокобаламин – сложная по структуре молекула с центральным атомом кобальта, который связан с четырьмя пиррольными кольцами и нуклеотидом. Витамин B12 имеет две коферментные формы – аденозилкобаламин и метилкобаламин. В крови человека основная форма витамина B12 – метилкобаламин.
Витамин B12 содержится только в продуктах животного происхождения (печень, почки, мясо, молоке и молочных продуктах). Небольшое количество этого витамина синтезируется в кишечнике человека. Цианокобаламин практически не содержится в продуктах растительного происхождения. У травоядных животных синтез витамина B12 происходит в желудке благодаря микроорганизмам, обитателям бобовых и корнеплодов, затем витамин попадает в паренхиматозные ткани и мышцы этих животных. Максимальная концентрация цианокобаламина в печени и почках животных (примерно 100 мкг/100 г продукта). В мясе содержание цианокобаламина гораздо ниже (примерно 0,5-2,0 мкг/100 г). Содержание витамина B12 в молоке и яйцах еще ниже, кроме этого, из-за прочной связи с протеином кобалафилином, содержащийся в этих продуктах витамин плохо усваивается. Цианокобаламин под действием протеолитических ферментов высвобождается в желудке и при кулинарной обработке продуктов.
Через стенки кишечника цианокобаламин попадает в кровь, где вступает в связь с транскобаламином II (транспортным протеином) и через воротную вену распределяется по кровеносной системе, откуда попадает в ткани-мишени.
Содержание цианокобаламина в организме взрослого человека составляет от 2 до 5 мг. Основной запас витамина B12, которого хватает на несколько лет (3-6), находится в печени. Экскреция (выведение из организма) цианокобаламина осуществляется через кишечник (с калом) и почки (с мочой), и составляет примерно 2-5 мкг в сутки. Суточная потребность организма взрослого человека в витамине B12 составляет 3-7 мкг.
Коферменты витамина B12 принимают участие в процессе синтеза ДНК, а также в регуляции функции системы гемопоэза и нервной системы. В крови содержится в большей степени активная форма витамина – метилкобаламин, который участвует в синтезе тетрагидрофолиевой кислоты, необходимой для образования тимидина.
Дефицит витамина B12 приводит к нарушению метаболизма фолатов и синтеза ДНК, в результате чего пролиферирующие кроветворные клетки не способны полностью созревать и нормально делиться. При этом в костном мозге развивается мегалобластический тип кроветворения, что приводит к появлению гигантских клеток миелопоэза и мегакариоцитопоэза. Из-за дефицита витамина B12 или B9 образуется недостаточное количество тетрагидрофолата, что вызывает развитие мегалобластной анемии по причине снижения синтеза нуклеиновых кислот.
Классическая картина B12-дефицитной анемии состоит из трех основных синдромов:
B12-дефицитная анемия, как правило, манифестирует в возрасте 50-60 лет (при этом такие пациенты часто выглядят старше своего возраста). Этот вид анемии наиболее широко распространен в Скандинавских странах, что обусловлено предрасположенностью к этой патологии голубоглазых блондинов.
B12-дефицитная анемия имеет три степени тяжести:
I степень: Легкая – концентрация гемоглобина в крови > 90 г/л
II степень: Средняя – концентрация гемоглобина в крови 70-90 г/л
III степень: Тяжелая – концентрация гемоглобина в крови 35 пг или цветового показателя > 1,1. Также увеличивается средний объем эритроцитов (> 100 фл и даже > 120 фл). В случаях, когда B12-дефицитная анемия сочетается с железодефицитной анемией или анемией хронического воспаления, средний объем эритроцитов может оставаться в пределах нормы. Выраженное повышение уровня ретикулоцитов (200-300% и выше) развивается на 5-8 день лечение витамином B12 – это повышение является подтверждением диагноза. Кроме этого, у многих пациентов наблюдается лейкопения (выраженность лейкопении часто коррелирует со степенью тяжести анемии). В некоторых случаях может наблюдаться снижение уровня тромбоцитов.
Большое диагностическое значение среди биохимических анализов крови имеет исследование уровня цианокобаламина. В миелограмме при нормальном или повышенном уровне миелокариоцитов обнаруживается выраженная гиперплазия эритроидного ростка и мегалобластический тип кроветворения (см рис. 1-7).
Рисунок 1. B12-дефицитная анемия. Костный мозг. Мегалобласты (окр. по Романовскому-Гимзе; ув. ×100)
Рисунок 2. B12-дефицитная анемия. Костный мозг. Мегалобласты. Гигантские палочкоядерные нейтрофилы (окр. по Романовскому-Гимзе; ув. ×100)
Рисунок 3. B12-дефицитная анемия. Костный мозг. Множественные базофильные мегалобласты – «синий костный мозг» (окр. по Романовскому-Гимзе; ув. ×100)
Рисунок 4. B12-дефицитная анемия. Препарат костного мозга. Мегалобластный тип кроветворения (окр. по Романовскому-Гимзе; ув. ×100)
Рисунок 5. B12-дефицитная анемия. Препарат костного мозга. Множественные базофильные мегалобласты – «синий костный мозг» (окр. по Романовскому-Гимзе; ув. ×100)
Рисунок 6. B12-дефицитная анемия. Препарат костного мозга. Мегалобласты, гигантские палочкоядерные нейтрофилы (окр. по Романовскому-Гимзе; ув. ×100)
Такие изменения миелограммы можно наблюдать только до начала терапии витамином B12. В аспирате костного мозга, полученного даже после однократной инъекции препарата, мегалобласты исчезают, а мегалобластический тип кроветворения сменяется нормобластическим. Отметим, что очень важным диагностическим критерием является высокий уровень лактатдегидрогеназы в крови.
Основа диагностики B12-дефицитной анемии в гематологии – анализ костного мозга на предмет наличия мегалобластов и миелоцитов с метамиелоцитами (гигантских клеток-предшественников гранулоцитопоэза). Но на практике эти клетки обнаруживаются не во всех случаях (даже если у больного явная форма анемии). Предположительно это происходит из-за того, что какое-то количество цианокобаламина больной все-таки как-то получил, что послужило причиной временного изменения гемопоэза, но не позволило полностью улучшить состояние. Но точные причины такого парадокса неизвестны. Поэтому с целью диагностики типичного случая B12-дефицитной анемии достаточно провести анализ периферической крови, с помощью которого можно определить гиперхромную макроцитарную анемию (при дифференциальной диагностике только патологий из группы миелодиспластических синдромов!). При этом могут обнаруживаться гиперсегментированные нейтрофилы (см рис. 7, 8), иногда метамиелоциты.
Рисунок 7. B12-дефицитная анемия. Препарат костного мозга. Множественные мегалобласты (окр. по Романовскому-Гимзе; ув. ×100) (а, б)
Рисунок 8. B12-дефицитная анемия. Костный мозг. (окр. по Романовскому-Гимзе; ув. ×100)
Если лабораторные исследования демонстрируют умеренную тромбоцитопению, незначительное повышение уровня непрямого билирубина и значительное повышение концентрации лактатдегидрогеназы, диагноз можно считать подтвержденным (в этом случае проведение дополнительных пункций – лишняя процедура).
При диагностике B12-дефицитной анемии важное значение играет фиброгастроскопия, с помощью которой можно подтвердить диагноз «атрофический гастрит» — главная причина дефицита цианокобаламина. Кроме этого, гастроскопия позволяет исключить злокачественную патологию желудка.
После назначения лечения витаминами B9 и B12 наблюдается следующая динамика изменения показателей лабораторных исследований:
— значительное повышение уровня эритроцитов и гемоглобина в течение 14 дней, показатель которых, в зависимости от выраженности дефицита, нормализуется через 8-12 недель с момента начала лечения; отметим, что уровень гемоглобина повышается медленнее, поэтому его показатель в периферической крови возвращается в норму через 1-2 месяца лечения;
— на 2-4-й день терапии начинает увеличиваться уровень ретикулоцитов, достигает максимума на 8-9-й день, и нормализуется к 14-му дню лечения; при этом повышается уровень тромбоцитов и лейкоцитов;
— на 10-14-й день терапии гиперсегментация ядер нейтрофилов сохраняется;
— в течение 24-48 часов после первого введения препарата в костном мозге исчезают мегалобласты; изменения морфологии ядер гранулоцитов сохраняется еще несколько суток;
— биохимический анализ крови показывает повышение уровня мочевой кислоты и холестерина (максимум достигается на пике ретикулоцитоза); концентрация лактатдегидрогеназы, щелочной фосфотазы и билирубина возвращаются в норму; может наблюдаться незначительное снижение концентрации калия в крови.
Пока врачи не могли использовать в терапии препараты цианокобаламина, B12-дефицитная анемия считалось фатальным заболеванием. В те времена ремиссию можно было получить с помощью эмпирического подбора рациона питания, трансфузионной терапии или спленэктомии, но после этого следовал очередные рецидивы, которые приводили к смерти пациента (как правило это происходило через 1-3 года с момента диагностирования патологии).
С целью профилактики развития B12-дефицитной анемии рацион питания должен содержать животный белок (печень, сердце, мясо, рыба, молочные продукты и др). Во время манифестации патологии нужно назначать цианокобаламин. Если у больного диагностированы глистные инвазии, дополнительно назначается противогельминтная терапия.
Сегодня для лечения B12-дефицитной анемии широко применяются два препарата: Цианокобаламин и Оксикобаламин. В нашей стране принято назначать Цианокобаламин: подкожно или внутримышечно 200-400 мкг 1 раз в день на протяжении 4-5 недель. В тяжелых случаях и при развитии фуникулярного миелоза суточная дозировка цианокобаламина повышают до 1000 мкг.
При условии назначения адекватного лечения явное улучшение состояния пациента и нормализацию картины костного мозга можно наблюдать уже на 3-4-е сутки лечения. Повышение уровня ретикулоцитов в периферической крови в среднем на 20-30% (ретикулоцитарный криз) развивается через 1-2 недели. Концентрация билирубина в крови возвращается в норму на протяжении 3-4 недель, лактатдегидрогеназы – через 7-14 дней.
При назначении цианокобаламина ремиссия наступает у всех больных B12-дефицитной анемией.
При отсутствии эффекта от терапии на протяжении нескольких недель, следует предполагать неверную трактовку генеза анемии. В этом случае пациенту необходимо провести дополнительную диагностику, чтобы уточнить причину анемического синдрома.
Эта патология относится к группе мегалобластных анемий. Дефицит фолиевой кислоты приводит к нарушению влияния цианокобаламина на процесс синтеза ДНК, что приводит к развитию мегалобластного типа кроветворения.
Дефицит витамина B9 может возникать из-за недостаточного поступления в организм фолиевой кислоты с пищей, патологий желудочно-кишечного тракта (нарушений усвоения фолиевой кислоты), а также при повышенной потребности организма в этом витамине.
Характерные жалобы пациентов с фолиево-дефицитной анемией – общая слабость и головокружения. Глоссит у таких больных, в отличие от больных B12-дефицитной анемией, развивается очень редко. Также при B9-дефицитной анемии не обнаруживаются признаки фуникулярного миелоза.
Как и при дефиците цианокобалавина, при дефиците фолиевой кислоты в периферической крови обнаруживается макроцитоз, повышается среднее содержание гемоглобина в эритроците и средний объем эритроцитов. В костном мозге появляются мегалобласты. Повышается уровень непрямого билирубина в крови, увеличивается активность лактатдегидрогеназы.
Дефицит фолиевой кислоты в организме приводит к повышению уровня гомоцистеина, что является фактором риска для образования венозных тромбов (из-за чрезмерного влияния гомоцистеина на эндотелий кровеносных сосудов). Гетерозиготное носительство мутации метилтетрагидрофолатредуктазы также является причиной высокого уровня гомоцистеина, однако риск образования тромбов при этом ниже.
Лечение фолиево-дефицитной анемии подразумевает применение препаратов фолиевой кислоты.
источник
В12-дефицитная анемия — довольно опасное заболевание, которое связано с нарушением нормальных процессов кроветворения, возникающих на фоне дефицита кобаламина в организме.
Современной медицине известно достаточно много причин, которые провоцируют развитие патологического состояния, но все они сводятся к недостатку витамина Б12 в организме человека. Поэтому причины В12 дефицитной анемии должны рассматриваться именно вкупе с причинами недостатка витамина.
Главными причинами развития заболевания являются:
Недостаточное поступление витамина B12 с пищей. Организм человека не в состоянии самостоятельно синтезировать данный витамин, он поступает только с пищей. Растения не содержат витамин B12, его источником служат только мясо, рыба, кисломолочные продукты. Как правило, эти продукты входят в рацион питания каждого человека, но в случае развития хронического алкоголизма или голодания, развитие В12 дефицитной анемии практически неминуемо.
Нарушение всасывания витамина В12 в кишечнике. Факторами, приводящими к нарушенной работе кишечника, являются:
- гастрит аутоиммунный или атрофический;
- рак желудка;
- врожденный дефицит внутреннего фактора Касла;
- воспалительные заболевания тонкого кишечника (энтериты);
- опухоли кишечника;
- паразитарные инфекции.
Повышенное использование организмом витамина B12. Взрослому человеку, для нормальной деятельности организма, требуется в сутки 3-5 мкг витамина. Но при определенных условиях потребность организма в витамине B12 значительно повышается, а произойти это может при:
- беременности – в плоде стремительно протекают процессы роста и деления клеток, что и требует большего количества витамина В12;
- гипертиреозе – в кровоток поступает большое количество гормонов щитовидной железы, обменные процессы усиливаются и организм требует большего количества рассматриваемого витамина;
- злокачественные опухоли – витамин Б12 активно потребляется такими новообразованиями и остальным отделам организма ничего не достается.
Наследственные заболевания, которые сопровождаются нарушением обмена витамина В12. К этому фактору можно отнести достаточно большую группу патологий, но мы выделим только несколько из них:
- синдром Имерслунд-Гресбека;
- дефицит транскобаламина II;
- нарушение использования витамина В12 в клетках.
Часто B12 дефицитная анемия развивается у веганов, не употребляющих животную пищу. Дело в том, что в пище растительного происхождения данный витамин не содержится, поэтому веганам следует употреблять продукты, искусственно обогащенные B12, а также специальные витаминные комплексы.
Запасы витамина B12 в организме человека достаточно большие, поэтому клинических проявлений анемии может и не быть длительное время. Заболевание развивается очень медленно и на начальных стадиях характеризуется слабостью, повышенной утомляемостью и сонливостью – абсолютно неспецифическими симптомами.
К основным клиническим проявлениям B12 дефицитной анемии относятся:
- головокружениями и частыми обмороками;
- бледностью кожных покровов;
- желтушностью слизистых оболочек;
- непереносимостью физических нагрузок;
- болями в области сердца;
- учащенным сердцебиением;
- появлением «мушек» перед глазами ;
- увеличением селезенки.
В принципе, при появлении только одного из вышеперечисленных проявлений, человек должен обратиться за квалифицированной помощью, ведь совсем необязательно, что одновременно будет присутствовать комплекс симптомов нарушения образования клеток крови.
Именно этот симптом является самым ранним признаком B 12 дефицитной анемии, а проявляться он будет:
- нарушением пищеварения;
- снижением аппетита;
- болью и жжением в полости рта;
- нарушением вкуса;
- боль в эпигастральной области после приема пищи;
- часто возникающими инфекциями в ротовой полости.
Обычно симптомы проявляются только в случае запущенной формы В12 дефицитной анемии и представляют собой:
- нарушения чувствительности в пальцах рук и запястьях;
- парестезии – онемения, «покалывания» в определенных местах тела;
- снижения мышечных сил;
- проблемы с мочеиспусканием и дефекацией.
Обратите внимание: все симптомы рассматриваемого заболевания являются неспецифичными, то есть могут свидетельствовать и о развитии других заболеваний. Поэтому врачи всегда их рассматривают только в комплексе с другими диагностическими данными.
Только лишь жалобы пациента на имеющиеся симптомы, которые описаны выше, не являются поводом диагностировать заболевание. Процесс диагностики Б12 дефицитной анемии достаточно сложный, так как понадобится провести следующие мероприятия:
- исследовать кровь путем проведения общего клинического и биохимического анализа в лабораторных условиях;
- сделать пункцию костного мозга.
А еще больного с подозрением или уже установленной В12 дефицитной анемией обязательно полностью обследуют, так как понадобится выяснить причину патологии.
Лечение проводится только комплексно, потому что перед врачами стоит задача максимально быстро восстановить нормальное функционирование кроветворной, пищеварительной и нервной систем.
Суть этого типа терапии заключается в введении витамина В 12 извне. Показаниями к назначению такого лечения являются подтвержденный диагноз Б12 дефицитной анемии и выраженная клиническая картина заболевания.
Чаще всего препарат витамина В12 вводится внутримышечно, но допускается и прием его внутрь в виде таблеток в случае точного установления факта недостаточного поступления витамина B12 с пищей.
Лечение заболевания начинают с внутримышечного введения 500-1000 мкг витамина В12 один раз в сутки. Продолжительность медикаментозного лечения составляет не менее 6 недель, затем врачи переводят пациента на поддерживающую терапию – дозировка в этом случае будет составлять 200-400 мкг препарата 2-4 раза в месяц. В некоторых случаях такая поддерживающая терапия проводится на протяжении всей жизни больного.
В период медикаментозного лечения B12 дефицитной анемии пациенту обязательно должен проводиться контроль эффективности терапии – 2-3 раза в неделю производят забор крови для лабораторного исследования. Как правило, уже через 1 месяц происходит полная нормализация показателей периферической крови, ослабление неврологических проявлений, восстанавливается работа пищеварительной системы. Как только пациент переводится на поддерживающую терапию, забор крови для анализа осуществляется один раз в месяц.

- тяжелая анемия, когда у пациента уровень гемоглобина составляет менее 70 г/л;
- анемическая кома, проявляющаяся потерей сознания.
Так как переливание крови назначается только при подтвержденном диагнозе, то одновременно с этой процедурой назначают и внутримышечное введение препарата витамина Б12. Но переливание крови или эритроцитарной массы прекращают сразу же, как только устранено угрожающее жизни состояние.
Часто В12 дефицитная анемия лечится диетой, но такое возможно только при своевременной диагностике заболевания. В меню больного должны быть включены продукты, богатые витамином B12 и важные для лечения анемии:
- сок сливы;
- зеленые овощи, зелень, салаты и зерновые завтраки;
- мясо, сливки и масло;
- свекла, морковь, кукуруза, помидоры;
- субпродукты – говяжья и куриная печень, сердце;
- треска, карп, скумбрия;
- крольчатина.
Важно питаться полноценно и разнообразно. Вот примерное меню на день для больных с диагностированной В12 дефицитной анемией:
- 1 завтрак – салат из свежей капусты с добавлением яблок и сметаны, омлет, каша овсяная молочная с молоком;
- 2 завтрак – чай и 100 грамм сыра (максимальное количество);
- обед – борщ на мясном бульоне со сметаной, курица жареная с отварным рисом и компот;
- полдник – отвар шиповника;
- ужин – зразы мясные с луком и яйцом, морковное пюре, запеканка из гречневой крупы с творогом, некрепкий чай;
- на ночь – кефир.
Если рассматриваемое заболевание было диагностировано на ранней стадии своего развития, сразу же было назначено и проводится лечение, а нормализация показателей периферической крови произошла уже через месяц — полтора, то прогнозы будут исключительно благоприятными. Как только будет проведена основная терапия, состояние здоровья восстанавливается и пациент возвращается к привычному ритму жизни. Но если есть:
- позднее начало лечения;
- симптомы поражения центральной нервной системы;
- отсутствие эффекта от проводимого лечения;
- наследственная форма В12 дефицитной анемии.
То прогнозы будут неблагоприятными. Скорее всего, больной вынужден будет проходить лечение всю жизнь, нередко тяжелая форма В12 дефицитной анемии заканчивается комой и летальным исходом.
B12 дефицитная анемия – состояние, не опасное для жизни, но весьма коварное. Если человек обращает внимание на самые ранние признаки болезни, то врач сможет быстро и установить причину развития заболевания, и провести эффективное лечение.
Понижение уровня гемоглобина в крови, преимущественно на фоне падения числа эритроцитов, в медицине известно как анемия – заболевание, являющееся симптомом разных патологических состояний. Одной из разновидностей анемии является гиперхромная, особенно часто поражающая лиц зрелого и преклонного возраста. Почему она возникает и как ее лечить?
Заболевание, известное большинству людей как малокровие, в официальной медицине названное «анемия», связано с падением уровня гемоглобина. При гиперхромной форме одновременно с этим снижается количество здоровых эритроцитов и появляются дефектные: содержащие в себе избыток железа. Благодаря этому веществу кровяные тельца становятся пресыщены гемоглобином, поэтому срединное просветление у них закрыто алым цветом (это видно при лабораторном исследовании анализов). Существует 2 вида анемии гиперхромной:
- Мегалобластная (макроцитарная) – характеризуется нарушением синтеза ДНК и РНК, что приводит к появлению очень крупных эритроцитов (мегалобластов и мегалоцитов) в костном мозге. Такая анемия может передаться по наследству.
- Немегалобластная – синтез ДНК в норме, костный мозг не продуцирует мегалобласты, но дефектные эритроциты присутствуют.
Большинство врачей не считают анемию самостоятельным заболеванием, поскольку она может развиться на фоне первичного поражения системы крови или при иных патологиях, никак с этим не связанных. По этой причине отсутствует строгая нозологическая классификация и, помимо уже упомянутого деления гиперхромного типа на 2 вида, существует группировка по состояниям, которым она соответствует:
- Витамин В12-дефицитная (пернициозная) анемия – болезнь Аддисона-Бирмера, злокачественное малокровие, обусловленное нехваткой витамина В12. Характеризуется образованием в костном мозге незрелых мегалобластов, может проявляться неврологическими расстройствами.
- Фолиеводефицитная анемия – тоже пернициозная, только возникает при дефиците фолиевой кислоты.
- Миелодиспластический синдром – характеризуется цитопенией (дефицит 1-ого или нескольких видов кровяных телец) в периферической крови, дисплазией (неправильным развитием) костного мозга. Заболевание склонно к переходу в острую форму лейкоза (недоброкачественное поражение системы кроветворения), тяжело поддается лечению (преимущественно проводится поддерживающая терапия). По официальной статистике 80% пациентов с миелодиспластическим синдромом старше 60-ти лет.
Дефицит витамина В12 (цианокобаламин) и фолиевой кислоты являются самыми распространенными отправными точками к развитию анемии гиперхромного типа, но эти состояния могут возникать под воздействием целого ряда факторов. Конкретный перечень причин для каждой ситуации свой. Нехватку цианокобаламина провоцируют:
- патологические процессы в подвздошной кишке, при которых происходит нарушение усвояемости питательных веществ за счет плохого всасывания ее стенками;
- инфекционные патологии кишечника, тоже нарушающие процесс всасывания витаминов;
- глисты – ленточные черви и бактерии активно поглощают витамин В12;
- атрофический гастрит, при котором в париетальных клетках желудка наблюдается недостаточный синтез внутреннего фактора Касла (фермент, который переводит цианокобаламин из неактивной формы в усваивающуюся).
У анемии гиперхромного типа, которая возникает как результат дефицита фолиевой кислоты, провоцирующие факторы выглядят иначе. Зачастую с таким состоянием сталкиваются женщины во время беременности, поскольку вся фолиевая кислота идет на строительство нервной трубки плода. Влияние могут оказывать и:
- алкоголизм;
- заболевания печени (особенно гепатит, цирроз, печеночная недостаточность).
Отдельно врачами упоминается гиперхромная макроцитарная анемия, которая носит наследственный характер (аутосомно-рецессивная передача – от родителей) и развивается на фоне генетических мутаций, а у женщин предпосылкой к ее возникновению является и прием гормональных препаратов. Если не рассматривать отдельные разновидности анемии, при которой у эритроцитов появляются гиперхромные ядра, в число общих причин можно включить:
- длительное голодание или нерациональное питание (с дефицитом витаминов и микроэлементов в пище);
- курение;
- наличие опухолей;
- инфекции (особенно ВИЧ) и вирусы;
- регулярная большая потеря крови во время менструации;
- рак желудка, гастрэктомия (его полное вырезание);
- гипотиреоз (дефицит гормонов щитовидной железы);
- прием лекарственных препаратов (Метформин, Неомицин, Дифенин);
- частые расстройства кишечника.
Заболевание имеет внешние и внутренние проявления: последние подразумевают изменения общего самочувствия, которые не всегда специфичны и не дают возможности поставить точный диагноз. К таким симптомам гиперхромного малокровия относятся:
- повышенная сонливость, усталость;
- снижение работоспособности;
- потеря концентрации внимания.
Данная клиническая картина характерна большинству случаев анемии, поэтому болезнь распознается исключительно после проведения лабораторных исследований. Если течение более тяжелое, могут добавиться:
- тахикардия (учащенный пульс);
- одышка при минимальных физических нагрузках (даже после быстрой ходьбы);
- шум в ушах (не постоянный);
- нарушения сна;
- потеря аппетита;
- головные боли;
- снижение либидо (полового влечения).
Почти во всех случаях гиперхромного малокровия можно наблюдать изменения во внешности: кожные покровы бледнеют, кожа истончается, становится сухой, на руках может приобрести желтоватый оттенок. В волосах появляется ранняя седина. Общая клиническая картина выраженной анемии дополняется следующими симптомами:
- потеря веса;
- расстройство зрения и слуха;
- тошнота, рвота;
- потеря вкуса, отсутствие влечения к ранее любимым продуктам и блюдам;
- мышечная слабость;
- онемение нижних конечностей;
- чувство зябкости;
- покраснение языка до малинового цвета, поверхность становится блестящей.
Лица, у которых гиперхромная анемия сочетается с миелопластическим синдромом, часто испытывают головокружения, повышенную утомляемость. Не исключены боли за грудиной при сильном сердцебиении и одышке. При сильном поражении нервной системы у пациента нарушается чувствительность пальцев (на ногах и руках), могут случаться потеря сознания, судороги. Артериальное давление преимущественно пониженное, печень увеличена (прощупывается при пальпации).
Авитаминоз по фолиевой кислоте для будущей матери – распространенное явление, поскольку этот элемент (вместе с цианокобаламином) требуется для полноценной жизнедеятельности плода. Потребность в витаминах В9 и В12 у беременной вырастает в 2 раза. При стремительном развитии и тяжелом течении анемия может спровоцировать преждевременные роды, недостаточный вес новорожденного, отслоение плаценты, внутриутробные кровотечения.
У детей анемия, при которой наблюдается гиперхромия эритроцитов, может привести к отставанию в развитии умственном и физическом, снижении защитных сил организма (ребенок будет часто подхватывать ОРВИ, тяжело переносить даже простуду). У взрослых распространенным осложнением анемии являются дефицит кислорода в крови, поражения нервной системы, на фоне чего возникают:
- гипоксия (кислородное голодание) мозга;
- ухудшение памяти и мышления;
- отмирание клеток головного мозга и нарушения работы его сосудов;
- сердечная недостаточность (может окончиться летальным исходом).
Отсутствие специфической клинической картины для анемии любого типа повышает значимость диагностических мероприятий для уточнения заболевания. Общий анализ крови является первичной проверкой, по результатам которой можно увидеть изменения в структуре эритроцитов (форма и размеры клеток), обнаружить ядерные тельца Жолли. При наличии подозрений на гиперхромное малокровие врач дополнительно назначает:
- биохимическое исследование крови – для определения уровня билирубина, сывороточного уровня железа;
- рентгеноскопию ОБП (органов брюшной полости);
- УЗИ органов пищеварения;
- иммунологическое исследование – помогает выявить антитела, которые специфичны против антигенов цитоплазмы париетальных клеток желудка и внутреннего фактора Касла.
Для легких форм гиперхромного малокровия основу терапевтической схемы составляет коррекция рациона питания, особенно если проблема кроется в дефиците фолиевой кислоты или витамина В12. Дополнительно за день важно принимать с едой 8 мг железа. Меню базируется на следующих продуктах:
- печень куриная, говяжья (2-3 раза в неделю);
- гречневая крупа;
- рыба (особенно треска);
- мясо (желательно ввести в рацион кролика);
- куриные яйца;
- сыры;
- бобовые культуры.
Обязательно употребление свежих овощей и фруктов, дополняющих список полезных при анемии продуктов. От острой и жареной пищи стоит отказаться, поскольку она раздражает пищеварительную систему. Кофеин тоже исключен, поскольку он мешает усваиваться железу. Такой диеты следует придерживаться несколько месяцев (в некоторых случаях – больше года), она актуальна для всех стадий заболевания, но не исключена индивидуальная коррекция рациона под конкретную клиническую картину. Медикаментозное лечение зависит от причин анемии и ее течения:
- Терапия легких дефицитных состояний начинается с назначения Цианокобаламина: синтетического аналога витамина В12, который принимается перорально или вводится внутримышечно. Если спустя 1-1,5 недели после начала его использования положительной динамики не наблюдается, врач выписывает Фолиевую кислоту (таблетки), Фемибион. В некоторых случаях проводится одновременное лечение обоими препаратами.
- При средней степени выраженности анемии Цианокобаламин или Оксикобаламин (более сильный препарат для тяжелых случаев) вводятся внутривенно и на 5-8 день отслеживается уровень ретикулоцитов: их количество должно возрасти на 20-30%.
- По необходимости назначаются препараты железа – Мальтофер, Гемофер (таблетки, инъекции), особенно если заболевание диагностировано у ребенка.
- Во время беременности (или после родов, если состояние не улучшается) врач может назначить пациентке внутривенное введение витаминных препаратов, начиная с больших доз. После они уменьшаются, а инъекционная форма заменяется на пероральную.
Восстановление показателей крови происходит быстро: уже через месяц можно видеть результат, а неврологические нарушения устраняются медленнее и могут требовать дополнительных препаратов. Если начальную (легкую) форму гиперхромного малокровия можно лечить амбулаторно (дома), то средняя и тяжелая требуют помещения пациента в стационар, где ему будут делать инъекции лекарственных средств и постоянно отслеживать состояние. Несколько моментов лечения таких случаев анемии:
- Резкое нарушение гемодинамики, падение гемоглобина ниже 70 г/л (тяжелая форма анемии) требуют немедленной гемотрансфузии – переливания крови.
- При миелодиспластическом синдроме обязательны госпитализация, гемотрансфузия (переливаются эритроцитарная и тромбоцитарная массы, зачастую с замещением клеток) и внутривенное введение препаратов, ускоряющих деление кровяных телец, чтобы предотвратить лейкоз.
- Если лечение подразумевает инъекционное введение лекарственных средств одновременно с приемом таблеток, такой курс длится 2-3 месяца. После раз в неделю делают 1 укол, оставляя таблетки, а через 2 месяца их ставят с частотой 1 раз в 14 дней. Основной формой лечения не тяжелых состояний являются таблетки.
Лечение анемии гиперхромной длится от полугода до года, дефицитные состояния за этот срок полностью устраняются. При миелодиспластическом синдроме терапия стационарная, прогноз неутешительный, поскольку препараты только способствуют увеличению срока жизни и сдвигают момент ремиссии. Шансы на исключение летального исхода возникают только при пересадке костного мозга.
Соблюдение принципов здорового питания, поддержание хорошего уровня витаминов В9 и В12, железа – самый простой и важный способ защиты от гиперхромного малокровия, особенно для беременных. Диета, используемая для его лечения, одновременно носит и профилактический характер. Дополнительно стоит:
- регулярно посещать гастроэнтеролога;
- заниматься спортом;
- отказаться от курения;
- не контактировать с ядохимикатами;
- гулять на свежем воздухе;
- своевременно лечить инфекционные заболевания, выводить паразитов;
- принимать витаминно-минеральные комплексы.
источник