Анемия – обширное заболевание с недостаточностью железа. Апластическая анемия – малокровие, которое развивается вследствие заболевания костного мозга. А именно – прекращения функционирования костного мозга.
Причина кроется в поражении систем организма различного происхождения. Сюда входит:
Какова же симптоматика апластической анемии? Симптомы разнообразны. В основном клиника напоминает любую другую анемию. К симптомам можно отнести:
— бледность слизистых оболочек;
В конечной стадии наблюдаются некрозы и сепсис.
Для более подробной информации зайдите на сайт: bolit.info
В любом случае проконсультируйтесь с врачом!
Апластическую анемию можно предупредить. Профилактика будет заключаться в постоянном медицинском наблюдении. Если вас беспокоят симптомы, напоминающие анемию. Срочно обратитесь к специалисту!
Проходите чаще лабораторные методы исследования крови! Анализ крови наиболее подробно покажет присутствующую патологию. Это поможет вовремя сменить профессию. Если условия труда неблагоприятны для работы.
Неспецифическая профилактика будет заключаться в изоляции с очага облучения. Как известно данный очаг неблагоприятно сказывается на здоровье организма. Особенно, если это касается костного мозга.
Прежде всего, врач должен обратить внимание на жалобы пациента. Диагностика будет заключаться на основе субъективных и объективных данных. Осмотр специалиста включает в себя образования на коже. А именно – кровоизлияния.
Затем собирается анамнез. То есть наследственные данные. Были ли случаи заболевания среди родственников. Также как давно пациента беспокоят данные симптомы. Есть ли вредные привычки.
Важным компонентом диагностики будет исследование крови. Лабораторные анализы покажут нам пониженное количество эритроцитов и снижение уровня гемоглобина.
Анализ мочи будет свидетельствовать о воспалительном процессе и кровоточивости. Можно отнести еще исследование костного мозга. В данном случае проводится пункция кости.
Апластическая анемия – явление достаточно редкое. У взрослых данное заболевание развивается остро с рецидивами и осложнениями. Апластической анемии подвержены одинаково, и женщины, и мужчины. Чаще молодого возраста.
Если своевременно начать лечение, то шансы есть. В чем же заключается лечение данного заболевания? Лечение будет заключаться в гемотрансфузии. То есть переливание крови и ее компонентов. А именно – эритроцитарная масса.
Хлористый кальций тоже используется в лечении. Витамин А, фолиевая кислота. Антибиотики – пенициллин и стрептомицин. Длительный курс лечения гормонами. К ним относят преднизалон и кортикозон.
Апластическая анемия у детей протекает не так тяжело, как у взрослых. С чем это может быть связано. Чаще у детей данное заболевание возникает как следствие вируса. А именно – дети, перенесшие вирусную инфекцию. Наследственные факторы тоже имеют место при заболевании. По статистике, вирусная инфекция – гепатит становится причиной апластической анемии. У детей осложнения наблюдаются реже. Диагностика будет заключаться в исследовании мочи и крови. А также анамнез и осмотр.
Лечение данного заболевания будет заключаться в приеме антибиотиков по возрастным показаниям. Симптоматическое лечение показано в любом возрасте. Конечной точкой будет пересадка костного мозга, но при условии необратимых осложнений.
Прогноз будет зависеть от своевременности лечения. Чем раньше начали лечение, тем лучше прогноз! Известно, что почти 90% больных погибают от апластической анемии. Данный факт опирается на своевременность лечения.
Если проведено трансплантация костного мозга, то шансов выжить гораздо больше. Все зависит от конкретного человека. Ну и, конечно же, от грамотного специалиста. Правильной диагностики данного заболевания.
Если прогноз неблагоприятный, то рассчитывать на хороший исход не придется. Все чаще не леченные вовремя болезни приводят к летальному исходу. Апластическая анемия – не исключение!
Если вы хотите сохранить жизнь себе и близким, то обращайтесь к врачу. Осложнения, которые вызваны данным заболеваниям все чаще приводят к смерти.
Инсульт, кома, хронические заболевания – неблагоприятный исход апластической анемии. Известно, что эти болезни не приведут к счастливой и долгой жизни!
У людей вовремя не вылеченных от данной болезни продолжительность жизни резко сокращается! По статистике в течение одно года погибает большее количество больных.
При трансплантации костного мозга выживаемость значительно возрастает. На четыре года больше. Примерно у 10 из 11 больных.
Если человеку вовремя провели лечебный курс, то выживаемость повышается. Больной может прожить и семь, и восемь лет. Поэтому не откладывайте визит к врачу! Будьте более внимательными к своему здоровью!
источник
При апластической анемии терапией намечаются следующие цели (Берчану):
1) устранение обусловившей заболевание причины;
2) достижение наиболее полной ремиссии путем:
а) замещающего лечения, чтобы обеспечить необходимое время для восстановления костного мозга;
б) лечения инфекционных осложнений;
3) стимулирование кроветворения.
Отдельные гигиенические мероприятия представляются обязательными, в этой связи больным указывать на необходимость избегать кожные инфекции — применением антисептических веществ, инфекции дыхательных путей — избегая места большого скопления людей. Рекомендуется также избегать физическую травму вызывающую кровотечение.
Замещающее лечение при апластической анемии. Наиболее целесообразным представляется переливание крови. Всеми рекомендуется этот способ лечения когда показатель гемоглобина понижается до менее 8 г/100 мл. Перфузия тромбоцитной массой показана при тяжелом геморрагическом синдроме, в то время как переливание концентрата гранулоцитов необходимо при осложнении болезни инфекцией неподдающейся обычной антибиотикотерапии.
Терапия инфекций при апластической анемии. Рекомендуются культуры крови, мочи, желчи, кожных поражений, мокроты и пр. в целях выявления возбудителя. Однако в срочных случаях до получения результата от культур и антибиограммы, целесообразно назначать антибиотик широкого диапазона действия, например ампициллин. Полезно не забывать, что у таких больных довольно редкие инфекции как, например, гистоплазмой, кандидой, аспергиллом — частое явление.
Страдающих тяжелой формой агранулоцитоза или нейтропении (менее 500/мм3) изолировать, преимущественно в стерильные комнаты.
Лечение кортикостероидными гормонами при апластической анемии. Такое мероприятие оправдывает себя во многих случаях апластической анемии (для стимулирования кроветворения, при геморрагическом синдроме, сопутствующем расплавлении крови и пр.). Большинством авторов рекомендуется 1—2 -месячный курс лечения умеренными дозами (от 30 до 50 мг. в сутки). Если за этот срок не отмечаются положительные результаты, прекратить лечение.
Лечение, стимулирующее костный мозг при апластической анемии. До настоящего времени, в частности у больных детского возраста, наиболее эффективным представляется применение андрогенных гормонов.
Видимо мужские гормоны обусловливают выделение эритропоэтина и сенсибилизацию кроветворной ткани к этому веществу. С особым успехом, в частности детям, применяется синтетический тестостерон (оксиметолон), причем медикамент назначается внутрь, дозами от 2 до 4 мг на кг. веса тела в сутки. Когда этот медикамент отсутствует, может оказаться полезным и тестостерон-пропионат принимаемый также внутрь из расчета 0,25 мг/кг веса тела/сутки. Лечение проводить не менее 3 месяцев.
Отдельные авторы назначают это лечение на сроки, достигающие 9 месяцев. Разные статистические материалы и данные разведочных исследований не выявляют какой-либо существенной разницы между леченными андрогенами и иными способами.
Многочисленные эксперименты доказали роль карбоната лития в поощрении продукции моноцитами фактора, стимулирующего колонии. До настоящего времени не проводились разведочные работы, однако авторы, сделавшие попытки в этом направлении рекомендуют назначение карбоната лития из расчета 450—600 мг/сутки в течении 3—4 недель, при условии наличия в костном мозге гранулоцитных предшественников и периодической проверки уровня лития в крови. Отсутствие положительного результата вскрывает нецелесообразность дальнейшего применения этого лечения (Williams, Ward).
При костномозговой аплазии после облучения смертельными дозами Mathe применял пересадку костного мозга с весьма хорошими результатами. После успешного завершения этого эксперимента и до настоящего времени в технике пересадки органов — — вообще, и костного мозга — в частности, достигнуты существенные прогрессы.
В данный момент пересадка составляет терапевтический метод выбора в случаях заболевания молодых людей тяжелой апластической анемией (Geary).
Критерии для постановки диагноза тяжелой апластической анемии следующие: анемия с наличием 1% ретикулоцитов, 500/мм3 гранулоцитов, 20 000/мм3 тромбоцитов и в результате биоптического исследования пораженного гипоплазией костного мозга — 25% нормальной клеточной массы.
Статистические данные центров (Seattle), применяющих эту терапию, указывают на полную ремиссию у 50% больных, в противоположность 10% — леченных условными способами (Thomas D., Sterb).
При этом возникают следующие проблемы:
— отбор доноров костного мозга путем стандартизации по системе «Human Leucocytes Antigen» (HLA) и осуществеления смешанных культур лимфоцитов. По статистическим материалам в системе HLA, у половины какой-либо данной группы больных отмечено сходство с их родственниками, в то же время в пределах семьи шансы совместимости оцениваются до 25%;
— даже при строгой совместимости — отдача трансплантата наблюдается в 26% случаев.
Существует ряд способов годготовки больных в целях облегчения пересадки и избежания явления отдачи.
Применение циклофосфамида составляет стандартный метод лечения, но больным, в отношении которых тест лимфоцитотоксичности показывает предварительную сенсибилизацию к костному мозгу донора, назначаются прокарбазин, глобулин антитимоцит и общее облучение. Недавно в Seattle начало применяться циклофосфамид в сочетании с периферическими одноядерными клетками донора для дополнения клеток-штамм, при этом полученные результаты — обнадеживающие.
Известно, что у примерно 80% больных с предварительной сенсибилизацией наблюдается явление отдачи трансплантата.
После пересадки назначается метотрексат в целях предупреждения явления «трансплантат против хозяина», которое, в течение ближайших трех месяцев после операции, составляет причину 20% смертных исходов.
Однако тяжелые инфекции составляют причину остальных, быть может даже большинства, смертных исходов.
Отмечается также развитие интерстициальной пневмонии у 68% больных и заболевание вызываемое цитомегалическим вирусом или Pneumocystis carinii (Silver).
До настоящего времени результаты обнадеживающие. В этой связи отмечаются большая продолжительность выживаемости страдающих костномозговой аплазией с хорощо приживленным трансплантатом, чем у леченных условными способами (Storb и Thomas) и, как уже было сказано, более высокий процент полной ремиссии.
Иммуносупрессорная терапия (циклофосфамидом и пр. средствами) испробована при генуинной апластической анемии, поскольку были выявлены некоторые иммунологические механизмы (Ascensao). Недавно была сделана попытка лечения этого заболевания либо только антилимфоцитным глубилином, либо сочетая его с костномозговой пересадкой (Geary). Статистическими данными еще не подтверждена эффективность такого лечения, однако прогрессы, достигнутые в деле выявления иммунологических механизмов при апластической анемии сделают возможным отбор больных для иммуносупрессорной терапии.
С той же иммуносупрессорной целью проводилась спленэктомия, но лишь с частично положительными результатами (Берчану).
источник
Новые медикаменты и пересадка костного мозга помогут людям с апластической анемией жить полноценной жизнью гораздо дольше.
Кровь — это жизнь. Но редкая болезнь под названием апластическая анемия лишает организм жизни, лишая организм крови. (23.03.2008 — HealthDay Новости). Кровь пациентов с апластической анемией становится обедненной клетками крови, так как костный мозг замедляет их производство. Симптомы заболевания могут варьироваться в зависимости от того, какого типа клеток крови больше всего не хватает. Это может быть хроническая усталость, болезни сердца, бесконечные инфекций, понижение свертываемости крови.
Но есть надежда. Не смотря на то, что как два десятилетия назад, так и как в последнее время, болезнь часто оканчивается смертельным исходом, в настоящее время апластическая анемия становится гораздо более управляемым заболеванием. Достижения в области медикаментозной терапии и успехи в области трансплантации позволили сократить число летальных исходов, что позволяет пациентам жить полноценной жизнью гораздо дольше.
«Мы совершенствуем методы лечение апластической анемии — либо полностью вылечиваем заболевание, либо лечим ее симптомы», говорит д-р Ярослав П. Мациежевский (Dr. Jaroslaw P. Maciejewski, Cleveland Clinic’s Department of Hematologic Oncology and Blood Disorders). И эти успехи помогают врачам лучше понять другие, имеющие более широкое распространение заболевания, такие как болезни сердца и лейкемия.
По данным Национальных институтов здравоохранения ежегодно в США регистрируется 50 тысяч случаев апластической анемии и 20-30 тысяч случаев миелодиспластического синдрома (миелодиспластический синдром или МДС — это подобное апластической анемии заболевание крови, которое возникает тогда, когда костный мозг начинает производить плохо функционирующие или незрелые клетки крови).
Важно отметить, что многие симптомы апластической анемии, такие как усталость и инфекции, также могут быть вызваны другими заболеваниями, говорит д-р Роналд Пакетт (Dr. Ronald Paquette, a blood disease researcher with the University of California, Los Angeles’ Jonsson Comprehensive Cancer Center) специалист по заболеваниям крови в Калифорнийском университете.
Костный мозг — это губчатый материал внутри кости, который производит стволовые клетки, которые в свою очередь превращаются в три типа клеток крови — эритроциты, лейкоциты и тромбоциты. «По существу, костный мозг – это завод крови», — говорит Мациежевский. У больных с апластической анемией, стволовые клетки повреждаются, вследствие чего происходит замедление или остановка производства всех клеток крови.
Причина повреждения стволовых клеток остается неизвестной в более чем половине случаев заболеваний апластической анемией. Согласно научным исследованиям Национального института здоровья есть предположение, что стволовые клетки повреждаются, когда иммунная система человека атакует свои собственные клетки организма по ошибке.
Некоторые случаи апластической анемии были связаны с воздействием токсинов, таких как пестициды, мышьяк и бензол. Инфекционные заболевания также могут привести к нарушениям приводящим к апластической анемии. Это инфекционные заболевания как гепатит, вирус Эпштейна-Барра, цитомегаловирус, парвовирус B19, ВИЧ, а также аутоиммунные заболевания, такие как системная красная волчанка и ревматоидный артрит. Наконец, некоторые генетические нарушения могут привести к апластической анемии.
Симптомы апластической анемии зависят от типа клеток крови, которых больше всего не хватает в организме:
— Недостаток эритроцитов может привести к нехватке кислорода в организме. Люди, у которых низкий уровень эритроцитов нередко чувствуют себя усталыми. Из-за того, что сердце должно работать быстрее и напряженнее, чтобы снабдить органы и ткани кислородом, со временем могут развиться сердечно-сосудистые заболевания.
— Недостаток лейкоцитов может ослабить иммунитет человека. Человек может чаще болеть инфекционными заболеваниями, и обычные болезни могут проходить в тяжелой форме.
— Недостаток тромбоцитов, снижает способность крови свертываться. Пациенты с низким уровнем тромбоцитов могут иметь большое количество синяков и гематом. Возможны кровотечения, которые трудно остановить.
«После того, как человеку поставлен диагноз апластическая анемия необходимо сразу начать лечение», — говорит д-р Пакетт. «Очень важно, чтобы лечение было в специализированном центре, так как это очень редкое заболевание» — сказал он. «Самое главное заключается в том, чтобы вас наблюдал специалист с большим опытом лечения заболеваний на ранней стадии».
Для пациентов моложе 30 лет трансплантация стволовых клеток является предпочтительным методом лечения. Для тех, у кого есть родственный донор (подходящие брат или сестра), проводят трансплантацию стволовых клеток, здоровые стволовые клетки донора заменяет дефектные клетки костного мозга больного человека. По данным Международного фонда апластической анемии и МДС более 80% процентов пациентов полностью выздоравливают (Aplastic Anemia & MDS International Foundation Inc.)
По мнению д-ра Пакетта достижения в области исследования стволовых клеток и препаратов против отторжения донорских клеток привели к тому, что трансплантации от неродственных доноров также становятся все более успешными.
Одним из перспективных направлений лечения является трансплантация стволовых клеток пуповинной крови. «Стволовые клетки пуповинной крови новорожденных младенцев можно замораживать и сохранять в банке клеток, чтобы позже использовать как донорские клетки, как для новорожденного (в случае возникновения у него тяжелых заболеваний), так и для неродственной трансплантации», говорит д-р Пакетт. — «Это очень обнадеживает».
Для пациентов с апластической анемией важно начать лечение как можно скорее. «Как показывают исследования, чем раньше была сделана пересадка костного мозга с момента постановки диагноза, тем лучше результат» — считает Пакетт.
Больные, у которых нет донора, или те, для которых трансплантация невозможна по медицинским показаниям, часто получают иммуносупрессивную терапию такими препаратами как антитимоцитарный глобулин и циклоспорин. По данным Международного фонда апластической анемии и МДС положительная динамика в результате иммуносупрессивной терапии наблюдается в 70-80% случаев.
Переливание крови от подходящего донора также помогает поддержать показатели крови на высоком уровне. Это помогает облегчить симптомы заболевания, хотя этот метод не является эффективными при длительном лечении.
«Так или иначе, вылечиваем ли мы болезнь или нет, в любом случае состояние пациента можно улучшить «, говорит д-р Ярослав П. Мациежевский. — «Теперь мы можем сохранить жизнь людям с апластической анемией или продлить им жизнь на долгие годы».
источник
Одним из самых редких, но тяжелых заболеваний системы кровообращения считается апластическая анемия, симптомы, причины, методы лечения этого вида малокровия бывают различны. Все зависит от формы, вида и степени тяжести данной патологии.
Люди, далекие от медицины, зачастую не имеют представления о том, что такое апластическая анемия. Так называется расстройство кроветворной функции костного мозга, ведущее к снижению выработки кровяных клеток. Это приводит к серьезным патологическим изменениям во всех системах человеческого организма. Очень часто заболевание заканчивается летально.
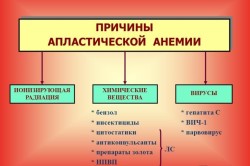
Этиология апластической анемии до сих пор досконально не изучена. Поэтому окончательный список причин данного заболевания все еще полностью не составлен. На данный момент основными причинами апластического малокровия считаются:
- плохая экология в регионе проживания;
- ионизирующая радиация;
- постоянные контакты с опасными химическими веществами в течение долгого времени;
- отдельные инфекционные заболевания: гепатит, цитомегаловирус;
- разрушение костного мозга под воздействием некоторых медикаментозных средств при их длительном приеме в высоких дозах, особенно левомицетина, мышьяка, бензола, химических препаратов, противоопухолевых средств, антибиотиков;
- генетическая предрасположенность;
- беременность;
- патологии костного мозга;
- злоупотребление алкоголем.
Возникновение апластической анемии у детей сразу после рождения может быть спровоцировано такими причинами, как:
- врожденный сифилис;
- токсоплазмоз;
- генерализованный мегалоцитоз.
Часто у детей диагностируется идиопатическая апластическая анемия. В этом случае определить точную причину возникновения патологии не представляется сегодня возможным.
При гипопластической анемии наблюдается еще более серьезное расстройство кроветворной функции костного мозга. В целом гипопластические и апластические анемии вызывают сходные патологии органов и систем организма, имеют похожую симптоматику и лечатся примерно одинаково.
Костный мозг образуется губчатой структурой и располагается в глубине трубчатых костей. Посредством его структуры происходит выработка различных клеток крови: лейкоцитов, тромбоцитов, эритроцитов.
При апластической анемии, прежде всего, нарушается эритрогенез. Стимулировать этот процесс медикаментозными средствами невозможно. В этом случае может помочь только пересадка донорского костного мозга.
Помимо этого, апластичная анемия развивается на фоне уменьшения количества и изменения функций стволовых клеток.
Причиной этого становится нарушение микроокружения, клеточное или гуморальное воздействие иммунного характера, препятствующее нормальному функционированию стволовых клеток.
Апластическая анемия, симптомы которой часто незаметны, является серьезной патологией. В отдельных случаях недуг начинается в острой форме с быстрым нарастанием симптоматических проявлений. Развитие болезни может быстро прогрессировать, приводя к летальному исходу. Возможно также хроническое с периодическими ремиссиями и рецидивами протекание анемии.
Апластическая анемия симптомы имеет следующие: анемический, геморрагический и лейкоцитопенический синдромы. Для каждого из них характерны определенные признаки.
Анемический синдром (снижение уровня гемоглобина) возникает при нарушении формирования эритроцитов и сопровождается такими симптомами, как:
- общая слабость;
- сонливость;
- бессонница;
- раздражительность;
- одышка;
- шум в ушах;
- тахикардия;
- бледность кожных покровов;
- быстрая утомляемость.
Геморрагический синдром (повышение кровоточивости) вызван понижением уровня тромбоцитов в крови. Его сопровождают такие симптомы, как:
- петехии, т. е. точечные кровоизлияния на коже и слизистых оболочках и гематомы;
- плохая свертываемость крови;
- десневые и носовые кровотечения;
- появление крови в моче;
- обильные менструальные выделения у женщин.

Он сопровождается следующими симптомами:
- появление хронических очагов инфекции в различных органах и на поверхности кожи больного;
- учащение инфекционных заболеваний, протекающих длительно и со многими осложнениями;
- стоматит;
- внезапная гипертермия без видимых причин.
По форме апластическая и гипопластическая анемия может быть как врожденной, так и приобретенной.
После проведения анамнестической беседы врач проводит общий осмотр пациента. При этом обязательно применяются такие методы, как:
- выслушивание (аускультация) сердечных шумов;
- простукивание (перкуссия) живота, показывающая увеличение таких органов, как печень и селезенка;
- прощупывание (пальпация) для уточнения результатов перкуссии.
Для получения дополнительных сведений больному назначается:
- общий анализ крови;
- биохимический анализ крови;
- клинический анализ крови — гемограмма;
- забор мазка — биопсия, костного мозга;
- анализ мазка костного мозга, на основании которого составляется миелограмма.
При необходимости больному проводятся специальное тестирование, помогающее уточнить причину заболевания.
На основании всех полученных данных составляется точная клиническая картина заболевания, необходимая для определения курса лечения.
Когда больному диагностируется апластическая анемия, лечение проводится по 3 направлениям: этиологическому, симптоматическому и патогенетическому. Если известна точная причина возникновения заболевания, ее необходимо ликвидировать: прекратить контакт с токсинами, сменить лекарственные препараты, используемые для лечения других заболеваний и т. д.
Восстановлению кроветворного функционирования костного мозга помогают следующие препараты:
- кортикостероиды;
- андрогены;
- цитоксины;
- иммуносупрессоры.
Помимо медикаментозной терапии лечение апластической анемии проводится при помощи таких процедур, как переливание крови и ТКМ. Посредством переливания донорской крови организм больного частично обеспечивается недостающими кровяными клетками.
В особых случаях больным проводится трансплантация костного мозга. Костный мозг донора должен максимально соответствовать костному мозгу реципиента. Поэтому этот метод особенно эффективен, если у больного есть однояйцевый близнец. Процент выживаемости после трансплантации костного мозга выше у реципиентов более молодого возраста.

Основными факторами, влияющими на получение положительных эффектов, являются:
- Степень тяжести заболевания.
- Правильный выбор и хорошая переносимость лечения.
- Возраст больного. Легкая апластическая анемия у детей и молодых людей, не достигших 30-летнего возраста, полностью вылечивается чаще, чем у людей среднего и старшего возраста. При тяжелых формах болезни прогнозы не столь благоприятные.
Основным условием ремиссии и значительного продления жизненного срока является хорошая переносимость патогенетической терапии и успешное проведение трансплантации костного мозга.
Профилактика анемии различного вида может быть первичной или вторичной. Первичная профилактика предполагает исключение возможности развития данной патологии у относительно здорового человека. Этого можно добиться при помощи таких способов, как:
- ведение здорового образа жизни;
- правильное питание;
- постоянное укрепление иммунной системы;
- исключение или сведение к минимуму контакта с ионизирующими излучателями и токсичными веществами, вызывающими патологии костного мозга;
- контролированный прием лекарственных препаратов во время лечения других заболеваний;
- периодические визиты к терапевту и гематологу;
- полный отказ от употребления алкоголя и никотина.
Вторичная профилактика анемии проводится для замедления развития заболевания, избегания его осложнения сопутствующими патологиями. Для этого необходимо:
- аккуратное проведение лечения;
- постоянный контроль специалистов — гематолога и терапевта;
- тщательное контролирование больным своего состояния, немедленное посещение врача при появлении новых симптомов;
- постоянный прием поддерживающих препаратов в течение долгого времени.
Апластическая анемия — опасная патология, которую лечат годами. Только под наблюдением специалиста можно добиться стойкой ремиссии патологии. Самолечение в этом случае неприемлемо и может привести к плачевным последствиям.
источник
На сегодняшний день существует множество различных нарушений в функционировании кровеносной системе человека, которые имеют отличные друг от друга причины возникновения, по-разному проявляются клинически. Различны и прогнозы протекания таких заболеваний. Одним из примеров таких заболеваний является апластическая анемия.
Когда человек впервые сталкивается с диагнозом апластическая анемия, естественно, у него сразу возникает вопрос, что это такое? В основе данного заболевания (другое его название – панмиелофтиз) лежит резкое угнетение процессов кроветворения в красном костном мозге, что клинически проявляется в уменьшении в крови содержания форменных ее клеток – эритроцитов, лейкоцитов и тромбоцитов.
Процент выявления апластической анемии среди населения относительно низок и частота выявленных случаев составляет всего 0,5 на 100 тысяч населения. Этот вид анемии не зависит от пола больного человека, но возможно установить некоторую зависимость от возраста.
Начиная с рождения и до 20 лет частота выявленных случаев среди этой возрастной категории постепенно увеличивается; в категории пациентов возрастом от 20 до 55 лет она сохраняется на одном уровне, а вот после 55 лет резко возрастает.
Согласно последним исследованиям в этой области, у небольшой группы пациентов была установлена генетическая предрасположенность к развитию апластической анемии.
Летальный исход наступает у более, чем половины больных. Некоторые источники отмечают, что этот процент достигает отметки 80.
Согласно МКБ 10-го пересмотра апластическая анемия входит в группу «другие анемии» под кодом D61.
В зависимости от клинической картины проявления заболевания различают:
- Наследственные апластические анемии. Данные патологии приводят к тотальному поражению системы кроветворения. Среди данного вида анемий выделяют два подвида:
- анемии Фанкони – если основное заболевание сопровождается формированием врожденных пороков развития;
- анемии Эстрена – Дамешека – если врожденные пороки отсутствуют;
- анемия Даймонда – Блекфена – форма анемии, при которой отмечается нарушение продукции только эритроцитарных клеток крови, обусловленное генетическими факторами.
- Приобретенные апластические (или гипопластические) анемии. Здесь также различают подвиды:
- формы анемий, которые характеризируются острым, подострым или хроническим процессом угнетения общего кроветворения;
- парциальная (красноклеточная) анемия – угнетается процесс формирования только эритроцитов.
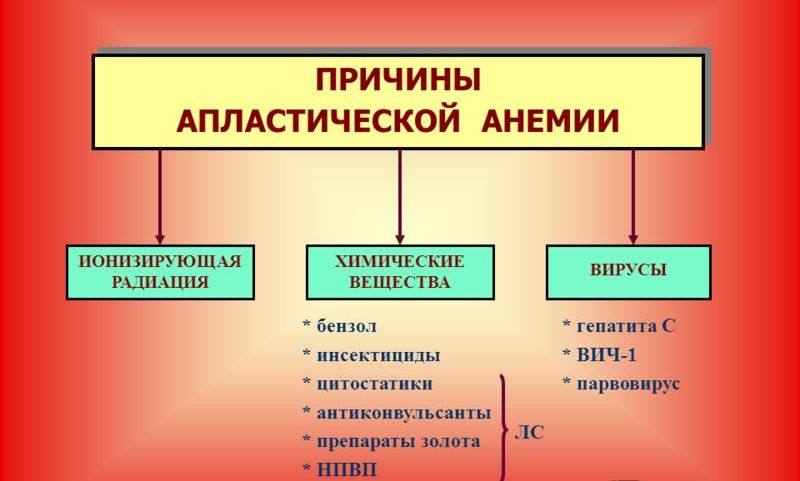
Причины апластической анемией следующие:
- Наличие внешних факторов, которые обладают миелотоксическим эффектом, то есть провоцируют цитостатические нарушения свертываемости крови. Сюда относятся и различные заболевания инфекционной и вирусной природы, и действие ионизирующего излучения, и некоторые лекарственные препараты (анальгин, противотуберкулезные препараты, некоторые виды антибиотиков), а также препараты, применяемые в химиотерапии.
- Эндогенные, то есть внутренние, причины апластической анемии – накопление токсических веществ в результате внутренних нарушений и эндокринных сдвигов, например, в случае развития гипотериоза, уремии.
- Аутоагрессия, когда у больного развивается индивидуальная чувствительность к антигенам и появляются антитела в крови.
- Идиопатические формы апластической анемии. Различают у половины больных, диагностируют в случае, если установить причину развития заболевания не удалось.
На современном этапе специалистам удалось изучить в наибольшей степени только врожденные виды апластических анемий. Так, в случае диагностирования анемии Фанкони причина заключается в изменениях в парных хромосомах I и VII. При анемии Даймонда – Блекфена мутируют гены хромосом I, XVI, XIX, и XIII. Свою роль в этих процессах может сыграть воздействие на организм свободных радикалов.
Современной медицине пока окончательно не известны механизмы и причины, которые приводят к формированию недоразвития костного мозга.
Выделяют несколько процессов развития апластической анемии:
- Развитие в организме процессов, приводящих к поражению стволовых клеток костного мозга.
- Действие защитных механизмов организма (клеточных, под влияние гормонов), в результате которого процессы образования клеток крови подавляются.
- Различные виды нарушений функционирования элементов микроокружения костного мозга (остеогенные, жировые клетки, макрофаги и другие).
- Недостаток в организме факторов, которые активизируют процессы кроветворения.
- Случаи, когда концентрация необходимых для кроветворения веществ сохраняется на должном уровне (в частности, железо в крови, витамин В12, протопорфирин), но они не усваиваются кроветворной тканью.
В случае развития у человека апластической анемии и поражения костного мозга, происходит разрушение клеток крови различной степени зрелости, но, в первую очередь, страдают эритроциты. Нарушается не только средний объем эритроцитов, но также уменьшается и длительность жизнедеятельности зрелых форм.
Заболевание анемии сопровождается нарушениями процессов выведения излишков железа, которое кумулируется в печени и селезенке.
Из-за понижения лейкоцитов в крови происходят сбои в работе иммунной системе организма. Снижением концентрации тромбоцитов в крови объясняется нарушение процессов свертываемости крови.
Повышение лимфоцитов, Отмечается «опустошение» костного мозга (панмиелофтиз).
Поскольку в крови снижается количество зрелых эритроцитов, это приводит к развитию хронической гипоксии в тканях, что влечет за собой дистрофические изменения внутренних органов. В первую очередь очень чувствительны к гипоксии (кислородное голодание) эндокринные железы.
В зависимости от того, насколько выражены нарушения процессов кроветворения, клинические проявления и симптомы апластической анемии очень разнообразны: различают переходные формы апластической анемии от частичного угнетения процессов образования клеток крови до выраженного недоразвития костного мозга.
В течении заболевания выделяют 3 основных синдрома апластических анемий:
- цитопенический;
- септико – некротический;
- геморрагический.
Эти синдромы анемии могут по-разному проявляться в организме человека в зависимости от степени развития заболевания. Различают 3 этапа развития болезни, при этом симптомы апластической анемии на каждом из них разнятся.
I этап характеризируется проявлением неспецифических симптомов, которые могут быть при любом другом патологическом процессе, — хроническая усталость и общая слабость. Очень часто больные приспосабливаются к существующей у них анемии и обращаются к специалисту только тогда, когда заболевание начнет прогрессировать. Также этот этап характеризуется такими проявлениями геморрагического синдрома, как маточное, носовое кровотечение и повышенная склонность к образованию кровоподтеков (синяки на теле без причины).
На II этапе у больных болеющие апластической анемией отмечается бледность кожи и видимых слизистых оболочек, также иногда могут возникать кровоподтеки. Если заболевание переходит в острую форму, помимо бледности кожных покровов также наблюдают геморрагический шок, некроз слизистых оболочек и высокую температуру. В организме активизируются различные воспалительные процессы (в частности, пневмония).
Обычно печень и селезенка не увеличиваются, но если диагностируют аутоиммунную форму апластической анемии, при которым в организме больного вырабатываются антитела к эритроцитом, может развиться умеренная спленомегалия (увеличение селезенки) и легкая желтушность кожи и склер, вызванных наличием в крови гемолитических компонентов.
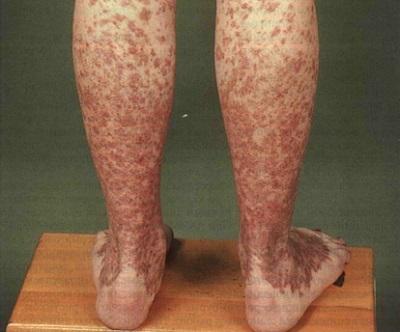
Наиболее ярко выраженным является III этап анемии, который характеризируется бурной картиной клинических проявлений. На этой стадии развития апластической анемии анализ крови показывает:
- в клиническом анализе крови определяется ярко выраженная анемия (как правило, нормохромная) – уровень гемоглобина уменьшается до 20 – 30 г/л, концентрация ретикулоцитов снижается (говорит о снижении функциональности костного мозга);
- возникает лейкопения, гранулоцитопения, то есть резко снижается уровень содержания в крови гранулярных лейкоцитов. При этом количество лимфоцитов не изменяется;
- понижение тромбоцитов, вплоть до нуля;
- при гистологическом исследовании ткани костного мозга отмечается катастрофическое исчезновение его клеток, которые замещаются жировой тканью;
- резко повышается СОЭ – до 30 – 50 мм/час;
- в сыворотке крови концентрация железа увеличивается.
Лечение апластической анемии зависит от главного фактора, который предположительно стал причиной развития патологического процесса.
Если заболевание выявлено впервые, больной обязательно подлежит госпитализации в стационар, отделение гематологии. Только в условиях лечебного учреждения можно корректно подобрать необходимый для лечения лекарственный препарат, а также определиться с его дозировкой.
Основными методиками коррекции и лечения апластической анемии у детей и взрослого являются:
- трансфузионные методы (переливание крови);
- трансплантационные методы;
- медикаментозные методы.
Трансфузионный терапевтический метод предполагает переливание больному цельной, эритроцитарной или тромбоцитарной массы, а также гранулоцитов крови. Препараты крови, использующие в трансфузии, готовятся на станциях переливания из донорской крови. Данный метод трансфузии — временный, так как он позволяет только восполнить дефицит клеток крови, но нарушения в костном мозге при этом не ликвидируются. Еще одним минусом трансфузии является то, что при диагностировании аутоиммунных форм апластической анемии применять его нельзя.

Если операции по переливанию крови больному делают довольно часто, это может привести к накоплению в его организме излишков железа, которые откладываются в печени и селезенке. Поэтому такой категории пациентов включают в терапию лекарственные препараты, влияющие на выведение железа из крови.
Наиболее эффективным методом лечения апластической анемии принято считать трансплантационный, при котором происходит пересадка костного мозга человека. Вероятность успеха операции по пересадке костного мозга зависит от возраста больного, процент успешного исхода тем выше, чем моложе пациент. В качестве донора может выступить один из ближайших родственников, имеющий такую же группу крови, что и больной. Для этого необходимо провести исследование на индивидуальную совместимость их групп крови.
Данная методика лечения требует определенной подготовки, чтобы снизить процент вероятности отторжения чужеродных тканей. Перед процедурой переливания крови отменяются, назначается проведение лучевой терапии, закрепленной в последствие курсом химиотерапевтических препаратов. Делается это с целью временного подавления иммунной системы больного, которая может спровоцировать отторжение донорских стволовых клеток. Трансплантация костного мозга при анемии – очень дорогостоящая операция, проводится только в специализированных клиниках.
Медикаментозная терапия при апластической анемии у человека включает применение следующих лекарственных средств:
- иммунодепрессанты – например, циклоспорин, специфические антиглобулины. Применение этих лекарственных форм показано в тех случаях, когда невозможно провести операцию по пересадке костного мозга. Назначаются они комплексно с кортикостероидами, чтобы предупредить развитие анафилактических реакций;
- лекарственные препараты, стимулирующие процессы кроветворения – например, филграстим, лейкомакс. Назначают их только в случае диагностирования лейкопении, поскольку они активируют процессы образования гранулярных лейкоцитов;
- для лечения апластической анемии у мужчин применяют препараты, содержащие андрогены (мужские половые гормоны) – тестостерона пропионат, сустанон;
- при выраженном геморрагическом синдроме показано назначение гемостатиков – дицинон, аминокапроновая кислота;
- одним из примеров препаратов, способствующих выведению железа из крови, является десферал.
Еще один метод лечения апластических анемий — спленэктомия, другими словами операция по удалению селезенки. Частота положительного эффекта составляет 85%. В основе этого метода лечения лежит прекращение аутоиммунных процессов в организме, когда вырабатываются антитела к собственным клеткам. Его можно проводить любым пациентам, у которых отсутствуют инфекционные осложнения.
Запрещено прибегать к использованию рецептов народной медицины при лечении апластической анемии. Лечение патологических нарушений в этом случае предусматривает точную дозировку лекарственных веществ, которую невозможно соблюдать при использовании фитопрепаратов.
Поскольку механизмы развития апластической анемии на данном этапе так и остаются до конца не выясненными, прогноз лечения апластической анемии в большинстве случаев неблагоприятный.
Самый высокий процент смертности отмечается у категории больных с тяжелыми формами заболевания. Из-за прогрессирующего и не поддающего коррекции недоразвития костного мозга возобновить процессы образования клеток крови не удается и это приводит к гибели больного из-за генерализированного сепсиса.
Если же течение заболевания менее тяжелое, у больного отмечается положительная реакция на трансплантацию донорских стволовых клеток, а также применение иммунодепрессантов оказывает эффективное действие – прогнозы перехода заболевания в стадию ремиссии колеблются в пределах 50 – 90%. Одна лишь медикаментозная терапия, без применения оперативных методов лечения, может дать положительный результат только у половины пациентов.
В случае развития наследственных форм апластических анемий клиническая картина зависит от вида заболевания.
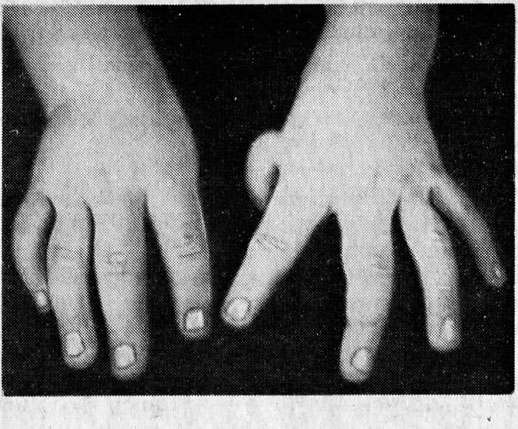
При диагностировании апластической анемии Фанкони у ребенка присутствуют такие врожденные пороки развития, как врожденные аномалии развития костной системы (отсутствие I пальца на кисти, искривление либо отсутствие лучевых костей и другие), пороки сердца и почек, аномалии развития глаз (маленькие глазные яблоки).
Симптомы апластической анемии у детей начинают появляться в возрасте 4 года, очень редко – в раннем возрасте. У ребенка наблюдается общая слабость, повышенная утомляемость, частые головные боли. Иммунитет снижается, ребенок становится более восприимчивым к простудным заболеваниям.
Геморрагический синдром проявляется склонностью к частым носовым кровотечениям. Лабораторное обследование дает характерную клиническую картину в анализах крови. Заболевание переходит в хроническую форму, прерываемую периодическими рецидивами.
Летальный исход при этой форме апластической анемии обусловлен присоединением инфекционного процесса или же развитием острой кровопотери из-за усилившегося геморрагического синдрома.
Случаи диагностирования апластической анемии Эстрена – Дамешека довольно редки. Данные виды болезни характеризируются нарушениями только кроветворных процессов.
При анемии Даймонда – Блекфена нарушаются процессы формирования только красных клеток крови. Геморрагический синдром отсутствует. При осмотре специалист отмечает бледность кожи, увеличение печени и спленомегалию. Концентрация тромбоцитов и лейкоцитов в крови может снизиться только в случае сильного поражения селезенки. Заболевание имеет хронически тяжелое течение. Прогноз крайне неблагоприятный. Смерть наступает до достижения 20-летнего возраста.
источник

Болезнь достаточно редкая. Сложность лечения связана с тем, что самым простым разделом кроме лекарственной является заместительная трансфузионная терапия эритроцитарной и/или тромбоцитарной массы. Для сложных случаев остается только пересадка костного мозга – дорогая, с целым рядом осложнений операция.
По статистике в зоне риска апластической анемии молодые люди до 20 лет (преобладает вирусная природа патологии), а также люди старше 65-ти лет (накопленные возрастные сбои биохимических процессов как причина).
Статистику можно посмотреть в видео в конце статьи.
В зависимости от степени выраженности угнетения кроветворения различают две формы:
- гипопластическая анемия (при этой форме функция кроветворения сохранена, но значительно снижена),
- апластическая анемия (полное угнетение кроветворения).
По сути они являются одним и тем же заболеванием разной степени выраженности. Нарушается продукция эритроцитов, тромбоцитов и лейкоцитов.
Клинические проявления могут быть разнообразными и на первых этапах напоминать общее недомогание за счет снижения эритроцитов – возникают слабость, головокружения, могут появиться обмороки.
За счет нехватки тромбоцитов развиваются кровотечения, кожные геморрагические высыпания.
Выделить единственную причину невозможно, так как вызвать апластическую анемию могут различные факторы. Они разительно отличаются друг от друга, но могут приводить к одинаково тяжелым последствиям.
Клиническая картина этих вариантов отличается. Во-первых, врожденные формы часто проявляются на ранних сроках жизни. Во-вторых, они могут сочетаться с аномалиями развития различных органов.
При манифестации во взрослом возрасте первыми симптомами могут быть общее недомогание и головокружение, которые являются неспецифичным и возникают при многих заболеваниях. Скорость прогрессирования апластической анемии зависит от выраженности нарушения кроветворной функции.
Врожденные формы включают в себя следующие варианты:
- Синдром Даймонда-Блекфена. При данной патологии происходит нарушение на уровне клеток-предшественников эритроцитов. Фенотипическим симптомом является бледная кожа. Увеличение печени и селезенки не характерно, но может развиваться с течением времени.
- Анемия Фанкони. Наследственное заболевание, которое проявляется на пятом десятке жизни. Возникает острый лейкоз и апластическая анемия. Для данной генной мутации характерны аномалии развития, которые проявляются уже на ранних сроках жизни. В основном это аномалии костной системы (низкий рост, маленький череп, недоразвитие первого пальца верхних конечностей, лучевой кости, тяжелая дисплазия бедра, дополнительное ребро) и неврологический дефицит (аномалии глазных яблок, косоглазие, птоз, нарушение слуха, умственные нарушения развития).
- Синдром Эстрена-Дамешека. Помимо нарушения кроветворения для данных детей характерна определенная внешность – светлые волосы, широко расставленные глаза, курносый нос. Апластическую анемию в этом варианте сопровождает увеличение печени и селезенки.
Приобретенные формы различают по факторам, которые вызывают апластическую анемию.
- Внешние (экзогенные) факторы:
- Медикаментозное влияние – прием сульфаниламидов, антибактериальных средств (тетрациклин, левомицитин, стрептомицин), средств для лечения туберкулеза (изониазид, ПАСК), анальгина, цитостатиков.
- Воздействие химических агентов – наиболее опасны нефтепродукты, бензольные производные, ртуть.
- Радиоактивное воздействие.
- Инфекции. Наиболее опасными являются вирус, вызывающий гепатит С, цитомегаловирус, герпес-вирус. Чаще всего они оказывают выраженное повреждающее действие лишь при активно перенесенном заболевании.
- Внутренние (эндогенные) факторы:
- Аутоиммунное поражение костного мозга. Чаще наблюдается в пожилом возрасте.
- Эндокринное влияние. Выявлена связь с нарушением функции щитовидной железы, и с заболеваниями яичников у женщин.
В настоящее время существует три теории, объясняющих механизм развития апластической анемии. Каждая из них получила подтверждение в ходе исследований.
Поэтому официально теории приняты, но изучение механизмов возникновения апластической анемии продолжается.
Теории патогенеза (возникновения) апластической анемии:
- аутоиммунная;
- стромальная;
- преждевременный апоптоз.
Возникла она в результате исследования материала биоптата костного мозга после развития апластической анемии.
В большом количестве случаев ученые увидели присутствие клеточного иммунитета (моноциты, Т-киллеры), а также факторов воспаления – фактор некроза опухолей, интенферон альфа и гамма.
После более детального изучения стало понятно, что скапливаются они из-за генной мутации. В результате нарушения работы гена PIG-A возникает дефицит специального гликопротеина, который необходим для того, чтобы снижать активность системы комплемента, входящей в состав иммунной системы.
В результате этой поломки защита собственных клеток костного мозга слабеет, они начинают восприниматься, как чужеродные и развивается аутоиммунная реакция. В зависимости от количества поврежденных клеток степень выраженности симптомов разнится.

Строма отвечает за выработку специальных веществ (интерлейкины и факторы стволовых клеток), которые необходимы для направления недифференцированных молодых клеток по пути образования эритроцитов, тромбоцитов или лейкоцитов.
Стимулируется эта выработка эритропоэтином.
В случае нарушения выделения факторов роста на уровне стромы возникают низкодифференцированные клетки, которые не могут выполнять свои функции. Они не достигают дифференцировки, достаточной для определения в крови при анализе.
Термином апоптоз в медицине обозначают естественный процесс гибели клетки, когда она в полном объеме выполнила свою функцию. Происходит это во всех тканях организма. После определенного времени клетки подвергаются мутации, начинают восприниматься организмом, как старые, и удаляются.
В норме процесс представляет собой защитный механизм, который способствует обновлению тканей. Мутировавшие клетки могут переродиться в опухолевый процесс, и функция апоптоза – не допустить этого. Однако, если этот процесс начинает происходить раньше времени, возможно чрезмерное удаление клеток ткани. При недостаточном синтезе новых клеток этот процесс приводит к нарушению функции.
Изучение механизмов развития апластической анемии до сих пор является зоной научных интересов исследователей всего мира. Однако это может внести вклад в лечение заболевания в будущем, но никак не сказывается на современных пациентах.
Дело в том, что на сегодняшний момент самым эффективным методом лечения апластической анемии остается пересадка костного мозга. Для замедления процесса используют стероидные гормоны.
Учитывая угнетение выработки кровяных телец, выделяют следующие синдромы апластической анемии:
- Анемический (возникает за счет недостаточности эритроцитов и, соответственно, гемоглобина);
- Геморрагический (возникает в результате нехватки тромбоцитов, которые в норме останавливают кровотечение, образовывая тромботические массы);
- Токсико-инфекционный (недостаточность лейкоцитов – клеток иммунитета, в результате чего даже незначительная инфекция может развиться до гнойного процесса).
Клиническая картина каждого синдрома отличается. Может наблюдаться как сочетание всех синдромов, так и превалирование одного.
- При анемическом синдроме преобладают:
- повышенная утомляемость;
- головокружение;
- тошнота;
- одышка даже при минимальной нагрузке;
- тахикардия;
- потемнение в глазах.
- При геморрагическом:
- Множественные, легко образующиеся синяки;
- Излишне замедленная остановка любого кровотечения;
- Возникновение носовых кровотечений;
- Обильные месячные;
- Кровоточивость из десен;
- Возникновение специфических высыпаний – тромбоцитопеническая пурпура (является по факту пропитыванием кожи кровью).
- При токсико-инфекционном:
- Тяжелое течение легких инфекционных заболеваний;
- Медленное заживление ран, часто с нагноением.
Эти признаки более характеры для развития апластической анемии во взрослом возрасте. Эти пациенты могут анализировать свое состояние и предъявлять жалобы на приеме у врача.
Апластическая анемия у детей имеет свои особенности. При возникновении заболевания в совсем раннем возрасте они не могут объяснить свои ощущения, но существуют так называемые стигмы (или особенности), которые позволяют заподозрить различные наследственные формы анемии и провести генетическое тестирование.
Обычно у детей при наличии апластической анемии отмечаются следующие особенности:
- маленькая голова,
- укорочение первого пальца верхних конечностей,
- дисплазия тазобедренного сустава при синдроме Фанконе,
- специфический фенотип (светлые волосы, курносый нос, широко поставленные глаза при синдроме Эстрена-Дамешека),
- гепато- и спленомегалия.
Сбор жалоб и осмотр пациента является первым звеном в постановке диагноза и дает врачу первоначальный вектор для дальнейшего 
Самым важным этапом является инструментальная и лабораторная диагностика, которая включает в себя:
- Стернальную пункцию костного мозга;
- Трепанобиопсию;
- биохимический анализ крови;
- общий анализ крови.
С помощью трепанобиопсии производят забор костного мозга из крыла подвздошной кости. Данный метод помогает помимо анализа клеток (цитологического) провести гистологический анализ. Это помогает получить информацию о строме, ее представленности, а также соотношении желтого (неактивного) и красного костного мозга.
Биохимический анализ позволяет получить информацию о:
- содержании сывороточного железа (необходимо для подтверждения анемии),
- эритропоэтина (повышается при недостаточной выработке факторов роста стромой), – антителах к вирусам (которые могут быть причиной заболевания),
- С-реактивного белка (высокоспецифичный показатель воспалительного процесса).
Общий анализ крови показывает количественное содержание клеток крови (эритроциты, тромбоциты, лейкоциты), а также оценивает качественные характеристики клеток.

Для симптоматического лечения синдромов могу применяться антибиотики, препараты для коррекции артериального давления, ферментные препараты.
Иммуносупрессивную терапию в качестве единственного лечения применяют лишь в начале апластической анемии. Далее стараются комбинировать с цитостатиками и препаратами для симптоматического лечения в зависимости от преобладания синдромов.
К сожалению, она не всегда проходит гладко. Выделяют несколько наиболее частых осложнений процедуры.
К основным осложнениям относят следующие:
- инфекционные осложнения. Как и при любом оперативном вмешательстве существует риск нагноения места пункции. У пациентов с апластической анемией снижен иммунитет, поэтому даже при должном соблюдении правил асептики и антисептики не исключено появление данного осложнения.
- Отторжение трансплантата. Любой пересаженный орган воспринимается иммунными клетками организма, как чужеродный. Возникает иммунная реакция с попыткой уничтожить инородную ткань.
- Реакция трансплантата против организма пациента. При пересадке стволовых клеток возникает образование клеточного иммунитета донора. Новые клетки начинают агрессивно себя вести по отношению к лимфоцитам пациента. Этот процесс приводит к образованию высыпаний, нарушениями работы сердечно-сосудистой системы и желудочно-кишечного тракта.
- отказ работы жизненно важных органов. Возникает из-за массивного стресса, оказываемого на организм процессом пересадки костного мозга, а также приемом большого количества препаратов.
Несмотря на возможность тяжелых осложнений, трансплантация костного мозга остается самым эффективным методом лечением апластической анемии.
Врожденные формы часто сложнее поддаются лечению, так как костный мозг первоначально генетически не полноценен. Так, при анемии Фалкони, медикаментозное лечение протекает крайне сложно, а пересадка костного мозга может иметь противопоказания из-за аномалий развития.
Кроме того, выраженность симптомов может варьировать в зависимости от выраженности повреждения костного мозга. При медленно текущем процессе с минимальными повреждениями, даже медикаментозное лечение протекает легче и приносит существенное облегчение.
источник