Анемии этой группы развиваются в результате острой потери эритроцитов при кровотечении (острая постгеморрагическая анемия) или при их разрушении — гемолизе (гемолитическая анемия). Характерным признаком постгеморрагической и гемолитической анемий является стимуляция эритропоэза.
В крови больных резко увеличивается число ретикулоцитов и повышается ретикулоцитарный индекс в два-три раза по сравнению с нормой. Ретикулоцитарный индекс (РИ) определяется по формуле:
РИ более 2–3% соответствует адекватному ответу костного мозга на анемию, а меньшая величина свидетельствует о подавлении кроветворения.
Острое кровотечение может быть результатом травматического разрыва сосуда или его разреза, эрозии артерии при пептической язве, варикозном расширении вен пищевода и разрыве аневризмы аорты. Кровотечение может быть явным (кровавая рвота, мелена) или скрытым (при внематочной беременности). Клинические проявления зависят от массивности и длительности кровотечения. Быстрая потеря 1/3 общего объема крови может быть смертельной, но постепенная потеря 2/3 объема крови за 24 ч не приводит к гибели больных.
В момент кровотечения развиваются симптомы коллапса. Характерны бледность, шум в ушах и головокружение, нарушение зрения, обморочное состояние, холодные на ощупь конечности, тахикардия, нитевидный пульс, снижение АД. При продолжающемся кровотечении развивается гиповолемический шок.
В первые часы после кровотечения число эритроцитов, содержание гемоглобина и гематокрита обманчиво нормальные или несколько повышенные, что обусловлено спазмом периферических артерий и выходом крови из депо (рефлекторная фаза компенсации).
Через 8–14 ч начинает поступать в циркулирующую кровь тканевая жидкость, разбавляя ее. Число эритроцитов и содержание гемоглобина снижаются. Развивается нормоцитарная анемия (гидремическая фаза компенсации).
Через 4–5 суток появляются признаки регенерации костномозгового кроветворения с выходом в кровь большого количества ретикулоцитов, ретикулоцитарный индекс становится более 3%. В мазках крови обнаруживают полихроматофилию, умеренный макроцитоз, иногда отдельные нормобласты и незрелые лейкоциты (костномозговая фаза компенсации).
Полное восстановление крови происходит через 4–6 месяцев.
Необходимо немедленно остановить кровотечение, восстановить объем крови и устранить проявления шока. Наиболее эффективным методом восстановления объема крови является гемотрансфузия. Заменителем крови может быть плазма. Переливание 5% раствора глюкозы или физиологического раствора дает кратковременное улучшение. В последующем назначают препараты железа для устранения его дефицита, развившегося при кровотечении.
Гемолитическая анемия – общее название анемий, развивающихся вследствие повышенного распада эритроцитов (гемолиз). Но гемолитическая анемия возникает лишь тогда, когда отсутствует усиленный эритропоэз в костном мозге, компенсирующий распад эритроцитов.
В зависимости от преимущественной локализации гемолиза выделяют анемии с внутрисосудистым и внесосудистым гемолизом.
Внутрисосудистый гемолиз развивается редко, протекает с лихорадкой, тахикардией и болью в спине. Свободный гемоглобин связывается с гемоглобином сыворотки. При избытке свободного гемоглобина возникает гемоглобинурия, которая может стать причиной почечной недостаточности. Через 5–7 дней после гемолитического криза в моче выявляется гемосидерин, образующийся в клетках почечных канальцев из реабсорбированного гемоглобина.
Внесосудистый гемолиз — это разрушение эритроцитов в ретикулоэндотелиальной системе, главным образом, в селезенке. При спленомегалии срок жизни эритроцитов сокращается в результате разрушения в ней эритроцитов с аномалиями или тепловыми антителами на поверхности. При этом развиваются желтуха и непрямая гипербилирубинемия, возрастает активность сывороточной ЛДГ. Уровень гемоглобина нормальный или слегка пониженный.
Усиленный распад эритроцитов может быть обусловлен экзоэритроцитарными (аутоантителами, механическим повреждением) и эндоэритроцитарными факторами (мембранопатиями, ферментопатиями и гемоглобинопатиями).
Первая группа факторов выявляется при гиперспленизме, иммунном гемолизе, микроангиопатии, инфекции и токсическом повреждении. Развившиеся гемолитические анемии при этих состояниях относятся к приобретенным.
Вторая группа факторов характерна для наследственного микросфероцитоза, овалоцитоза, пароксизмальной почечной гемоглобинурии и шпороклеточной анемии. Гемолитические анемии при этих заболеваниях относятся к врожденным (наследственным).
Данные анемии развиваются при внутрисосудистом гемолизе нормальных эритроцитов, обусловленном антителами и токсинами, гиперактивностью клеток ретикулоэндотелиальной системы, естественными или механическими препятствиями кровотоку. Подробнее читайте в этой статье.
Данные анемии — это результат врожденного дефекта гемоглобина, ферментов или мембран эритроцитов. Соответственно выделяют три группы наследственных гемолитических анемий. Подробнее читайте в этой статье.
источник
Эритроциты (красные кровяные тельца, RBC) относятся к клеткам, которые содержат гемоглобин. Увеличение RBC чаще связано с патологиями кровеносной системы либо с кислородным голоданием тканей. Подробнее читайте в нашем материале.
Эритроциты (RBC) – кровяные тельца красного оттенка. Яркую окраску RBC имеют за счет большого содержания гемоглобина. Место образования – костный мозг.
Важно! Основная функция эритроцитов – доставка кислорода к органам и тканям, а также последующее выведение углекислого газа из организма.
Оптимальное значение RBC в женском организме выше, нежели в мужском. Так, норма среди слабого пола равна 3,4-5,2*10 г/л, а среди сильного – не более 5*10 г/л.
При понижении эритроцитов менее 3*10 г/л важно обратиться к врачу для проведения дополнительного исследования и диагностирования заболевания.
Кроме того, можно самостоятельно определить признаки пониженного содержания эритроцитов по следующим симптомам:
- Бледность кожи.
- Сонливость.
- Слабость и усталость.
- Частые инфекционные и простудные заболевания.
- Пониженное давление.
Важно! Несмотря на тот факт, что эритроциты называются красными кровяными тельцами, подобный оттенок возникает постепенно. Так, вначале созревания в тельцах мало гемоглобина и поэтому RBC имеют синий цвет.
Медики различают абсолютный и относительный показатель снижения эритроцитов. В первом случае снижение свидетельствует о нестабильной работе костного мозга.
Во втором случае снижение происходит вследствие разжижения крови, что вызвано внутривенным введением жидкости, обильным питьём или развитием инфекционного заболевания. Обычно подобное явление не требует медицинского вмешательства.
К основной причине снижения эритроцитов относится анемия, которая может возникать внезапно, переходя в сложную форму. К первым признакам подобного нарушения относят: бледность; головокружение; одышка; сбои в менструальном цикле.
Важно! При анемии страдают нервные клетки, отвечающие за импульсы организма.
Кроме того, к причинам понижения эритроцитов, которые не требуют лечения, относят:
- Неполноценное и несбалансированное питание, диета, голодание.
- Дефицит витаминов В12, фолиевой кислоты, железа.
- Злоупотребление кофе.
- Прием медикаментов.
- Чрезмерные физические нагрузки.
- Вредные привычки.
- Беременность.
- Стрессовые ситуации.
Если исключаются вышеперечисленные причины, тогда врач проводит дополнительное обследование организма для выявления одной из следующих патологий:
- Гранулематозная болезнь – наследственная патология, связанная с недостатком клеток иммунной системы, которые защищают организм от вредного внешнего воздействия.
- ВИЧ–инфекция.
- Гипотиреоз – болезнь, связанная со снижением концентрации гормонов щитовидной железы.
- Ревматоидный артрит.
- Почечная недостаточность.
- Отсутствие части желудка.
- Онкология.
Нормальный уровень эритроцитов зависит от возрастных параметров ребенка и по мере взросления изменяется. Так, нижней границей нормы RBC среди детей будет:
- Новорождённые – 5*10 12 /л.
- Груднички с 5 дня жизни – 4,5 *10 12 /л.
- Старше года – 4*10 12 /л.
Уменьшенное число эритроцитов возникает при следующих патологиях:
- Анемия.
- Гемоглобинопатия – наследственное изменение структуры белков гемоглобина.
- Лейкоз.
- Гемолитическая болезнь – возникает по причине иммунологического конфликта несовместимости материнской крови с кровью плода, приводящая к гемолизу эритроцитов ребенка под влиянием материнских антител.
- Злокачественные опухоли.
- Микседема – патология, связанная с недостаточным обеспечением органов и тканей гормонами щитовидной железы.
- Гемофилия – наследственное заболевание, связанное с нарушением свёртываемости крови.
- Гломерулонефрит – воспаление почек инфекционно–аллергического характера, которое проявляется в форме отеков, повышения артериального давления, снижения выделений мочи.
- Дифтерия, коклюш и другие инфекции.
- Цирроз печени.
- Коллагенозы – группа заболеваний, которые связаны с изменениями, со стороны соединительной ткани.
- Хроническая почечная недостаточность.
- Язвенное поражение ЖКТ.
Кроме того, снижение RBC может быть вызвано избыточным количеством жидкости в организме, но подобное состояние не требует медицинского вмешательства.
Важно! Когда врач диагностирует снижение эритроцитов, тогда необходимо 1 раз в 6 месяцев проходить плановый осмотр и сдавать необходимый перечень анализов.
В организме беременной женщины происходят большие перемены физического, физиологического, гормонального, химического характера. Вследствие этого изменяется состав крови, в том числе и уровень RBC.
Норма RBC изменяется в зависимости от срока беременности. Так, в 1 триместре нормальное значение варьируется между 4,2–5,5*10 12 /л.; во 2 триместре – от 3,5 до 4,8*10 12 /л; в 3 триместре – 3,5–7*10 12 /л.
При понижении RBC беременным женщинам стоит обращать внимание на следующие симптомы:
- Постоянная усталость и сонливость.
- Сухость и бледность кожных покровов.
- Обмороки.
- Пониженное артериальное давление.
Чаще причиной низкого содержания эритроцитов является железодефицитная анемия, при которой назначаются витаминные комплексы, и рекомендуется употребление продуктов питания с высоким содержанием железа.
Подробнее об анемии смотрите в следующем видеоматериале:
Количество RBC определяется при развернутом анализе крови. Часто в медицинском бланке встречается аббревиатура MCV с числовым показателем, который означает среднее число эритроцитов. Единица измерения – микрометр кубический или fl – фемтолитр.
Средний объём эритроцитов изменяется после появления ребенка на свет, а затем значение устанавливается в строгом диапазоне, а именно (в fl):
- Новорождённые: до 128.
- 1 неделя: до 100.
- До года: 77–79.
- 1–2 года: 72–89.
- 3–6 лет: 75–90.
- 7–12: 76–90.
- 13–16: 79–93.
- 20–29: 82–96.
- 30–39: 85–95.
- 40–49: 80–95.
- 50–59: 82–95.
- Старше 60 лет: 80–100.
При снижении MCV чаще развивается малокровие или анемия. Кроме того, понижение указанного показателя возможно при: интоксикация; наследственность патологий крови; обезвоживание; нарушение синтеза составной части гемоглобина.
В кровяном составе здорового пациента содержатся эритроциты, которые идентичны по форме, размеру и окраске. Благодаря индексу распределения эритроцитов (RDW) можно определить форму и размер эритроцитов. Если данные параметры сильно отличаются между собой, значит, стоит говорить о развитии патологий.
Важно! RDW фиксируется в процентах, нормальный уровень варьируется между 11,5–14,7.
С помощью RDW врачи определяют, например, наличие железодефицитной анемии у ребенка. Кроме того, причинами понижения данного индекса могут быть:
- Гемолиз – разрушение эритроцитов.
- Хирургическое вмешательство.
- Травмы с большой кровопотерей.
- Нарушенный обмен веществ.
- Нехватка витаминов В или железа.
- Гормональный дисбаланс.
При снижении RDW врач назначает повторный анализ, а также комплекс дополнительных исследований для исключения либо выявления патологий.
Ширина распределения эритроцитов или RDW CV – показатель, с помощью которого врачи определяют разницу между большими и маленькими эритроцитами, а также область их распределения.
Нормальным значением RDW CV для взрослого пациента считается 11,5–14,5%, для детей до 6 месяцев 14,9–18,7%, а для детей старше 6 месяцев – 11,5–14,8%.
К причинам снижения RDW CV относят:
- Большая кровопотеря.
- Авитаминоз и недостаток железа.
- Патологические процессы в кроветворных органах.
- Анемия – пациент чувствует общую слабость, хроническую усталость, склонность к обморокам.
В итоге эритроциты занимают не последнее место при исследовании крови. Поэтому при обнаружении сбоя в показателях RBC важно обратиться к доктору и пройти допобследование с целью выявления причин подобного отклонения. И главное – не занимайтесь самолечением.
источник
Железодефицитная анемия — это анемия, обусловленная дефицитом железа в сыворотке крови, костном мозге и депо. Люди, страдающие скрытым дефицитом железа и железодефицитной анемией, составляют 15-20% населения Земли. Наиболее широко железодефицитная анемия распространена среди детей, подростков, женщин детородного возраста, пожилых людей. Общепринято выделять две формы железодефицитных состояний: латентный дефицит железа и железодефицитную анемию. Латентный дефицит железа характеризуется уменьшением количества железа в его депо и снижением уровня транспортного железа крови при еще нормальных показателях гемоглобина и эритроцитов. Для железодефицитной анемии характерно уменьшение всех метаболических фондов железа, в том числе и транспортного, снижение количества эритроцитов и гемоглобина.
Основные сведения об обмене железа
Железо играет в организме человека важнейшую роль, так как участвует в регуляции обмена веществ, в процессах переноса кислорода, в тканевом дыхании и оказывает огромное влияние на состояние иммунологической резистентности. Почти все железо, содержащееся в организме человека, входит в состав различных белков и ферментов. Можно выделить две его основные формы: гемовое (входящее в состав гема) и негемовое (входящее в состав белков и ферментов, не содержащих гема). Гем входит в состав гемоглобина, миоглобина. Железо гема мясных продуктов всасывается без участия соляной кислоты. Однако ахилия может в определенной мере способствовать развитию железодефицитной анемии при наличии значительных потерь железа из организма и высокой потребности в железе. Главными местами всасывания железа являются двенадцатиперстная кишка и верхние отделы тощей кишки. В слизистой оболочке этих отделов тонкой кишки имеется транспортная система, регулирующая всасывание железа в зависимости от потребности организма в нем. При выраженном дефиците железа всасывание его может происходить и в остальных отделах тонкого кишечника. При уменьшении потребности организма в железе происходит снижение скорости поступления его в плазму крови и увеличение отложения в энтероцитах в виде ферритина, который в дальнейшем через несколько дней элиминируется при физиологическом слущивании эпителиальных клеток кишечника.
Влияние различных веществ на всасывание железа
Вещества, усиливающие всасывание железа
Вещества, тормозящие всысывание железа
Органические кислоты (лимонная,
Апельсиновый сок (улучшает усвоение железа из хлеба и овощей)
Аминокислоты гистидин, лизин, цистеин
Антацидные препараты (магния трисиликат и др.)
Энтеросорбенты (беласорб, активированный уголь и др.)
Растительные волокна, отруби
Фитаты растительных продуктов
При увеличении потребности организма в железе и при снижении его запасов усиливается поступление железа в плазму и резко уменьшается его отложение в энтероцитах в виде ферритина. В крови железо циркулирует в комплексе с плазменным трансферином. Этот белок, относящийся к b-глобулиновой фракции синтезируется преимущественно в печени.
Трансферин захватывает железо из энтероцитов, а также из депо в печени и селезенке и переносит его к рецепторам на эритрокариоцитах костного мозга. В норме трансферин насыщен железом не полностью, а приблизительно на 30%. Трансферин может также связывать хром, медь, магний, цинк, кобальт, однако сродство к этим микроэлементам значительно ниже, чем к железу. Комплекс трансферин-железо взаимодействует со специфическими рецепторами на мембране эритрокариоцитов и ретикулоцитов костного мозга, после чего путем эндоцитоза проникает в них; железо переносится в их митохондрии, где включается в протопрорфирин и таким образом участвует в образовании гема. Освободившийся от железа трансферин неоднократно участвует в переносе железа. Затраты железа на эритропоэз составляют 25 мг в сутки, что весьма значительно превышает возможности всасывания железа в кишечнике. В связи с этим для гемопоэза постоянно используется железо, освобождающееся при распаде эритроцитов в селезенке. Хранение (депонирование) железа осуществляется в депо — в составе белков ферритина и гемосидерина. Они представляют собой своеобразный резервный пул, куда поступает железо, не использованное для синтеза гема в эритроцитах.
Наиболее распространенная форма депонирования железа в организме — ферритин. Он представляет собой водорастворимый гликопротеиновый комплекс, состоящий из расположенного в центре железа, покрытого белковой оболочкой из апоферритина. Каждая молекула ферритина содержит от 1000 до 3000 атомов железа. Ферритин определяется почти во всех органах и тканях, но наибольшее его количество обнаруживается в макрофагах печени, селезенки, костного мозга, эритроцитах, в сыворотке крови, в слизистой оболочке тонкой кишки.
При нормальном балансе железа в организме устанавливается своеобразное равновесие между содержанием ферритина в плазме и депо (прежде всего в печени и селезенке). Уровень ферритина в крови отражает количество депонированного железа. Ферритин создает запасы железа в организме, которые могут быстро мобилизоваться при повышении потребности тканей в железе. Другая форма депонирования железа — гемосидерин — малорастворимое производное ферритина с более высокой концентрацией железа, состоящее из агрегатов кристаллов железа, не имеющих апоферритиновой оболочки. Гемосидерин накапливается в макрофагах костного мозга, селезенки, в купферовских клетках печени.
Физиологические потери железа
Потеря железа из организма мужчин и женщин происходит следующими путями:
с калом (железо, не всосавшееся из пищи; железо, выделяющееся с желчью; железо в составе слущивающегося эпителия кишечника; железо эритроцитов в кале);
со слущивающимся эпителием кожи;
Указанными путями как у мужчин, так и у женщин происходит выделение около 1 мг железа за сутки. Кроме того, у женщин детородного периода дополнительные потери железа возникают за счет менструаций, беременности, родов, лактации
источник
Человеческая кровь по своему составу представляет смесь плазмы (жидкой основы) и элементарных твердых частиц, представленных тромбоцитами, лейкоцитами и эритроцитами. В свою очередь тромбоциты отвечают за свертываемость, лейкоциты поддерживают в норме иммунитет, а эритроциты являются переносчиками кислорода.
Если по каким-либо причинам содержание в крови эритроцитов (гемоглобина) понижается, то такая патология называется малокровием или анемией. Общие симптомы заболевания проявляются в виде бледности, слабости, головокружения и пр. В результате анемии в тканях нашего организма начинается острая нехватка кислорода.
Анемия чаще всего выявляется у женщин, нежели у мужчин. Эта патология может возникнуть на фоне каких-либо заболеваний, а также развиться как самостоятельная болезнь.
Спровоцировать анемию может довольно много факторов. Одними из наиболее частых причин анемии по праву считаются нехватка фолиевой кислоты, железа или витамина В12. Также анемия развивается из-за обильных кровотечений во время менструации или на фоне некоторых онкологических болезней. Часто малокровие проявляется из-за недостаточности веществ, которые отвечают за выработку гемоглобина, а также сбои в процессе образования эритроцитов. Передающиеся по наследству заболевания и воздействие ядовитых веществ тоже могут стать причиной развития малокровия.
Чаще всего у страдающих анемией отмечаются следующие симптомы:
- Желтоватая, шелушащаяся, холодная на ощупь и бледная кожа.
- Слабость, быстрая утомляемость, сонливость и головокружения, в тяжелых случаях сопровождающиеся обмороками.
- Пониженное артериальное давление.
- Желтоватый оттенок глазных белков.
- Отдышка.
- Ослабленный мышечный тонус.
- Учащенное биение сердца.
- Увеличение размеров селезенки.
- Измененный цвет стула.
- Липкий, холодный пот.
- Рвота, тошнота.
- Покалывания в ногах и руках.
- Начинают выпадать волосы и ломаться ногти.
- Частые головные боли.
Эти анемии представляют собой комплекс патологий, характеризующихся функциональной недостаточностью костного мозга. Апластическое малокровие отличается от гипопластического более угнетенным кроветворением.
Чаще всего возникновению гипопластической анемии способствует радиация, определенные инфекции, негативное влияние химических или лекарственных препаратов, либо наследственность. Все возможные формы гипо- и апластических анемий имеют постепенный характер развития.
Проявляются эти анемии повышением температуры, ангиной, сепсисом, лишним весом, бледностью, носовыми и десенными кровотечениями, мелкоточечными капиллярными кровоизлияниями на слизистых и коже, жжением во рту. Часто заболевание сопровождается осложнениями инфекционной природы, например, абсцесс после укола, пневмония и пр.). Часто страдает и печень – она, как правило, становится больше.
Железообмен в организме нарушается, при этом количество железа в крови повышенное. Лейкоцитов в составе крови становится гораздо меньше, как и гемоглобина, а вот молодые формы эритроцитов вовсе отсутствуют. В каловых массах и моче часто присутствуют кровянистые примеси.
Формирование клеток крови из костного мозга. При апластической и гипопластической анемиях наблюдаются нарушения при выработке лейкоцитов
В тяжелой степени апластическая анемия (как и гипопластическая) чревата летальным исходом. Лечение даст хорошие результаты только в случае своевременности. Оно проводится только в стационаре и подразумевает повышенный гигиенический уход за ротовой полостью и кожными покровами. При этом осуществляется неоднократное переливание крови, антибиотикотерапия, прием витаминов и гормонов, а также желательно полноценное питание при анемии. Иногда врачи прибегают к пересадке (переливанию) костного мозга (это возможно при наличии донора, совместимого по HLA-системе, которая предусматривает специальный подбор).
Это довольно редко встречающаяся разновидность врожденных анемий, связанная с хромосомными аномалиями, дефектами в стволовых клетках. Встречается предпочтительно у мальчиков. У новорожденных эта патология, как правило, не наблюдается. Для нее характерны симптоматические проявления в 4-10-летнем возрасте в виде кровотечений и кровоизлияний.
В костном мозге наблюдается увеличение жировых тканей, при этом клеточность понижена, а кроветворение имеет угнетенный характер. Исследования показывают, что у детей с анемией Фанкони эритроциты живут ≈ в 3 раза меньше нормы.
Для внешности больного с этой анемией характерна ненормальная пигментация, маленький рост, недоразвитость черепа или скелета, косолапость. Нередко эти симптомы дополняются умственной отсталостью, косоглазием, глухотой, недоразвитостью половых органов, почек, пороком сердца.
Анализы крови показывают изменения, схожие с апластической анемией, только выражены они гораздо меньше. Анализ мочи у большинства пациентов показывает на высокое содержание в ней аминокислот.
Анемия Фанкони – частный случай апластической анемии с нарушением образования эритроцитов в костном мозге
Больные анемией Фанкони, согласно исследованиям, имеют высокую предрасположенность к острому лейкозу.
По своей сути, анемия Фанкони является тяжелой формой апластической анемии, описанной выше. Лечение заключается в удалении селезенки, с применением после этого антилимфоцитарного глобулина. Также применяются иммунодепрессанты, андрогены. Но самым эффективным лечением зарекомендовала себя пересадка костного мозга (доноры – сестра или брат больного или чужие люди, совпадающие по HLA-фенотипу).
Данная патология еще недостаточно изучена. Хотя, несмотря на врожденную природу, эта анемия у грудничков не проявляется. Если же заболевание диагностировано поздно, то такие больные не проживают больше 5 лет. Смерть наступает по причине кровоизлияний в желудок или мозг.
Эти анемии являются как наследственными, так и приобретенными. Для них характерно наличие мегалобластов в костном мозге. Это такие ядросодержащие клетки, которые являются предшественниками эритроцитов и содержат неконденсированный хроматин (в такой клетке молодое ядро, но окружающая его цитоплазма уже старая).
И В-12-дефицитная, и фолиеводефицитная анемии относятся к подвидам мегалобластной анемии. Иногда даже диагностируется смешанная В-12-фолиеводефицитная анемия, но встречается она довольно редко.
В-12-дефицитное малокровие развивается из-за нехватки витамина В-12. Этот микроэлемент необходим для правильного функционирования нервной системы, а также он нужен костному мозгу для образования и роста в нем эритроцитов. В-12 участвует непосредственно в синтезе РНК и ДНК, потому-то и нарушается процесс образования развития эритроцитов при его нехватке.
Для В12-дефицитной анемии отличительным признаком является некоторая шаткость в походке, онемение и ощущение покалывания в пальцах. Также болезнь сопровождается сердечными болями, отеками конечностей, слабостью, пониженной работоспособностью, бледной желтушностью и одуловатостью лица, шумом в ушах, жжением и зудом на языке.
Обычно нехватка В-12 наступает из-за нарушений его всасывания. Этому больше подвержены люди, имеющие атрофию желудочных слизистых, хронический энтерит, глютеновую болезнь. Дефицит В-12 может стать последствием панкреатита. Часто он встречается у вегетарианцев, а также людей пожилого возраста.
Такое малокровие еще называют пернициозной анемией. Развивается заболевание очень медленно, переходя, как правило, в хроническую рецидивирующую форму.
Лечение осуществляется с помощью парентерального применения витамина В-12 (делают ежедневные внутримышечные инъекции). Также показан рацион, обогащенный В-12-содержащими продуктами: печень, яйца, молочные продукты, мясо, сыр, почки.
Фолиеводефицитное малокровие представляет собой острую нехватку в организме фолиевой кислоты. Она тоже (как и В-12) активно участвует в образовании эритроцитов. Фолиевая кислота доставляется в наш организм через продукты питания (мясо, шпинат и пр.), но при термической обработке этих продуктов она теряет свою активность.
Фолиеводефицитной анемии обычно подвержены люди, страдающие глютеновой болезнью, наркоманией и алкоголизмом. Наблюдается она и у лиц, которые долго принимают лекарства от судорог (фенобарбита, дифенин и пр.). Также спровоцировать эту анемию могут полипы или рак желудка, кишечные патологии и паразиты, гепатиты и цирроз печени.
Такая анемия зачастую проявляется у детей, вскормленных козьим или порошковым молоком, и у беременных женщин. При этом болезнь сопровождается головокружением и слабостью, одышкой и утомляемостью. Кожа становится суховатой и приобретает бледный желтовато-лимонный оттенок. Больного может часто знобить и лихорадить.
Изменения в крови идентичны В-12-дефицитной анемии. Как правило, гемоглобин остается в норме, а иногда даже повышен. В составе крови присутствуют макроциты – это эритроциты, имеющие увеличенный размер. Для фолиеводефицитной анемии вообще характерно пониженное количество всех кровяных клеток при увеличении их размера. Это гиперхромная анемия с довольно высоким показателем цвета. Биохимия крови показывает, что свободный билирубин немного повышен.
Фолиеводефицитное малокровие лечат с помощью лекарственных препаратов фолиевой кислоты в таблетированной форме. Помимо этого следует подкорректировать и питание пациента (предпочтительны листовые овощи, печень, больше фруктов).
Отдельно следует отметить, что В-12- и фолиеводефицитная анемия являются разновидностями макроцитарной анемии – это патология, характеризующаяся увеличением размеров эритроцитов из-за острой нехватки В-12 или фолиевой кислоты.
Все разновидности этих анемий обусловлены чрезмерным разрушением эритроцитов. В норме продолжительность жизни эритроцитов составляет ≈120 суток. Когда же у человека появляются антитела против его же эритроцитов, то начинается резкое эритроцитарное разрушение, т.е. жизнь эритроцитов становится значительно короче (≈13суток). Гемоглобин в крови начинает распадаться, из-за чего у больного развивается желтуха на фоне гемолитической анемии.
Лабораторным симптомом такой анемии является повышенный билирубин, присутствие в моче гемоглобина и пр.
Значительное место среди таких анемий занимают наследственные разновидности. Они являются последствиями множества дефектов в образовании эритроцитов на генетическом уровне. Приобретенные разновидности гемолитических анемий развиваются на фоне определенных факторов, оказывающих на эритроциты разрушающее действие (воздействие механического характера, различные яды, антитела и т. д.).
Одной из распространенных наследственных гемолитических анемий является серповидно-клеточная. Это заболевание подразумевает присутствие патологического гемоглобина в эритроцитах. Эта патология чаще поражает афроамериканцев, но встречается и у светлокожих людей.
Наличие в крови серповидных эритроцитов, характерное для этой патологии, ее носителю обычно ничем не грозит. Но если и мать, и отец имеют в крови этот патологический гемоглобин, то их дети рискуют родиться с тяжелейшей формой серповидно-клеточного малокровия, именно поэтому такая анемия опасна.
фото: кровь при гемолитической анемии. Эритроциты – неправильной формы
Сопровождается эта разновидность анемии ревматическими болями, слабостью, болями в животе и голове, сонливостью, припухлости голеней, кистей и стоп. Врачебный осмотр обнаруживает бледность слизистых и кожи, увеличенную селезенку и печень. Для имеющих эту патологию людей характерно худое телосложение, высокий рост и искривленный позвоночник.
Анализ крови показывает умеренную, либо тяжелую степень анемии, причем показатель цвета будет в норме.
Данная патология – тяжелейшее заболевание. Основная масса пациентов умирает, как правило, не дожив до десятилетнего возраста, по причине какой-либо инфекции (чаще туберкулеза) или внутреннего кровоизлияния.
Лечение этого малокровия является симптоматическим. Хоть оно и считается хронической анемией, дети довольно легко переносят низкое содержание эритроцитов и гемоглобина. Именно поэтому им довольно-таки редко проводят переливание крови (чаще в случаях апластического или гемолитического криза). Следует избегать всевозможных инфекций, особенно детям.
Среди приобретенных разновидностей чаще встречается аутоимунная гемолитическая анемия. Она подразумевает воздействие образовавшихся в организме больного антител. Такая разновидность встречается, как правило, при хронических циррозах и гепатитах, ревматоидных артритах, остром лейкозе, либо хроническом лимфолейкозе.
Бывает хроническая, а также острая форма аутоимунной гемолитической анемии. Хроническая форма протекает практически без характерных симптомов. При острой форме больной страдает желтухой, одышкой, слабостью, лихорадкой, частым сердцебиением. Каловые массы по причине чрезмерного содержания стеркобилина имеют темно-коричневый оттенок.
Хотя и редко, но можно встретить аутоиммунную анемию с полными холодовыми антителами, которая свойственна людям преклонного возраста. Холод в подобных случаях выступает в качестве6 провоцирующего фактора, приводящего к отеку и посинению пальцев рук, лица, стоп. Часто аутоиммунная анемия такого типа сопровождается синдромом Рейно, который, к сожалению, может закончиться гангреной пальцев. Кроме этого, у больных с холодовой аутоиммунной анемией невозможно определить группу крови традиционными методами.
Лечение осуществляется с помощью глюкокортикоидных гормонов. Важную роль в лечении играет его длительность и правильная дозировка препаратов. Также в лечении врачи используют цитостатические препараты, проводят плазмаферез, а при необходимости – спленэктомию.
Следует помнить, что многие разновидности анемий при неправильном их лечении могут иметь тяжелейшие последствия для организма, вплоть до летального исхода. Поэтому не надо заниматься самолечением. Диагноз должен поставить квалифицированный врач, равно как и назначить эффективное и правильное лечение!
источник
Важным при диагностике многих заболеваний является определение уровня эритроцитов. Для этого проводят исследование крови.
Исходя из его результатов делают выводы о диагнозе и лечении. Часто обнаруживается, что эритроциты в крови понижены. Такое патологическое состояние в медицинской терминологии называют эритропенией.
Что это за нарушение, какие симптомы обычно возникают, могут ли быть осложнения – об этом пойдет речь в данной статье.
Красные кровяные тельца называются эритроцитами. В их состав входит гемоглобин, который является специфическим белком, имеющим форму двояковыгнутого диска.
Эти клетки преимущественно вырабатываются в костном мозге. Они выполняют очень важные функции в организме:
- перенесение кислорода к тканям организма;
- выведение газа углекислого;
- обеспечение щелочно-кислотного баланса.
При любом отклонении от нормы у человека возникает плохое самочувствие в результате гипоксии. Такое состояние может быть вызвано рядом серьезных и опасных заболеваний.
Нормальный уровень красных клеток должен быть следующим:
- после рождения и до одного года – от 4,3 до 7,7 млн в мкл;
- до 14 лет – от 3,5 до 4,8 млн в мкл;
- у женщин – от 3,6 до 4,7 млн в мкл;
- у лиц мужского пола значение должно составлять от 3,5 до 4,8 единиц.
У людей преклонного возраста показатель колеблется от 4 до 4,3.
Отклонение от нормы в любую сторону может свидетельствовать о различных патологических процессах, происходящих в организме, и вызывать развитие нежелательных и опасных последствий.
Низкое содержание эритроцитов приводит к тому, что у человека может развиваться анемия. При таком состоянии кислород плохо распространяется по тканям, а выведение углекислого газа замедляется.
Снижение эритроцитов сопровождается следующими признаками:
- общая слабость;
- нарушение сна;
- повышение потливости;
- гипертония;
- влажные и холодные кожные покровы;
- понижение работоспособности;
- потеря аппетита;
- бледность слизистых и кожи;
- учащение пульса;
- головокружения и головные боли;
- нарушение координации.
В некоторых случаях может наблюдаться обморочное состояние, понижается давление. Нередко бывает одышка.
Если у человека проявляются такие симптомы, то ему необходимо обратиться за помощью к специалисту, который даст направление на диагностику и после выяснения основной причины назначит соответствующее лечение.
Основным диагностическим методом для определения числа красных телец является общий анализ крови.
Сдавать биоматериал важно на голодный желудок. Перед исследованием не разрешается употреблять алкогольсодержащие напитки, курить, выполнять тяжелую физическую работу.
Материал для исследования берут из вены или пальца верхней конечности.
Для определения причины понижения кровяных клеток применяются дополнительные методы диагностики.
Низкий показатель эритроцитов бывает относительного и абсолютного типа. При последнем варианте организм вырабатывает небольшое количество эритроцитов. Это происходит вследствие форсированной гибели клеток или потери крови.
При относительном возможно ложное снижение эритроцитов. Часто такое случается при нарушениях разжижения крови. Обычно это наблюдается в период вынашивания ребенка. Поэтому при беременности у женщин часто падает гемоглобин.
Специалисты определяют следующие причины снижения эритроцитов:
- гемолиз;
- гиповитаминоз;
- анемия;
- пиелонефрит;
- нефрит;
- лейкозы;
- паразитарные инвазии;
- гломерулонефрит;
- мочекаменная болезнь;
- цирроз;
- колит;
- гастрит;
- болезнь Крона;
- гемоглобинопатия;
- эндокринные нарушения.
Понижается количество эритроцитов при генетической предрасположенности, при таких наследственных болезнях кровеносной системы, как микросфероцитоз и овалоцитоз.
В некоторых случаях причинами становятся инфекции, например, дифтерия или коклюш.
Еще одним фактором, провоцирующим патологию, является дефицит витаминов группы В или железа.
Также понижаются эритроциты в детской крови. Причинами могут быть:
У мужчин патологическое состояние может развиваться в результате аденомы предстательной железы.
У женщин показатель эритроцитов снижается при менструации.
К другим факторам, вызывающим дефицит красных клеток в анализе крови у взрослого, относятся:
- онкологические заболевания;
- вегетарианское питание;
- кровопотери при операциях, ранениях, переломах;
- внутренние кровотечения;
- ослабление иммунной системы;
- использование некоторых лекарственных препаратов;
- применение антибиотикотерапии;
- аутоиммунные болезни;
- нарушение свертываемости крови;
- болезни кишечника, мочевыводящей системы.
Если костный мозг вырабатывает клетки на низкой скорости, то это также приводит к эритропении.
Лечение при пониженном содержании этих клеток зависит от основной причины, которая спровоцировала данную патологию. Оно должно быть направлено на устранение заболевания, которое сопровождается дефицитом эритроцитов. Важно, чтобы терапия осуществлялась с комплексным подходом.
Обычно для нормализации уровня применяют медикаментозные средства с содержанием витаминов группы В (в частности В9 и В12) и железа.
При очень сниженных эритроцитах назначаются внутривенные инъекции с фолиевой кислотой и цианокобаламином. Используются также железосодержащие лекарства в таблетированной форме.
- Тотема;
- Ферретаб;
- Гемобин;
- Тардиферрин;
- Феозор;
- Гемофер;
- Актиферрин;
- Ферроплекс;
- Мальтофер;
- Хеферол;
- Венофер;
- Феррум Лек;
- Сорбифер Дурулес.
При различных заболеваниях, на фоне которых падают эритроциты, применяются различные методы лечения:
- Если нарушена их выработка клеток в мозге, то назначаются лекарства, которые стимулируют этот процесс.
- В случае кровопотерь показано оперативное вмешательство. Также может потребоваться переливание.
- При онкологических процессах используется хирургический метод лечения, химио- или лучевая терапия.
- При беременности также показатель можно повысить применением препаратов железа.
- Для лечения паразитарных заболеваний применяются Бильтрицид и Фенасал.
В любом случае показано диетическое питание, включающее продукты с большим содержанием железа и витамина В.
Важно понимать, что при понижении эритроцитов противопоказано самолечение. Сначала специалист должен провести дополнительную диагностику, затем выяснить основную причину состояния и только после этого назначить соответствующий метод лечения.
Основным осложнением уменьшения процентного содержания красных телец считается кислородное голодание органов. Такое патологическое состояние может привести к развитию нежелательных последствий.
К ним относится обморочное состояние, отмирание тканей. При тяжелых патологиях, сопровождающихся понижением эритроцитов, может быть летальный исход.
Чтобы избежать недостатка эритроцитов, необходимо соблюдать следующие правила профилактики:
- сдавать на проверку кровь не менее двух раз в год;
- придерживаться полноценного и рационального питания;
- принимать витаминно-минеральные комплексы;
- вести здоровый образ жизни;
- выполнять все врачебные предписания;
- включить в рацион свежие фрукты, овощи и зелень;
- полноценно и регулярно высыпаться;
- чередовать труд с отдыхом;
- не допускать постоянных физических нагрузок;
- избегать стрессовых ситуаций;
- ежегодно проходить профилактические медицинские осмотры.
Если человек заметил симптомы эритропении, ему необходимо своевременно обратиться к врачу за помощью.
Важно помнить, что болезнь труднее лечить, чем предупредить. Поэтому необходимо придерживаться основных рекомендаций относительно профилактики патологии.
Таким образом, красные клетки выполняют важную роль в организме, которая в первую очередь заключается в переносе гемоглобина ко всем тканям. Понижение в крови эритроцитов обычно указывает на патологическое состояние, которое происходит в человеческом организме. Часто такое явление может указывать на тяжелые и смертельные заболевания.
Очень важно вовремя обнаружить патологию, установить на фоне чего она могла развиваться и начать лечение.
источник
Красные кровяные тельца, которые называются эритроцитами, содержат в себе гемоглобин. Этот белок является очень важным для организма, ведь именно он отвечает за процесс обмена железом, также транспортирует кислород к каждой клеточке нашего тела. Но при каких показателях анемия диагностируется у человека? Это происходит в том случае, когда количество эритроцитов и уровень гемоглобина начинают стремительно снижаться.
О том, что в организме начинает протекать такое заболевание, как малокровие, можно узнать по определенным симптомам, но только лабораторные исследования крови помогут специалисту действительно засвидетельствовать этот факт и установить тип малокровия и степень его тяжести.
Для того чтобы специалист мог установить максимально точный диагноз протекающего недуга, пациенту необходимо сдать несколько анализов:
- Общий анализ крови.
- Расширенный анализ крови.
- Биохимический анализ крови.
Если дополнительные анализы могут назначаться специалистом по требованию, то общий анализ крови является обязательным. Основным признаком малокровия будет сниженный уровень гемоглобина. Также учитывается цветовое изменение эритроцитов при анемии. Оптимальный его показатель составляет не ниже 0,8, но при малокровии он всегда будет падать.
Также гемограмма при анемиях (тот же общий анализ крови) позволяет установить специалисту степень тяжести малокровия:
- Легкая степень. Гемоглобин снижается до 90 г/л.
- Средняя степень. Концентрация гемоглобина снижается до 70 г/л.
- Тяжелая степень. Гемоглобин опустился ниже 70 г/л.
Расшифровка картины результатов общего анализа крови будет включать следующие моменты:
- Количество красных кровяных телец.
- Уровень лейкоцитов. Они выполняют защитную функцию в теле человека.
- Тромбоциты. Это бесцветные и очень мелкие клетки в крови. Они отвечают за процесс свертывания крови, а также является первой помощью при повреждениях.
- Гемоглобин. Является белком, основу которого составляет железо. Именно гемоглобин придает эритроцитам их нормальный цвет, а также переносит кислород по кровеносной системе.
- СОЭ. Этот показатель свидетельствует о скорости оседания эритроцитов. На основании полученных результатов, специалист может оценить уровень свертываемости крови.
- Цветовой показатель. Он позволяет оценить содержание гемоглобина в каждом эритроците.
Исходя из полученных результатов, специалист может диагностировать форму недуга, а также назначить правильное лечение малокровия. Стоит отметить, что общий анализ крови необходимо сдавать не только при проявлениях симптоматики малокровия. Если делать это систематически, то можно быстрее среагировать на протекающий недуг и пресечь любые осложнения.
Также общий анализ крови позволяет специалист определит размер эритроцитов, их форму и цветовой показатель. Анизоцитоз при анемии будет свидетельствовать о том, что размер эритроцитов отдалился от нормы. Если диагностировано серьезное отклонение, то без оперативного лечения могут возникнуть серьезные осложнения.
Чаще всего у пациентов диагностируется железодефицитная анемия. Вместе с этим, отмечается анемия и тромбоцитоз, который и возникает в результате резкого снижения железа, что может быть спровоцировано сильными кровотечениями или обычными процессами, протекающими во время беременности.
На основании этого анализа, специалист может судить о патогенности процесса, который протекает в организме пациента. Если СОЭ повышен при анемии, то это свидетельствует о сниженном гемоглобине в эритроцитах. Показатели скорости оседания эритроцитов практически всегда зависят от уровня гемоглобина. Это значит, что если уровень гемоглобина увеличен, то СОЭ буден снижен. Если у пациента диагностируется низкий уровень гемоглобина, но высокий показатель оседания эритроцитов, то специалисты диагностируют развитие патогенного процесса в организме пациента. Если быстро компенсировать дефицит гемоглобина, то всего за несколько дней можно нормализировать положение.
Ретикулоцитами называют клетки эритроидного ряда, которые являются основной для создания будущих эритроцитов. Трансформация одной клетки в другую происходит в результате влияния определенного гормона – эритропоэтина. Если же эритроциты начинают быстро разрушаться, то костный мозг начинает вырабатывать ретикулоциты в больших количествах, чтобы компенсировать недостачу.
Специалисты проверяют ретикулоцитоз при анемиях для того, чтобы оценить состояние костного мозга, почек, а также патогенный процесс разрушения эритроцитов. Стоит отметить, что увеличение количества этих клеток не всегда является негативным проявлением.
источник
Что делать, если эритроциты понижены? Какие патологии могут приводить к снижению количества эритроцитов?
Наиболее часто понижение уровня эритроцитов выявляют у женщин, в особенности у беременных. Связанно это с тем, что большое количество железа, входящее в состав гемоглобина, расходуется в ходе формирования как плода, так и плаценты.
Стоит отметить тот факт, что снижение эритроцитов в большинстве случаев сопровождается с одновременным уменьшением уровня гемоглобина, что проявляется анемией или малокровием.
| Возраст | Пол | Единицы измерения (10 12 клеток на литр) |
| Новорожденные дети | ||
| С 1 по 3 день | 4,0 – 6,6 | |
| С 3 по 7 день | 3,9 – 6,3 | |
| С 8 по 14 день | 3,6 – 6,2 | |
| Грудничковые дети | ||
| С 15 по 30 день | 3,0 – 5,4 | |
| С 2 до 3 месяцев | 2,7 – 4,9 | |
| С 3 до 5 месяцев | 3,1 – 4,5 | |
| С 6 месяцев до 2 лет | мальчики | 3,4 – 5,0 |
| девочки | 3,7 – 5,2 | |
| Дети дошкольного возраста | ||
| С 3 до 6 лет | 3,9 – 5,3 | |
| Дети младшего школьного возраста | ||
| С 7 до 12 лет | 4,0 – 5,2 | |
| Пубертатный период | ||
| С 13 до 18 лет | мальчики | 4,5 – 5,3 |
| девочки | 4,1 – 5,1 | |
| Взрослые | ||
| С 18 лет | мужчины | 3,9 – 5,5 |
| женщины | 3,5 – 4,7 | |
Необходимо заметить, что в зависимости от того? какие методы подсчета, а также инструменты используются, в различных лабораториях показатели могут несколько отличаться от вышеуказанных.

При обнаружении снижения уровня эритроцитов следует повторно сдать общий анализ крови. Если в анализе вторично выявляют эритропению (снижение эритроцитов ниже 3,5 – 3,9х10 12 клеток на 1 литр), то в этом случае необходимо как можно скорее записаться на прием к врачу.
В зависимости от степени эритропении у людей могут возникать различные симптомы. К самым частым из них относят головную боль, общую слабость, одышку, снижение артериального давления и бледность кожных покровов, а также слизистых оболочек. Стоит отметить, что данные симптомы также характерны и для анемии.
Наиболее часто к понижению уровня эритроцитов приводят следующие патологические состояния:
- авитаминоз;
- кровотечение;
- лейкоз (злокачественное перерождение клеток крови);
- наследственные ферментопатии (нарушение функциональной активности некоторых ферментов);
- наследственные мембранопатии эритроцитов (дефект мембран эритроцитов);
- серповидно-клеточная анемия (наследственное заболевание, связанное с нарушением строения гемоглобина);
- гемолиз (разрушение эритроцитов).

Стоит также отметить, что витамин В12 участвует в другом очень важном процессе – миелинизации нервных волокон. Благодаря веществу миелину по отросткам нервных клеток биоэлектрический импульс способен проводиться почти в 10 раз быстрее, чем по немиелинизированным волокнам. Нарушение миелинизации может происходить на уровне периферической и/или центральной нервной системы и приводить к различным неврологическим симптомам.
К дефициту витамина В9 и В12 в организме могут приводить следующие ситуации:
- Уменьшение поступления витамина В12 и фолиевой кислоты с пищей. Стоит отметить, что ни витамин В12, ни фолиевая кислота не способны синтезироваться в человеческом организме. Именно поэтому необходимо периодически пополнять запасы данных витаминов. Витамин В12 в больших количествах содержится в таких продуктах животного происхождения как мясо, печень, почки, куриные яйца, молоко, рыба. В свою очередь, фолиевой кислотой богаты продукты растительного происхождения (листья салата, капуста, огурцы, фасоль, горох, апельсины и др.).
- Заболевания подвздошной кишки. Дело в том, что различные воспалительные процессы, которые локализуются на уровне толстого кишечника (нижняя часть подвздошной кишки), приводят к тому, что витамин В12 не способен нормально всасываться в кровоток. К таким заболеваниям можно отнести колит (воспаление толстого кишечника), болезнь Крона (хроническое заболевание желудочно-кишечного тракта с преимущественным поражением подвздошной кишки), опухоли толстого кишечника.
- Недостаточность фактора Касла. Фактор Касла (внутренний фактор) представляет собой гликопротеин (состоит из аминокислот и углеводов), который переводит неактивную форму витамина В12, поступающей с пищей, в активную. Внутренний фактор вырабатывается в желудке (фундальными железами). Частичное удаление желудка (резекция желудка), рак желудка или атрофический гастрит (замещением функциональной ткани желудка на соединительную) могут привести к нарушению синтеза внутреннего фактора. Кроме того, к фактору Касла могут образовываться антитела, которые не позволяют данным молекулам выполнять функцию по трансформации витамина В12. Стоит отметить, что фактор Касла является крайне важным еще и потому, что он усиливает работу системы кроветворения.
- Паразитарные или бактериальные заболевания также могут становиться причиной нарушения всасывания витамина В12. Некоторые ленточные черви (свиной и бычий цепень), а также бактерии (актиномицеты) используют на свои нужды данный витамин, тем самым, лишая его организм человека.
Для диагностики дефицита витамина В12 (в том числе и В12-дефицитной анемии) необходимо учитывать как результаты клинического анализа крови, так и основываться на клинических проявлениях данной патологии. Для этого необходимо проконсультироваться с врачом-гематологом.
В общем анализе крови помимо пониженных эритроцитов также выявляют следующие отклонения:
- снижение уровня гемоглобина;
- наличие мегалобластов (клетки-предшественники эритроцитов, которые имеют более крупные размеры и аномальную форму);
- повышение цветового показателя (повышение относительного содержания гемоглобина в красных кровяных тельцах);
- снижение уровня белых кровяных телец (лейкоциты расходуются в иммунных реакциях);
- снижение уровня тромбоцитов (участвуют в процессе свертывания крови);
- понижение молодых форм эритроцитов (ретикулоциты).
Главным критерием, который говорит в пользу дефицита В12 в организме, служит выявление в анализе мегалобластов. Данные клетки представляют собой крупные и аномальной формы клетки, отвечающие за эритропоэз (образование эритроцитов), и которые, однако, не в состоянии давать в дальнейшем нормальную популяцию красных кровяных телец.
| Симптом | Механизм возникновения |
| Замедление роста и развития у детей | Витамин В12 участвует в процессе кроветворения. Уменьшение поступления или нарушение всасывания данного витамина в детском возрасте нередко приводит к В12-дефициной анемии. Снижение количества эритроцитов, а также понижение уровня гемоглобина приводит к кислородному голоданию (гипоксия) и крайне неблагоприятно сказывается на работе головного мозга, легких и сердца. Также данный витамин принимает участие в синтезе ДНК, и его дефицит приводит к замедлению и нарушению роста практически всех тканей организма. |
| Неврологические нарушения | Нарушение миелинизации нервных волокон (образование специальной мембраны на отростках нервных клеток) может сопровождаться нарушением чувствительности, парезами (нарушение двигательной функции мышц), воспалением периферических нервов, появлением патологических рефлексов. |
| Анемия | Дефицит витамина В12 негативно сказывается на синтезе и созревании форменных элементов крови. В конечном счете, количество эритроцитов постепенно уменьшается. Внешне анемия проявляется бледностью кожи и слизистых оболочек. |
| Снижение иммунитета | Кроме снижения количества красных кровяных телец и гемоглобина, также наблюдается снижение лейкоцитов (белые кровяные тельца). Эти клетки участвуют в клеточном иммунитете и при необходимости нейтрализуют болезнетворные микроорганизмы. Уменьшение количества лейкоцитов (лейкопения) повышает риск возникновения разного рода инфекционных заболеваний. |
| Атрофический глоссит (глоссит Гюнтера-Хантера) | Является одним из специфических проявлений дефицита витамина В12 в организме. Сосочки на языке могут уменьшаться в размере или полностью исчезать, при этом язык становится блестящим и гладким. Также возникает атрофия (уменьшение объема мышечной ткани) мышц языка, что приводит к уменьшению его размеров. |
| Поражение желудочно-кишечного тракта | Витамин В12 абсолютно необходим для нормального функционирования пищеварительной системы. Наиболее чувствительным к дефициту цианокобаламина является желудок. Чаще всего наблюдают снижение секреции желудочного сока вследствие атрофии слизистой оболочки желудка. |
Подбор необходимой тактики лечения авитаминоза у взрослых и, в особенности у детей, должен проводиться грамотным доктором. В зависимости от причины возникновения в организме дефицита витамина В12 принципы лечения могут несколько отличаться.
Лечение авитаминоза В12 подразумевает:
- Полноценное питание позволяет в быстрые сроки восстановить запасы витамина В12 в организме. В день следует употреблять не менее 70 – 80 грамм белковых продуктов животного происхождения, в которых содержится данный витамин (мясо, молоко, яйца, печень, рыба).
- Дополнительный прием витамина В12 необходим в абсолютном большинстве случаев, так как авитаминоз чаще всего возникает на фоне нарушения всасывания данного витамина в кишечнике. Наиболее предпочтительным является внутримышечный способ введение витамина (также возможно и внутрикожное введение). В течение первой недели пациенту каждый день вводят 100 мкг витамина В12. За первые полтора месяца лечения необходимо ввести не менее 2 грамм цианокобаламина (2000 мкг). В дальнейшем переходят на поддерживающее лечение, в ходе которого пациенту вводят 100 мкг витамина один раз в месяц. Стоит отметить, что поддерживающая терапия должна проводиться на протяжении всей жизни.
- Дегельминтизация нужна в том случае, если в организме пациента находят ленточных червей. Основными противопаразитарными препаратами являются фенасал и бильтрицид. Дозировку и способ применения данных лекарственных средств определяет лечащий врач.
- Лечение сопутствующих заболеваний. Нередко всасывание цианокобаламина возникает на фоне имеющихся патологий кишечника. В этом случае необходимо подобрать щадящую диету (стол №4), а также принимать препараты, которые способствуют улучшению пищеварения (панкреатин, пангрол).
| Степень тяжести кровотечения | Количество потерянной крови (мл) |
| Легкое кровотечение | до 500 |
| Среднее кровотечение | 500 – 1000 |
| Тяжелое кровотечение | 1000 – 1500 |
| Смертельное кровотечение | 2500 – 3000 |
| Критерии | Артериальное кровотечение | Венозное кровотечение |
| Цвет крови | Ярко-алый из-за большого содержания оксигемоглобина (гемоглобин, связанный с кислородом). Именно оксигемоглобин придает артериальной крови ярко-красный оттенок. | В венозной крови содержится гемоглобин, связанный с углекислым газом (карбгемоглобин), что придает более темный оттенок крови (темно-красный или темно-вишневый). |
| Скорость кровопотери | Из крупных артерий (бедренная, плечевая или сонная) кровь изливается с большой силой, фонтаном. Из более мелких артерий кровь может изливаться прерывистыми толчками, которые соответствуют сердечным сокращениям. | Кровь истекает непрерывно, но в гораздо меньшем объеме, чем при артериальном кровотечении. В некоторых случаях, при повреждении вен малого калибра кровь может остановиться самопроизвольно за счет образования тромба. |
| Общее состояние пострадавшего | Сильная кровопотеря приводит к повышению частоты сердечных сокращений (тахикардия), в то время как пульс становится едва ощутимым. Кожные покровы резко бледнеют, возможна потеря сознания. | Как правило, остается стабильным. |
Выявление внутреннего кровотечения, в особенности незначительного может быть сильно затруднено. Заподозрить данный вид кровотечения позволяет наличие таких неспецифических симптомов как гипотония (снижения артериального давления), ослабление силы пульса вместе с его учащением, появление бледности лица, слабости, недомогания.
К более характерным проявлениям относят наличие рвоты «кофейной гущей» при желудочном кровотечении или дегтеобразный стул (мелена) при кишечном кровотечении. В свою очередь, при кровотечении в плевральную полость (полость из двух листков, которая непосредственно граничит с каждым легким) может наблюдаться нарушение дыхания, одышка, а при значительном скоплении крови – смещение сердца (при этом могут наблюдаться аритмии). При кровоизлиянии в полость перикарда (сердечная сумка) наблюдаются нарушения в работе сердца, которые могут быть выявлены в ходе проведения эхокардиографии сердца (УЗИ сердца), а также электрокардиограммы (ЭКГ). В том случае, если кровь скапливается в брюшной полости, то тогда наблюдается притупление перкуторного звука при простукивании брюшной стенки, а также симптомы, указывающие на раздражение брюшины (серозная оболочка, которая покрывает брюшную полость изнутри).
Подтвердить наличие внутреннего кровотечения позволяет диагностическая пункция, в ходе которой из полости производят забор скопившейся жидкости (в данном случае это кровь). При необходимости подтвердить наличие внутрибрюшного кровотечения прибегают к диагностической лапароскопии (доступ к брюшной полости достигается с помощью небольшого отверстия в стенке живота).
Для того чтобы оценить величину кровопотери, прибегают к использованию различных формул и методик. Ориентировочно о степени кровопотери можно судить, основываясь на данных о гипотонии (снижение артериального давления) и тахикардии (увеличение частоты сердечных сокращений) в позиции лежа и сидя. Также судить о количестве потерянной крови позволяет снижение показателя гематокрита (объем эритроцитов в крови). Однако данный способ может быть использован лишь спустя 5 – 8 часов после самого кровотечения. Самым точным способом является определение объема циркулирующей крови с помощью специальной формулы. Вычисленная степень кровопотери в дальнейшем используется врачом для определения способа, объема и скорости трансфузионной терапии (восполнение потерянной крови).
Тактика лечения зависит от степени и скорости кровопотери. Наиболее опасным является артериальное кровотечение, которое при повреждении таких крупных артерий как сонная (в области шеи), бедренная или плечевая может закончиться смертельным исходом всего за несколько минут (5 – 10 мин). Именно поэтому при обнаружении артериального кровотечения следует немедленно вызвать бригаду скорой помощи, а также оказать первую помощь пострадавшему.
Оказание первой помощи при артериальном кровотечении включает следующие мероприятия:
- Приподнять поврежденную конечность. При повреждении артерий среднего или мелкого калибра конечность следует приподнять, а затем пережать поврежденную артерию пальцами выше места кровотечения (на 2 – 5 см от места повреждения). В том случае если повреждена сонная артерия, то тогда поврежденный сосуд необходимо прижать пальцами к позвоночнику (к поперечным отросткам шейных позвонков).
- При сильном кровотечении наложить жгут. В случае если кровь вытекает пульсирующей струей, следует наложить жгут. Жгут накладывается поверх тугого валика, который прижимает артерию к костному выступу (тем самым, просвет артерии полностью смыкается). Также под жгут следует подложить ткань или накладывать его поверх штанов или рукава, для того чтобы избежать травматизации кожи. При кровотечении из нижней конечности жгут накладывают на бедренную артерию в области верхней трети бедра. При кровотечении из верхней конечности следует наложить жгут на плечевую артерию в области середины плечевой кости. При правильно наложенном жгуте происходит не только остановка кровотечения, но также не прощупывается пульс ниже места его наложения. При необходимости в качестве импровизированного жгута можно использовать обычный ремень, веревку или шарф.
- Указать время наложение жгута. После того как был наложен жгут следует приложить к нему записку, в которой указывают точное время наложения жгута. Жгут накладывают на конечность не более чем на 40 минут. В противном случае возникает ишемия (прекращение притока артериальной крови к тканям) и отмирание тканей.
- Наложить стерильную повязку на рану. Во избежание попадания инфекции, на рану следует наложить стерильную повязку.
В том случае, если возникает венозное кровотечение, на рану необходимо наложить давящую повязку. Для этого в качестве перевязочного материала можно использовать марлю, бинт или любую другую чистую ткань (например, чистый носовой платок).
Стоит отметить, что потеря крови в количестве менее 200 мл практически никак не влияет на общее состояние пострадавшего. В том случае, если степень кровопотери превышает 500 мл, то тогда необходимо проводить инфузионно-трансфузионную терапию. На первом этапе проводят мероприятия по устранению гиповолемии (уменьшение объема циркулирующей крови), а затем, при необходимости, используют некоторые препараты крови.
Препаратами, которые могут быть использованы в трансфузионной терапии, являются:
- Кристаллоиды представляют собой группу инфузионных растворов (вводятся внутривенно), которые содержат электролиты (натрий, калий, хлор, кальций). Кристаллоидные растворы позволяют не только восполнить объем циркулирующей крови, но также и регулировать кислотно-щелочной и водно-электролитный баланс крови. К кристаллоидам относят раствор Рингера, изотонический раствор хлорида натрия (физраствор), раствор Гартмана и др. Недостатком кристаллоидов служит их относительно короткое действие (не более нескольких часов). Именно поэтому кристаллоиды используют лишь на первом этапе инфузионной терапии. В дальнейшем, для устранения гиповолемии на более продолжительное время используют коллоидные растворы.
- Коллоидные растворы содержат органические полимеры, которые поддерживают осмотическое давление крови (зависит от концентрации различных электролитов в крови). Коллоиды стабилизируют объем циркулирующей крови, а также позволяют поддерживать нормальные значения артериального давления. К коллоидным растворам относят такие препараты как реополиглюкин, полиглюкин, желатиноль, волювен.
- Препараты крови используются для компенсации потери различных форменных элементов крови. К препаратам данной группы относят эритроцитарную массу (содержит около 70 – 80% эритроцитов) или тромбоцитарную массу (тромбоциты нужны для восстановления свертывания крови).
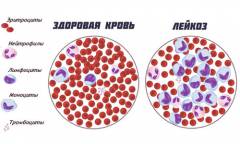
На начальном этапе возникает точечное (локальное) поражение костного мозга. В дальнейшем злокачественный клон в составе опухолевой ткани постепенно заменяет нормальные ростки кроветворения. Прямым следствием лейкоза является снижение численности одного или сразу нескольких видов форменных элементов крови. Стоит отметить, что дальнейшее прогрессирование лейкоза приводит к снижению количества всех клеток крови, приводя к панцитопении (опухолевая ткань вытесняет другие клетки в костном мозге).
Причины лейкоза остаются не до конца изученными. Однако доказано, что к озлокачествлению клеток приводят радиотерапия и химиотерапия (методы лечения онкологических заболеваний), которые негативно влияют на функционирование костного мозга. Также данное заболевание может возникать вследствие генетической предрасположенности.
Прогрессирующее снижение уровня эритроцитов вызывает острый эритроидный лейкоз (эритромиелоз, эритролейкоз, болезнь Ди Гульельмо), при котором клетка-предшественница эритроцитов становится злокачественной. Стоит отметить, что данный вид лейкоза, хотя и отличается прогрессирующим течением, все же встречается относительно редко (в сравнении с другими видами лейкоза).
Диагностикой острого эритроидного лейкоза занимается врач-гематолог. Для того чтобы поставить точный диагноз, необходимо учитывать данные клинического анализа крови, а также провести биопсию костного мозга (цитохимическое исследование образца красного костного мозга).
В клиническом анализе крови при остром эритроидном лейкозе выявляют следующие отклонения:
- Снижение уровня красных кровяных телец возникает из-за того что злокачественный клон клетки-предшественницы эритроцитов дает начало лишь дефектным и слабодифференцированным эритроцитам. В конечном счете, количество зрелых и нормальных красных кровяных телец постепенно снижается. Помимо этого, также снижается уровень белка гемоглобина, который в необходимом количестве могут переносить лишь нормальные эритроциты.
- Преобладание слишком мелких или крупных эритроцитов (анизоцитоз). В норме количество нормоцитов (эритроциты нормального размера) может достигать 60 – 70%, а количество микроцитов и макроцитов (мелкие или крупные эритроциты) не должно превышать 12 – 15%. На фоне уменьшения численности нормальных эритроцитов наблюдается заметное увеличение числа макроцитов. Данные клетки по сравнению с нормоцитами отличает наличие довольно хрупкой клеточной мембраны, а также неправильная овальная форма.
- Снижение количества тромбоцитов и лейкоцитов. Опухолевая ткань постепенно вытесняет другие клетки-предшественницы, которые дают начало тромбоцитам и лейкоцитам. В итоге количество белых кровяных телец, а также кровяных пластинок может резко сокращаться, что проявляется частыми инфекциями и возникновением кровотечений.
- Наличие большого количества клеток-предшественников эритроцитов (эритробластных клеток), которые находятся на различных стадиях созревания. Прогрессирование данного онкологического заболевания приводит к значительному повышению эритробластных клеток.
В свою очередь, при цитологическом исследовании костного мозга (кусочек ткани костного мозга изучают под микроскопом для детального изучения всех клеток) выявляют большое количество незрелых клеток-предшественников эритроцитов, с одновременным уменьшением клеток-предшественников лейкоцитов.
Кроме того, существует целый ряд клинических симптомов, которые возникают при данном онкологическом заболевании кроветворной системы.
| Симптом | Механизм возникновения |
| Анемия (снижение гемоглобина) | Продолжительность жизни эритроцитов при лейкозе в 2 – 3 раза меньше, чем у обычных эритроцитов. Постепенное снижение красных кровяных телец приводит к тому, что гемоглобин транспортируется в меньших количествах, так как только эти эритроциты способны транспортировать данные белковые молекулы (гемоглобин). У людей с анемией кожные покровы приобретают бледный оттенок. |
| Слабость, недомогание, быстрое утомление | Данные симптомы возникают из-за понижения уровня гемоглобина в крови, что, в конечном счете, вызывает кислородное голодание (гипоксия). Самым чувствительным органом к гипоксии является головной мозг человека. В данном случае нервные клетки, входящие в состав центральной нервной системы, не способны длительное время выполнять свои функции в условиях гипоксии, что и проявляется появлением слабости, недомогания, а также снижением трудоспособности. |
| Увеличение селезенки и печени (спленомегалия и гепатомегалия) | Данные симптомы возникают на более поздних этапах болезни. Злокачественные клетки способны в больших количествах проникать в ткани печени и селезенки и приводить к их увеличению в размере (злокачественная инфильтрация). |
| Желтуха | Вследствие того, что эритроциты быстро разрушаются, содержащийся в них гемоглобин выходит в кровяное русло. В дальнейшем гемоглобин преобразуется в желчный пигмент билирубин. Именно большие концентрации билирубина в крови придают слизистым оболочкам и коже желтый цвет. |
| Частые кровотечения | Вытеснение опухолевой тканью клеток-предшественников тромбоцитов приводит к сильному снижению количества кровяных пластинок в крови. Вследствие этого при любых даже незначительных порезах или травмах может возникать сильное кровотечение. |
Химиотерапия является основным способом лечения лейкозов. В основе химиотерапии лежит использование специальных препаратов (цитостатики), которые останавливают рост опухолевой ткани. Необходимо заметить, что в каждом отдельном случае дозу препаратов и длительность химиотерапии подбирают индивидуально.
На первом этапе лечения (первый курс химиотерапии) главной целью является полная остановка роста опухолевой ткани. В том случае, если первый курс химиотерапии дал положительные результаты, назначают поддерживающую терапию. На данном этапе, как правило, используют те же препараты, в тех же дозировках. Затем следует завершающий курс (профилактический), который позволяет на длительное время (в некоторых случаях до конца жизни) устранить все проявления данного онкологического заболевания (достижение стадии ремиссии).
| Название препарата | Механизм действия | Форма выпуска | Дозировка |
| Меркаптопурин | Тормозит образование новых клеток, в том числе и злокачественных, за счет блокировки образования ДНК. Обладает выраженным противоопухолевым действием. | Таблетки по 50 миллиграмм. | Дозировка подбирается индивидуально. Как правило, доза составляет 2,5 миллиграмма препарата на 1 килограмм массы тела в сутки. Дозировка может корректироваться в зависимости от результатов лечения или появления побочных явлений. |
| Митоксантрон | Нарушает структуру ДНК и, тем самым, тормозит бесконтрольное деление злокачественных клеток. Оказывает противоопухолевое и иммунодепрессивное действие (угнетает иммунную систему). | Раствор для инъекции по 10 миллилитров. | Используют для достижения стадии ремиссии. Для взрослых доза составляет 10 – 12 миллиграмм на 1 м 2 . Вводят препарат внутривенно медленно в течение 4 – 5 минут. Суммарная доза составляет 55 – 60 мг/м 2 (препарат вводят на протяжении 5 дней). |
| Цитарабин | Блокирует фермент (ДНК полимераза), который отвечает за образование молекул ДНК, входящих в состав новых клеток. Тормозит рост опухолевой ткани. | Ампулы, содержащие 100 мг порошка, для приготовления раствора для инъекций. | Препарат можно вводить внутривенно, интраректально или подкожно. Внутривенно вводят по 100 мг/м 2 в сутки. Доза за курс составляет 500 – 1000 миллиграмм. Подкожно вводят по 20 мг/м 2 от 2 до 3 раз в день. Курс лечения, как правило, составляет 5 – 7 дней. |
Для коррекции анемии используют переливание эритроцитарной массы. В том случае, если химиотерапия не способствует улучшению состояния или наблюдается рецидив (повторное появление заболевания), то тогда прибегают к операции по пересадке костного мозга.
Во время процесса созревания эритроциты теряют большинство своих внутренних структур (ядро, митохондрии, рибосомы), что делает их неспособными синтезировать новые белковые молекулы, делиться, а также производить большое количество молекул АТФ (аденозинтрифосфат), которые, по сути, являются источником энергии для различных биохимических процессов в клетках. Нарушение структуры ферментов, отвечающих за анаэробный гликолиз (получение энергии в результате преобразования молекулы глюкозы в условиях отсутствия достаточного количества кислорода) приводит к тому, что эритроциты не получают необходимую энергию. В конечном счете, в клетке эритроцитов нарушаются различные процессы, в том числе связанные с поддержанием нормального функционирования клеточной мембраны. Вследствие этого эритроциты не способны проходить через очень мелкие сосуды (не обладают достаточной пластичностью) в результате чего они либо преждевременно погибают внутри сосудов, либо захватываются в селезенке (ретикуло-эндотелиальная система) и подвергаются разрушению. Данные нарушения приводят к хронической гемолитической несфероцитарной анемии (снижение эритроцитов и гемоглобина на фоне разрушения красных кровяных телец).
Врожденные ферментопатии эритроцитов наследуются аутосомно-рецессивно. Это значит, что патология проявляется лишь в случае, когда мутантный ген передается от обоих родителей. В абсолютном большинстве случаев такое наблюдается при близкородственных браках. Если мутантный ген передается лишь от одного родителя, то активность фермента нарушается не полностью, а лишь частично (фермент активен лишь на 50%), что, однако позволяет более чем в достаточной мере обеспечивать энергией эритроциты.
Наиболее часто встречаемые виды наследственных ферментопатий эритроцитов следующие:
- Недостаточность глюкозо-6-фосфатдегидрогеназы. Данный энзим является первым в цикле пентозофосфатного гликолиза, который обеспечивает клетки энергией. Недостаточность этого фермента приводит к тому, что эритроциты становятся крайне чувствительными к воздействию свободных радикалов (агрессивные формы кислорода).
- Недостаточность пируваткиназы является одной из наиболее часто встречаемых ферментопатий у человека (наследуемая аутосомно-рецессивно). Пируваткиназа представляет собой предпоследний фермент, который участвует в реакциях анаэробного гликолиза. Данная энзимопатия встречается в популяции с частотой 1:20000.
Для того чтобы подтвердить наличие какой-либо ферментопатии, нужно определить степень активности данного энзима в эритроцитах. Для диагностики наследственных энзимопатий могут использовать спектрофотометрический анализ (помогает определить строение и состав молекулы энзима) или флуоресцентный капельный анализ, который позволяет за достаточно короткое время (является экспресс методом) узнать, является данный энзим дефектным или нет.
Так, например, при определении дефицита пируваткиназы при помощи флуоресцентного анализа, в кровь пациента дополнительно вносят несколько ферментов (НАДН, лактатдегидрогеназа, фосфоенолпируват). Затем исследуемый образец изучают в ультрафиолетовом свете. В норме флуоресценция исчезает примерно через 15 – 20 минут, тогда как при дефиците фермента флуоресценция наблюдается не менее 50 – 60 минут.
Помимо этого, в семейном анамнезе (наличие у других членов семьи подобных заболеваний) при гемолитических несфероцитарных анемиях, вызванных недостаточностью ферментов, характерно выявление таких патологических состояний как анемия, желтуха, увеличение селезенки (спленомегалия), желчнокаменная болезнь (холелитиаз).
Также важным диагностическим признаком наследственных ферментопатий служит выявление в красных кровяных тельцах небольших и круглых включений (тельца Гейнца-Эрлиха). В нормальных условиях данные тельца образуются в крайне малых количествах, в то время как при ферментопатиях их количество в одном эритроците может достигать 4 или 5 штук.
В клиническом анализе крови чаще всего обнаруживают следующие проявления наследственных ферментопатий:
- снижение уровня гемоглобина (ниже 120 г/л);
- снижение объема эритроцитов в крови до 20 – 40% (в норме у женщин показатели находятся в пределах 36 – 46%, а у мужчин – 40 – 48%);
- увеличение количество ретикулоцитов до 3 – 15% (эритроциты, которые еще не утратили внутриклеточные структуры);
- выявление более крупных и деформированных эритроцитов (макроцитоз).
Чаще всего лечение пациентов с наследственной ферментопатией не требуется. В том случае, если наблюдается массивное разрушение эритроцитов, то врач может назначить принимать фолиевую кислоту по 1 миллиграмму в сутки. Фолиевая кислота способствует нормальному созреванию и образованию нормальных клеток-предшественников эритроцитов, а также и самих зрелых форм красных кровяных телец. При гемолитических кризах (эпизоды с выраженным разрушением эритроцитов) нередко прибегают к внутривенному вливанию эритроцитарной массы для нормализации уровня эритроцитов в крови и улучшения функции газообмена на тканевом уровне.
При тяжелом течении хронической гемолитической несфероцитарной анемии, вызванной наследственной ферментопатией, могут прибегнуть к удалению селезенки (спленэктомия). Дело в том, что дефектные эритроциты при попадании в селезенку быстро захватываются и разрушаются. Селезенку удаляют в том случае, если данный орган увеличен в размере, при частых гемолитических кризах или если возникает угроза разрыва селезенки.
Лицам с диагностированной наследственной ферментопатией крайне нежелательно использовать различные медикаменты с оксидативным эффектом (например, аспирин), которые способны нарушать окислительные процессы в клетках и вызывать массивное повреждение эритроцитов (острый гемолиз).
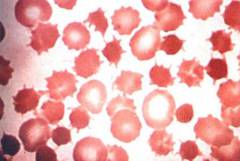
Как и любые наследственные заболевания, данная патология, как правило, проявляется уже в детском возрасте. Для нее характерно невыраженная гемолитическая анемия (снижение уровня гемоглобина и количества эритроцитов за счет разрушения красных кровяных телец в селезенке) с увеличением селезенки и желтушностью кожных покровов и слизистых оболочек.
Всего выделяют 4 основных типа наследственных мембранопатий эритроцитов, для каждого из которых характерен свой особый механизм возникновения.
Выделяют следующие варианты нарушения строения и формы эритроцитов:
- Эллиптоцитоз (сфероцитоз или болезнь Минковского-Шоффара) является самой часто встречаемой врожденной мембранопатией эритроцитов (частота в популяции составляет 1:4500). Данная патология наследуется по аутосомно-доминантному типу (самый частый вид наследования), т.е. существует 50% вероятность унаследовать дефектный ген от одного больного родителя. В основе данной мембранопатии лежат дефекты в структуре двух белков (спектрин, анкирин), в результате чего эритроциты приобретают аномальную сферическую форму (сфероциты). Попав в селезенку, данные сфероциты, не обладая необходимой пластичностью, либо подвергаются полному разрушению, либо теряют часть мембраны и трансформируются в микросфероциты (мелкие эритроциты сферической формы).
- Стоматоцитоз также наследуется аутосомно-доминантным путем (частота неизвестна) и характеризуется появлением эритроцитов, которые с одной стороны выпуклые, а с одной – вогнутые (в норме эритроциты имеют двояковогнутую форму). Для данной формы мембранопатии характерно повышение проницаемости мембраны. В результате этого соотношение ионов калия и натрия может сильно варьироваться. Все это может приводить к появлению двух типов клеток. У одних больных эритроциты становятся сморщенными, содержание гемоглобина в них увеличивается, концентрация воды и ионов снижается. У другой группы больных красные кровяные тельца становятся набухшими, количество переносимого гемоглобина заметно снижается, а концентрация ионов и воды увеличивается (наблюдается при дефекте белка стоматина).
- Акантоцитоз возникает из-за того, что один из липидов (сфингомиелин), участвующих в образовании клеточной стенки, практически полностью заменяется на другой липид – лецитин. В конечном счете, клеточная стенка становится менее стабильной и в ней возникают многочисленные выросты (эритроцит похож на лист аканта). Акантоцитоз может возникать на фоне нарушения метаболизма жиров (абеталипопротеинемия) или сопровождать некоторые врожденные неврологические заболевания (хорея-акантоцитоз, синдром Маклеода).
- Пиропикноцитоз является одной из наиболее редких форм наследственных мембранопатий красных кровяных телец. При данной патологии выявляют сморщенные и деформированные эритроциты. Одной из особенностей таких эритроцитов является то, что они разрушаются при температуре 45 – 46ºС, в то время как нормальные эритроциты выдерживают температуру 50ºС (проба с пиротестом).
Диагностика данного рода наследственных заболеваний не представляет особого труда. При обследовании периферической крови, взятой для проведения общего анализа крови, выявляют эритроциты с характерными изменениями формы, цвета и структуры (морфологические изменения). Так как мембранопатии эритроцитов являются врожденными патологиями, то обнаружить заболевание, как правило, удается в раннем детском возрасте.
Для наследственных мембранопатий эритроцитов характерно:
- Наличие дефектных эритроцитов в крови является наиболее достоверным признаком данной патологии. Так, например, при стоматоцитозе эритроциты уменьшаются или набухают, при эллиптоцитозе эритроциты приобретают нехарактерную сферическую форму (в некоторых случаях выявление сфероцитов может наблюдаться и у здоровых людей), при пиропикноцитозе клетки становятся сморщенными, а при акантоцитозе – на поверхности мембраны выявляют множество выростов. Дефектные эритроциты не способны переносить гемоглобин в достаточном количестве, что приводит к различной степени гипоксии тканей (кислородное голодание). Кроме того, такие эритроциты активно захватываются в селезенке и подвергаются уничтожению.
- Возникновение гемолитических кризов. Под гемолитическими кризами понимают такую патологическую ситуацию, когда за довольно короткий промежуток времени разрушается большое количество эритроцитов. Данные кризы на начальном этапе проявляются лихорадкой, ознобом, тошнотой и слабостью. Затем может возникать рвота, тахикардия (повышение числа сердечных сокращений), болевые ощущения в животе или поясничной области. В редких случаях при тяжелом течении гемолитических кризов артериальное давление может значительно падать (коллапс), а выделение мочи практически полностью прекращается (анурия). Стоит отметить, что нередко гемолитические кризы возникают на фоне различных инфекционных заболеваний.
- Патологические изменения костной ткани у детей. Вследствие тяжелых гемолитических кризов, которые иногда могут иметь рецидивирующее течение (возникают повторные случаи), у маленьких детей возможно ранее зарастание черепных швов, что формирует так называемый башенный череп. При данной патологии выявляют крутой подъем затылочной и теменных костей с одновременным несущественным увеличением поперечных размеров черепа. Для данной патологии характерно возникновение головных болей, головокружения, а иногда и падение остроты зрения. Кроме того, нередко наблюдается изменение позиции зубов, а также высокое расположение верхнего неба.
- Увеличение селезенки (спленомегалия) возникает из-за того, что на уровне сосудов данного органа происходит усиленный распад эритроцитов. В норме эритроциты, имея больший диаметр, чем самые узкие сосуды селезенки (синусы), способны проходить через них благодаря своей пластичности. При наследственных мембранопатиях красные кровяные тельца теряют данную способность. Поэтому эритроциты в большом количестве задерживаются в синусах и активно разрушаются макрофагами (клетки, выстилающие синусы селезенки, одна из функций которых является захват и разрушение старых или дефектных эритроцитов). В конечном итоге, это приводит к увеличению в объеме внутренней стенки (эндотелий) синусов селезенки. Также возникает умеренное или выраженное кровенаполнение тканей селезенки, что и проявляется увеличением органа в размере. Спленомегалия проявляется возникновением болей в левом подреберье (из-за перерастягивания капсулы органа). Во время гемолитических кризов боли могут усиливаться.
- Желтуха появляется вследствие повышения содержания билирубина (несвязанная фракция) в крови. При разрушении эритроцитов гемоглобин также попадает в макрофаги, где пройдя целый ряд промежуточных стадий, трансформируется в желчный пигмент билирубин. После этого билирубин попадает в кровь и далее в печень. Здесь он подвергается связыванию (конъюгация), после чего он направляется в желчь и затем выделяется с калом или мочой. В том случае, если макрофаги в селезенке и кровеносных сосудах поглощают и разрушают большое количество эритроцитов, то в дальнейшем в кровь поступает значительное количество билирубина, который и окрашивает слизистые оболочки, а также кожные покровы в характерный желтый или лимонный цвет.
- Желчнокаменная болезнь (холелитиаз) нередко возникает на фоне врожденных мембранопатий эритроцитов. Все дело в том, что повышение выделения билирубина приводит к тому, что он в больших количествах накапливается в желчном пузыре. Это, в свою очередь, приводит к повышению выработки других желчных пигментов. Чрезмерное накопление данных пигментов наряду с нерациональным питанием (недоедание или переедание) и нарушениями обменных процессов, является предрасполагающим фактором к возникновению желчнокаменной болезни.
Стоит отметить, что обнаружение морфологически измененных эритроцитов (форма и структура) в мазке крови еще ни о чем не говорит. В некоторых случаях выявление эритроцитов с аномальной формой (сферическая, овальная или другая) может наблюдаться и у здоровых людей. Лечение необходимо в том случае, когда пациентов беспокоят характерные клинические проявления наследственных мембранопатий эритроцитов (гемолитические кризы, желтуха, желчнокаменная болезнь).
Наиболее действенным и подчас единственным способом лечения данного рода врожденных патологий является удаление селезенки (спленэктомия). Именно благодаря спленэктомии возможно практически полное прекращение возникновения рецидивов гемолитических кризов, а также устранение анемического состояния. Хотя данная хирургическая операция и не способна устранить наличие дефектов мембраны красных кровяных телец, однако ее результаты позволяют значительно улучшить качество жизни пациентов с наследственной мембранопатией.
| Относительные показания | Абсолютные показания |
| Наличие гемолитических кризов | Упорная желтуха (длительное течение) |
| Значительное увеличение селезенки | Трофические язвы голеней |
| Выраженная анемия | |
| Желчнокаменная болезнь |
Стоит отметить, что операцию, как правило, проводят пациентам, чей возраст находится в промежутке от 10 до 26 лет. Удалять селезенку детям до 10 – 12 лет считается нецелесообразно из-за того, что данный орган играет важную роль в формировании иммунного статуса (в селезенке проходят дифференциацию и активируются Т-лимфоциты и В-лимфоциты, происходит образование антител и т. д.). Кроме того, некоторые инфекционные заболевания при удалении селезенки в раннем детском возрасте могут носить фульминантный характер (молниеносный) или приводить к сепсису (заражение крови).
На сегодняшний день спленэктомию проводят лапароскопическим методом. Данный метод позволяет через небольшие отверстия (в среднем, 0,5 – 1,0 см) в брюшной стенке обеспечить доступ к различным органам брюшной полости, в том числе и к селезенке. Через одно из отверстий хирург вводит лапароскоп, который, по сути, представляет собой телескопическую трубку, которая снабжена видеокамерой и способна передавать изображение на экран монитора. Благодаря лапароскопу, врач имеет возможность наблюдать за ходом операции и в реальном времени корректировать все свои действия.
Непосредственно перед операцией (за 30 – 40 минут) внутривенно вводят антибиотики широкого спектра действия (подавляют различные виды болезнетворных бактерий). В случае необходимости также могут вводиться глюкокортикостероиды (стероидные гормоны, подавляющие воспалительную реакцию), а также препараты крови (эритроцитарная и тромбоцитарная масса).
При выявлении желчнокаменной болезни целесообразно проводить удаление не только селезенки, но также и желчного пузыря.

В норме каждая молекула гемоглобина (гемоглобин A) состоит из 2 α-цепей и 2 β-цепей. В основе серповидноклеточной анемии лежит точечная мутация, в результате которой происходит незначительное изменение полипептидной цепи (белковая молекула), входящей в состав β-цепи, что, однако непременно меняет его свойства. В итоге, измененная молекула гемоглобина (гемоглобин S) в условиях снижения концентрации кислорода начинает кристаллизоваться и, тем самым, изменяет форму эритроцита с двояковогнутого диска на серповидную (такие эритроциты также называют дрепаноцитами). Такое изменение структуры и формы эритроцитов приводит к снижению их способности транспортировать кислород. Помимо этого, данные эритроциты очень часто подвергаются гемолизу (разрушение эритроцитов) в селезенке и/или кровеносных сосудах.
Стоит отметить, что серповидноклеточная анемия наследуется аутосомно-рецессивным путем. В том случае, если ген, который кодирует видоизмененный гемоглобин S, унаследован только от одного из родителей (гомозиготная форма), то заболевание практически никак себя не проявляет. Однако в условиях сильной гипоксии у данных людей могут появиться такие признаки данного заболевания как бледность кожи (вследствие анемии), усталость, головокружение, желтуха, приступы болей различной локализации. Если же человек унаследовал дефектный ген не от одного, а от обоих родителей (гомозиготная форма), то тогда заболевание протекает особенно тяжело (возникновение частых гемолитических кризов, сепсис), так как эритроциты могут переносить лишь дефектный гемоглобин S.
Постановка диагноза серповидноклеточная анемия основывается на данных общего анализа крови, а также клинической картины заболевания. Стоит отметить, что в периферической крови даже у больных данным заболеванием не всегда удается обнаружить серповидные эритроциты. При подозрении на серповидноклеточную анемию прибегают к использованию реакции с пиросульфитом натрия (метабисульфит натрия). Благодаря данной пробе, возможно воссоздать условия гипоксии (пиросульфит натрия снижает содержание кислорода в мазке), что позволяет в дальнейшем выявить серповидные красные кровяные тельца. Если в течение первых 2 – 3 минут после постановки данной пробы в поле зрения микроскопа обнаруживают эритроциты в форме полумесяца, то тогда это говорит в пользу того, что пациент унаследовал дефектный ген от двух родителей. В том случае, когда серповидные эритроциты выявляют лишь после 3 – 5 минут от начала пробы, то это свидетельствует о том, что данный человек унаследовал ген только от одного родителя. Если в лаборатории нет в наличии пиросульфита натрия, то тогда прибегают к простому наложению жгута на основание пальца. Данный способ также приводит к локальной гипоксии тканей.
Кроме того, существует другой способ определить наличие гемоглобина S в крови. Для этого используют электрофорез. В электрическом поле происходит разделение различных фракций гемоглобина (А, А2, S, C), что приводит к образованию ряда полос на бумаге, которые могут быть в дальнейшем идентифицированы и соотнесены с реальными фракциями. Помимо этого, данный метод помогает выявить количественное содержание различных фракций гемоглобина. Так, например, у больных серповидноклеточной анемией в крови находится более 50% гемоглобина S и менее 50% гемоглобина А (в норме гемоглобин А составляет более 96% общего гемоглобина).
| Симптом | Механизм возникновения |
| Анемия (снижение уровня гемоглобина) | Замена гемоглобина А на дефектный гемоглобин S приводит к тому, что эритроциты, переносящие данный транспортный белок, изменяют свою обычную форму на серповидную. Попав в селезенку, данные измененные эритроциты быстро захватываются и подвергаются уничтожению уже на ранней стадии своего существования. Уменьшение количества эритроцитов также приводит и к снижению гемоглобина. |
| Слабость, недомогание, быстрое утомление | Вследствие того, что эритроциты любой дефектной формы (в том числе серповидной) быстро подвергаются разрушению в селезенке или внутри кровеносных сосудов, количество переносимого гемоглобина постепенно уменьшается. Так как главной функцией гемоглобина является доставка кислорода к тканям, то в дальнейшем возникает клиническая картина, характерная для кислородного голодания или гипоксии. Ткани центральной нервной системы являются крайне чувствительными к кислородному голоданию и именно поэтому при возникновении анемического (снижение гемоглобина ниже 110 грамм на 1 литр крови) или преданемического состояния возникают такие симптомы как слабость, быстрое утомление, снижение работоспособности, головокружение. |
| Гемолитические кризы (эпизоды, массивного разрушения эритроцитов внутри сосудов) | Принимая форму серпа, эритроциты становятся ломкими и не способны проходить чрез мелкие сосуды (синусы) в селезенке. В результате этого с некоторой частотой возникают эпизоды, когда в селезенке происходит массивный гемолиз (разрушение эритроцитов). |
| Увеличение селезенки (спленомегалия) | Разрушение эритроцитов внутри синусов селезенки приводит к разрастанию внутренней стенки данных сосудов. В свою очередь, это усугубляет течение гемолитических кризов, а также приводит к переполнению кровью тканей селезенки. Селезеночная конгестия (переполнение крови в органе) приводит к увеличению в размере органа. |
| Желтуха | Желтуха возникает на фоне гипербилирубинемии (повышенное содержание билирубина в крови). Дело в том, что при массивном разрушении эритроцитов в кровь высвобождается гемоглобин. В свободном состоянии гемоглобин является токсичным веществом, поэтому он подвергается трансформации в билирубин (желчный пигмент). Однако повышение билирубина в крови также оказывает на организм отрицательное влияние. Нередко субъективно это проявляется зудом кожи (билирубин раздражает нервные окончания, находящиеся в коже). Кроме того, именно несвязанный билирубин отвечает за окрашивание кожи и слизистых в желтый цвет. Стоит отметить, что для желтухи при серповидноклеточной анемии характерен специфический лимонный оттенок. |
| Закупорка мелких сосудов (капилляров) | Серповидные эритроциты легко проходят через крупные кровеносные сосуды, но попадав в очень мелкие капилляры, они не способны «складывать» и поэтому приводят к их закупорке. Стоит отметить, что эритроциты могут закупоривать капилляры практически в любом органе. Так, например, если красные кровяные тельца закупоривают артерии сетчатки глаза, то может наблюдаться потеря остроты зрения вплоть до полной слепоты (вследствие отслоения сетчатки). Если эритроциты блокируют коронарные артерии, которые питают сердечную мышцу, то тогда возникает клиника инфаркта миокарда (омертвение тканей сердечной мышцы). При закупорке поверхностных сосудов кожи конечностей нередко возникают участки, где кожа подвергается изъязвлению. При несвоевременной обработке антисептиками кожный покров инфицируется, что может привести к нагноению язв. В некоторых случаях могут возникать болевые приступы разной локализации. Связанно это с тем, что при закупорке сосудов возникает ишемия тканей (прекращение кровоснабжения), что приводит к отмиранию болевых рецепторов. |
| Изменение костной ткани | У детей на фоне серповидноклеточной анемии нередко возникают различные патологические изменения костей черепа, а также зубов. Связанно это с ранним зарастанием черепных швов, что приводит к формированию башенного черепа. Данная патология характеризуется увеличением затылочной и теменных костей с незначительным увеличением поперечных размеров черепа. Вследствие этого у детей, как правило, возникают головные боли, головокружение, а в некоторых случаях наблюдается снижение остроты зрения. Иногда может наблюдаться нарушение психики, слабоумие, эпилепсия. Также характерно изменение положения зубов. У взрослых на рентгенограммах обнаруживается расширение костномозгового слоя, а также истончение кортикального слоя, что приводит к истончению костей и возникновению остеопороза. |
Так как серповидноклеточная анемия представляет собой наследственное заболевание, то полностью излечить от данного недуга на сегодняшний день не представляется возможным. Однако при соблюдении некоторых общих рекомендаций возможно не только улучшить качество жизни людей с данным заболеванием, но и практически полностью избежать гемолиза (разрушение дефектных серповидных эритроцитов). Образ жизни имеет особенно важное значение для пациентов с серповидноклеточной анемией. Для того чтобы не провоцировать разрушение эритроцитов из-за воздействия гипоксии, человек должен избегать проживания, а также путешествий в горной местности (выше 1200 – 1500 метров над уровнем моря). Важно не подвергать организм чрезмерно высоким или низким температурам. Следует избегать любой тяжелой физической нагрузки. По возможности необходимо исключить любое воздействие на организм табачного дыма (активное или пассивное курение) и алкоголя. Стоит отметить, что данные рекомендации помогают предотвращать возникновение гемолитических кризов и поддерживать количество эритроцитов и гемоглобина на приемлемом уровне у гетерозиготных носителей заболевания (дефектный ген унаследован только от одного из родителей).
Также существуют различные терапевтически методы, которые позволяют устранить анемию и последствия гемолиза.
Предотвращение осложнений серповидноклеточной анемии основывается на следующем:
- Оксигенотерапия необходима для купирования гемолитических кризов. Под оксигенотерапией понимают вдыхание газовой смеси, с повышенной концентрацией кислорода (чаще всего от 40 до 70%). Благодаря этому создаются условия для устранения кислородного голодания. Оксигенотерапия позволяет практически полностью предупредить или остановить гемолиз эритроцитов. Необходимо заметить, что чем раньше начата оксигенотерапия при возникновении гемолитического криза, тем больше вероятность избежать таких нежелательных последствий как анемия, желтуха, боль в левом подреберье.
- Устранение анемии сводится к восполнению эритроцитов и гемоглобина. Именно устранение анемии является наиболее важным звеном в терапии больных с серповидноклеточной анемией. При возникновении гемолитических кризов, как правило, используют внутривенное введение эритроцитарной массы, которая на 70 – 75% состоит из взвеси эритроцитов (остальная часть приходится на плазму и другие форменные элементы крови). Стоит отметить, что при разрушении гемоглобина в кровь попадает большое количество железа, которое имеет токсическое действие на весь организм в целом. Кроме того, железо может накапливаться в печени, поджелудочной железе, сердечной мышце, центральной нервной системе, нарушая работу данных органов и тканей. Именно поэтому при гемолитических кризах также необходимо провести выведение избытка железа с помощью таких препаратов как дефероксамин или деферазирокс.
- Лечение и профилактика инфекционных болезней. При серповидноклеточной анемии могут наблюдаться множественные поражения различных органов и тканей вследствие тромбоза и ишемии (уменьшение кровоснабжения из-за закупорки артерии). Кроме того, разрушение эритроцитов в селезенке приводит к нарушению ее иммунной функции. Все это создает благоприятные условия для внедрения и циркуляции в организме инфекционных агентов (бактерии, вирусы, простейшие, грибы). Для лечения бактериальных инфекций чаще всего используются такие антибиотики широкого спектра действия (активны по отношению ко многим видам возбудителей) как амоксициллин, тетрациклин, эритромицин, имипенем и другие.

Выделяют следующие причины гемолиза:
- Механическое повреждение эритроцитов. К данной группе относят так называемую маршевую гемоглобинурию (появление в моче гемоглобина). Было замечено, что при очень длительной ходьбе у некоторых солдат возникала гемоглобинурия, при которой моча становилась темного цвета. Затем было установлено, что разрушение эритроцитов у данных солдат происходит на уровне капилляров (мельчайшие сосуды) стоп. Механизм возникновения маршевой гемоглобинурии до сих пор остается неизученным. Интересен тот факт, что у некоторых людей данные изменения возникают даже после непродолжительных пеших прогулок. Стоит, однако, отметить, что данный вид механической гемолитической анемии является довольно редким и, по сути, практически никогда не приводит к анемии (количество разрушенной крови не превышает 40 – 50 мл). В эту группу также входит и болезнь Мошковича (микроангиопатическая гемолитическая анемия). При данной патологии наблюдается стеноз артерий (сужение просвета) или их полное закупоривание тромбами, что также приводит к внутрисосудистому разрушению эритроцитов. Болезнь Мошковича может быть спровоцирована некоторыми хроническими заболеваниями почек (стеноз почечных артерий), артериальной гипертонией (повышение артериального давления), диссеминированным внутрисосудистым свертыванием (спонтанное образование тромбов). Кроме того, данная патология может быть врожденной. Механическое повреждение эритроцитов может возникать вследствие протезирования клапанов сердца. Чаще всего гемолиз возникает у пациентов с протезированным аортальным клапаном (примерно в 8 – 10% случаев). К гемолизу приводит прямое механическое воздействие на эритроциты створок клапана во время их смыкания, а также высокое давление на мембрану эритроцита во время проталкивания крови через узкое клапанное отверстие.
- Токсическое повреждение эритроцитов чаще всего возникает при остром отравлении некоторыми химическими веществами, в том числе солями тяжелых металлов (свинец, мышьяк, анилин, резорцин, нитраты, нитриты, хлороформ и др.), а также лекарственными препаратами (изониазид, аналог витамина К, хлорамфеникол, сульфаниламиды и др.). Для токсической гемолитической анемии характерен внутрисосудистый гемолиз (эритроциты разрушаются не в селезенке, а внутри кровеносных сосудов). Механизмы воздействия токсических веществ на красные кровяные тельца могут быть разными. Некоторые из них способны напрямую воздействовать и нарушать целостность клеточной мембраны эритроцитов, в то время как другие отрицательно воздействуют на отдельные ферментативные системы. Существуют и такие ядовитые вещества, которые запускают различные патологические иммунные механизмы, что в дальнейшем приводит к образованию аутоантител к эритроцитам (организм считает собственные эритроциты чужеродными).
- Аутоиммунные анемии возникают из-за образования антител (молекулы, специфически связывающиеся с чужеродными объектами) к собственным аутоантигенам (специфические белковые молекулы), которые расположены на эритроцитах. По сути, развитие данного вида анемии может возникнуть из-за таких аутоиммунных заболеваний как системная красная волчанка (аутоиммунное заболевание с поражением соединительной ткани), лимфома Ходжкина (злокачественная болезнь, при которой поражается лимфоидная ткань), ревматоидный артрит (поражение мелких суставов на фоне заболевания соединительной ткани), хронический лимфолейкоз (злокачественное поражение лимфатической ткани). Стоит отметить, что аутоиммунная анемия является одной из самых распространенных форм гемолитической анемии.
- Наследственные варианты гемолитической анемии. К данной группе относят различные врожденные мембранопатии, при которых характерно возникновение дефектов на уровне мембраны эритроцитов (акантоцитоз, эллиптоцитоз, пиропикноцитоз и стоматоцитоз). Наследственными бывают и различные ферментопатии (нарушение функционирование ферментных систем). Дефекты могут наблюдаться в работе ферментов, отвечающих за гликолиз (расщепление глюкозы), при использовании клеткой АТФ (АТФ является главным источником энергии в клетках) и некоторых других системах ферментов. Третья группа врожденных гемолитических анемий представлена гемоглобинопатиями, для которых характерно появление различных дефектов в структуре гемоглобина. К гемоглобинопатиям причисляют талассемию (дефект возникает на уровне одной из белковых цепей, формирующих гемоглобин), а также серповидноклеточную анемию (нарушение структуры гемоглобина с образованием серповидных эритроцитов).
Гемолиз может возникать по самым разнообразным причинам. Крайне важно не только установить сам факт внутриклеточного или внеклеточного гемолиза, но и определить вследствие чего был запущен данный патологический процесс. В некоторых случаях наблюдается незначительный гемолиз, который, как правило, не способен как-либо повлиять на общее состояние пациента. В других же случаях, чаще всего при воздействии больших доз высокотоксичных химических веществ или при передозировке некоторыми медикаментами, количество разрушенных эритроцитов может достигать высоких значений, что проявляется тяжелой анемией, желтухой, изменением цвета мочи и кала, а в некоторых случаях увеличением селезенки. Также могут возникать болевые приступы различной локализации (чаще всего в пояснице или в мелких суставах рук и ног). Из-за нарастания кислородного голодания (состояние гипоксии) ткани не способны функционировать в оптимальном режиме. Наиболее чувствительными к гипоксии являются нервные клетки головного мозга. Именно поэтому для любой гемолитической анемии характерно появление таких признаков гипоксии головного мозга как головная боль, головокружение, шум в ушах, предобморочное или обморочное состояние.
Общий анализ крови помогает обнаружить красные кровяные тельца с различной аномальной формой (стоматоциты, овалоциты, пиропикноциты, акантоциты, серповидные эритроциты), что позволяет предполагать наличие врожденной мембранопатии. При наследственных ферментопатиях в эритроцитах выявляют небольшие и круглые включения (тельца Гейнца-Эрлиха) в количестве 5 – 6 штук (в норме они встречаются намного реже). Помимо этого, при некоторых патологиях (эллиптоцитоз, аутоиммунная гемолитическая анемия) выявляют пониженную осмотическую резистентность красных кровяных телец (устойчивость к гипотоническому раствору хлорида натрия).
При повторных гемолитических кризах, когда происходит массивное разрушение красных кровяных телец, уровень гемоглобина может опускаться вплоть до 60 – 70 г/л, при норме 120 – 140 г/л у женщин и 130 – 160 г/л у мужчин.
Для того чтобы подтвердить спленомегалию (увеличение размеров селезенки), прибегают к УЗИ органов брюшной полости. Субъективно спленомегалия проявляется возникновением болей в левом подреберье. Связанно это с перерастягиванием капсулы органа, где находится большое количество болевых рецепторов.
Желтушность кожных покровов и слизистых, возникает из-за разрушения гемоглобина, который в дальнейшем превращается в билирубин (желчный пигмент). При гемолитических анемиях в крови обнаруживается высокая концентрация билирубина (гипербилирубинемия). Как правило, билирубин поднимается до значений 1,8 – 2,0 мг% (норма 0,2 – 0,6 мг%). Билирубин выделяется из организма через мочевыделительную систему и желудочно-кишечный тракт, что приводит к окрашиванию кала и мочи в темный цвет.
Стоит отметить, что при любой форме гемолитической анемии характерно усиление эритропоэза (процесс образования эритроцитов). Данный механизм запускается на уровне костного мозга и способствует более быстрому устранению анемического состояния. Именно поэтому в клиническом анализе крови обнаруживают как снижение количества эритроцитов и гемоглобина вследствие гемолиза, так и увеличение числа ретикулоцитов, которые являются молодыми формами красных кровяных телец.
| Формы гемолитической анемии | Диагностические признаки анемии |
| Токсическая гемолитическая анемия | Воздействие гемолитических ядов на организм может быть острым или хроническим. Для острой токсической гемолитической анемии характерен внутрисосудистый гемолиз, который приводит к разрушению эритроцитов и выходу гемоглобина в кровяное русло (гемоглобинемия). К тому же гемоглобин в больших количествах также обнаруживается и в моче (гемоглобинурия). В некоторых случаях гемолиз может быть столь массивным, что это приводит к нарастанию гипоксии (кислородное голодание) и нарушению работы центральной нервной системы (головная боль, головокружение, сильная слабость, недомогание, потеря сознания, тошнота, рвота), сердечно-сосудистой системы (появление патологических сердечных шумов, значительное снижение артериального давления), печени и других органов. Помимо этого, токсические вещества могут дополнительно воздействовать на различные органы-мишени. Так, например, свинец дополнительно поражает все отделы головного мозга (при остром отравлении), вызывая разрушение миелина нейронов (специальная оболочка, которая обхватывает некоторые нервные отростки), что ведет к потере памяти (амнезия) и нарушению координации движений (атаксия). При отравлении лекарственными средствами может возникать не только гемолиз эритроцитов, но также и токсическое угнетение активности костного мозга. Это приводит к уменьшению количества всех форменных элементов крови (эритроциты, тромбоциты, лейкоциты). |
| Аутоиммунная гемолитическая анемия | В некоторых случаях аутоиммунная гемолитическая анемия возникает под влиянием низких температур (холодовая агглютининовая болезнь). Для данной патологии характерно появление недомогания, раздражительности, слабости, головных болей, головокружения. Кожа и слизистые приобретают желтый оттенок. Довольно часто наблюдается увеличение селезенки. При аутоиммунных гемолитических анемиях также может возникать острая почечная недостаточность, которая приводит к практически полной остановке выделения мочи (анурия), повышению артериального давления (гипертония), появления эритроцитов в моче (гематурия). Также возникают почечные отеки. Для определения аутоиммунной природы гемолитической анемии используют пробу Кумбса (определение неполных антител к эритроцитам). |
| Механическая гемолитическая анемия | Выраженность симптомов механической гемолитической анемии может сильно варьироваться. В некоторых случаях единственным признаком, подтверждающим наличие данной патологии, является выявления в крови мелких фрагментов эритроцитов (шизоциты), которые подверглись гемолизу в синусах селезенки. При массивном гемолизе может наблюдаться тромбоз мелких сосудов. Это, в свою очередь, приводит к ишемии тканей (уменьшение или прекращение артериального кровоснабжения) и может вызывать сильнейшие боли из-за отмирания нервных окончаний. |
| Врожденная гемолитическая анемия | Данная патология может проявляться по-разному (в зависимости от формы). Так, например, серповидноклеточная анемия, унаследованная от одного из родителей, практически никак не проявляется. В свою очередь, если дефектный ген наследуется от обоих родителей, то тогда данное наследственное заболевание проявляется крайне тяжело уже в детском возрасте (гемолитические кризы, частые инфекционные заболевания, патологическое изменение костной ткани). При мембранопатиях и ферментопатиях также могут возникать гемолитические кризы (массивный гемолиз), а также желтуха, желчнокаменная болезнь, увеличение селезенки. |
Лечение должно начинаться с определения причины гемолитической анемии. Также важно определить насколько массивным оказался гемолиз, для того чтобы в дальнейшем оказать адекватную и своевременную медицинскую помощь.
Основные принципы лечения и профилактики гемолитической анемии следующие:
- Избегание воздействия гемолитических ядов на организм. Важным условием профилактики гемолитической анемии является соблюдение всех правил техники безопасности на производствах, где используются различные соли тяжелых металлов или химические вещества, способные вызывать гемолиз. Крайне важно пользоваться всеми предусмотренными мерами безопасности, включая индивидуальные меры защиты (специальные респираторы, комбинезоны, перчатки, ботинки). При остром отравлении необходимо как можно быстрее прервать контакт с токсическим веществом. В случае если это жидкость, то следует обильно промыть в проточной воде глаза или кожу, которые непосредственно контактировали с токсическим веществом. Наиболее опасным считается отравление токсичными газами. Дело в том, что легкие имеют большую площадь поверхности и именно поэтому ингаляционный путь (вдыхание газов) чаще всего приводит к острым отравлениям. При отравлении токсичными газами пострадавшего следует транспортировать в хорошо проветриваемое помещение или на свежий воздух, а также при необходимости обеспечить адекватный приток кислорода (расстегнуть верхние пуговицы рубашки, ослабить ремень). Важно как можно раньше доставить пострадавшего в больницу для оказания адекватной дезинтоксикационной терапии (выведение токсина из организма или его обезвреживание).
- Избегание длительного нахождения в условиях гипоксии (кислородного голодания). Иногда некоторые виды гемолитических анемий (мембранопатии) проявляются лишь в том случае, когда организм человека не получает с воздухом достаточное количество кислорода. Данная ситуация может возникать из-за нахождения человека на большой высоте (пониженное парциальное давление кислорода в воздухе), при интенсивной физической работе (несоответствие между поступающим воздухом и воздухом, необходимым для обменных процессов) или сильном стрессе.
- Удаление селезенки (спленэктомия) в некоторых случаях является единственным способом уменьшения выраженности гемолитической анемии. Дело в том, что проходя по узким сосудам селезенки (синусы), красные кровяные тельца, которые имеют поврежденную или дефектную структуру, активно захватываются макрофагами (клетки, способные захватывать чужеродные объекты) и разрушаются. Удаление селезенки способствует удлинению жизненного цикла эритроцитов. Как правило, данный способ лечения применяется при наследственных мембранопатиях (эллиптоцитоз, акантоцитоз, пиропикноцитоз, стоматоцитоз). Также удаление селезенки необходимо в том случае, когда у пациента уже имеется спленомегалия (увеличение селезенки в размере).
- Переливание эритроцитарной массы необходимо при повторных (рецидивирующих) гемолитических кризах. Частое разрушение большого количества эритроцитов и гемоглобина, которое возникает вследствие гемолитических кризов, может приводить к снижению гемоглобина ниже 70 г/л (выраженная степень анемии). Это, в свою очередь, приводит к тому, что все ткани организма не получают кислород в необходимом количестве. Для того чтобы избежать нарушения функционирования центральной нервной системы, сердечно-сосудистой системы, а также печени и почек (органы наиболее чувствительные к кислородному голоданию) прибегают к внутривенному введению эритроцитарной массы.
- Применение глюкокортикоидов является основным звеном в лечении аутоиммунной гемолитической анемии. Глюкокортикоиды, по сути, представляют собой гормоны надпочечников синтетического происхождения, которые способны подавлять иммунный ответ, в том числе и патологические иммунные реакции. К тому же, данные стероидные гормоны усиливают эритропоэз (образование эритроцитов) на уровне костного мозга, что позволяет в более быстрые сроки восстановить нормальное количество красных кровяных клеток.
- Применение препаратов, связывающих железо. Во время гемолитических кризов происходит усиленное разрушение гемоглобина, в результате чего в кровь высвобождается большое количество железа. Из кровяного русла железо может попадать, накапливаться и токсически воздействовать на клетки поджелудочной железы, миокарда (сердечная мышца), центральной нервной системы. Для того что связать и вывести из организма избыток железа прибегают к использованию таких медикаментов как деферазирокс или дефероксамин.
В некоторых случаях понижение красных кровяных телец возникает уже в первые часы после рождения (или даже на стадии формирования плода). Данная патологическая ситуация носит название гемолитическая болезнь новорожденных и возникает в том случае, когда имеется несоответствие крови плода и матери по резус-фактору или по группе крови.
Данные конфликты между системой мать-плод появляются из-за сенсибилизации организма матери. Если у плода имеются на поверхности эритроцитов белковые молекулы (антигены), которых нет на эритроцитах матери, то тогда, проникнув в кровоток, данные антигены вызывают образование антител (первичный иммунный ответ). Главной функцией антител является специфическое связывание с антигеном, что приводит к запуску поглощения данного комплекса специальными клетками (макрофаги). При повторном попадании (например, при повторной беременности) в организм матери данные антигены быстро распознаются, что приводит к синтезу большого количества антител и массивному разрушению эритроцитов (гемолиз). По сути, эритроцитарные антигены плода организмом матери воспринимаются как чужеродные.
Выделяют следующие причины гемолитической болезни новорожденных:
- Конфликт между резус-отрицательной матерью и резус-положительным плодом. Данный конфликт, как правило, возникает после первой беременности, когда антигены от первого плода (резус-положительного) попали через плаценту в кровь матери и привели к образованию антител (сенсибилизация). При последующих беременностях организм матери способен вырабатывать большое количество антител, связывающихся с антигенами на эритроцитах и запускающих гемолиз (разрушение красных кровяных телец). Разрушенные эритроциты не способны удерживать на своей поверхности гемоглобин и, в конечном счете, теряют его. Гемоглобин, в свою очередь, подвергается трансформации в билирубин (представляет собой желчный пигмент). Данный пигмент в больших концентрациях является довольно токсичным веществом, которое может накапливаться в различных тканях и вызывать нарушение функций клеток, вплоть до их разрушения. Также на ткани влияет нарастающая гипоксия (кислородное голодание). Без необходимого количества кислорода органы не способны развиваться и функционировать в нормальном режиме. Именно поэтому дети при гемолитической болезни новорожденных рождаются с различными пороками развития. В особенности страдает головной мозг, так как именно ткани мозга наиболее чувствительны к воздействию билирубина и гипоксии.
- Конфликт между матерью с первой группой крови и плодом второй или третьей группы крови. В отличие от резус-конфликта, в данном случае сенсибилизация организма матери может быть и не связанна с предыдущими родами. Иногда сенсибилизация возникает на фоне частых иммунизаций (вакцинация) или после некоторых перенесенных инфекционных заболеваний.
Другой причиной гемолитической болезни новорожденных может стать инфекция. Некоторые вирусные (краснуха, цитомегалия), бактериальные (врожденный сифилис) и паразитарные заболевания (токсоплазмоз, малярия) способны приводить к гемолизу и в определенной степени снижать уровень эритроцитов в крови.
Кроме того, понижение эритроцитов может также наблюдаться при различных наследственных мембранопатиях или ферментопатиях. Наследственные мембранопатии проявляются дефектом мембраны эритроцитов. В свою очередь, при ферментопатиях наблюдается нарушение функционирования одного из ферментов, участвующего в энергетических процессах. В результате тех или иных дефектов, длительность жизни красных кровяных телец значительно сокращается.
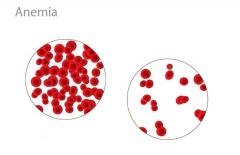
Так, например, белок гемопексин связывает ту часть гемоглобина, в которой содержится железо (гем). Также гемопексин способен специфически связываться со свободным гемом. Данный комплекс затем с кровью попадает в печень, где гем в дальнейшем идет либо на синтез различных желчных пигментов (в том числе билирубина), либо же связывается с трансферрином (белок переносчик молекул, содержащих железо) и переносится в костный мозг для последующего участия в процессе создания эритроцитов. В свою очередь, белок гаптоглобин связывает свободный глобин или глобин, входящий в состав гемоглобина. Затем полученный комплекс попадает в селезенку и дальше дезинтегрируется на нетоксичные молекулы.
Выделяют следующие причины снижения эритроцитов и лейкоцитов:
- Дефицит витаминов группы В может приводить к нарушению функции кроветворения, в результате чего, костный мозг не способен синтезировать достаточное количество клеток-предшественников форменных элементов крови. Витамины В1, В9 и В12 крайне необходимы для нормального функционирования костного мозга. Витамин В1 в больших количествах содержится в орехах, крупах (гречневая, овсяная, ячменная), мясе, яйцах. Витамин В9, в свою очередь, содержится в печени, мясе, различных овощах (салат, капуста, петрушка, морковь, огурцы и т. д.). Цианокобаламин (витамин В12) находится в больших количествах в рыбе, печени, молочной продукции, яйцах, сое.
- Апластическая анемия представляет собой патологию кроветворной системы, при которой функция костного мозга по кроветворению резко угнетается. Чаще всего апластическая анемия возникает на фоне острого отравления мышьяком, солями тяжелых металлов или бензолом. Одной из причин возникновения данного вида анемии является воздействие ионизирующего облучения на организм. Передозировка некоторыми лекарственными препаратами (цитостатики, хлорамфеникол, аминазин) может также приводить к апластической анемии. Для данной патологии характерно снижение количества всех форменных элементов крови (лейкоциты, эритроциты и тромбоциты).
- Лейкоз – злокачественное заболевание системы кроветворения. В некоторых случаях опухоль может замещать клетки-предшественники сразу нескольких ростков кроветворения. В конечном счете, нормальная ткань костного мозга замещается на опухолевые клетки, которые не способны выполнять специфической функции. Это ведет к угнетению образованию эритроцитов, лейкоцитов, а также тромбоцитов (в зависимости от типа лейкоза).
В свою очередь, при анемии объем жидкой части крови остается неизмененным. Для анемии чаще всего характерно снижение как эритроцитов, так и гемоглобина (белок, который переносит кислород к тканям). Наиболее частой причиной анемии во время беременности является дефицит железа. Дело в том, что железо в больших количествах расходуется на образование плаценты, а также на нужды плода. В свою очередь, потребность в железе в полтора раза превышает скорость, с которой этот микроэлемент может всасываться в тонком кишечнике. Железодефицитная анемия во время беременности может привести к преждевременным родам, а также повышает риск послеродовой инфекции. Кроме того, ткани плода не получают кислород в необходимом количестве, что может приводить к задержке роста и развития плода (в особенности страдает головной мозг).
Другой частой причиной анемии во время беременности является дефицит витамина В12 (цианокобаламин). При уменьшении поступления данного витамина с пищей наблюдается нарушение процесса кроветворения, что приводит к пернициозной анемии (В12-дефицитная анемия). Помимо этого, для пернициозной анемии характерно поражение центральной и периферической нервной системы.
источник







