Дефицит железа является наиболее частой причиной анемии и, как правило, обусловлен кровопотерей. Железодефицитная анемия обычно имеет неспецифическую симптоматику.
Эритроциты имеют тенденцию к микроцитозу и гипохромии, запасы железа снижены, что отражается в низких цифрах сывороточного ферритина и железа с высокими показателями сывороточного трансферрина. При установлении железодефицитной анемии предполагается наличие кровопотери. Лечение направлено на восстановление запасов железа и лечение кровопотери.
Железо в организме распределяется в активный метаболизм и пул хранения. Общие запасы железа в организме составляют около 3,5 г у здоровых мужчин и 2,5 г у женщин; различия связаны с размером тела, более низкими уровнями андрогенов и недостаточным запасом железа у женщин, обусловленным потерей железа с менструациями и беременностью. Распределяется железо в организме людей следующим образом: гемоглобин — 2100 мг, миоглобин — 200 мг, тканевые (гемовые и негемовые) ферменты — 150 мг, транспортная система железа — 3 мг. Запасы железы в виде ферритина находятся в клетках и плазме (700 мг) и в клетках в виде гемосидерина (300 мг).
Абсорбция железа происходит в двенадцатиперстной кишке и верхних отделах тощей кишки. Абсорбция железа определяется типом молекулы железа и компонентами проглатываемой пищи. Абсорбция железа происходит наилучшим образом, когда пища содержит железо в виде гема (мясо). Негемовое железо должно уменьшить статус железа и освободиться от пищевых компонентов с помощью желудочного секрета. Абсорбцию негемового железа снижают другие компоненты пищи (например, танины чая, отруби) и некоторые антибиотики (например, тетрациклин). Аскорбиновая кислота является единственным компонентом обычной пищи, повышающим абсорбцию негемового железа.
Средний пищевой рацион содержит 6 мг элементарного железа на 1 ккал пищи, что обеспечивает адекватный гомеостаз по железу. Из 15 мг железа, потребляемого с пищей, у взрослых абсорбируется только 1 мг, что приблизительно соответствует ежедневной потери железа с десквамацией клеток кожи и кишечника. При дефиците железа абсорбция повышается, и, хотя точные механизмы регуляции неизвестны, абсорбция повышается до 6 мг в день до тех пор, пока не произойдет восстановление его запасов. У детей потребности в железе больше, чем у взрослых, и абсорбция выше, чтобы компенсировать эту потребность.
Железо из клеток слизистой оболочки кишечника переносится к трансферрину, железотранспортному протеину, синтезируемому печенью. Трансферрин может транспортировать железо из клеток (кишечника, макрофагов) на специфические рецепторы эритробластов, клеток плаценты и печеночных клеток. Для синтеза гема трансферрин переносит железо к митохондриям эритробластов, которые включают железо в состав протопорфирина, в результате чего последний превращается в гем. Трансферрин (период его полужизни в плазме крови составляет 8 дней) затем высвобождается для реутилизации. Синтез трансферрина повышается при дефиците железа, но снижается при всех типах хронических заболеваний.
Железо, не используемое для эритропоэза, переносится трансферрином в пул хранения, который представлен двумя формами. Наиболее важным является ферритин (гетерогенная группа протеинов, окружающая ядро железа), которая является растворимой и активной фракцией, локализуемой в печени (в гепатоцитах), костном мозге, селезенке (в макрофагах), эритроцитах и плазме. Железо, хранимое в ферритине, готово к использованию для нужд организма. Концентрация сывороточного ферритина соотносится с его запасом (1 нг/мл = 8 мгжелеза в пуле хранения). Вторым пулом хранения железа в организме является гемосидерин, который относительно нерастворим, и его запасы сосредоточены главным образом в печени (в купферовских клетках) и костном мозге (в макрофагах).
Вследствие ограниченности абсорбции железа организм сохраняет и реутилизирует его. Трансферрин связывает и реутилизирует доступное железо из старых эритроцитов, подвергающихся фагоцитозу мононуклеарами. Этот механизм обеспечивает около 97 % дневной потребности в железе (примерно 25 мг железа). С возрастом пул железа в организме имеет тенденцию к росту вследствие того, что элиминация его замедляется.

источник
Анемия (в просторечии называют малокровием) – патологическое состояние, о котором мы говорим, когда происходит уменьшение количества эритроцитов (красных кровяных телец), уровня гемоглобина, отвечающего за транспорт кислорода в крови и показателя, называемого гематокритом (отношение объема эритроцитов в крови к общему объему).
Болезнь диагностируют, если эти показатели падают более чем на 2 стандартных отклонения от нормального значения.
Существуют различные классификации анемии. Одна из них основывается на степени тяжести заболевания:
- Легкая анемия – уровень гемоглобина составляет от 10 до 12 г/дл;
- Средняя анемия – уровень гемоглобина составляет от 8 до 9,9 г/дл;
- Тяжелая анемия – уровень гемоглобина составляет от 6,5 до 7,9 г/дл;
- Анемия с риском для жизни – уровень гемоглобина ниже 6,5 г/дл.
Другим элементом, по которому классифицируют виды анемии – ее причины. Принимая во внимание факторы, вызывающие заболевания выделяет следующие типы анемии:
Как следует из названия, этот вид анемии является последствием острой или хронической потери крови. Острая потеря крови происходит чаще всего в результате посттравматического кровоизлияния или массивного кровотечение желудочно-кишечного тракта или половых путей.
Предполагается, что потеря примерно 20% объема циркулирующей крови может вызвать симптомы анемии. Хроническая потеря крови, как правило, связана с заболеваниями желудочно-кишечного тракта.
Анемия из-за дефицита железа является следствием слишком малого содержания железа в организме. Основные причины дефицита железа в организме человека – это его потеря вместе с кровью. Поэтому, чаще всего, анемия из-за дефицита железа имеет место у женщин, у которых железо теряется вместе с менструальной кровью, особенно при слишком частом или обильном кровотечении.
В некоторых случаях можно наблюдать увеличение спроса на железо – это период полового созревания, в период беременности и кормления грудью, а также у преждевременно родившихся детей и новорожденных некормленых молоком матери.
Причиной дефицита железа, а также может быть плохое всасывание этого элемента в желудочно-кишечном тракте. Особенно это касается пациентов после удаления желудка или участка кишечника, людей, страдающих хроническими воспалительными заболеваниями кишечника (болезнь Крона).
Многие хронические заболевания также могут привести к возникновению анемии. Это связано с процессом воспалений и нарушениями производства факторов, определяющих правильную функцию костного мозга.
Поэтому особо часто к анемии приходят при таких заболеваниях, как: рак, аутоиммунные заболевания (ревматоидный артрит, красная волчанка), хронические бактериальные воспаления, грибковые или вирусные инфекции, а также заболеваний почек, желудочно-кишечного тракта и т.д.
Название мегалобластная анемия связано с увеличением красных клеток. В первую очередь, из-за дефицита витамина B12 и фолиевой кислоты. Витамин В12 необходим для нормального синтеза ДНК.
Следовательно, его недостаток приводит к нарушению этого процесса, что быстро отражается на быстроделящихся клетках и приводит к их неправильному росту и уменьшению количества.
Фолиевая кислота, как и витамин В12, участвует в процессах синтеза ДНК и также ее недостаток приводит к нарушению деления – эритроциты получаются неестественно большими.
Причины анемии, вызванной дефицитом витамина В12:
- неправильная диета, бедная витамином В12;
- алкоголизм;
- заболевания, связанные с недостаточностью или нарушением функции фактора Касла (фактор производится клетками желудка), который отвечает за усвоение кобаламина или витамина В12;
- нарушение всасывания комплекса цианкобаламинам.
Причины анемии с дефицитом фолиевой кислоты:
- синдром нарушения всасывания;
- нехватка в рационе питания;
- хронический алкоголизм;
- период повышенного спроса, – беременность, кормление грудью, онкологические заболевания;
- прием некоторых лекарственных препаратов (например, метотрексат), противоэпилептических препаратов (например, фенитоин) и противотуберкулезных лекарственных препаратов.
Гемолитическая анемия – это очень сложная группа заболеваний, характеризующаяся неправильным, преждевременным распадом эритроцитов.
Гемолиз, то есть процесс разложения могут происходить внутри сосудов и вне сосудов (селезенка, печень). Этот тип анемии может давать симптомы в виде желтухи, потому что при чрезмерно активном разрушении красных кровяных клеток выделяется значительное количество гемоглобина, который после цикла биохимических изменений в печени, будет преобразована в билирубин, которая, при высоком уровне, придает коже и глазам характерный желтый оттенок.
Гемолитическая анемия делится на:
- врожденную, вызванную дефектом устройства кровяных клеток, например, врожденный эритроцитоз (кровяные клетки имеют не правильную клеточную мембрану), талассемия, серповидно-клеточная анемия;
- приобретенная, при которой нормальные красные кровяные тельца разрушаются под действием иммунной системы или токсинов (например, тяжелые металлы), лекарств (серосодержащие, производные платины), «механические повреждения», например, искусственный затвор сердца или инфекции (малярия, токсоплазмоз, лейшманиоз).
Апластическая анемия – это заболевание, которое включает в себя расстройства функции костного мозга и уменьшение количества элементов крови (в данном случае не только эритроцитов).
Апластическая анемия может коснуться человека в любом возрасте, у некоторых она врожденная, у других – приобретенная. Анемия иногда появляется внезапно или развивается постепенно, в течение длительного времени, даже в течение нескольких месяцев. Апластическая анемия может иметь тяжелую форму и привести к смерти.
Причины возникновения этой тяжелой болезни не до конца известны, но есть основательные подозрения, что большое значение имеют следующие факторы:
- лучевая терапия и химиотерапия – в списке их побочных эффектов значится апластическая анемия;
- контакт с инсектицидами и гербицидами;
- аутоиммунные расстройства;
- условия труда;
- вирусные инфекции;
- прием некоторых лекарственных препаратов, например, некоторых антибиотиков и средств от ревматоидного артрита;
- гемолитическая анемия;
- заболевания соединительной ткани;
- ночная гемоглобинурия.
Кроме дефицита железа и потери крови можно указать и другие причины анемии:
- недостаток витамина В12. Этот тип анемии появляется при нарушении всасывания витамина В12 из желудочно-кишечного тракта. Это может быть результатом плохого питания, вегетарианства или алкоголизма;
- трещины красных кровяных телец, вызванные атакой антител;
- инфицирование нематодой;
- заболевания костного мозга (лейкемия, множественная миелома) – костный мозг не вырабатывает достаточного количества красных кровяных клеток, что является причиной анемии;
- некоторые лекарства;
- вирус ВИЧ и СПИД .
Клинические проявления зависят, в первую очередь, от типа анемии.
Явная железодефицитная анемия в мазке периферической крови
Однако существуют некоторые общие черты, такие как:
- бледность кожи и конъюнктивы глаз;
- одышка после нагрузки;
- апатия;
- сонливость;
- скотома;
- шум в ушах;
- проблемы с памятью и концентрацией;
- поверхностное дыхание;
- обмороки;
- депрессия;
- повышенная температуру тела;
- ощущение холода;
- болезненные симптомы в области сердца.
В случае постгеморрагической анемии симптомы зависят от количества потерянной крови. Если происходит быстрая потеря крови (острое кровотечение), в объеме от 1,5 до 2 литров, это может привести к снижению температуры тела, холодному поту, беспокойству, расстройства мочеиспускания и развитию так называемого гиповолемического шока – падает артериальное давление, что приводит к нарушению сознания, и даже потере сознания. Если потеря крови хроническая, то чаще всего мы наблюдаем признаки железодефицитной анемии.
Анемия из-за дефицита железа связано с появлением общих симптомов анемии, а также других специфических, в виде: расстройства аппетита, выпячивание и сглаживания поверхности языка, болезненные трещины в углах рта (так называемый заеды), сухая и слишком бледная кожа, хрупкие ногти. Характерным симптомом может быть чрезмерное выпадение волос.
Хроническая анемия сопровождается, как правило, расстройствами, связанными с основным заболеванием. Как правило, анемия проявляется только через несколько месяцев после появления первых симптомов хронического заболевания.
Симптомы мегалобластной анемии зависят от типа дефицита. При дефиците витамина B12, могут появляться расстройства со стороны нервной системы, такие как: расстройства личности, а также парестезия (покалывание) рук и ног, ощущение прохождения тока через позвоночник при наклоне головы вперед, онемения рук и ног.
В случае тяжелой анемии могут появиться: расстройства чувствительности, нарушения походки (нарушение равновесия), нарушения мочеиспускания и ослабление зрения. Другие симптомы – потеря вкусовых ощущений, жжение языка, потеря массы тела, а также симптомы со стороны желудочно-кишечного тракта, тошнота, рвота или диарея.
Дефицит фолиевой кислоты не вызывает расстройств со стороны нервной системы, но характерным симптомом может быть окраска кожи. Дефицит фолиевой кислоты особенно опасен во время беременности, так как это может привести к врожденным дефектам у детей.
Гемолитическая анемия может быть связана с появлением желтухи и увеличением печени и селезенки.
Апластическая анемия может вызывать симптомы, связанные с поражением костного мозга и, следовательно, не только производства красных кровяных телец, а также тромбоцитов и лейкоцитов в крови. Как правило, появляется одышка и слабость.
Нарушение производства крови приводит к увеличенной склонности к кровоподтекам и – в более серьезных случаях – спонтанным кровотечениям различных органов и систем.
Одним из параметров диагностики анемии является гемоглобин (Hb). Это белок, встречающийся в эритроцитах, отвечает за «прием» кислорода в легких и транспортировку его в клетки тела, а затем прием углекислого газа и доставку его в легкие.
Допустимые значения при лабораторном исследовании довольно широкие, но колеблются в пределах: у женщины 12-16 г/дл у мужчин 14-18 г/дл, а также у новорожденных 14,5-19,5 г/дл. Следующим параметром является гематокрит. Это отношение объема элементов крови (в основном красных кровяных клеток (эритроцитов)) к объема цельной крови.
Hct принимает следующие значения:
- для женщин 35-47%;
- для мужчин 42-52%;
- а для новорожденных 44-80% (в первые дни жизни).
В результатах исследований, мы также принимается во внимание количество эритроцитов:
- для женщин 4,2-5,4 млн/мм 3 ;
- для мужчин 4,7-6,2 млн/мм 3 ;
- а для новорожденных 6,5-7,5 млн/мм 3 .
Когда значение этих показателей снижены, можно говорить об анемии.
Основой диагноза анемии ставится на исследовании морфологии периферической крови, при котором наблюдается снижение количества эритроцитов, гемоглобина и гематокрита.
Важным параметром, который может указывать на анемию – объем эритроцитов (MCV), которая должна составлять (в зависимости от нормы лаборатории) от 80 до 92 fl. Если он ниже нормы, анемия называется микроцитарная, если находится в норме – нормоцитарная, а если выше нормы – макроцитарная.
В случае постгеморрагической анемии, имеющей место в чрезвычайных ситуациях, MCV в норме. В случае хронической постгеморрагической анемии наблюдаются симптомы дефицита железа.
Анемия из-за дефицита железа связано со снижением MCV (микроцитарная анемия). Количество тромбоцитов в крови может быть правильным или уменьшенным.
Дополнительным исследованием, подтверждающим анемию из-за дефицита железа является, конечно, исследование уровня железа в крови. Происходит также снижение концентрации ферритина в крови и повышения TIBC. В диагностике причин дефицита железа важна консультация у гинеколога (женщины) и диагностика желудочно-кишечного тракта.
При анемии хронических заболеваний, MCV, как правило, в норме. Кроме того, можно наблюдать рост параметров воспаления. Поэтому требуются другие исследования, позволяющие распознать основную болезнь.
Анемия из-за дефицита витамина В12 диагностируется на основании увеличения объема эритроцитов (MCV), а также исследования уровня витамина В12 в крови. В диагностике значение имеет оценка состояния желудочно-кишечного тракта, как основной причины нарушения всасывания этого витамина. В случае анемии с дефицитом фолиевой кислоты, MCV также увеличивается.
Для диагностики апластической анемии врачи обычно рекомендуют биопсию костного мозга. Подозрение на апластическую анемию возникает также на основе определенных изменений в крови, кроме недостатка гемоглобина, происходит снижения уровня лейкоцитов (лейкопения) и тромбоцитов в крови.
В случае гемолитической анемия, MCV, как правило, находится в пределах нормы, но иногда может быть увеличен. В мазке крови можно наблюдать неправильные эритроциты. Эритроциты живут 100-120 дней. Во время своей жизни, проходят 250 км пути, постоянно перемещаются, доставляют клеткам кислород и принимают от них углекислый газ.
Иногда, однако, путешествие этих клеток заканчивается преждевременно и длится около 50 дней. Тогда говорят о преждевременном распаде эритроцитов в их гемолизе, а болезнь называется гемолитической анемией. К такому положению вещей может привести гиперспленический синдром, то есть повышенная активность селезенки.
Селезенка несет ответственность за разрушение старых эритроцитов. В случае гиперспленического синдрома селезенка «утилизирует» также и молодые клетки. Широко известной причиной гемолитической анемии является малярия, а также другие инфекции, например, токсоплазмоз, цитомегаловирус. Разрушение клеток может произойти также после переливания крови. В данном случае причиной гемолиза это несоответствие в системе антигеннов крови.
Для лечения анемии следует, конечно, учитывать ее причину. Острая постгеморрагическая анемия проявляется у взрослых после потери примерно 20% от общего объема крови. Лечение заключается, прежде всего, в задержке и остановке кровотечения, переливании концентрата эритроцитов, а также введения кровезаменительных препаратов и инфузионных растворов.
В случае анемии с дефицитом железа лечение заключается в восполнении его уровня в организме. Перед началом лечения следует определить причину потери железа. В случае тяжелой анемии применяется, как правило, железо в виде инъекций, при мягких формах, можно назначать лечение в виде пищевых добавок.
Конечно, необходимо также обогащение диеты продуктами, содержащими большое количество железа, такими как: красное мясо, овощи, продукты из цельного зерна, бобовые и чернослив, инжир.
В случае анемии с дефицитом витамина В12 необходимо подача его извне в виде инъекций (в препаратах для приема внутрь он плохо всасывается), которые во многих случаях применяются в соответствующей схеме до конца жизни. Чтобы избежать дефицита витамина В12, следует позаботиться о том, чтобы в вашем рационе были продукты животного происхождения.
Фолиевую кислоту, в отличие от железа и витамина В12 можно применять внутрь. Анемия, вызванную дефицитом фолиевой кислоты, можно предотвратить путем обогащения диеты большим количеством овощей и фруктов. Женщины, которые беременны должны помнить о ежедневном приеме препарата, содержащего кислоту.
К основным методам лечения апластической анемии относятся: пересадка костного мозга и лечение иммуносупрессантами (в случае, когда апластическая анемия появилась на фоне аутоиммунных расстройств). Кроме того, лечение включает в себя симптоматические меры, то есть переливание тромбоцитов и концентрата эритроцитов.
Больным, также назначаются антибиотики и противогрибковые препараты. С учетом нарушений иммунитета у лиц с апластической анемией рекомендуется избегать пребывания в местах больших скоплений людей, где можно легко заразиться инфекцией, а также соблюдение особой личной гигиены (мытье рук).
Лечение гемолитической анемии и состоит, если это, конечно, возможно, в лечении основной болезни, вызывающей это заболевание крови. В случае анемии на фоне аутоиммунных расстройств применяются глюкокортикоиды и иммуносупрессивные препараты.
Если есть подозрения, что причиной заболевания являются различные препараты, то, если это только возможно, необходимо приостановить их прием. Бывает, однако, что единственным выходом являются периодические переливания концентратов красных кровяных телец.
Прогноз зависит от причины анемии. Раннее выявление и быстрое развертывание программы лечения постгемморагической анемии связано с хорошим прогнозом.
В случае анемии с дефицитом железа, фолиевой кислоты или витамина В12, необходимо дополнение и изменение диеты, а также объяснение причин потери этих важных компонентов. Более плохой прогноз касается других видов анемии, при которых не всегда удается получить исцеление.
Анемия или малокровие – это опасное заболевание. Если вы подозреваете, что имеете анемию, обратитесь к врачу, чтобы начать лечение как можно скорее. Отсутствие лечения анемии может привести к истощению организма и многим осложнениям.
Для профилактики анемии особое значение имеет правильное питание, а также быстрая диагностика возможных проблем с желудочно-кишечным трактом или родовыми путями у женщин. Важно, чтобы каждый, по крайней мере, один раз в год, проходил исследование мазка крови.
источник

Железодефицитная анемия является самой распространенной патологией системы крови и самой часто встречаемой анемией. По данным ВОЗ (всемирной организации здравоохранения), более 2 миллиардов людей на планете имеют дефицит железа в организме. Несколько чаще данным недугом страдают женщины, что связано с беременностью, кормлением грудью, а также периодической кровопотерей во время менструаций.
Интересные факты
- Первое задокументированное упоминание о железодефицитной анемии датируется 1554 годом. В те времена данным недугом страдали преимущественно девушки 14 – 17 лет, в связи с чем заболевание называлось «de morbo virgineo», что в переводе означает «болезнь девственниц».
- Первые попытки лечения заболевания препаратами железа были предприняты в 1700 году.
- Латентный (скрытый) дефицит железа может отмечаться у детей в период интенсивного роста.
- Потребность в железе у беременной женщины в два раза больше, чем у двух здоровых взрослых мужчин.
- За время беременности и родов женщина теряет более 1 грамма железа. При обычном питании данные потери восстановятся лишь через 3 – 4 года.
Размер зрелого эритроцита колеблется в пределах от 7,5 до 8,3 микрометров (мкм). Он имеет форму двояковогнутого диска, которая поддерживается благодаря наличию в клеточной мембране эритроцита особого структурного белка – спектрина. Такая форма обеспечивает максимально эффективный процесс газообмена в организме, а наличие спектрина позволяет эритроцитам видоизменяться при прохождении через мельчайшие кровеносные сосуды (капилляры) и после этого восстанавливать свою первоначальную форму.
Более 95% внутриклеточного пространства эритроцита заполнено гемоглобином – веществом, состоящим из белка глобина и небелкового компонента – гема. Молекула гемоглобина состоит из четырех глобиновых цепей, в центре каждой из которых находится гем. Каждый эритроцит содержит более 300 миллионов молекул гемоглобина.
За транспортировку кислорода в организме отвечает небелковая часть гемоглобина, а именно атом железа, входящего в состав гема. Обогащение крови кислородом (оксигенация) происходит в легочных капиллярах, при прохождении через которые каждый атом железа присоединяет к себе 4 молекулы кислорода (формируется оксигемоглобин). Оксигенированная кровь разносится по артериям ко всем тканям организма, где происходит переход кислорода к клеткам органов. Взамен из клеток выделяется углекислый газ (побочный продукт клеточного дыхания), который присоединяется к гемоглобину (формируется карбгемоглобин) и по венам транспортируется к легким, где выделяется в окружающую среду вместе с выдыхаемым воздухом.
Помимо переноса дыхательных газов, дополнительными функциями эритроцитов являются:
- Антигенная функция. Эритроциты обладают собственными антигенами, которые определяют принадлежность к одной из четырех основных групп крови (по системе АВ0).
- Транспортная функция. К наружной поверхности мембраны эритроцитов могут прикрепляться антигены микроорганизмов, различные антитела и некоторые медикаменты, которые разносятся с током крови по всему организму.
- Буферная функция. Гемоглобин принимает участие в поддержании кислотно-щелочного равновесия в организме.
- Остановка кровотечений. Эритроциты включаются в состав тромба, формирующегося при повреждении сосудов.
В организме человека эритроциты формируются из так называемых стволовых клеток. Эти уникальные клетки образуются на стадии эмбрионального развития. Они содержат ядро, в котором находится генетический аппарат (ДНК – дезоксирибонуклеиновая кислота), а также множество других органелл, обеспечивающий процессы их жизнедеятельности и размножения. Стволовые клетки дают начало всем клеточным элементам крови.
Для нормального процесса эритропоэза необходимы:
- Железо. Данный микроэлемент входит в состав гема (небелковой части молекулы гемоглобина) и обладает способностью обратимо связывать кислород и углекислый газ, что и определяет транспортную функцию эритроцитов.
- Витамины (В2, В6, В9 и B12). Регулируют образование ДНК в кроветворных клетках красного костного мозга, а также процессы дифференцировки (созревания) эритроцитов.
- Эритропоэтин. Гормональное вещество, вырабатываемое почками, которое стимулирует процесс образования эритроцитов в красном костном мозге. При уменьшении концентрации красных кровяных телец в крови развивается гипоксия (недостаток кислорода), что является основным стимулятором выработки эритропоэтина.
Образование эритроцитов (эритропоэз) начинается в конце 3 недели эмбрионального развития. На ранних этапах внутриутробного развития красные клетки крови образуются, в основном, в печени и селезенке. Примерно на 4 месяце беременности происходит миграция стволовых клеток из печени в полости костей таза, черепа, позвонков, ребер и других, в результате чего в них формируется красный костный мозг, который также принимает активное участие в процессе кроветворения. После рождения ребенка кроветворная функция печени и селезенки угнетается, и костный мозг остается единственным органом, обеспечивающим поддержание клеточного состава крови.
В процессе превращения в эритроцит, стволовая клетка претерпевает целый ряд изменений. Она уменьшается в размерах, постепенно теряет ядро и практически все органеллы (в результате чего дальнейшее ее деление становится невозможным), а также накапливает гемоглобин. Конечным этапом эритропоэза в красном костном мозге является ретикулоцит (незрелый эритроцит). Он вымывается из костей в периферический кровоток, и в течение суток происходит его созревание до стадии нормального эритроцита, способного в полной мере выполнять свои функции.
Средняя продолжительность жизни красных клеток крови составляет 90 – 120 дней. По истечении этого периода их клеточная мембрана становится менее пластичной, в результате чего теряет способность обратимо деформироваться при прохождении через капилляры. «Старые» эритроциты захватываются и разрушаются особыми клетками иммунной системы – макрофагами. Данный процесс происходит, в основном, в селезенке, а также (в значительно меньшей степени) в печени и красном костном мозге. Незначительно малая доля эритроцитов разрушается непосредственно в сосудистом русле.
При разрушении эритроцита из него выделяется гемоглобин, который быстро распадается на белковую и небелковую части. Глобин подвергается ряду превращений, в результате чего формируется пигментный комплекс желтого цвета – билирубин (несвязанная форма). Он нерастворим в воде и весьма токсичен (способен проникать в клетки организма, нарушая процессы их жизнедеятельности). Билирубин быстро транспортируется в печень, где связывается с глюкуроновой кислотой и выводится вместе с желчью.
Небелковая часть гемоглобина (гем) также подвергается разрушению, в результате чего происходит выделение свободного железа. Оно токсично для организма, поэтому быстро связывается с трансферрином (транспортным белком крови). Большая часть железа, выделяющегося при разрушении эритроцитов, транспортируется в красный костный мозг, где повторно используется для синтеза эритроцитов.
В организме взрослого человека содержится около 4 грамм железа. Эта цифра варьирует в зависимости от пола и возраста.
Концентрация железа в организме составляет:
- у новорожденных – 75 мг на 1 килограмм массы тела (мг/кг);
- у мужчин – более 50 мг/кг;
- у женщин – 35 мг/кг (что связано с ежемесячной потерей крови).
Основными местами содержания железа в организме являются:
- гемоглобин эритроцитов – 57%;
- мышцы – 27%;
- печень – 7 – 8%.
Кроме того, железо входит в состав целого ряда других белковых ферментов (цитохромов, каталазы, редуктазы). Они участвуют в окислительно-восстановительных процессах в организме, в процессах клеточного деления и регуляции многих других реакций. Дефицит железа может привести к недостатку данных ферментов и появлению соответствующих нарушений в организме.
Всасывание железа в организме человека происходит преимущественно в двенадцатиперстной кишке, при этом все железо, поступающее в организм, принято разделять на гемовое (двухвалентное, Fe +2 ), содержащееся в мясе животных и птиц, в рыбе, и негемовое (трехвалентное, Fe +3 ), основным источником которого являются молочные продукты и овощи. Важным условием, необходимым для нормального всасывания железа, является достаточное количество соляной кислоты, входящей в состав желудочного сока. При уменьшении ее количества всасывание железа значительно замедляется.
Всосавшееся железо связывается с трансферрином и транспортируется в красный костный мозг, где используется для синтеза эритроцитов, а также к органам-депо. Запасы железа в организме представлены, в основном, ферритином – комплексом, состоящим из белка апоферритина и атомов железа. Каждая молекула ферритина содержит в среднем 3 – 4 тысячи атомов железа. При снижении концентрации данного микроэлемента в крови, происходит выделение его из ферритина и использование для нужд организма.
Скорость всасывания железа в кишечнике строго ограничена и не может превышать 2,5 мг в сутки. Этого количества достаточно лишь для того, чтобы восстанавливать ежедневные потери данного микроэлемента, которые в норме составляют около 1 мг у мужчин и 2 мг у женщин. Следовательно, при различных патологических состояниях, сопровождающихся нарушением всасывания железа либо повышенными его потерями, может развиться дефицит данного микроэлемента. При снижении концентрации железа в плазме уменьшается количество синтезируемого гемоглобина, в результате чего образующиеся эритроциты будут иметь меньшие размеры. Кроме того, нарушаются процессы роста эритроцитов, что приводит к уменьшению их количества.
Причиной дефицита железа в организме может быть:
- недостаточное поступление железа с пищей;
- повышение потребности организма в железе;
- врожденный недостаток железа в организме;
- нарушение всасывания железа;
- нарушение синтеза трансферрина;
- повышенная кровопотеря;
- алкоголизм;
- применение лекарственных препаратов.
Нарушение питания может привести к развитию железодефицитной анемии как у детей, так и у взрослых.
Основными причинами недостаточного поступления железа в организм являются:
- длительное голодание;
- вегетарианство;
- однообразная диета с малым содержанием животных продуктов.
У новорожденных и детей грудного возраста потребности в железе полностью покрываются при кормлении грудным молоком (при условии, что мать не страдает железодефицитным состоянием). Если же слишком рано переводить ребенка на искусственное вскармливание, у него также могут появиться симптомы дефицита железа в организме.
В нормальных, физиологических условиях может возникать повышенная потребность в железе. Это характерно для женщин во время беременности и в период кормления грудью.
Несмотря на то, что определенная часть железа в период беременности сохраняется (ввиду отсутствия менструальных кровотечений), потребность в нем увеличивается в несколько раз.
| Причина | Примерное количество расходуемого железа |
| Увеличение объема циркулирующей крови и количества эритроцитов | 500 мг |
| Железо, передаваемое плоду | 300 мг |
| Железо, входящее в состав плаценты | 200 мг |
| Кровопотеря во время родов и в послеродовом периоде | 50 – 150 мг |
| Железо, теряемое с грудным молоком за весь период кормления | 400 – 500 мг |
Организм ребенка получает от матери все необходимые питательные вещества, в том числе и железо. Однако при наличии определенных заболеваний у матери или плода, возможно рождение ребенка с дефицитом железа.
Причиной врожденного дефицита железа в организме может быть:
- тяжелая железодефицитная анемия у матери;
- многоплодная беременность;
- недоношенность.
В любом из вышеперечисленных случаев концентрация железа в крови новорожденного значительно ниже нормы, и симптомы железодефицитной анемии могут проявляться уже с первых недель жизни.
Всасывание железа в двенадцатиперстной кишке возможно лишь при нормальном функциональном состоянии слизистой оболочки данного отдела кишечника. Различные заболевания желудочно-кишечного тракта могу повреждать слизистую оболочку и значительно снижать скорость поступления железа в организм.
К уменьшению всасывания железа в двенадцатиперстной кишке может привести:
- Энтерит – воспаление слизистой оболочки тонкого кишечника.
- Целиакия – наследственное заболевание, характеризующееся непереносимостью белка глютена и связанным с этим нарушением всасывания в тонком кишечнике.
- Helicobacter Pylori – инфекционный агент, поражающий слизистую оболочку желудка, что, в конечном итоге, приводит к уменьшению секреции соляной кислоты и нарушению всасывания железа.
- Атрофический гастрит – заболевание, связанное с атрофией (уменьшением размеров и функции) слизистой оболочки желудка.
- Аутоиммунный гастрит – заболевание, вызванное нарушением работы иммунной системы и выработкой антител к собственным клеткам слизистой оболочки желудка с последующим их разрушением.
- Удаление желудка и/или тонкой кишки – при этом уменьшается как количество образуемой соляной кислоты, так и функциональная площадь двенадцатиперстной кишки, где происходит всасывание железа.
- Болезнь Крона – аутоиммунное заболевание, проявляющееся воспалительным поражением слизистой оболочки всех отделов кишечника и, возможно, желудка.
- Муковисцидоз – наследственное заболевание, проявляющееся нарушением секреции всех желез организма, в том числе слизистой оболочки желудка.
- Рак желудка или двенадцатиперстной кишки.
Нарушение образования данного транспортного белка может быть связано с различными наследственными заболеваниями. Симптомов дефицита железа у новорожденного не будет, так как он получал данный микроэлемент из организма матери. После рождения основным способом поступления железа в организм ребенка является всасывание в кишечнике, однако из-за недостатка трансферрина всосавшееся железо не может быть доставлено к органам-депо и к красному костному мозгу и не может использоваться в синтезе эритроцитов.
Так как трансферрин синтезируется только в клетках печени, различные ее поражения (цирроз, гепатиты и другие) также могут привести к уменьшению концентрации данного белка в плазме и развитию симптомов железодефицитной анемии.
Одноразовая потеря большого количества крови обычно не приводит к развитию железодефицитной анемии, так как запасов железа в организме достаточно, чтобы возместить потери. В то же время при хронических, длительных, часто незаметных внутренних кровотечениях организм человека может терять по несколько миллиграмм железа ежедневно, на протяжении нескольких недель или даже месяцев.
Причиной хронической кровопотери может быть:
- язва желудка или двенадцатиперстной кишки;
- геморрой;
- неспецифический язвенный колит (воспаление слизистой толстого кишечника);
- болезнь Крона;
- полипоз кишечника;
- распадающиеся опухоли желудочно-кишечного тракта (и другой локализации);
- грыжа пищеводного отверстия диафрагмы;
- эндометриоз (разрастание клеток внутреннего слоя стенки матки);
- системная красная волчанка;
- системный васкулит (воспаление кровеносных сосудов различной локализации);
- сдача крови донорами более 4 раз в год (300 мл донорской крови содержат около 150 мг железа).
Если причина кровопотери не будет своевременно выявлена и устранена, высока вероятность развития железодефицитной анемии у больного, так как всасывающееся в кишечнике железо способно лишь покрывать физиологические потребности в данном микроэлементе.
Прием некоторых лекарственных препаратов может нарушать процессы всасывания и утилизации железа в организме. Обычно это происходит при длительном приеме больших доз медикаментов.
Препаратами, которые могут вызвать дефицит железа в организме, являются:
- Нестероидные противовоспалительные средства (аспирин и другие). Механизм действия данных препаратов связан с улучшением текучести крови, что может привести к появлению хронических внутренних кровотечений. Кроме того, они способствуют развитию язвы желудка.
- Антациды (Ренни, Алмагель). Данная группа препаратов нейтрализует или уменьшает скорость выделения желудочного сока, содержащего соляную кислоту, необходимую для нормального всасывания железа.
- Железосвязывающие препараты (Десферал, Эксиджад). Данные препараты обладают способностью связывать и выводить из организма железо, причем как свободное, так и входящее в состав трансферрина и ферритина. В случае передозировки возможно развитие железодефицитного состояния.
Во избежание развития железодефицитной анемии принимать данные препараты следует только по назначению врача, строго соблюдая дозировку и длительность использования.
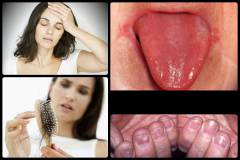
Проявлениями железодефицитной анемии являются:
- мышечная слабость;
- повышенная утомляемость;
- одышка;
- учащенное сердцебиение;
- изменения кожи и ее придатков (волос, ногтей);
- поражение слизистых оболочек;
- поражение языка;
- нарушение вкуса и обоняния;
- склонность к инфекционным заболеваниям;
- нарушения интеллектуального развития.
Как говорилось ранее, железо входит в состав множества ферментов, участвующих в процессах клеточного дыхания и деления. Дефицит данного микроэлемента приводит к повреждению кожи — она становится сухой, менее эластичной, шелушится и трескается. Кроме того, привычный красный или розоватый оттенок слизистым оболочками и коже придают эритроциты, которые находятся в капиллярах данных органов и содержат оксигенированный гемоглобин. При снижении его концентрации в крови, а также в результате уменьшения образования эритроцитов, может отмечаться бледность кожных покровов.
Волосы истончаются, теряют привычный блеск, становятся менее прочными, легко ломаются и выпадают. Рано появляется седина.
Поражение ногтей является весьма специфичным проявлением железодефицитной анемии. Они истончаются, приобретают матовый оттенок, расслаиваются и легко ломаются. Характерной является поперечная исчерченность ногтей. При выраженном дефиците железа может развиться койлонихия – края ногтей приподымаются и изгибаются в обратную сторону, приобретая ложкообразную форму.
Слизистые оболочки относятся к тканям, в которых процессы клеточного деления происходят максимально интенсивно. Вот почему их поражение является одним из первых проявлений дефицита железа в организме.
При железодефицитной анемии поражается:
- Слизистая оболочка полости рта. Она становится сухой, бледной, появляются участки атрофии. Затрудняется процесс пережевывания и проглатывания пищи. Также характерно наличие трещин на губах, образование заед в углах рта (хейлоз). В тяжелых случаях изменяется цвет и снижается прочность зубной эмали.
- Слизистая оболочка желудка и кишечника. В нормальных условиях слизистая оболочка данных органов играет важную роль в процессе всасывания пищи, а также содержит в себе множество желез, вырабатывающих желудочный сок, слизь и другие вещества. При ее атрофии (вызванной дефицитом железа) нарушается пищеварение, что может проявляться диареей или запорами, болями в животе, а также нарушением всасывания различных питательных веществ.
- Слизистая оболочка дыхательных путей. Поражение гортани и трахеи может проявляться першением, чувством наличия инородного тела в горле, что будет сопровождаться непродуктивным (сухим, без мокроты) кашлем. Кроме того, слизистая оболочка дыхательных путей в норме выполняет защитную функцию, предотвращая попадание чужеродных микроорганизмов и химических веществ в легкие. При ее атрофии повышается риск развития бронхита, пневмонии и других инфекционных заболеваний органов дыхания.
- Слизистая оболочка мочеполовой системы. Нарушение ее функции может проявляться болями при мочеиспускании и во время полового акта, недержанием мочи (чаще у детей), а также частыми инфекционными заболеваниями в пораженной области.
Как уже говорилось, слизистая оболочка языка богата вкусовыми рецепторами, расположенными преимущественно в сосочках. При их атрофии могут появляться различные вкусовые нарушения, начиная со снижения аппетита и непереносимости некоторых видов продуктов (обычно кислой и соленой пищи), и заканчивая извращением вкуса, пристрастием к поеданию земли, глины, сырого мяса и других несъедобных вещей.
Нарушения обоняния могут проявляться обонятельными галлюцинациями (ощущением запахов, которых на самом деле нет) либо пристрастием к непривычным запахам (лака, краски, бензина и другим).
Склонность к инфекционным заболеваниям
При дефиците железа нарушается образование не только эритроцитов, но и лейкоцитов – клеточных элементов крови, обеспечивающих защиту организма от чужеродных микроорганизмов. Недостаток данных клеток в периферической крови повышает риск развития различных бактериальных и вирусных инфекций, который еще больше возрастает при развитии анемии и нарушении микроциркуляции крови в коже и других органах.
Важно отметить, что лечение железодефицитной анемии будет неэффективным, если не выявить и не устранить причину ее возникновения.
В диагностике железодефицитной анемии применяется:
- опрос и осмотр пациента;
- общий анализ крови;
- биохимический анализ крови;
- пункция костного мозга.
Первое, что должен сделать врач при подозрении на железодефицитную анемию – это тщательно опросить и обследовать пациента.
Врач может задать следующий вопросы:
- Когда и в какой последовательности начали появляться симптомы заболевания?
- Как быстро они развивались?
- Имеются ли схожие симптомы у членов семьи или ближайших родственников?
- Как питается пациент?
- Страдает ли пациент какими-либо хроническими заболеваниями?
- Каково отношение к алкоголю?
- Принимал ли пациент какие-либо медикаменты в течение последних месяцев?
- Если больна беременная женщина – уточняется срок беременности, наличие и исход предыдущих беременностей, принимает ли она препараты железа.
- Если болен ребенок – уточняется его масса при рождении, родился ли он доношенным, принимала ли мать препараты железа во время беременности.
Во время обследования врач оценивает:
- Характер питания – по степени выраженности подкожно-жировой клетчатки.
- Цвет кожи и видимых слизистых оболочек – особое внимание уделяется слизистой полости рта и языку.
- Придатки кожи – волосы, ногти.
- Мышечную силу – врач просит пациента сжать свою руку или использует специальный прибор (динамометр).
- Артериальное давление – оно может быть снижено.
- Вкус и обоняние.
Это первый анализ, назначаемый всем пациентам при подозрении на анемию. Он позволяет подтвердить или опровергнуть наличие анемии, а также дает косвенную информацию о состоянии кроветворения в красном костном мозге.
Кровь для общего анализа может браться из пальца или из вены. Первый вариант более подходит в том случае, если общий анализ является единственным лабораторным исследованием, назначенным пациенту (когда достаточно небольшого количества крови). Перед взятием крови кожу пальца всегда обрабатывают ватой, смоченной в 70% спирте, чтобы избежать занесения инфекции. Прокол производится специальной одноразовой иглой (скарификатором) на глубину 2 – 3 мм. Кровотечение в данном случае несильное и полностью останавливается практически сразу после взятия крови.
В том случае, если планируется выполнять сразу несколько исследований (например, общий и биохимический анализ) – берут венозную кровь, так как ее легче получить в больших количествах. Перед забором крови на среднюю треть плеча накладывается резиновый жгут, что приводит к наполнению вен кровью и облегчает определение их местоположения под кожей. Место прокола также должно быть обработано спиртовым раствором, после чего медсестра одноразовым шприцем прокалывает вену и набирает кровь для анализа.
Полученную одним из описанных методов кровь направляют в лабораторию, где она исследуется в гематологическом анализаторе – современном высокоточном приборе, имеющемся в большинстве лабораторий мира. Часть полученной крови окрашивают специальными красителями и исследуют в световом микроскопе, что позволяет визуально оценить форму эритроцитов, их строение, а при отсутствии или неисправности гематологического анализатора – произвести подсчет всех клеточных элементов крови.
При железодефицитной анемии мазок периферической крови характеризуется:
- Пойкилоцитозом – наличием в мазке эритроцитов различных форм.
- Микроцитозом – преобладанием эритроцитов, размер которых меньше нормы (могут встречаться и нормальные эритроциты).
- Гипохромией – цвет эритроцитов изменяется с ярко-красного на бледно-розовый.
| Исследуемый показатель | Что обозначает? | Норма | Возможные изменения при железодефицитной анемии |
| Концентрация эритроцитов (RBC) | При истощении запасов железа в организме нарушается эритропоэз в красном костном мозге, ввиду чего общая концентрация эритроцитов в крови будет снижена. | Мужчины (М): 4,0 – 5,0 х 10 12 /л. | Менее 4,0 х 10 12 /л. |
| Женщины (Ж): 3,5 – 4,7 х 10 12 /л. | Менее 3,5 х 10 12 /л. | ||
| Средний объем эритроцита (MCV) | При дефиците железа нарушаются процессы образования гемоглобина, в результате чего уменьшается размер самих эритроцитов. Гематологический анализатор позволяет максимально точно определить данный показатель. | 75 – 100 кубических микрометров (мкм 3 ). | Менее 70 мкм 3 . |
| Концентрация тромбоцитов (PLT) | Тромбоциты – клеточные элементы крови, отвечающие за остановку кровотечений. Изменение их концентрации может наблюдаться в том случае, если дефицит железа вызван хронической кровопотерей, что приведет к компенсаторному увеличению их образования в костном мозге. | 180 – 320 х 10 9 /л. | В норме или увеличена. |
| Концентрация лейкоцитов (WBC) | При развитии инфекционных осложнений концентрация лейкоцитов может значительно повышаться. | 4,0 – 9,0 х 10 9 /л. | В норме или увеличена. |
| Концентрация ретикулоцитов (RET) | В нормальных условиях естественным ответом организма на анемию является увеличение скорости образования эритроцитов в красном костном мозге. Однако при дефиците железа развитие данной компенсаторной реакции невозможно, ввиду чего снижается количество ретикулоцитов в крови. | М: 0,24 – 1,7%. | Уменьшена либо находится на нижней границе нормы. |
| Ж: 0,12 – 2,05%. | |||
| Общий уровень гемоглобина (HGB) | Как уже говорилось, дефицит железа приводит к нарушению образования гемоглобина. Чем дольше длится заболевание, тем ниже будет данный показатель. | М: 130 – 170 г/л. | Менее 120 г/л. |
| Ж: 120 – 150 г/л. | Менее 110 г/л. | ||
| Среднее содержание гемоглобина в одном эритроците (MCH) | Данный показатель более точно характеризует нарушение образования гемоглобина. | 27 – 33 пикограмм (пг). | Менее 24 пг. |
| Гематокрит (Hct) | Данный показатель отображает количество клеточных элементов по отношению к объему плазмы. Так как основное большинство клеток крови представлено эритроцитами, уменьшение их количества приведет к снижению гематокрита. | М: 42 – 50%. | Менее 40%. |
| Ж: 38 – 47%. | Менее 35%. | ||
| Цветовой показатель (ЦП) | Цветовой показатель определяется путем пропускания через взвесь эритроцитов световой волны определенной длины, которая поглощается исключительно гемоглобином. Чем меньше будет концентрация данного комплекса в крови, тем ниже будет значение цветового показателя. | 0,85 – 1,05. | Менее 0,8. |
| Скорость оседания эритроцитов (СОЭ) | Все клетки крови, а также эндотелий (внутренняя поверхность) сосудов, имеют отрицательный заряд. Они отталкиваются друг от друга, что способствует поддержанию эритроцитов во взвешенном состоянии. При уменьшении концентрации эритроцитов расстояние между ними увеличивается, и сила отталкивания уменьшается, в результате чего они будут оседать на дно пробирки быстрее, чем в нормальных условиях. | М: 3 – 10 мм/час. | Более 15 мм/час. |
| Ж: 5 – 15 мм/час. | Более 20 мм/час. |
В ходе данного исследования удается установить концентрацию различных химических веществ, находящихся в крови. Это дает информацию о состоянии внутренних органов (печени, почек, костного мозга и других), а также позволяет выявить множество заболеваний.
Существует несколько десятков биохимических показателей, определяемых в крови. В данном разделе будут описаны только те из них, которые имеют значение в диагностике железодефицитной анемии.
| Исследуемый показатель | Что обозначает? | Норма | Возможные изменения при железодефицитной анемии |
| Концентрация сывороточного железа | Вначале данный показатель может быть в норме, так как дефицит железа будет компенсироваться выделением его из депо. Только при длительном течении заболевания концентрация железа в крови начнет снижаться. | М: 17,9 – 22,5 мкмоль/л. | В норме или снижена. |
| Ж: 14,3 – 17,9 мкмоль/л. | |||
| Уровень ферритина в крови | Как говорилось ранее, ферритин является одним из основных видов депонирования железа. При недостатке данного элемента начинается мобилизация его из органов-депо, ввиду чего уменьшение концентрации ферритина в плазме является одним из первых признаков железодефицитного состояния. | Дети: 7 – 140 нанограмм в 1 миллилитре крови (нг/мл). | Чем дольше длится дефицит железа, тем меньше уровень ферритина. |
| М: 15 – 200 нг/мл. | |||
| Ж: 12 – 150 нг/мл. | |||
| Общая железосвязывающая способность сыворотки | Данный анализ основан на способности трансферрина, находящегося в крови, связывать железо. В нормальных условиях, каждая молекула трансферрина только на 1/3 связана с железом. При дефиците данного микроэлемента печень начинает синтезировать больше трансферрина. Концентрация его в крови повышается, однако количество железа, приходящегося на каждую молекулу, снижается. Определив, какая доля молекул трансферрина находится в несвязанном с железом состоянии, можно сделать выводы о выраженности дефицита железа в организме. | 45 – 77 мкмоль/л. | Значительно выше нормы. |
| Концентрация эритропоэтина | Как было упомянуто ранее, эритропоэтин выделяется почками, если ткани организма испытывают недостаток в кислороде. В норме данный гормон стимулирует эритропоэз в костном мозге, однако при дефиците железа данная компенсаторная реакция малоэффективна. | 10 – 30 международных миллиединиц в 1 миллилитре (мМЕ/мл). | Значительно выше нормы. |
Данное исследование заключается в прокалывании одной из костей организма (обычно грудины) специальной полой иглой и заборе нескольких миллилитров вещества костного мозга, которое потом исследуется под микроскопом. Это позволяет напрямую оценить выраженность изменения структуры и функции органа.
В начале заболевания никаких изменений в пунктате костного мозга не будет. При развитии анемии может отмечаться разрастание эритроидного ростка кроветворения (увеличения количества клеток-предшественниц эритроцитов).
Для выявления причины железодефицитной анемии применяется:
- анализ кала на наличие скрытой крови;
- рентгенологическое исследование;
- компьютерная томография;
- эндоскопические исследования;
- консультация других специалистов.
Причиной появления крови в кале (мелены) может стать кровотечение из язвы, распад опухоли, болезнь Крона, неспецифический язвенный колит и другие заболевания. Обильные кровотечения легко определяются визуально по изменению цвета каловых масс на ярко-красный (при кровотечении из нижних отелов кишечника) или черный (при кровотечении из сосудов пищевода, желудка и верхнего отдела кишечника).
Массивные однократные кровотечения практически не приводит к развитию железодефицитной анемии, так как быстро диагностируются и устраняются. Опасность в этом плане представляют длительные, небольшие по объему кровопотери, возникающие при повреждении (или изъязвлении) мелких сосудов желудочно-кишечного трата. В таком случае выявить кровь в кале возможно только с помощью специального исследования, которое назначается во всех случаях анемии неясного генеза.
С целью выявления опухолей или язв желудка и кишечника, которые могли стать причиной хронического кровотечения, применяется рентген с контрастом. В роли контраста используется вещество, которое не поглощает рентгеновские лучи. Обычно это взвесь бария в воде, которую пациент должен выпить непосредственно перед началом исследования. Барий покрывает слизистые оболочки пищевода, желудка и кишечника, в результате чего на рентгеновском снимке становится четко различима их форма, контур и различные деформации.
Перед проведением исследования необходимо исключить прием пищи в течение последних 8 часов, а при исследовании нижних отделов кишечника назначаются очистительные клизмы.
В данную группу включен ряд исследований, суть которых заключается во введении в полости организма специального аппарата с видеокамерой на одном конце, подсоединенной к монитору. Этот метод позволяет визуально исследовать слизистые оболочки внутренних органов, оценить их строение и функцию, а также выявить опухоль или кровотечение.
С целью установления причины железодефицитной анемии используется:
- Фиброэзофагогастродуоденоскопия (ФЭГДС) – введение эндоскопа через рот и исследование слизистой оболочки пищевода, желудка и верхних отделов кишечника.
- Ректороманоскопия – исследование прямой и нижнего отдела сигмовидной кишки.
- Колоноскопия – исследование слизистой оболочки толстого кишечника.
- Лапароскопия – прокалывание кожи передней стенки живота и введение эндоскопа в брюшную полость.
- Кольпоскопия – исследование влагалищной части шейки матки.
При выявлении заболевания различных систем и органов гематолог может привлекать специалистов из других областей медицины с целью постановки более точного диагноза и назначения адекватного лечения.
Для выявления причины железодефицитной анемии может понадобиться консультация:
- Диетолога – при выявлении нарушения питания.
- Гастролога – при подозрении на наличие язвы или других заболеваний желудочно-кишечного тракта.
- Хирурга – при наличии кровотечения из желудочно-кишечного тракта или другой локализации.
- Онколога – при подозрении на опухоль желудка или кишечника.
- Акушера-гинеколога – при наличии признаков беременности.
| Название продукта | Содержание железа в 100 г продукта |
| Продукты животного происхождения | |
| Печень свиная | 20 мг |
| Печень куриная | 15 мг |
| Печень говяжья | 11 мг |
| Яичный желток | 7 мг |
| Мясо кролика | 4,5 – 5 мг |
| Баранина, говядина | 3 мг |
| Куриное мясо | 2,5 мг |
| Творог | 0,5 мг |
| Коровье молоко | 0,1 – 0,2 мг |
| Продукты растительного происхождения | |
| Плоды шиповника | 20 мг |
| Морская капуста | 16 мг |
| Чернослив | 13 мг |
| Гречка | 8 мг |
| Семена подсолнечника | 6 мг |
| Смородина черная | 5,2 мг |
| Миндаль | 4,5 мг |
| Персик | 4 мг |
| Яблоки | 2,5 мг |
Основным направлением в терапии данного заболевания является использование препаратов железа. Диетотерапия, хотя и является важным этапом лечения, не в состоянии самостоятельно восполнить дефицит железа в организме.
Методом выбора являются таблетированные формы препаратов. Парентеральное (внутривенное или внутримышечное) введение железа назначается в случае, если невозможно полноценное всасывание данного микроэлемента в кишечнике (например, после удаления части двенадцатиперстной кишки), необходимо быстро восполнить запасы железа (при массивной кровопотере) либо при развитии побочных реакций от применения пероральных форм препарата.
| Название препарата | Механизм лечебного действия | Способ применения и дозы | Контроль эффективности лечения |
| Гемофер пролонгатум | Препарат сульфата железа, восполняющий запасы данного микроэлемента в организме. | Принимать внутрь, за 60 минут до или через 2 часа после еды, запивая стаканом воды. |
Рекомендуемые дозы:
- детям – 3 миллиграмма на килограмм массы тела в сутки (мг/кг/сут);
- взрослым – 100 – 200 мг/сут.
Перерыв между двумя последующими приемами железа должен составлять не менее 6 часов, так как в этот период клетки кишечника невосприимчивы к новым дозам препарата.
Длительность лечения – 4 – 6 месяцев. После нормализации уровня гемоглобина переходят на поддерживающую дозу (30 – 50 мг/сутки) еще на 2 – 3 месяца.
- Повышение количества ретикулоцитов в анализе периферической крови на 5 – 10 день после начала приема препаратов железа.
- Повышение уровня гемоглобина (обычно отмечается через 3 – 4 недели лечения).
- Нормализация уровня гемоглобина и количества эритроцитов на 9 – 10 неделе лечения.
- Нормализация лабораторных показателей – уровня сывороточного железа, ферритина крови, общей железосвязывающей способности сыворотки.
- Постепенное исчезновение симптомов дефицита железа отмечается на протяжении нескольких недель или месяцев.
Данные критерии используются для контроля эффективности лечения всеми препаратами железа.
Рекомендуемые дозы:
- взрослым для лечения анемии – 2 таблетки 2 раза в день;
- женщинам при анемии во время беременности – 1 – 2 таблетки 1 раз в сутки.
После нормализации уровня гемоглобина переходят на поддерживающую терапию (20 – 50 мг 1 раз в сутки).
- сульфат железа;
- фолиевую кислоту;
- витамин В12.
Данный препарат назначается женщинам во время беременности (когда повышается риск развития дефицита железа, фолиевой кислоты и витаминов), а также при различных заболеваниях желудочно-кишечного тракта, когда нарушается всасывание не только железа, но и многих других веществ.
При внутривенном введении железа высок риск передозировки, поэтому данная процедура должна выполняться только в условиях стационара под контролем специалиста.
Важно помнить, что некоторые лекарственные средства (и другие вещества) могут в значительной степени ускорять либо замедлять скорость всасывания железа в кишечнике. Применять их совместно с препаратами железа стоит осторожно, так как это может привести к передозировке последних, или, наоборот, к отсутствию лечебного эффекта.
| Медикаменты, способствующие всасыванию железа | Вещества, препятствующие всасыванию железа |
|
|
При неосложненном течении и правильно проводимом лечении необходимости в данной процедуре нет.
Показаниями к переливанию эритроцитов являются:
- массивная кровопотеря;
- снижение концентрации гемоглобина менее 70 г/л;
- стойкое снижение систолического артериального давления (ниже 70 миллиметров ртутного столба);
- предстоящее хирургическое вмешательство;
- предстоящие роды.
Эритроциты следует переливать максимально короткий промежуток времени, пока не будет устранена угроза жизни пациента. Данная процедура может осложниться различными аллергическими реакциями, поэтому перед ее началом необходимо провести целый ряд тестов на определение совместимости крови донора и реципиента.

Причиной затруднений в лечении железодефицитной анемии может быть:
- неправильно выставленный диагноз;
- неустановленная причина дефицита железа;
- поздно начатое лечение;
- прием недостаточных доз препаратов железа;
- нарушение режима приема медикаментов или диеты.
При нарушениях в диагностике и лечении заболевания возможно развитие различных осложнений, некоторые из которых могут представлять опасность для здоровья и жизни человека.
Осложнениями железодефицитной анемии могут быть:
- Отставание в росте и развитии. Данное осложнение характерно для детей. Оно обусловлено ишемией и связанными с ней изменениями в различных органах, в том числе в ткани головного мозга. Отмечается как задержка физического развития, так и нарушение интеллектуальных способностей ребенка, которые при длительном течении заболевания могут оказаться необратимыми.
- Анемическая кома. Развитие комы обусловлено критическим снижением доставки кислорода к головному мозгу. Внешне это проявляется потерей сознания, отсутствием реакции на речь и болевые раздражители. Кома является опасным для жизни состоянием, требующим срочной медицинской помощи.
- Развитие недостаточности внутренних органов. При длительном дефиците железа и наличии анемии могут поражаться практически все органы человека. Наиболее характерным является развитие сердечной недостаточности, почечной недостаточности и печеночной недостаточности.
- Инфекционные осложнения. Часто рецидивирующие инфекции могут сопровождаться поражением внутренних органов и развитием сепсиса (попадания гноеродных бактерий в кровоток и ткани организма), что особенно опасно у детей и людей пожилого возраста.
источник
