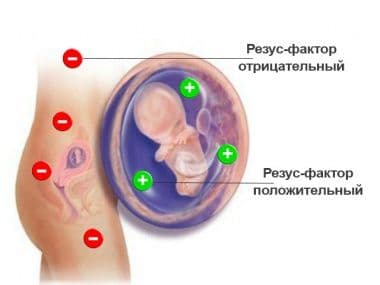
Стоит отметить, что в последние годы значительно участились случаи проявления гемолитической болезни — примерно один случай на 250-300 родов. Как правило, данная патология возникает из-за резус конфликта женщины и ребенка. Если же говорить о несовместимости по группе крови, то таких случаев в несколько раз меньше. Несовместимость же другим эритроцитарным антигенам вообще считается редкостью, ведь такие случаи единичные.
Если гемолитическая болезнь развивается по резус-фактору, то она протекает в 3-6% случаев довольно легко, но в то же время ее очень трудно диагностировать. Известны случаи, когда гемолитическая болезнь данного типа была обнаружена у новорожденного уже в запущенной стадии, когда лечение не приносит ощутимого результата.
Когда у новорожденного начинает развиваться гемолиз или разрушение эритроцитов, то очень быстро в его крови повышается уровень билирубина и провоцирует развитие анемии. Когда уровень билирубина слишком высокий и превышает критический показатель, то он начинает выделять токсины, которые влияют на головной мозг и многие другие органы ребенка. Кроме того начинает очень быстро прогрессировать анемия и организм для того, чтобы компенсировать недостаток кислорода начинает делать все возможное. Таким образом начинает увеличиваться в размерах печень, а за ней и селезенка.
На сегодняшний день врачи выделяют следующие клинические формы гемолитической анемии:
- Отечная форма ГБН. Данная форма является самой тяжелой и начинает развиваться она еще внутриутробно. Как результат уничтожения эритроцитов у ребенка развивается тяжелая форма анемии, нарушается обмен веществ, отекают ткани и снижается уровень белка. Если ГБН начала развиваться на раннем сроке беременности, то все может закончиться выкидышем. Если же ребенок все таки выживет, то родится он очень бледный, с ярко выраженными отеками.
- Желтушная форма ГБН. Такую форму можно встретить чаще всего. Основные симптомы — это ранее развитие желтухи, анемии и значительное увеличение печени и селезенки. Желтуха может появиться сразу же после рождения или примерно через 1-2 суток, что не свойственно для физиологической желтухи. Чем раньше она появилась, тем более тяжело будет протекать ГБН. Признаками заболевания становится зеленоватый цвет кожи, темная моча и бесцветный кал.
- Анемическая форма ГБН. Такая форма есть наиболее щадящей и легкой. Проявляется она на протяжении семи дней после рождения ребенка. Не всегда можно сразу отметить появление бледности кожи, а поэтому ГБН могут диагностировать на 2-3 неделю жизни малыша. Внешне ребенок остается прежним, но начинает увеличиваться в размерах печень и селезенка. Уровень билирубина будет повышенным, но немного. Такую форму заболевания можно легко вылечить без вредных последствий для здоровья малыша.
Нужно очень внимательно следить за состоянием ребенка и при малейших подозрениях усложнений обращайтесь немедленно к врачу.
Антенатальная диагностика проводится еще на протяжении беременности у женщин, которые входят в группу риска. Если у женщины отрицательный резус, то на протяжении беременности она должна пройти три раза определение наличии антител в крови. Очень важно учитывать результаты в динамике, ведь они могут показать высокий риск заболевания ребенка. Для того, чтобы окончательно убедится в диагнозе нужно исследовать околоплодные воды на наличие уровня билирубина, железа, глюкозы и белка. Кроме того подозрения могут вызвать изменения в развитии плода, которые можно обнаружить путем УЗИ.
Постнатальная диагностика проводится после рождения ребенка и полностью заключается в изучении клинических симптомов заболевания у ребенка. При этом нужно изучать совершенно все данные, при чем как в комплексе, так и в динамике.
Если у ребенка была обнаружена тяжелая форма гемолитической болезни, то тогда врачи прибегают к крайним мерам лечения: заменное переливание крови, гемосорбция или же плазмофорез. Благодаря переливанию крови из организма можно вывести излишек билирубина, а также пополнить запасы эритроцитов и гемоглобина. На сегодняшний день врачи уже перестали переливать цельную кровь, а для переливания используют эритроцитарную массу и свежезамороженную плазму.
- Уровень непрямого билирубина превышает критический показатель;
- уровень билирубина увеличивается каждый час примерно на 6-10 мкмоль/л;
- наблюдается тяжелая форма анемии.
Если у ребенка отмечена более легкая форма заболевания, то лечение проводится старым методом, который также позволяет снизить уровень билирубина в крови. Для этого могут переливать растворы глюкозы или же белковые препараты. Очень часто могут использовать фототерапию, которая при легких формах заболевания также дает хороший результат. Для того, чтобы провести фототерапию ребенка кладут в специальный кувез, где его начинают облучать специальным светом, который стимулирует распад билирубина в такую форма, которая могла бы вывестись из организма естественным путем.
Кроме того для лечения гемолитической болезни могут использовать витамины В2, В6, С, активированный уголь, преднизалон, кокарбоксилазу или фенобарбитал. Стоит отметить, что раньше считали, что если ребенок более гемолитической болезнью, то его нельзя прикладывать к груди. Сегодня же доказано, что антитела, которые есть в молоке у женщины не попадают в кровь ребенка и полностью разрушаются под воздействием соляной кислоты желудка малыша. Поэтому не надо ничего бояться и прикладывайте ребенка как можно чаще к груди. Это поможет ему быстрее окрепнуть и начать самостоятельно бороться с заболеванием.
источник
операция заменное переливание крови
резус – изоиммунизация плода и новорожденного
АВО — изоиммунизация плода и новорожденного
АД ? артериальное давление
БЭ ? билирубиновая энцефалопатия
ГБН ? гемолитическая болезнь новорожденных
ДВС ? диссеминированное внутрисосудистое свертывание крови
КОС ? кислотно-щелочное состояние
МКБ ? международная классификация болезней -10
ОЗПК ? операция заменного переливания крови
ОРИТН ? отделение реанимации и интенсивной терапии новорожденных
ОЦК ? объем циркулирующей крови
ПИТН — палата реанимации и интенсивной терапии новорожденных
СЗП- свежезамороженная плазма
ЧСС ? частота сердечных сокращений
Гемолитическая болезнь плода и новорожденного (ГБН) – изоиммунная гемолитическая анемия, возникающая в случаях несовместимости крови матери и плода по эритроцитарным антигенам, при этом антигены локализуются на эритроцитах плода, а антитела к ним вырабатываются в организме матери.
Гемолитическая болезнь плода и новорожденного (ГБН) – изоиммунная гемолитическая анемия, возникающая в случаях несовместимости крови матери и плода по эритроцитарным антигенам (АГ), при этом АГ локализуются на эритроцитах плода, а антитела (АТ) к ним вырабатываются в организме матери [1, 7, 14, 15].
Возникновение иммунологического конфликта возможно, если на эритроцитах плода присутствуют антигены, отсутствующие на мембранах клеток у матери. Так, иммунологической предпосылкой для развития ГБН является наличие резус-положительного плода у резус-отрицательной беременной. При иммунологическом конфликте вследствие групповой несовместимости у матери в большинстве случаев определяется O (I) группа крови, а у плода A (II) или (реже) B (III). Более редко ГБН развивается из-за несовпадения плода и беременной по другим групповым (Дафф, Келл, Кидд, Льюис, MNSs и т.д.) системам крови.
К попаданию эритроцитов плода в кровоток матери и возникновению иммунологического конфликта в случаях антигенной несовместимости по факторам крови предрасполагает предшествовавшая изосенсибилизация, вследствие абортов, выкидышей, внематочной беременности, родов, при которых иммунная система матери вырабатывает антитела к эритроцитарным антигенам. Если АТ относятся к иммуноглобулинам класса G (к подклассам IgG1, IgG3, IgG4) ? они беспрепятственно проникают через плаценту. С увеличением их концентрации в крови повышается вероятность развития гемолитической болезни плода и новорожденного. Антитела подкласса IgG2 обладают ограниченной способностью трансплацентарного транспорта, антитела класса IgM, к которым относятся в том числе ?- и ?-агглютинины, не проникают через плаценту.
Реализация ГБН по резус-фактору, как правило, происходит обычно при повторных беременностях, а развитие ГБН в результате конфликта по групповым факторам крови возможно уже при первой беременности. При наличии иммунологических предпосылок для реализации обоих вариантов ГБН чаще развивается по системе АВО. При этом возникновение гемолиза вследствие попадания в кровь ребенка II группы материнских анти-А- антител встречается чаще, чем при попадании в кровь ребенка III группы анти-В-антител. Однако в последнем случае проникновение анти-В-антител приводит к более тяжелому гемолизу, нередко требующему заменного переливания крови [17]. Тяжесть состояния ребенка и риск развития ядерной желтухи при ГБН по АВО-системе менее выражены по сравнению с ГБН по резус-фактору. Это объясняется тем, что групповые антигены А и В экспрессируются многими клетками организма, а не только эритроцитами, что приводит к связыванию значительного количества антител в некроветворных тканях и препятствует их гемолитическому воздействию [17].
ГБН в России диагностируется приблизительно у 0,6% всех новорожденных.
Гемолитическая болезнь плода и новорожденного (P55):
P55.0 — Резус – изоиммунизация плода и новорожденного
P55.1 — АВО — изоиммунизация плода и новорожденного
P55.8 — Другие формы гемолитической болезни плода и новорожденного
P55.9 — Гемолитическая болезнь плода и новорожденного неуточненная
1.5.1 По конфликту между матерью и плодом по системе АВО и другим эритроцитарным факторам крови:
- несовместимость по системе АВО;
- несовместимость эритроцитов матери и плода по резус- фактору;
- несовместимость по редким факторам крови.
1.5.2 По клиническим проявлениям выделяют формы заболевания:
отечная (гемолитическая анемия с водянкой);
желтушная (гемолитическая анемия с желтухой);
анемическая (гемолитическая анемия без желтухи и водянки).
1.5.3 По степени тяжести желтухи в желтушной форме:
1.5.4 По наличию осложнений:
билирубиновая энцефалопатия: острое поражение центральной нервной системы;
ядерная желтуха: необратимое хроническое поражение центральной нервной системы;
резус- принадлежность и группа крови матери;
инфекции во время беременности и родов;
наследственные заболевания (дефицит Г6ФДГ, гипотиреоз, другие редкие заболевания);
наличие желтухи у родителей;
наличие желтухи у предыдущего ребенка;
вес и гестационный возраст ребенка при рождении;
вскармливание ребенка (недостаточное вскармливание и/или рвота).
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
Общий отечный синдром (анасарка, асцит, гидроперикард), выраженная бледность кожи и слизистых, гепатомегалия и спленомегалия, желтуха отсутствует или слабо выражена. Возможен геморрагический синдром, развитие ДВС синдрома.
При рождении могут быть желтушно прокрашены околоплодные воды, оболочки пуповины, первородная смазка. Характерно раннее развитие желтухи, бледность кожных покровов и видимых слизистых оболочек, увеличение печени и селезенки.
На фоне бледности кожных покровов отмечают вялость, плохое сосание, тахикардию, увеличение размеров печени и селезенки, возможны приглушенность тонов сердца, систолический шум.
Ядерная желтуха – билирубиновая интоксикация- вялость, снижение аппетита, срыгивания, патологическое зевание, мышечная гипотония, исчезновение 2 фазы рефлекса Моро, далее возникает клиника энцефалопатии – опистотонус, «мозговой» крик, выбухание большого родничка, судороги, патологическая глазодвигательная симптоматика – симптом «заходящего солнца», нистагм. Синдром сгущения желчи – желтуха приобретает зеленоватый оттенок, печень увеличена, насыщенный цвет мочи.
- Рекомендуется по Rh-фактору установление уже в первые часы жизни ребенка на основании анамнеза (прирост титра анти-D антител у Rh(–)
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1в).
Всем женщинам с отрицательным резус-фактором во время беременности рекомендуется определение уровня иммунных АТ в крови в динамике [11].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
Коментарии: ГБН по АВ0-системе, как правило, не имеет специфических признаков в первые часы после рождения.
Если кровь матери характеризуется отрицательным резус-фактором или принадлежностью к О (I) группе, новорожденному рекомендуется обязательно проводить исследование концентрации общего билирубина в пуповинной крови и определение группы и резус-фактора крови
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
При подозрении на ГБН рекомендуется провести следующие лабораторные тесты [1, 7, 14,15, 26]:
- Групповая и резус принадлежность крови матери и ребенка.
- Общий анализ крови.
- Биохимический анализ крови (общий билирубин и фракции, альбумин, уровень глюкозы; другие параметры (фракции билирубина, кислотно-щелочное состояние (КОС), электролиты и др.) — по показаниям);
- Серологические тесты: Реакция Кумбса.
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 3 ).
Комментарии: Прямая проба Кумбса становится положительной при наличии фиксированных антител на поверхности эритроцитов, что, как правило, наблюдается при ГБН по резус-фактору. Из-за небольшого количества фиксированных на эритроцитах антител, при ГБН по АВО чаще наблюдается слабо положительная прямая проба Кумбса в первые сутки жизни, которая уже может стать негативной через 2-3 дня после рождения.
Непрямая проба Кумбса предназначена для выявления неполных антител, присутствующих в исследуемой сыворотке. Это более чувствительный тест для выявления материнских изоантител, чем прямая проба Кумбса. Непрямая проба Кумбса может применяться в индивидуальных случаях, когда причина гемолиза неясна.
Следует помнить, что выраженность реакции Кумбса не коррелирует с тяжестью желтухи! (Уровень доказательности D)
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
кровь на ИФА (на наличие инфекции);
кровь на ПЦР (на наличие инфекции);
бактериологическое исследование крови.
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 4).2%
Рекомендуется фототерапия (ФТ), как наиболее эффективный метод консервативной терапии ГБН.
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарии: Особенности проведения ФТ при ГБН:
Возможно применение как стандартных ламп, так и фиброоптической и светодиодной ФТ, целесообразно комбинировать несколько методов ФТ;
Источник света располагается на расстоянии 50 см над ребенком. Для усиления эффекта фототерапии лампа может быть приближена на расстояние 10-20 см от ребенка при постоянном наблюдении медицинского персонала и контроле температуры тела [11];
Проведение фототерапии при ГБН (особенно у детей с риском ОЗПК) должно выполняться в непрерывном режиме;
Поверхность тела ребенка на фоне ФТ должна быть максимально открыта. Подгузник может быть оставлен на месте;
Глаза и половые органы должны быть защищены светонепроницаемым материалом;
Суточный объем жидкости, который ребенок получает энтерально или парентерально, необходимо увеличить на 10-20% по сравнению с физиологической потребностью ребенка;
Спустя 12 часов после окончания фототерапии необходимо выполнить контрольное исследование билирубина;
Фототерапия проводится до, во время (при помощи фиброоптической системы) и после операции заменного переливания крови.
Рекомендуется внутривенное введение иммуноглобулина человека нормального . Высокие дозы стандартных иммуноглобулинов блокируют Fc-рецепторы клеток ретикуло-эндотелиальной системы и тем самым позволяют снизить гемолиз и, следовательно, уровень билирубина, что в свою очередь уменьшает число ОЗПК [7, 19, 22].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1b.).
Комментарии: Препараты иммуноглобулина человеческого новорожденным с ГБН вводятся по следующей схеме:
в первые часы жизни новорожденного внутривенно медленно (по возможности, в течение 2 часов), но с обязательным соблюдением требований инструкции к лекарственному препарату;
доза ? 0,5-1,0 г/кг (в среднем 0,8 г/кг)*
*В случае назначения дозы иммуноглобулина, превышающей указанную в инструкции к препарату, необходимо как можно подробнее обосновать данное действие в истории болезни и оформить коллегиальное разрешение на проведение ребенку терапии «Off-label». Применение терапии «вне инструкции» («off-label») также требует обязательного оформления добровольного информированного согласия законного представителя пациента, в котором подробно разъясняются особенность применения такой терапии, возможные риски и побочные явления, а также разъясняется право отказаться от проведения терапии «off-label»;
повторное введение иммуноглобулина при необходимости осуществляется через 12 часов от предыдущего;
введение иммуноглобулина при ГБН возможно в течение первых 3 суток жизни.
Не рекомендуется допаивание детей на грудном вскармливании [11].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1b).
Комментарии: Исключение составляют случаи, когда грудного молока недостаточно, чтобы увеличить суточный объем на 10-20%. Если состояние ребенка не позволяет увеличить объем жидкости энтерально, только тогда проводится инфузионная терапия.
Желчегонная терапия рекомендована в случае развития синдрома холестаза на фоне ГБН. Проводится только препаратом урсодезоксихолевой кислоты в виде суспензии из расчета 20-30 мг/кг/сут .
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 3).
Введение альбумина человека . Доказательств того, что инфузия альбумин человека увеличивает долгосрочные исходы у детей с тяжелой гипербилирубинемией нет, поэтому его рутинное применение не рекомендуется [24].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 3).
Фенобарбитал** – эффект при ГБН не доказан, применение не допустимо [11].
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 3).
Другие медикаментозные средства ( препараты группы гепатопротекторов ) – применение при ГБН не доказано [1] и не допустимо.
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 3).
Рекомендована операция заменного переливания крови.
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарии: Показания для ОЗПК:
в случае неэффективности фототерапии рекомендуется заменное переливание крови;
в случае появления клинических симптомов острой билирубиновой энцефалопатии (мышечный гипертонус, опистотонус, лихорадка, «мозговой» крик) заменое переливание крови проводится независимо от уровня билирубина;
при ГБН, вызванной изолированным резус-конфликтом используется Rh- отрицательная одногруппная с кровью ребенка ЭМ и СЗП по возможности АВ (IV) группы крови в соотношении ЭМ к СЗП — 2:1;
при ГБН, вызванной изолированным групповым конфликтом, используется ЭМ первой (I) группы, совпадающая с резус-принадлежностью эритроцитов ребенка и одногруппная или АВ (IV) группы СЗП в соотношении 2:1;
при несовместимости крови матери и крови ребенка по редким факторам необходимо использовать кровь от индивидуально подобранных доноров.
При ГБН используют только свежеприготовленную ЭМ (срок хранения не более 72 часов);
ОЗПК проводится в асептических условиях в отделении интенсивной терапии или операционной;
Во время операции должен быть обеспечен мониторный контроль за частотой сердцебиений, дыхания, артериальным давлением, насыщением гемоглобина кислородом, температурой тела. Перед началом операции пациенту вводится назогастральный зонд;
Переливание производят через пупочную вену с помощью поливинилового катетера (№ 6, 8, 10). Глубина введения катетера зависит от массы тела пациента (не более 7 см.).
Расчет объема для ОЗПК
V общий = m?ОЦК?2, где V- объем, m- масса тела в кг,
ОЦК – для недоношенных – 100-110 мл/кг, для доношенных – 80-90 мл/кг.
Пример: ребенок массой тела 3 кг.
Общий объем (V общ.) = 3?85?2 = 510 мл
Абсолютный объем эритроцитов (V абс.), необходимый для получения Ht 50% V общий: 2 = 510: 2 = 255 мл
(V эр.массы) = Vабс : 0,7 (примерный Ht эритроцитов) = 255: 0,7 = 364 мл
Фактический объем СЗП = V общ. — V эр. Массы = 510 – 364 = 146 мл
Вначале через катетер выпускают 10 мл крови, которую используют для определения концентрации билирубина. Затем вводят такой же объем донорской крови со скоростью 3-4 мл/мин.
Введение и выведение крови чередуются объемом 20 мл у доношенных и 10 мл у недоношенных детей.
Объем одной эксфузии-инфузии не должен превышать 5-10% ОЦК. Общая продолжительность операции составляет около 2-х часов.
После операции провести ОАМ и через два часа по окончании трансфузии рекомендуется определить концентрацию глюкозы в крови.
Об эффективности проведенной ОЗПК свидетельствует более, чем двукратное снижение концентрации билирубина в конце операции.
исключительно грудное вскармливание;
медицинский отвод от профилактических прививок на 1 месяц.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Рекомендована профилактика Rh-иммунизации после родов Rh-отрицательным родильницам, не имеющим анти-резусных антител, родивших резус-положительного ребенка. Выполняется в первые 72 часа после родов путем введения 300 мкг анти-Д(Rh)-иммуноглобулина [1, 7].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
- Рекомендовано:
- наблюдение врача-педиатра участкового, врача общей практики;
- каждый месяц контроль ОАК;
- в 6 месяцев детям после ОЗПК – кровь на ВИЧ;
- вопрос о профилактических прививках решают после 6 месяцев жизни.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Дополнительные факторы, повышающие риск развития билирубиновой энцефалопатии:
- Факторы, повышающие проницаемость ГЭБ для билирубина: гиперосмолярность крови, ацидоз, кровоизлияния в мозг, нейроинфекции, артериальная гипотензия.
- Факторы, повышающие чувствительность нейронов головного мозга к токсическому действию неконъюгированного билирубина: недоношенность, тяжелая асфиксия, голодание, гипогликемия, анемия.
- Факторы, снижающие способность альбумина крови прочно связывать неконъюгированный билирубин: недоношенность, гипоальбуминемия, инфекция, ацидоз, гипоксия, повышение уровня неэстерифицированных жирных кислот в крови, использование сульфаниламидов, фуросемида, фенитоина , диазепама, индометацина, салицилатов, полусинтетических пеницилинов, цефалоспоринов.
Критерии качества
Уровень достоверности доказательств
Уровень убедительности рекомендаций
Выполнено исследование уровня общего билирубина и уровня общего гемоглобина в пуповинной крови у новорожденного при рождении (при отрицательном резус факторе и/или группы крови 0(I) у матери)
Выполнено определение основных групп крови (A, B, 0) и определение резус-принадлежности у новорожденного в пуповинной крови при рождении
Выполнен прямой антиглобулиновый тест (прямая проба Кумбса) и/или непрямой антиглобулиновый тест (тест Кумбса)
Выполнено повторное исследование уровня общего билирубина и определен почасовой прирост общего билирубина не позднее 6 часов и 12 часов от момента рождения
Выполнен общий (клинический) анализ крови с определением количества ретикулоцитов7%
Выполнена фототерапия кожи и/или операция заменного переливания крови после оценки уровня общего билирубина в зависимости от массы тела при рождении (при наличии показаний)
Выполнена операция частичного заменного перелевания крови не позднее 3 часов от момента рождения (при отечной форме гемолитической болезни)
- Неонатология. Национальное руководство. Краткое издание / под ред. акад. РАМН Н.Н. Володина. ? М. : ГЭОТАР-Медиа, 2013. ? 896 с.
- Новые технологии в диагностике, лечении и профилактике гемолитической болезни плода и новорожденного, Коноплянников А.Г. Автореферат на соискание ученой степени доктора медицинских наук, Москва 2009
- Отечная форма гемолитической болезни новорожденных (диагностика, лечение, отдаленные результаты), Чистозвонова Е.А. Автореферат на соискание ученой степени кандидата медицинских наук, Москва 2004
- Приказ Минздрава России от 1 ноября 2012 г. N 572н «Об утверждении Порядка оказания медицинской помощи по профилю «акушерство и гинекология (за исключением использования вспомогательных репродуктивных технологий)».
- Приказ Минздрава России от 15 ноября 2012 года N 921н «Об утверждении Порядка оказания медицинской помощи по профилю «неонатология».
- Приказ Минздрава России от 2 апреля 2013 г. N 183н «Об утверждении правил клинического использования донорской крови и (или) ее компонентов».
- Шабалов Н.П. Неонатология / Н.П.Шабалов. ? 5-е изд., испр. и доп., в 2 томах. ? М.: МЕДпресс-информ, 2009. ? 1504 с.
- ABM Clinical protocol 22: Guidelines for management of jaundice in the breastfeeding infant equal to or greater than 35 weeks gestation // Breastfeeding medicine. ? 2010. ? Vol. 5. ? N 2. ? P. 87-93.
- Alcock G.S., Liley H. Immunoglobulin infusion for isoimmune haemolytic jaundice in neonates (Cochrane Review). In: The Cochrane Library, Issue 2, 2004. Chichester, UK: John Wiley & Sons, Ltd.
- Altunyurt S., Okyay E., Saatli B., Canbahishov T., Demir N., Ozkan H. Neonatal outcome of fetuses receiving intrauterine transfusion for severe hydrops complicated by Rhesus hemolytic disease // Int. J. Gynaecol. Obstet. ? 2012. ? Vol. 117. ? N 2. ? P. 153-156.
- Barrington K.J., Sankaran K. Canadian Paediatric Society Fetus and Newborn Committee Abridged version // Paediatr Child Health. ? 2007. ? Vol. 12. ? P. 1-12.
- Buonocore G.,Bracci R., Weindling M. Neonatology: A Practical Approach to Neonatal Management, 2012
- Christensen RD, Henry E. Hereditary spherocytosis in neonates with hyperbilirubinemia // Pediatrics. ? 2010. ? Vol. 125. ? N 1. ? P. 120-125.
- Gleason C.A., Devaskar S.U. Avery’s diseases of the newborn // 9th Ed. Elsevier Saunders. ? 2011. ? 1520 p.
- Gomella T.L. Neonatology: Management, Procedures, On-Call Problems, Diseases, and Drugs // 7th edition; Medical Publishing Division. ? 2013. ? 1113 p.
- Hudon L., Moise K.J.Jr., Hegemier S.E., et al. Long-term neurodevelopmental outcome after intrauterine transfusion for the treatment of fetal hemolytic disease // Am J Obstet Gynecol. ? 1998. ? Vol. 179. ? N 4. ? Р. 858-863.
- Kaplan M., Na»amad M., Kenan A., et al. Failure to predict hemolysis and hyperbilirubinemia by IgG subclass in blood group A or B infants born to group O mothers // Pediatrics. ? 2009. ? Vol. 123. ? N 1. ? e132-137.
- Maisels M.J.,Watchoko J.F. Neonatology: A Practical Approach to Neonatal Management/ Treatmen of Hyperbilirubinemia- 2012- P 629
- Management of Hyperbilirubinemia in the Newborn Infant 35 or More Weeks of Gestation // Pediatrics. ? 2004. ? Vol. 114. ? P. 297-316.
- Mary Beth Ross, Pedro de Alarcon. Hemoliytic Disease of Fetus and Newborn. NeoReviews Vol.14 No.2 February 2013
- Matthews D.C., Glader B. Erythrocyte disorders in infancy // In: Avery’s diseases of the newborn. Ninth edition. Elsevier-Saunders. ? 2012. ? P. 1087-1092.
- Miqdad A.M., Abdelbasit O.B., Shaheed M.M., Seidahmed M.Z., Abomelha A.M., Arcala O.P. Intravenous immunoglobulin G (IVIG) therapy for significant hyperbilirubinemia in ABO hemolytic disease of the newborn // J Matern Fetal Neonatal Med. ? 2004. ? Vol. 16. ? P. 163-166.
- Moise K.J. Jr. Management of Rhesus alloimmunization in pregnancy // Obstet Gynecol. ? 2008. ? Vol. 112. ? P. 164-176.
- Smits-Wintjens V.E.H.J., Walther F.J., Lopriore E. Rhesus haemolytic disease of the newborn: Postnatal management, associated morbidity and long-term outcome // Seminars in Fetal & Neonatal Medicine. ? 2008. ? Vol. 13. ? P. 265-271.
- Steiner L.A., Bizzarro M.J., Ehrenkranz R.A., Gallagher P.G. A decline in the frequency of neonatal exchange transfusions and its effect on exchange-related morbidity and mortality // Pediatrics. ? 2007. ? Vol. 120. ? N 1. ? Р. 27-32.
- Wagle S., Deshpande P.G., Itani O., Windle M.L., Clark D.A., Wagner C.l. Rosenkrantz T. Hemolytic Disease of Newborn. Updated: Sep 26, 2014. http://emedicine.medscape.com/article/974349
- Oxford handbook of Neonatology Ed. Fox G., Hoque N., Watts T // Oxford, New York, Oxford University Press, 2010. — 523.
Антонов А.Г. ?
Аронскинд Е.В. ?
Байбарина Е.Н. ?
Володин Н.Н. ? д.м.н., академик РАН, Президент Российской ассоциации специалистов перинатальной медицины, ФГБУ «Федеральный научный клинический центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Минздрава России.
Дегтярев Д.Н. ?
Дегтярева А.В. ?
Мухаметшин Ф.Г. ?
Паршикова О.В. ?
Целевая аудитория данных клинических рекомендаций – специалисты, имеющие высшее медицинское образование по специальностям:
Методы, использованные для сбора/селекции доказательств:
поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств: доказательной базой для рекомендаций являются публикации, вошедшие в Кохрановскую библиотеку, базы данных MEDLINE и EMBASE. Глубина поиска составляла 25 лет.
Методы, использованные для оценки качества и силы доказательств:
оценка значимости в соответствии с рейтинговой схемой для оценки степени обоснованности («силы») рекомендаций (табл. П1, П2).
Таблица П1 – Уровни достоверности доказательств в соответствии с международными критериями
Уровень достоверности
Мета-анализ рандомизированных контролируемых исследований
По крайней мере, 1 рандомизированное контролируемое исследование
По меньшей мере, 1 контролируемое исследование без рандомизации
По крайней мере, 1 квази-экспериментальное исследование
Описательные исследования, такие как сравнительные исследования, корреляционные исследования или «случай-контроль» исследования
Отчет экспертного комитета или мнение и/или клинический опыт призванного авторитета
Таблица П2 – Уровни убедительности рекомендаций
Уровень убедительности
Основание рекомендации
Уровень доказательства 2 или экстраполированные рекомендации уровня доказательства 1
Уровень доказательства 3 или экстраполированные рекомендации уровней доказательства 1 или 2
Уровень доказательства 4 или экстраполированные рекомендации уровней доказательства 2 или 3
Индикаторы доброкачественной практики (Good Practice Points – GPPs):
рекомендуемая доброкачественная практика базируется на клиническом опыте членов рабочей группы по разработке рекомендаций.
Экономический анализ:
анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Методы валидизации рекомендаций:
Внешняя экспертная оценка;
Внутренняя экспертная оценка.
Порядок обновления клинических рекомендаций – пересмотр 1 раз в 3 года.
Международная классификация болезней, травм и состояний, влияющих на здоровье, 10-го пересмотра (МКБ-10) (Всемирная организация здравоохранения) 1994.
Номенклатура медицинских услуг (Министерство здравоохранения и социального развития Российской Федерации) 2011.
Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации» от 21.11.2011 № 323 Ф3.
Перечень жизненно необходимых и важнейших лекарственных препаратов на 2016 г. (Распоряжение Правительства РФ от 26.12.2015 № 2724-р.)
Порядок оказания медицинской помощи по профилю «неонатология» (Приказ Минздрава России от 15 ноября 2012 г. N 921н).
Тактика ведения детей с ГБН в возрасте более 24 часов жизни:
зависит от абсолютных значений билирубина (табл. 1) или динамики этих показателей.
при появлении желтухи в течение первых 24 часов жизни – неотложное исследование ОБ, дальнейшая тактика ведения зависит от величины почасового прироста билирубина;
заказать необходимые препараты крови (плазма + эрмасса), стабилизировать жизненно важные функции организма.
источник
Гемолитическая болезнь новорождённых (ГБН) — патологическое состояние новорождённого, сопровождающееся массивным распадом эритроцитов, является одной из основных причин развития желтухи у новорождённых.
Гемолитическая болезнь новорожденных диагностируется у 0,6% новорожденных. Гемолитическая болезнь новорожденных проявляется в 3 основных формах: анемической, желтушной, отечной.
Гемолитическая болезнь новорожденных (morbus haemoliticus neonatorum) — гемолитическая анемия новорожденных, обусловленная несовместимостью крови матери и плода по резус- фактору, группе крови и другим факторам крови. Заболевание наблюдается у детей с момента рождения или выявляется в первые часы и дни жизни.
Гемолитическая болезнь новорожденных, или фетальный эритробластоз, является одним из тяжелых заболеваний детей периода новорожденности. Возникая в антенатальный период, это заболевание может быть одной из причин спонтанных абортов и мертворождений. По данным ВОЗ (1970), гемолитическая болезнь новорожденных диагностируется у 0,5% новорожденных, смертность от нее составляет 0,3 на 1000 детей, родившихся живыми.
Причина гемолитической болезни новорожденных стала известна только в конце 40-х годов XX в. в связи с развитием учения о резус-факторе. Этот фактор был открыт Landsteiner и Wiener в 1940 г. у обезьян Macacus rhesus. В дальнейшем эти же исследователи установили, что резус- фактор присутствует в эритроцитах 85% людей.
Дальнейшие исследования показали, что гемолитическая болезнь новорожденных может быть обусловлена несовместимостью крови матери и плода как по резус-фактору, так и по группе крови. В редких случаях заболевание возникает в результате несовместимости крови матери и плода по другим факторам крови (М, N, М5, N3, Rell, Kidd, Luis и др.).
Резус-фактор находится в строме эритроцитов. Он не имеет связи с полом, возрастом и принадлежностью к системам АВО и MN. Имеется шесть основных антигенов системы резус, передаваемых по наследству тремя парами генов и обозначаемых либо С, с, D, d, Е, е (по Фишеру), либо rh’, hr’, Rh, hr, rh», hr» (по Виннеру). В возникновении гемолитической болезни новорожденных наиболее важное значение имеет D- антиген, отсутствующий у матери и присутствующий у плода в результате наследования его от отца.
Гемолитическая болезнь новорожденных, обусловленная несовместимостью по системе АВО, чаще встречается у детей с группами крови А(II) или В (III). У матерей этих детей имеется 0(I) группа крови, в которой содержатся агглютинины α иβ. Последние могут блокировать эритроциты плода.
Установлено, что матери, дети которых родились с проявлениями гемолитической болезни, в большинстве случаев еще до наступления данной беременности были сенсибилизированы к эритроцитарным антигенам этого плода за счет предшествующих гемотрансфузий, а также беременностей резус-поло- жительным плодом.
В настоящее время известно три вида резус-антител, образующихся в сенсибилизированном организме людей с резус- отрицательной кровью: 1) полные антитела, или агглютинины, 2) неполные, или блокирующие, 3) скрытые.
Полные антитела — это антитела, способные путем обычного контакта вызывать агглютинацию эритроцитов, специфичных для данной сыворотки; эта реакция не зависит от солевого или коллоидного состояния среды. Неполные антитела могут вызывать агглютинацию эритроцитов лишь в среде, содержащей высокомолекулярные субстанции (сыворотка, альбумин, желатин). Скрытые резус-антитела находятся в сыворотке человека с резус-отрицательной кровью в очень высокой концентрации.
В возникновении гемолитической болезни новорожденных наиболее важная роль принадлежит неполным резус-антителам, способным легко проникать через плаценту в организм плода в связи с небольшим размером молекулы.
Нормальное течение беременности предусматривает синтез женщиной антител к поступающим к ней генетически чужеродным антигенам плода отцовского происхождения. Установлено, что в плаценте и околоплодных водах материнские антитела связываются антигенами плода. При предшествующей сенсибилизации, при патологическом течении беременности барьерные функции плаценты снижаются, и материнские антитела могут поступить к плоду. Наиболее интенсивно это происходит во время родов. Поэтому гемолитическая болезнь новорожденных, как правило, начинается после рождения.
В патогенезе гемолитической болезни основное значение имеет возникновение гемолиза эритроцитов у плода или новорожденного ребенка за счет повреждения мембраны клеток красного ряда материнскими антителами. Это приводит к преждевременному внесосудистому гемолизу. При распаде гемоглобина образуется билирубин (из каждого грамма гемоглобина образуется 35 мг билирубина).
Интенсивный гемолиз эритроцитов и ферментативная незрелость печени плода и новорожденного ребенка приводят к накоплению в крови свободного (непрямого) билирубина, который обладает токсическими свойствами. Он нерастворим в воде, не выводится с мочой, зато легко проникает в ткани, богатые липидами: головной мозг, надпочечники, печень, нарушая процессы клеточного дыхания, окислительного фосфорилирования и транспорта некоторых электролитов.
Тяжелым осложнением гемолитической болезни является ядерная желтуха (kernicterus), обусловленная токсическим действием непрямого билирубина на ядра основания мозга (субталамические, гипокампа, стриарного тела, мозжечка, черепных нервов). Возникновению этого осложнения способствуют недоношенность, ацидоз, гипоальбуминемия, инфекционные заболевания, а также высокий уровень непрямого билирубина в крови (более 342 мкмоль/л). Известно, что при уровне билирубина в сыворотке крови 342-428 мкмоль/л ядерная желтуха возникает у 30% детей.
В патогенезе гемолитической болезни новорожденных определенную роль играет нарушение функции печени, легких, сердечно-сосудистой системы.
Клинически различают три формы гемолитической болезни новорожденных: отечную, желтушную и анемичную.
Отечная форма является наиболее тяжелой. Для нее хахарактерны выраженные отеки с накоплением жидкости в полостях (плевральной, брюшной), бледность кожных покровов и слизистых оболочек, значительное увеличение размеров печени и селезенки. У некоторых новорожденных наблюдаются небольшие кровоподтеки и петехии.
Большие изменения наблюдаются в составе периферической крови. У таких больных количество гемоглобина снижено до 30-60 г/л, число эритроцитов часто не превышает 1×10 12 /л, выражены анизоцитоз, пойкилоцитоз, полихромазия, нормо- и эритробластоз; общее число лейкоцитов увеличено, отмечается нейтрофилез с резким сдвигом влево. Анемия у таких детей бывает настолько выраженной, что в сочетании с гипопротеинемией и повреждением стенки капилляров приводит к развитию сердечной недостаточности, которая и считается основной причиной смерти до рождения ребенка или вскоре после него.
Желтушная форма является самой частой клинической формой гемолитической болезни новорожденных. Первым симптомом заболевания является желтуха, возникающая на 1-2-й день жизни. Интенсивность и оттенок желтухи постепенно меняются: вначале апельсиновый, потом бронзовый, затем лимонный и, наконец, цвет незрелого лимона. Отмечается желтушное прокрашивание слизистых оболочек, склер. Увеличиваются размеры печени и селезенки. Внизу живота наблюдается пастозность тканей. Дети становятся вялыми, адинамичными, плохо сосут, у них снижаются рефлексы новорожденных.
При исследовании периферической крови выявляются анемия разной степени выраженности, псевдолейкоцитоз, который возникает за счет увеличения молодых ядросодержащих клеток красного ряда, воспринимающихся в камере Горяева как лейкоциты. Значительно увеличивается количество рети- кулоцитов.
Для желтушной формы гемолитической болезни новорожденных характерным является повышение уровня непрямого билирубина в крови. Уже в пуповинной крови его уровень может быть выше 60 мкмоль/л, а в дальнейшем он достигает 265-342 мкмоль/л и более. Четкой связи между степенью желтушности кожи, тяжестью анемии и выраженностью гипер- билирубинемии обычно не бывает, но считается, что желтуш- ность ладоней свидетельствует об уровне билирубина 257 мкмоль/л и выше.
Тяжелыми осложнениями желтушной формы гемолитической болезни новорожденных являются поражение нервной системы и развитие ядерной желтухи. При возникновении этих осложнений у ребенка вначале появляются нарастающая вялость, снижение мышечного тонуса, отсутствие или угнетение рефлекса Моро, срыгивания, рвота, патологическое зевание. Затем появляются классические признаки ядерной желтухи: мышечная гипертония, ригидность затылочных мышц, вынужденное положение тела с опистотонусом, негнущимися конечностями, сжатыми в кулак кистями, резкий «мозговой» крик, гиперстезия, выбухание родничка, подергивание мышц лица, судороги, симптом «заходящего солнца», нистагм, симптом Грефе; периодически возникает апноэ.
Другим сравнительно частым осложнением является синдром сгущения желчи. Его признаками являются обесцвеченный стул, насыщенный цвет мочи, увеличение печени. При исследовании крови обнаруживают повышение уровня прямого билирубина.
Анемическая форма наблюдается у 10-15% больных гемолитической болезнью новорожденных. Ранними и постоянными симптомами ее следует считать общую выраженную вялость и бледность кожных покровов и слизистых оболочек. Бледность отчетливо выявляется к 5-8-му дню после рождения, так как в первое время она маскируется небольшой желтухой. Наблюдается увеличение размеров печени и селезенки.
В периферической крови при этой форме содержание гемоглобина снижено до 60-100 г/л, количество эритроцитов находится в пределах 2,5×10 12 /л-3,5×10 12 /л, наблюдается нормобластоз, ретикулоцитоз. Уровень билирубина нормальный или умеренно повышенный.
Диагноз гемолитической болезни новорожденных основывается на данных анамнеза (сенсибилизация матери за счет предшествующих гемотрансфузий; рождение детей в данной семье с желтухой, смерть их в периоде новорожденности; указания матери на бывшие у нее ранее поздние выкидыши, мертворождения), на оценке клинических симптомов и на данных лабораторных исследований. Последние в диагностике заболевания имеют ведущее значение.
В первую очередь проводится определение группы крови и резус-принадлежности матери и ребенка, исследуется содержание ретикулоцитов в периферической крови и уровень билирубина в венозной крови у ребенка.
При резус-несовместимости определяют титр резус-анти- тел в крови и молоке матери, проводят прямую пробу Кумбса с эритроцитами крови ребенка и непрямую с сывороткой крови матери. При несовместимости по системе АВО в крови и молоке матери определяют титр а- или р-агглютининов в солевой и белковой средах. Иммунные антитела в белковой среде имеют титр в четыре раза выше, чем в солевой. Эти антитела относятся к иммуноглобулинам класса G и проникают через плаценту, вызывая развитие гемолитической болезни новорожденных. Прямая реакция Кумбса при АВО-несовместимости, как правило, отрицательная.
Если клинико-лабораторные данные четко указывают на гемолиз, а кровь матери и ребенка совместимы по резус-фактору и системе АВО, то целесообразно поставить реакцию Кумбса, провести пробу на индивидуальную совместимость крови матери и эритроцитов ребенка, искать антитела к антигенам, редко вызывающим гемолитическую болезнь новорожденных: с, d, е, Kell, Diffy, Kidd.
Для антенатальной диагностики прогностическое значение имеет определение билирубина в околоплодных водах при сроках беременности 32-38 нед: при оптической спектрофотометрической плотности околоплодных вод (при фильтре 450 нм) 0,15-0,22 ед. развивается легкая форма гемолитической болезни новорожденных, выше 0,35 ед. — тяжелая форма. Отечную форму гемолитической болезни новорожденных в антенатальном периоде можно диагностировать с помощью ультразвукового исследования.
Выявлению сенсибилизированных к резус-антигенам женщин способствует определение титра резус-антител в крови беременных. Однако не всегда степень повышения титра резус-антител в крови беременной соответствует тяжести гемолитической болезни. Прогностически неблагоприятным считают скачущий титр резус-антител беременной женщины.
Гемолитическую болезнь новорожденных приходится дифференцировать с рядом заболеваний и физиологических состояний. В первую очередь нужно установить гемолитический характер заболевания и исключить гипербилирубинемию печеночного и механического происхождения.
Среди причин, вызывающих появление желтух второй группы у новорожденных детей, наибольшее значение имеют врожденные заболевания инфекционной природы: вирусный гепатит, сифилис, туберкулез, листериоз, токсоплазмоз, цито- мегаловирусная инфекция, а также сепсис, приобретенный не только внутриутробно, но и после рождения.
Общими признаками желтух этой группы являются следующие: отсутствие признаков гемолиза (анемии, признаков раздражения красного ряда кроветворения, повышения уровня непрямого билирубина, увеличения селезенки) и повышение уровня прямого билирубина.
Следует также помнить, что у новорожденных детей может наблюдаться механическая желтуха, которая появляется, как правило, в связи с аномалией развития желчных путей — агенезией, атрезией, стенозом и кистами внутрипеченочных желчных протоков. В этих случаях желтуха появляется обычно к концу 1-й недели, хотя может появиться и в первые дни жизни. Она прогрессивно усиливается, и кожа приобретает темно-зеленый, а в некоторых случаях и коричневатый оттенок. Кал может быть слабо окрашенным. При аномалиях развития желчных путей количество билирубина в сыворотке крови очень высокое, может достичь 510-680 мкмоль/л за счет повышения прямого билирубина. В тяжелых и далеко зашедших случаях может увеличиться и непрямой билирубин вследствие невозможности конъюгации его за счет переполнения клеток печени билирубином желчи. Моча темная и окрашивает пеленки в желтый цвет. Количество холестерина и щелочной фосфатазы обычно повышено. Печень и селезенка увеличены и с усилением желтухи уплотняются. Постепенно у детей развивается дистрофия, появляются признаки гиповитаминоза К, Д и А. Развивается билиарный цирроз печени, от которого дети умирают, не достигнув возраста 1 года.
При высоком уровне непрямого билирубина в крови и при отсутствии других признаков повышенного гемолиза эритроцитов возникает подозрение на конъюгационный характер желтухи. В таких случаях целесообразно в сыворотке крови ребенка исследовать активность лактатдегидрогеназы и ее первой фракции — гидроксибутиратдегидрогеназы. При гемолитической болезни новорожденных уровень этих ферментов резко повышен, а при конъюгационной желтухе соответствует возрастной норме.
Нельзя забывать о существовании достаточно редкого заболевания, известного как синдром Криглер — Найяра (Krigler и Najar). Это негемолитическая гипербилирубине- мия, сопровождаемая развитием ядерной желтухи. Заболевание наследуется по аутосомно-рецессивному типу. Мальчики болеют чаще девочек.
В основе синдрома Криглер — Найяра лежит резкое нарушение образования билирубиндиглюкоронида (прямого билирубина) вследствие полного отсутствия УДФ-глюкоронил- трансферазы, конъюгирующей билирубин. Основной симптом заболевания — желтуха, которая появляется в первые сутки после рождения и интенсивно нарастает, удерживаясь на протяжении жизни ребенка. Желтуха связана с резким повышением в крови непрямого билирубина, количество которого очень быстро достигает 340-850 мкмоль/л. На фоне резкого повышения в крови непрямого билирубина развиваются симптомы ядерной желтухи. Анемии не наблюдается. Количество молодых форм эритроцитов не повышено. Количество уробилина в моче в пределах нормы. Желчь лишена прямого, конъюгированного билирубина. Поражение центральной нервной системы приводит к гибели ребенка в первые месяцы жизни. Дети редко доживают до 3 лет.
Наследственные гемолитические анемии диагностируются на основании (специфических морфологических признаков эритроцитов, измерения их диаметра, осмотической стойкости, исследования активности ферментов эритроцитов (прежде всего глюкозо-6-фосфатдегидрогеназы и др.), типов гемоглобина.
Лечение гемолитической болезни новорожденных с высоким уровнем непрямого билирубина может быть консервативным или оперативным (операция заменного переливания крови).
Для новорожденных с гемолитической болезнью очень важно достаточное питание.
Консервативное лечение гемолитической болезни новорожденных включает следующие мероприятия:
- мероприятия, направленные на уменьшение гемолиза за счет стабилизации мембраны эритроцитов (внутривенные вливания 5% раствора глюкозы, назначение АТФ, эревита);
- терапию, способствующую ускорению метаболизма и экскреции билирубина из организма (прием фенобарбитала из расчета до 10 мг/кг в сутки, разделенный на три приема, внутрь);
- назначение веществ, адсорбирующих билирубин в кишечнике и ускоряющих его экскрецию с фекалиями (агар- агар по 0,1 г три раза в день внутрь; 12,5% раствор ксилита или сульфата магния внутрь по 1 чайной ложке три раза в день или аллохол по ‘/2 измельченного драже также три раза в день внутрь);
- использование средств и мероприятий по уменьшению токсичности непрямого билирубина (фототерапия); в последнее время появились сообщения об эффективности в борьбе с токсическим действием непрямого билирубина малых доз ультрафиолетового облучения.
Полезно проводить инфузионную терапию. Объем инфузионной терапии следующий: в первые сутки — 50 мл/кг и далее добавляют по 20 мл/кг в сутки, доведя до 150 мл/кг к 7-му дню.
Состав инфузионного раствора: 5% раствор глюкозы с добавлением на каждые 100 мл 1 мл 10% раствора кальция, со второго дня жизни-1 ммоль натрия и хлора, с третьих суток — 1 ммоль калия. Скорость вливания — 3-5 капель в 1 мин. Добавление 5% раствора альбумина показано лишь детям с инфекционными заболеваниями, недоношенным, при выявлении гипопротеинемии (ниже 50 г/л). Вливания гемодез и реополиглюкина при гемолитической болезни новорожденных не показаны.
Заменное переливание крови проводится по определенным показаниям. Абсолютным показанием к заменному переливанию крови является гипербилирубинемия выше 342 мкмоль/л, а также темп нарастания билирубина выше 6 мкмоль/л в 1 час, уровень его в пуповинной крови выше 60 мкмоль/л.
Показаниями к заменному переливанию крови в первые сутки жизни являются анемия (гемоглобин менее 150 г/л), нормобластоз и доказанная несовместимость крови матери и ребенка по группе или резус-фактору.
При резус-конфликте для заменного переливания крови используют кровь той же группы, что и у ребенка, резус-отрица- тельную не более 2-3 дней консервации, в количестве 150- 180 мл/кг (при уровне непрямого билирубина более 400 мкмоль/л — в объеме 250-300 мл/кг). При АВО-конфликте переливают кровь группы 0(I) с низким титром а- и ß-агглютининов, но в количестве 250-400 мл; при этом, как правило, на следующий день надо сделать повторную заменную трансфузию в том же объеме. Если у ребенка имеется одновременно несовместимость по ресуз- и АВО-антигенам, то ребенку надо переливать кровь 0(I) группы.
При проведении заменного переливания крови катетер в пупочную вену вводят на длину не более чем 7 см. Кровь должна быть подогрета до температуры не менее 28° С. Содержимое желудка до операции отсасывают. Начинают процедуру с выведения 40-50 мл крови ребенка, количество введенной крови должно быть на 50 мл больше выведенной. Операция проводится медленно (3-4 мл в 1 мин), чередуется выведение и введение по 20 мл крови. Продолжительность всей операции не менее 2 ч. Следует помнить, что на каждые 100 мл введенной крови надо ввести 1 мл 10% раствора глюконата кальция. Это делается для предупреждения цитратного шока. Через 1-3 ч после заменного переливания крови следует определить уровень глюкозы в крови.
К осложнениям заменного переливания крови относятся: острая сердечная недостаточность при быстром введении больших количеств крови, нарушения ритма сердечной деятельности, трансфузионные осложнения при неправильном подборе донора, электролитные и обменные расстройства (гиперкалиемия, гипокальциемия, ацидоз, гипогликемия), геморрагический синдром, тромбозы и эмболии, инфекционные осложнения (гепатит и др.), некротический энтероколит.
После заменного переливания крови назначают консервативную терапию. Показанием к повторному заменному переливанию крови служит темп прироста непрямого билирубина (заменное переливание крови показано при темпе прироста билирубина более 6 мкмоль/л в 1 ч).
Для проведения заменного переливания крови необходимо иметь следующий набор инструментов: стерильные полиэтиленовые катетеры № 8, 10, пуговчатый зонд, ножницы, два хирургических пинцета, иглодержатель, шелк, четыре-шесть шприцев вместимостью 20 мл и два-три шприца вместимостью 5 мл, два стакана по 100-200 мл.
Техника катетеризации пупочной вены заключается в следующем: после обработки операционного поля конец пуповинного остатка срезают поперек на расстоянии 3 см от пупочного кольца; осторожными вращательными движениями вводят катетер, направляя его после прохождения пупочного кольца вверх вдоль брюшной стенки, по направлению к печени. Если катетер введен правильно, то через него выделяется кровь.
Основные принципы профилактики гемолитической болезни новорожденных заключаются в следующем. Во-первых, учитывая большое значение предшествующей сенсибилизации в патогенезе гемолитической болезни новорожденных, к каждой девочке следует относиться как к будущей матери, в связи с чем проводить гемотрансфузии девочкам нужно только по жизненным показаниям. Во-вторых, важное место в профилактике гемолитической болезни новорожденных отводится работе по разъяснению женщинам вреда аборта. Для предупреждения рождения ребенка с гемолитической болезнью новорожденных всем женщинам, имеющим резус-отрицательный фактор крови, в первый день после аборта (или после родов) рекомендуется введение анти-О-глобулина в количестве 250-300 мкг, который способствует быстрой элиминации эритроцитов ребенка из крови матери, предотвращая синтез резус-антител матерью. В-третьих, беременных с высоким титром антирезус-антител госпитализируют на 12-14 дней в дородовые отделения в сроки 8, 16, 24, 32 нед, где им проводят неспецифическое лечение: внутривенные вливания глюкозы с аскорбиновой кислотой, кокарбоксилазой, назначают рутин, витамин Е, глюконат кальция, кислородную терапию; при развитии угрозы прерывания беременности назначают прогестерон, эндоназальный электрофорез витаминов В1, С. За 7-10 дней до родов показано назначение фенобарбитала по 100 мг три раза в день. В-четвертых, при нарастании у беременной женщины титров антирезус-антител родоразрешение проводится досрочно на 37-39-й неделе путем операции кесарева сечения.
Гемолитическая болезнь новорожденных: последствия могут быть опасными, вплоть до смерти ребёнка, могут нарушиться функции печени и почек у ребёнка. Начинать лечение надо сразу.
Прогноз гемолитической болезни новорожденных зависит от формы заболевания и адекватности проводимых профилактических и лечебных мероприятий. Больные отечной формой нежизнеспособны. Прогноз при желтушной форме благоприятен при условии проведения адекватного лечения; прогностически неблагоприятно развитие билирубиновой энцефалопатии и ядерной желтухи, поскольку в группе таких больных очень высок процент инвалидности. Анемическая форма гемолитической болезни новорожденных прогностически благоприятна; у больных этой формой наблюдается самоизлечение.
Современный уровень развития медицины, правильная диагностическая и лечебная тактика позволяют избежать выраженных последствий гемолитической болезни новорожденных.
источник

Чтобы предупредить развитие тяжелых осложнений, все беременные в обязательном порядке должны наблюдаться у врача. Повышенное внимание уделяется женщинам с Rh- кровью, 1-ой группой крови и ГБH в прошлых родах.
Для возникновения конфликта несовместимости, необходимо присутствие в материнской крови высоко специфичных антител, работающих против отсутствующих у нее эритроцитарных Д-антигенов (Rh-фактора). Несочетаемость по резусной системе развивается у трети пациентов с ГБН и носит название Rh-эритробластоза.
Гемолитическая болезнь возникает также из-за несочетаемости материнской и плодной крови по АBO системе. Конфликтность по антителам к группам крови носит название АBO-эритробластоза и встречается у двух третей пациентов.
Для того, чтобы возникла гемолитическая болезнь, материнская кровь должна быть резусно-отрицательной, а отцовская, иметь резус+.
Rh+ мужчина может иметь гомозиготный (ДД) или гетерозиготный (Дд) набор генов резус системы.
У гомозиготного мужчины, все дети будут иметь + резус (стопроцентная наследуемость Д-антигена).
У гетерозиготного мужчины – семьдесят пять процентов детей будут резус + и двадцать пять процентов —.
По наличию Rh-фактора, всех пациентов разделяют на резус + и -.
Rh или Д-антиген является липопротеином со сложной структурой антигенов. Он располагается только на внутренней поверхности эритроцитарной мембраны. Присутствие Д-антигенов на эритроцитарных мембранах свидетельствует о том, что кровь пациента резус +. У резус отрицательных людей, Д-антигена нет.
Д-антиген могут содержать только эритроцитарные мембраны, в других клетках и тканях организма его быть не может. Также, у человека не существует собственных, естественных антител к резусу -антигену.
Процессы дифференцировки Д-антигена начинаются у плода на пятой неделе развития. Максимальная активность резус фактора наблюдается к пятому-шестому месяцу. Иммунизация резусно-отрицательной крови матери (образование анти-О-антител) происходит при попадании в Rh- кровь Rh+ эритроцитов.
Однако, для образования иммунного ответа необходимо несколько антигенных стимулов. То есть, изоиммунизация (образование анти-О-антител) при первой беременности возможна только в 2% случаев.
Как правило, после рождения от резуса – матери резус + ребенка, организм матери первично сенсибилизируется. Это происходит в результате процесса микро-трансфузии в отрицательную кровь матери, положительных эритроцитов ребенка.
Усиливают микро-трансфузию аборты, отслойка плаценты, гестозы беременности, воспалительные болезни, сопровождающиеся нарушением плацентарной проницаемости и т.д. Все эти факторы усиливают проникновение в материнскую кровь Rh+ эритроцитов и увеличивают образование направленных против них анти-О-антител.
Поражение плода развивается при проникновении в кровь плода достаточного количества анти-О-антител, вызывающих гемолиз (разрушение) эритроцитов .
Каждая следующая беременность, усиливает материнскую специфическую иммунную реакцию и усиливает риск появления гемолитической болезни новорожденного по Rh.
При 1-ой беременности резусный конфликт возможен, если женщина уже иммунизирована в результате переливания ей резус- или АВО-несовместимой крови.
Гемолитическая болезнь новорожденных является результатом иммуноагрессивной реакции организма матери на собственный плод.
После повреждения эритроцитов антителами, они распадаются в печени и селезенке.
Первичный гемолиз является внесосудистым. Вследствие этого процесса, гемоглобин из распавшихся эритроцитов не поступает в кровоток, а трансформируется тканевыми макрофагами в желчный пигмент – билирубин.
Риск развития несочетаемости по Rh возрастает с каждой следующей беременностью.
Возникновению ГБН способствует наличие у женщины:
- одного или нескольких абортов;
- самопроизвольных прерываний (выкидышей);
- беременности и родов Rh+ плодом;
- переливаний крови;
- отслойки плаценты, гестозов и тяжелых инфекционно-воспалительных патологий в анамнезе матери;
- инфицировании околоплодных вод;
- трансплантаций органов и тканей;
- ГБН во время предыдущих родов.
Для развития групповой несочетаемости, у матери должна быть группа 0 (1-я группа крови), а у малыша вторая (A) или третья (B) группа.
Наиболее часто несовместимость возникает у матерей с первой (0) и плодом с второй (A) группой. Антиген B и в-агглютинины третьей группы обладают значительно меньшей антигенной активностью, чем антиген A и а-агглютинины.
источник