Нормальный качественный и количественный состав крови человека – это важное условия здорового функционирования всех органов и систем. Под воздействием различных провоцирующих факторов возникает заболевание, сопровождающееся уменьшением в крови эритроцитов и гемоглобина. Лечение анемии должно проводиться своевременно, иначе существует риск развития тяжелых осложнений для больного.
Анемия или малокровие – это патологическое состояние, вследствие которого снижается количество гемоглобина и число эритроцитов на единицу объема крови.
Эритроциты, или красные кровяные тела, выполняют чрезвычайно важную функцию для организма. Благодаря им, осуществляется транспортировка кислорода, углекислого газа, белков, углеводов и некоторых других веществ. Кроме этого, эритроциты выполняют защитную роль, так как способны связывать и выводить из организма некоторые токсины, также участвуют в процессе свертывания крови.
В союзе с гемоглобином красные кровяные тела выполняют регуляторную функцию, поддерживая рН крови. Гемоглобин при этом связывает молекулы углекислого газа, уменьшая концентрацию Н2С03.
Классифицируется болезнь по нескольким признакам. К ним относят механизм развития, тяжесть течения, цветной показатель, способность костного мозга к восстановлению, морфологические особенности.
Патогенез заболевания имеет разный характер. Развивается патология из-за больших кровопотерь, что обусловлено серьезными травмами, переломами, массивными внутренними кровотечениями. Еще одна причина болезни – недостаточный синтез красных кровяных телец вследствие врожденных или приобретенных заболеваний. Катализатором патологии выступает также выраженное разрушение телец под воздействием каких-либо факторов.
Классификация анемии по тяжести протекания включает 3 стадии. Каждая из них характеризуется определенными показателями. Например, легкое течение – это снижение гемоглобина до 90 г/л, средняя тяжесть – до 70 г/л, тяжелое течение – ниже 70 /л.
Эритроциты при различных типах заболевания могут иметь неодинаковый размер. У здорового человека диаметр их должен составлять от 7 до 8 микрометров (мкм). Виды анемии по морфологическому признаку можно увидеть на картинке.
Первые 3 варианта встречаются наиболее часто из всех случаев заболевания. Мегалоцитарное считается редким видом.
Цветным показателем называют степень насыщенности красных кровяных телец гемоглобином. Рассчитывается он по специальной медицинской формуле. В зависимости от этого различают гипохромное (коэффициент окраски меньше 0,8), нормохромное (0,8 – 1,05) и гиперхромное малокровие (цветовой показатель – 1,05).
Выработка эритроцитов происходит в костном мозге. О его способности к регенерации свидетельствуют такие вещества в крови, как ретикулоциты. По их количеству можно определить, насколько интенсивно проходит процесс образования новых кровяных телец. В медицинской практике различают регенераторный, гипорегенераторный, гиперрегенераторный и апластический вид анемии у взрослых и детей.
Болезнь анемия может быть вызвана самыми разнообразными причинами. Патология бывает врожденной и приобретенной. К основным провоцирующим факторам относят потерю крови, нарушение производства эритроцитов или процессы, ведущие к разрушению красных кровяных телец. Рассмотрим каждую из причин более подробно.
Диагноз анемия часто ставят пациентам, потерявшим большое количество крови. При этом кровотечение может носить длительный хронический или кратковременный интенсивный характер. Спровоцировать это могут такие состояния у больного:
- язвенная болезнь желудка и кишечника;
- геморрой;
- гастрит;
- длительный прием препаратов, разжижающих кровь (на этом фоне могут возникать кровотечения);
- онкологические новообразования;
- перенесение хирургического вмешательства;
- переломы и травмы мягких тканей, например, в результате аварии;
- регулярный забор крови с целью донорской помощи.
У женщин часто диагностируется послеродовая анемия, так как при рождении ребенка случаются массивные кровопотери. Иногда дефицит гемоглобина развивается на фоне обильных менструаций.
У здорового человека жизненный цикл эритроцитов составляет от 110 до 120 суток. После этого клетка разрушается, заменяется новой. Различные патологии негативно влияют на этот процесс, выводят красное кровяное тело из строя раньше срока. Костный мозг не успевает синтезировать новые эритроциты, что и влечет за собой развитие малокровия.
Выясним, от чего бывает этот вид заболевания:
- ответ иммунной системы на раздражители;
- прием некоторых медикаментозных средств;
- негативное воздействие токсических веществ на организм;
- гемодиализ почек;
- при серповидно-клеточном виде малокровия эритроциты имеют неправильную форму, их жизненный цикл сокращен. Это мешает нормальному обмену веществ в организме, ведет к негативным симптомам анемии.
Увеличение селезенки – еще одна распространенная причина снижения количества красных кровяных телец в крови. Такое состояние органа часто наблюдается у людей с хроническими заболеваниями, опухолями, при тяжелых инфекционных поражениях. Нередко таким пациентам проводят спленэктомию (операцию по удалению селезенки).
При нарушении выработки костным мозгом красных кровяных телец развивается тяжелая анемия, сопровождающаяся ухудшением функционирования всех органов и систем.
Это состояние может быть вызвано такими провоцирующими факторами:
- снижение количества или полное отсутствие стволовых клеток. Это заболевание чаще носит врожденный характер, требует трансплантации костного мозга, переливания крови. Это так называемая аутоиммунная анемия. Иногда нарушение функции костного мозга возникает под действием некоторых лекарств, травм, химиотерапии и прочих факторов;
- сбой гормонального баланса организма. При недостаточной выработке гормона эритропоэтина стимуляция костного мозга становится невозможной, так как именно этот гормон предназначен для выполнения данной функции. В результате красные кровяные тела образовываются в недостаточном количестве;
- первый и второй триместр вынашивания ребенка. Во время беременности у женщины количество плазмы увеличивается быстрее, чем самих красных кровяных телец. Следствием такого процесса является развитие малокровия, влекущее за собой уменьшение концентрации железа и фолиевой кислоты.
Нередко нарушения в составе крови проявляются вследствие длительного соблюдения диеты с целью похудения. Из-за недостатка в пище железа возникает железодефицитный вид болезни.
Рассмотрим, как проявляется анемия. Признаки заболевания всегда зависят от его вида и стадии. Существует несколько разновидностей болезни.
Считается, что этот вид спровоцирован недостатком в организме витамина В12 и фолиевой кислоты. В12-дефицитная анемия возникает чаще из-за дефицита этого витамина или повышенной потребности организма в нем, например, в период быстрого роста, при интенсивных физических нагрузках, во время вынашивания 2 и более детей. Кроме этого, болезнь встречается у людей при циррозе печени, раке желудка, гастрите.
Симптомы анемии этого типа:
- быстрая утомляемость;
- приступы головокружения и головной боли;
- желтушность кожи;
- мушки перед глазами;
- онемение пальцев рук и ног;
- отдышка;
- скачки артериального давления, тахикардия.
Со стороны желудочно-кишечного тракта В12-дефицитная анемия может проявляться в виде покраснения и жжения языка, образования язвочек на слизистой оболочке рта, потери аппетита. Пациент теряет вес, после еды появляется чувство дискомфорта и тяжести, развиваются запоры.
К невралгическим признакам относят судороги, дрожь в конечностях, мышечную слабость, покалывание в области пальцев рук и ног.
Гипохромная или железодефицитная анемия (ЖДА) сопровождается снижением количества в крови гемоглобина, железа. Цветовой показатель у таких больных ниже нормы.
К причинам следует отнести нарушение обмена веществ, недостаточное всасывание железа. Часто возникает эта анемия после родов, в период грудного вскармливания. Риску заболевания подвержены люди с хроническими болезнями легких, пороками сердца. Дефицит железа наблюдается у пациентов с тяжелыми патологиями, сопровождающимися нагноением тканей, сепсисом.
Частый провоцирующий фактор нехватки железа – внутренние кровотечения. Они могут быть обусловлены травмами и заболеваниями внутренних органов, часто встречается такая анемия после операции.
- общее нарушение самочувствия;
- снижение памяти и концентрации внимания;
- частые головные боли, приступы головокружения;
- сбои сердечного ритма.
Среди внешних признаков выделяют ломкость и тусклость волос, образование белых пятен на ногтевых пластинах, бледность и шелушение дермы, хейлиты в уголках рта. Больной может жаловаться на изменение вкусовых предпочтений, развитие судорог при движении ногами.
Данный вид заболевания является следствием нехватки фолиевой кислоты. Это вещество синтезируется в кишечнике, но достаточное его количество должно поступать с пищей. При нарушении этого баланса развивается малокровие.
Спровоцировать болезнь могут такие факторы, как недостаточное употребление пищи, богатой витамином В9, патологии печени, органов пищеварительной системы, онкологические образования (злокачественная анемия).
Клиническая картина у пациента:
- разбитость;
- мышечная слабость;
- бледность дермы;
- учащенное сердцебиение;
- утрата трудоспособности.
Эта патология возникает при нарушении кроветворной функции, сопровождается угнетением или полным прекращением образования и роста клеточных линий в костном мозге. Данное отклонение возникает под воздействием генетических причин, на фоне приема некоторых медикаментов, при наличии вирусных поражений (ВИЧ, парвовирусная инфекция).
- бледный оттенок кожи;
- частые головные боли;
- нарушение сердечного ритма и отдышка;
- анемия ног (нарушение чувствительности, покалывание в конечностях);
- кровоточивость десен;
- частые бактериальные и вирусные заболевания;
- гематомы и мелкие высыпания на теле;
- образование афт и язв на слизистой оболочке рта.
При поражении печени может появляться желтый оттенок дермы и глазных яблок. При обнаружении описанных симптомов следует обязательно пройти медицинское обследование, так как последствия дальнейшего развития патологии могут быть самыми негативными.
Этот вид заболевания часто встречается у пожилых людей и больных с генетическими нарушениями системы кроветворения. Гемолиз – это разрушение эритроцитов раньше времени. При этом костный мозг не справляется со своей функцией, вырабатывает недостаточное количество красных кровяных телец, что влечет за собой развитие малокровия.
Патология имеет врожденные или приобретенные причины. В первом случае речь идет о генетических нарушениях (энзимопатия, талассемия, наследственный сфероцитоз). К приобретенным относят инфекционные болезни, отравление ядами, токсинами, некоторыми препаратами.
- бледность дермы и слизистых оболочек;
- алопеция, хрупкость ногтей;
- температура при анемии (чаще в пределах 37–37,5 градусов);
- учащенное дыхание;
- язвы на нижних конечностях;
- желтушность кожи;
- нарушение стула, болевой синдром в области живота, беспричинная рвота.
Диагностика анемии требует полного медицинского обследования. При обращении пациента врач должен ознакомиться с историей болезни человека, собрать анамнез. При этом учитываются такие факторы, как вкусовые предпочтения больного, быстрая утомляемость, головные боли, цвет кожи, размер лимфатических узлов, оттенок слизистых оболочек, наличие патологий пищеварительной системы и другие.
Лабораторная диагностика анемий включает следующие анализы:
- общий анализ – позволяет оценить качественный и количественный состав всех кровяных клеток, скорость оседания эритроцитов (СОЭ) и другие показатели;
- биохимический анализ – проводится для выявления отклонений в работе всех органов и систем;
- исследование кала на скрытую кровь – помогает выяснить, есть ли у больного внутреннее кровотечение.
Для выяснения причин нарушения состава крови проводятся такие инструментальные методы, как пункция костного мозга, рентген легких, колоноскопия, УЗИ внутренних органов, магнитно-резонансная и компьютерная томография.
Тактика терапии малокровия подбирается в зависимости от типа болезни и ее первопричины. В таблице можно найти методы лечения того или иного типа болезни.
Препараты при анемии этого вида должны включать витамин В12 и ферменты. Кроме этого, человеку необходимо насыщать рацион продуктами питания, богатыми этим витамином
Устранение причины дефицита железа, прием железосодержащих лекарств и витамина С
Для снижения недостатка фолиевой кислоты больному рекомендуется кушать пищу, включающую это вещество
Данная патология требует применения таких радикальных методов, как переливание крови, пересадка костного мозга, прием иммуносупрессоров, стимуляторов костного мозга и прочих препаратов
Лечение здесь зависит от фактора, спровоцировавшего болезнь. Во время терапии усилия направлены на устранение основного заболевания и его симптомов
Прием любых таблеток в период лечения должен осуществляться под строгим контролем лечащего врача в четком соответствии с инструкциями.
Сбалансированное питание – важный аспект лечения состояний, сопровождающихся дефицитом железа и гемоглобина. Постараемся выяснить, что есть при анемии для улучшения состава крови.
- свиная, куриная, говяжья печень;
- говяжье, свиное сердце;
- мясо курицы, индейки, говядина;
- черная икра, мидии, устрицы, сардина;
- отрубной хлеб;
- гранат, морская капуста, свекла;
- гречневая и овсяная крупа;
- перепелиные яйца;
- курага, чернослив;
- лук, чеснок, свежая зелень.
Строгих ограничений для пациентов с малокровием нет, но все же рекомендуется отказаться от тортов, пирожных, конфет, жирных сортов мяса, рыбы. Исключить нужно острые соусы, майонез, приправы, специи, копченые, соленые блюда. Пищу лучше готовить методом варки, тушения, запекания. Овощи и фрукты употреблять с кожурой, особенно яблоки. Заменить сладости можно препаратом под названием гематоген. Средство предназначено для коррекции метаболических процессов организма, повышения железа и гемоглобина.
Что делать для профилактики анемии и как предотвратить заболевание? В связи с тем, что эта патология имеет множество причин, предотвратить ее можно, придерживаясь комплексных мероприятий. К ним относятся:
- регулярная сдача общего анализа крови;
- при появлении первых тревожных симптомов следует записаться на прием к врачу;
- сбалансированное питание, включающее все необходимые витамины и минералы;
- достаточная двигательная активность, занятия спортом. Это поможет держать обменные процессы на здоровом уровне;
- отказ от вредных привычек;
- людям с малоподвижным образом жизни и сидячей работой следует чаще гулять на свежем воздухе, заниматься фитнесом, бегом и другими видами спорта.
Профилактика анемии включает своевременное лечение обменных, вирусных, инфекционных заболеваний. Важно своевременно выявлять скрытые кровотечения, генетические патологии. Некоторые специалисты считают, что особую роль играет психосоматика. Человеку необходимо настроиться на положительный лад, научиться противостоять стрессам и адекватно реагировать на них. Эти и другие мероприятия помогут исключить многие болезни, включая малокровие.
источник
Комплексное исследование с учетом количественного и качественного состава клеток, а также биохимических показателей крови, которое позволяет выявить признаки железодефицитной анемии.
Результаты исследований выдаются с бесплатным комментарием врача.
Синонимы английские
Iron deficiency anemia screening.
Колориметрический фотометрический метод, проточная цитометрия, SLS(натрий лаурилсульфат)-метод, кондуктометрический метод, иммунотурбидиметрия.
Мкмоль/л (микромоль на литр), *10^9/л (10 в ст. 9/л), *10^12/л (10 в ст. 12/л), г/л (грамм на литр), % (процент), фл (фемтолитр), пг (пикограмм).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Исключить из рациона алкоголь за 24 часа до исследования.
- Не есть в течение 12 часов до исследования.
- Не принимать лекарственные препараты в течение 24 часов перед анализом (по согласованию с врачом).
- Исключить физическое и эмоциональное перенапряжение за 30 минут до исследования.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Анемия – патологическое состояние, характеризующееся снижением количества эритроцитов и/или гемоглобина в крови. Причины анемий разнообразны и могут быть тесно связаны с хроническими соматическими заболеваниями (с патологией почек и печени, аутоиммунными, инфекционными и воспалительными заболеваниями, сахарным диабетом, опухолями), с острой и хронической потерей крови, наследственными болезнями и неполноценным питанием, нехваткой витаминов и микроэлементов. Они возникают при недостаточном образовании эритроцитов в костном мозге (например, при дефиците железа, витаминов В12 и В6, истощении костного мозга) или преждевременном и чрезмерном разрушении эритроцитов в кровяном русле (например, при гемолизе).
Наиболее распространенная форма анемии – железодефицитная – выявляется у 80-90 % пациентов, у которых снижено количество эритроцитов и/или гемоглобина в крови.
Дефицит железа развивается постепенно. Вначале создается отрицательный баланс железа, при котором потребности организма в нем и его потери превышают объемы его поступления с пищей. Это может быть связано с кровопотерей, беременностью, кормлением грудью, скачками роста в период полового созревания, нарушением всасывания микроэлементов в желудочно-кишечном тракте или недостаточным употреблением продуктов, содержащих железо, как при вегетарианстве.
В норме железо всасывается в тонком кишечнике, но при некоторых хронических заболеваниях желудка и кишечника возникает синдром мальабсорбции с нарушением всасывания из пищи питательных веществ и микроэлементов. В крови железо переносится белком трансферрином к местам использования или накопления. При железодефиците количество свободного трансферрина в крови увеличивается, а уровень сывороточного железа уменьшается. Синтез гемоглобина в костном мозге происходит менее активно, и развивается железодефицитная анемия с клиническими проявлениями малокровия. В общем анализе крови обнаруживаются небольшие бледно окрашенные эритроциты, снижаются показатели МНС (среднее содержание гемоглобина в эритроците), MCV (средний объем эритроцита), МСНС (средняя концентрация гемоглобина в эритроците), падает уровень гемоглобина и гематокрит. Без лечения количество гемоглобина снижается все больше, изменяется форма красных кровяных телец, сокращается интенсивность деления клеток в костном мозге. В связи с уменьшением количества гемоглобина и эритроцитов нарушается транспорт кислорода и углекислоты в тканях, появляются симптомы анемии: бледность кожных покровов, головная боль, ухудшение памяти, сонливость, мушки перед глазами, головокружение, обмороки, учащенное сердцебиение, снижение артериального давления, боль в области сердца, мышечная слабость.
Кроме самочувствия, отрицательные изменения происходят во внешности: сухость кожи (как следствие, ранние морщины), ломкость ногтей, выпадение волос.
Дети, подверженные анемии, чаще здоровых сверстников страдают простудными заболеваниями.
Кроме того, при дефиците железа у больного может возникать нарушение вкуса и обоняния: появляется желание есть мел, глину, сырые крупы и вдыхать запахи ацетона, бензина, скипидара.
Часто люди не обращают внимания на главные признаки анемии – постоянную усталость, бледность, сухость кожи, – считая их недостаточным поводом для обращения к врачу. Конечно, такие симптомы действительно не всегда говорят о болезни, нельзя диагностировать ее только по их наличию. И тем более нельзя самостоятельно начинать прием железосодержащих препаратов – это может привести к тяжелым осложнениям.
Важно знать, чем именно вызвана анемия. Например, у пожилых людей к ней часто приводит внутреннее кровотечение из-за опухоли желудочно-кишечного тракта. Есть разновидность анемии, связанная с плохим усвоением витамина B12. Но чтобы ее выявить, для начала необходимо убедиться, что в организме достаточно железа и эритроциты насыщены им.
При этом просто сдать кровь на гемоглобин – недостаточно для полноценной диагностики анемии. Например, у курящих уровень гемоглобина и эритроцитов зачастую в норме: моноокись углерода, содержащаяся в сигаретах, соединяясь с гемоглобином, образует вещество карбоксигемоглобин, такая форма гемоглобина не обладает способностью переносить кислород, и для компенсации кислородного голодания уровень гемоглобина повышается. Получается, что необходим комплексный анализ, отражающий истинные запасы этого микроэлемента в организме: определение уровней сывороточного железа, трансферрина, ретикулоцитов, общий анализ крови, лейкоцитарная формула.
Кроме того, важно, что своевременная диагностика анемии позволяет выявить заболевания, первым симптомом которых она является: некоторые злокачественные опухоли, хронические воспалительные процессы, глистные инвазии и др.
Для чего используется исследование?
- Для диагностики железодефицитной анемии.
- Для дифференциальной диагностики анемии.
- Для обследования пациентов с высоким риском развития анемии.
- Чтобы оценить эффективность лечения железодефицитной анемии.
Когда назначается исследование?
- При симптомах недостаточности железа в организме (бледность и/или желтушность кожных покровов, общая слабость, утомляемость, сонливость, головокружение, шум в ушах, мелькание мушек перед глазами, обмороки, атрофия слизистой языка, изменение структуры ногтей, аномальные вкусовые предпочтения).
- При снижении количества эритроцитов и/или гемоглобина по данным клинического анализа крови.
- При наличии факторов риска развития анемии (беременность, кормление грудью, нарушения менструального цикла, недостаточное питание, вегетарианство, заболевания желудка и кишечника с нарушением всасывания питательных веществ, хронический стресс).
- При обследовании детей в период интенсивного роста.
- При обследовании пациентов с астенией неясного генеза и выраженной утомляемостью.
- При контроле за эффективностью применения препаратов, содержащих железо.
источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
В диагностике и лечении различных заболеваний крови специализируется врач-гематолог (записаться). Поэтому, теоретически, при анемии необходимо обращаться к врачу-гематологу, однако на практике это не совсем оправдано. Ведь часто анемия может быть вызвана заболеваниями, которые входят в компетенцию другого специалиста, и в таких случаях для успешной терапии анемии нужно одновременно принимать специфические гематологические препараты и лечить основную патологию, спровоцировавшую анемический синдром.
На практике представляется рациональным при анемии обращаться к врачу-терапевту (записаться), который назначит необходимые обследования, выявит возможную причину снижения уровня гемоглобина в крови и на основании этого предложит лечение. А если терапевт не сможет назначить лечение из-за нехватки специфических знаний, врач просто направит больного к гематологу.
Такое обращение к терапевту при анемии представляется оправданным – так как большинство анемий обусловлено дефицитом железа, фолиевой кислоты или витамина В12 или же хронической кровопотерей при заболеваниях пищеварительного тракта, с этими проблемами справится именно врач-терапевт, назначив и лечение основной патологии, и порекомендовав диету, и выписав препараты железа и необходимых витаминов. И только если анемия вызвана непосредственно патологией системы крови (например, апластические анемии), врач-терапевт направит пациента к гематологу, так как в подобной ситуации наблюдать и вести человека должен очень узкий специалист с весьма специфическими знаниями, каковым и является гематолог.
При сборе анамнеза врачу необходимо выяснить:
- место рождения и проживания пациента с анемией;
- увлечения и хобби (например, усиленные занятия спортом);
- чувствует ли больной повышенную утомляемость и слабость в повседневной жизни;
- пищевые предпочтения (необходимо выяснить, какие продукты пациент ест и которых избегает, а также оценить количество их потребления);
- какие лекарственные препараты пациент принимает на данный момент или принимал ранее в течение длительного времени;
- у женщины необходимо уточнить количество беременностей, заканчивались ли они осложненными родами, имелись ли аборты, а также характер менструаций (обильные или нет, субъективная оценка ежемесячных потерь);
- имелись ли острые или хронические кровопотери вследствие травм, ранений или заболеваний (например, язва желудка и двенадцатиперстной кишки, миома матки, раковая опухоль);
- имеются ли заболевания пищеварительной системы (например, гастриты, язва желудка и двенадцатиперстной кишки, неспецифический язвенный колит);
- имелись ли за последнее время у пациента изменения в массе тела (снижение массы тела может быть связано с наличием у больного синдрома мальабсорбции (нарушение всасывания питательных веществ в тонком кишечнике) или недавно перенесенным инфекционным заболеванием, а увеличение веса может быть вследствие гормональных нарушений);
- не беспокоит ли пациента ломкость ногтей, а также сечение или раннее поседение волос;
- ощущает ли больной жжение языка (при В12 дефицитной анемии);
- беспокоят ли больного чувство онемения в конечностях;
- имелась ли у близлежащих родственников анемия, желчекаменная болезнь, хронические заболевания желудочно-кишечного тракта или выделительной системы;
- была ли у кого-то в семье произведена спленэктомия (удаление селезенки).
- наличие у больного заболеваний сердца (например, пороки сердца), почек (например, рак почек) или печени (например, гепатит).
При осмотре пациента врач обследует:
- Кожу и слизистые оболочки. Выявляется бледность кожных покровов, неправильная пигментация или желтуха. Также на поверхности кожи у больного могут наблюдаться кровоподтеки, петехии или ангиомы (могут быть вследствие тромбоцитопении или других причин, приводящих к потере крови). В уголках рта могут присутствовать хейлиты.
- Лимфатические узлы. Их увеличение, а также болезненность может указывать на наличие воспалительного или неопластического (злокачественного) процессов.
- Пищеварительную систему. С помощью пальпации можно определить, имеются ли у пациента боли в эпигастральной зоне, увеличение размеров печени или селезенки.
- Дыхательную систему. У больного может наблюдаться увеличение количества дыхательных движений (тахипноэ), а также одышка.
- Нервную систему. Позволяет определить наличие нарушений периферической чувствительности.
- Сердечно-сосудистую систему. При измерении артериального давления у больного наблюдается гипотония, при определении частоты пульса отмечается тахикардия.
Метод диагностики, который заключается в исследовании всех видов клеток крови, в определении соотношения их объема к жидкой части крови, а также выявления уровня гемоглобина и лейкоцитарной формулы.
При анемии в общем анализе крови определяются следующие показатели:
- уровень эритроцитов, их средний объем, а также распределение по объему;
- гемоглобин;
- ретикулоциты;
- гематокрит (соотношение клеток крови к плазме);
- среднее содержание и концентрация гемоглобина в эритроците;
- уровень лейкоцитов;
- уровень тромбоцитов.
Биохимический анализ крови
Анализ, позволяющий оценить работу внутренних органов и систем организма.
При анемии определяются следующие показатели:
- уровень ферритина (определяет резервы железа в организме);
- трансферрин (белок, переносящий железо);
- сывороточное железо (определяет уровень железа в сыворотке крови);
- железосвязывающая способность сыворотки крови (указывает на способность сыворотки крови связывать железо);
- уровень витамина В12 и фолиевой кислоты;
- уровень билирубина.
Исследование, позволяющее выявить наличие кровотечения в желудочно-кишечном тракте. За три дня до сдачи анализа пациенту необходимо будет начать соблюдать диету, исключив из рациона продукты, содержащие железо (например, печень, яблоки), а также некоторые лекарственные препараты (например, слабительные и нестероидные противовоспалительные средства, препараты железа).
Собранные каловые массы исследуются с помощью бензидиновой или гваяковой пробы.
Реакция окрашивания может быть:
- слабоположительной;
- положительной;
- резко положительной.
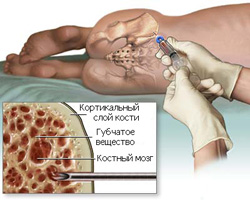
Костный мозг — это губчатое вещество, которое находится внутри костей. В большей степени оно располагается в тазовых костях, ребрах, а также грудине.
Костный мозг является важнейшим органом, отвечающим за кроветворение, так как именно здесь формируются все клетки крови.
Как производится пункция красного костного мозга?
Больного укладывают на бок (или на живот), производят местное обезболивание, после чего перпендикулярно сверлящими движениями вводят специальную иглу в гребень подвздошной кости. Проникновение иглы в кость происходит на глубину два сантиметра, после чего производится аспирация (забор) красного костного мозга. Взятый материал впоследствии наносится на предметные стекла для микроскопического исследования.
В результатах исследования определяют следующие показатели:
- индекс созревания нейтрофилов и эритробластов;
- количество клеточных элементов костного мозга;
- абсолютное содержание миелокариоцитов и мегакариоцитов.
Также во время данного исследования производится трепан-биопсия подвздошной кости. Впоследствии устанавливается соотношение паренхимы, жировой и костной ткани.
Рентгенологическое исследование легких, при котором выявляются анатомические изменения органа, костей, а также мягких тканей.
Рентген может помочь выявить заболевания, ставшие причиной развития анемии у пациента, например, туберкулез, а также рак легких.
Эндоскопическое исследование, позволяющее с помощью гастроскопа осмотреть пищевод, желудок и двенадцатиперстную кишку. Также данное исследование позволяет во время проведения процедуры взять кусочек ткани на биопсию (записаться) с последующим исследованием полученного материала под микроскопом.
С помощью данного исследования можно выявить следующие заболевания:
- варикозное расширение вен пищевода;
- атрофический гастрит;
- язва желудка и двенадцатиперстной кишки;
- полипы желудка;
- рак желудка.
Метод исследования с помощью ультразвуковых волн. Помогает изучить расположение, форму, а также структуру органов и мягких тканей.
При анемии могут исследоваться органы брюшной полости, забрюшинного пространства, а также органы малого таза:
- печень (увеличение размеров органа, цирроз);
- селезенка (увеличение размеров органа);
- почки (рак почек, наличие камней в почках, инфекционно-воспалительных заболеваний);
- матка (миома матки, внематочная беременность, рак матки).
Эндоскопический метод диагностики, позволяющий исследовать толстый кишечник. Процедура производится под общим наркозом.
Данное исследование поможет выявить следующие заболевания:
- кровоточащие язвы желудочно-кишечного тракта;
- полипы;
- неспецифический язвенный колит;
- болезнь Крона;
- дивертикулез толстого кишечника;
- злокачественную опухоль.
Метод диагностики, с помощью рентгеновского излучения позволяющий послойно исследовать органы и ткани. При необходимости перед проведением процедуры пациенту внутривенно могут ввести контрастное вещество для лучшей визуализации исследуемых органов и систем.
При анемии может быть назначено исследование:
- печени (например, гепатит, цирроз печени);
- легких (например, туберкулез, рак легких);
- почек (например, рак, туберкулез почек).
Профилактически проводить противопаразитарное лечение
Кишечные паразиты, находясь в организме человека, часто могут стать причиной развития анемии. Это происходит вследствие того, что паразиты, присасываясь к стенке органа, потребляют питательные вещества, что впоследствии может привести развитию дефицита того или иного витамина или микроэлемента. Также существуют паразиты, которые питаются клетками крови (например, шистосомы, личинки аскарид), поэтому их наличие в организме человека по истечении времени приведет к анемии. Исходя из этого, очень важно регулярно мыть руки перед едой, а также овощи и фрукты перед их употреблением. При наличии домашних животных необходимо ежегодно профилактически проводить противопаразитарное лечение.
Скудное и нерегулярное питание приводит к тому, что в организм не поступают витамины и микроэлементы, необходимые для кроветворения. С течением времени это может привести к развитию железодефицитной, В12 или фолиеводефицитной анемии. Для профилактики анемии человеку ежедневно необходимо потреблять белки (в особенности животного происхождения), так как именно они участвуют в формировании стромы эритроцитов и синтезе гемоглобина. Из-за того, что жиры подавляют кроветворение, их употребление рекомендуется снизить, в особенности жирные сорта мяса и рыбы. Предпочтение необходимо отдать таким продуктам как оливковое, подсолнечное и сливочное масла, так как данные жиры легко усваиваются. Прием углеводов должен оставаться в пределах нормы (для взрослого человека 300 – 500 грамм в сутки), в питании следует увеличить потребление меда, ягод, овощей, фруктов и различных каш (например, овсяная, гречневая, рисовая). Следует заметить, что важную роль в здоровье человека играет адекватное поступление в организм витаминов. Так, например, витамины B9 (фолиевая кислота) и В12 принимают участие в кроветворении, а такие микроэлементы как железо, медь и цинк способствуют формированию гемоглобина и эритроцитов.
Снизить контакт с ядохимикатами
Регулярный контакт с ядохимикатами (например, пестициды, бензол) приводит к кому что они, попадая в кровь, действуют негативно на ее элементы. Так, например, при хроническом отравлении бензолом (входит в состав бензина) в крови наблюдается снижение уровня эритроцитов и гемоглобина, а также увеличение ретикулоцитов. Эритроциты приобретают различную форму (пойкилоцитоз) и размер (анизоцитоз). У человека появляются такие симптомы как повышенная утомляемость, головная боль, головокружение, потеря аппетита, тошнота. Также может наблюдаться развитие маточных, десневых или носовых кровотечений. Именно поэтому человеку, по возможности, строго рекомендуется ограничивать контакт с ядохимикатами.
Курение негативно влияет на все органы и системы организма человека. Со стороны кровеносной системы табачный дым действует негативно на кровеносные сосуды, а также на состав крови, сгущает ее (увеличивает риск образования тромбов). Угарный газ, входящий в табачный дым, связываясь с гемоглобином, снижает его способность доставлять кислород к органам и тканям. Поэтому очень важно избегать контакта с посторонним сигаретным дымом, а также отказаться от самостоятельного курения.
Ежедневно выполнять умеренные физические нагрузки
Регулярное занятие спортом действует благоприятно на кровообращение, улучшая микроциркуляцию в органах и тканях, а также увеличивая количество эритроцитов в крови. Умеренные физические нагрузки снижают риск образования тромбов. Для профилактики развития анемии рекомендуется ежедневно выполнять гимнастику и осуществлять прогулки на свежем воздухе.
Своевременно лечить заболевания желудочно-кишечного тракта
Заболевания желудочно-кишечного тракта влияют на процессы переваривания и усвоения пищи, а также на всасываемость витаминов и микроэлементов. Так, например, фолиевая кислота и витамин B12 всасываются в тонком и толстом кишечнике, нарушение работы данных органов может привести к развитию недостатка данных витаминов и со временем привести к развитию В12 или фолиеводефицитной анемии. Такие заболевания как полипы желудка или кишечника, язва желудка и двенадцатиперстной кишки могут привести к развитию у человека хронического кровотечения. То есть, в течение длительного времени организм будет регулярно терять небольшое количество крови, что со временем приведет к развитию анемии. Поэтому очень важно при наличии риска развития желудочно-кишечных заболеваний (например, наследственная предрасположенность, перенесенные заболевания органов пищеварения) регулярно наблюдаться у врача, своевременно лечить имеющееся заболевание, соблюдать диету и предписанное лечение.
Соблюдать правила введения прикорма для детей
Дети попадают в группу риска развития анемии, в большинстве случаев это связано с неправильным питанием. Очень важно с самого раннего возраста организовать правильное питание и режим ребенка. Начиная с шести месяцев необходимо начать вводить в прикорм такие продукты как овощные пюре, яйца, мясо и каши. Начиная с восьми месяцев вводится рыба. Частота прикорма до восьми месяцев должна составлять три раза в день, в девять – одиннадцать месяцев четыре раза в день, в один год пять – шесть раз в день.
Правильно питаться во время беременности
Часто анемия развивается во время беременности. Дефицит железа или фолиевой кислоты может привести к серьезным осложнениям, связанным с течением беременности и развитием плода. Так, например, дефицит железа у беременной может привести к задержке развития плода, фетоплацентарной недостаточности, патологическим родам, развитию кровотечения. Беременной рекомендуется придерживаться правильного питания – ежедневно потреблять мясо, рыбу, свежие овощи и фрукты. При необходимости женщине может быть назначен прием профилактических доз препаратов железа (например, Сорбифер, Ферретаб).
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Ш ирокий спектр самых разнообразных заболеваний, приводящих к анемии наряду с различными механизмами развития анемического синдрома позволяет считать целесообразным осуществление диагностического поиска в определенной последовательности с решением конкретной диагностической задачи на каждом из этапов поиска.
На начальном этапе диагностического поиска основной целью является определение так называемого патогенетического варианта анемии (АН), т.е. основного механизма, обусловливающего снижение уровня гемоглобина у конкретного пациента.
На основании преобладающего механизма (не причины!) формирования различных видов анемий можно условно выделить несколько патогенетических вариантов:
– сидероахрестические (железонасыщенные) АН
– В12– дефицитные и фолиеводефицитные АН
– анемии при костно–мозговой недостаточности
– анемии при уменьшении объема циркулирующей крови
– анемии со смешанным механизмом развития.
На данном этапе фактически речь идет о синдромной диагностике, так как каждый из патогенетических вариантов представляет собой лишь отдельный анемический синдром (синдром железодефицитной, синдром гемолитической анемии и т.д.). Указанные варианты отражают лишь ведущий патогенетический механизм, в то время как причины развития АН при каждом патогенетическом варианте могут быть различными. Например, причиной железодефицитной анемии могут быть хронические кровопотери из ЖКТ, патология кишечника с нарушением всасывания, алиментарная недостаточность и др. Сидероахрестические анемии могут развиваться у больных хронической свинцовой интоксикацией, на фоне лечения некоторыми лекарственными препаратами (изониазид и др.).
На следующем этапе диагностического поиска после определения патогенетического варианта анемии задачей врача является распознавание заболевания или патологического процесса, лежащего в основе имеющегося анемического синдрома, т.е. выявление причины анемии у конкретного больного. Данный этап диагностического поиска может быть условно обозначен, как нозологическая диагностика. Последняя приобретает важное значение, поскольку позволяет во многих случаях проводить не только патогенетическую терапию анемии, например, препаратами железа, но и воздействовать на основное заболевание (устранение хронической кровопотери при железодефицитной анемии, купирование инфекционно–воспалительного процесса и т.д.).
Основным патогенетическим механизмом развития железодефицитной анемии (ЖДА) является недостаток в организме железа – главного строительного материала для построения молекулы гемоглобина, в частности, его железосодержащей части – гема. Основными критериями ЖДА являются следующие:
– низкий цветовой показатель
– гипохромия эритроцитов, микроцитоз
– снижение уровня сывороточного железа
– повышение общей железосвязывающей способности сыворотки
– снижение содержания ферритина в сыворотке.
На этапе нозологической диагностики поиск причины ЖДА должен проводиться с использованием наиболее информативных методов исследования для конкретной клинической ситуации (данные анамнеза, объективного обследования, дополнительные методы и т.д.) (рис. 1).
Рис. 1. Алгоритм диагностического поиска при гипохромной и нормо-/гиперхромной анемии
Основные причины развития ЖДА:
1. Хронические кровопотери различной локализации:
1. Хронические кровопотери различной локализации:
– желудочно–кишечные (гастроэзофагальная рефлюксная болезнь, эрозивно–язвенные поражения желудка, опухоли желудка и толстой кишки, терминальный илеит, неспецифический язвенный колит, дивертикулиты, кровоточащий геморрой и др.);
– маточные (меноррагии различной этиологии, миома, эндометриоз, внутриматочные контрацептивы;
– носовые (наследственная геморрагическая телеангиэктазия и другие геморрагические диатезы);
– почечные (IgA–нефропатия, геморрагический нефрит, опухоли почек, перманентный внутрисосудистый гемолиз);
– ятрогенные и искусственные кровопотери (частые кровопускания и заборы крови для исследований, лечение гемодиализом, донорство и др.).
2. Нарушение всасывания железа (энтериты различного генеза, синдром недостаточности всасывания, резекции тонкой кишки, резекция желудка с выключением 12–перстной кишки).
3. Повышенная потребность в железе (беременность, лактация, интенсивный рост и пубертатный период, В12 –дефицитная анемия, леченная цианокобаламином).
4. Нарушение транспорта железа (гипопротеинемии различного генеза).
5. Алиментарная недостаточность.
Лечение. При выявлении причины развития ЖДА основное лечение должно быть направлено на ее устранение (оперативное лечение опухоли желудка, кишечника, лечение энтерита, коррекция алиментарной недостаточности и др.). В целом ряде случаев (меноррагии и др.) основное значение приобретает патогенетическая терапия лекарственными препаратами железа (ПЖ).
В клинической практике ПЖ применяются внутрь или парентерально. Путь введения препарата у больных ЖДА определяется конкретной клинической ситуацией. В большинстве случаев для коррекции дефицита железа при отсутствии специальных показаний ПЖ следует назначать внутрь. На российском фармацевтическом рынке имеется широкий выбор ПЖ для приема внутрь. Они различаются количеством содержащихся в них солей железа, в том числе двухвалентного железа, наличием дополнительных компонентов (аскорбиновая и янтарная кислоты, витамины, фруктоза и др.), лекарственными формами (таблетки, драже, сиропы, растворы), переносимостью, стоимостью (табл. 1)
Клинические рекомендации лечения ПЖ для приема внутрь:
– назначение ПЖ в виде солей внутрь с достаточным содержанием двухвалентного железа;
– назначение ПЖ в виде солей внутрь с достаточным содержанием двухвалентного железа;
– назначение ПЖ, содержащих вещества, усиливающие всасывание железа;
– нежелательность одновременного приема пищевых веществ и лекарственных препаратов, уменьшающих всасывание железа;
– целесообразность назначения препаратов железа, содержащих фолиевую кислоту, цианокобаламин при наличии смешанного характера анемии;
– назначение препаратов железа парентерально при нарушении кишечного всасывания;
– достаточная продолжительность насыщающего курса терапии (не менее 1–1,5 мес);
– необходимость проведения поддерживающей терапии ПЖ в соответствующих ситуациях.
При выборе лекарственного ПЖ следует ориентироваться на содержание в нем двухвалентного железа, которое только и всасывается в кишечнике. Входящие в состав многих лекарственных форм ПЖ аскорбиновая кислота, цистеин, фруктоза усиливают всасывание железа. Назначение препаратов железа в высоких дозах (300 мг в сутки) не приводит к увеличению всасывания ионов железа, однако вызывает значительное увеличение числа побочных эффектов. С учетом этого комбинированные препараты, содержащие в своем составе фолиевую кислоту, как необходимый компонент для нормального синтеза и созревания эритроцитов, и цианокобаламин, необходимый для нормального обмена фолиевой кислоты, являющийся основным фактором образования из нее активной формы, приводят к значительному увеличению скорости синтеза гемоглобина и повышают эффективность терапии железодефицитной анемии. Всем этим критериям удовлетворяет комплексный антианемический препарат Ферро–фольгамма, содержащий в своем составе, кроме сульфата железа, 100 мг аскорбиновой кислоты, 10 мкг цианокобаламина, 5 мг фолиевой кислоты. Так, например, при назначении препарата с низким содержанием двухвалентного железа количество принимаемых таблеток должно быть не менее 8–10 в сутки, в то время как препараты с высоким содержанием двухвалентного железа (Ферро–фольгамма) можно принимать в количестве 1–2 таблеток в сутки. Необходимо учитывать, что всасывание железа может уменьшаться под влиянием некоторых содержащихся в пище веществ (фосфорная кислота, соли кальция и др.), а также при одновременном применении ряда медикаментов (тетрациклины, соли магния). Во избежание этого в препарате Ферро–фольгамма все активные компоненты находятся в специальной нейтральной оболочке, обеспечивающей их всасывание главным образом в верхнем отделе тонкой кишки. Отсутствие местного раздражающего действия на слизистую желудка способствует хорошей переносимости.
Среди побочных проявлений на фоне применения ПЖ внутрь наиболее часто возникают тошнота, анорексия, металлический привкус во рту, запоры, реже – поносы.
Показаниями для применения ПЖ парентерально могут быть следующие клинические ситуации:
– непереносимость ПЖ для приема внутрь, не позволяющая дальнейшее продолжение лечения;
– необходимость более быстрого насыщения организма железом, например, перед оперативным вмешательством (миома матки, геморрой и др.).
Алгоритм ведения больших ЖДА представлен на рисунке 2.
Рис. 2. Алгоритм ведения больных железодефицитной анемией
Существует группа гипохромных анемий, при которых содержание железа в организме и его запасы в депо находятся в пределах нормы или даже повышены, однако включение железа в молекулу гемоглобина (в силу различных причин) нарушено, в связи с чем железо не используется для синтеза гема. Такие анемии обозначаются, как сидероахрестические («ахрезия» – неиспользование). Их удельный вес в структуре гипохромных анемий невелик. Тем не менее верификация сидероахрестической («железонасыщенной») анемии и ее дифференциальная диагностика с ЖДА имеют важное практическое значение. Ошибочная диагностика ЖДА у больных с сидероахрестическими анемиями обычно влечет за собой неоправданное назначение препаратов железа, которые в данной ситуации не только не оказывают эффекта, но еще больше «перегружают» запасы железа в депо. Критериями сидероахрестических анемий являются следующие:
Существует группа гипохромных анемий, при которых содержание железа в организме и его запасы в депо находятся в пределах нормы или даже повышены, однако включение железа в молекулу гемоглобина (в силу различных причин) нарушено, в связи с чем железо не используется для синтеза гема. Такие анемии обозначаются, как сидероахрестические («ахрезия» – неиспользование). Их удельный вес в структуре гипохромных анемий невелик. Тем не менее верификация сидероахрестической («железонасыщенной») анемии и ее дифференциальная диагностика с ЖДА имеют важное практическое значение. Ошибочная диагностика ЖДА у больных с сидероахрестическими анемиями обычно влечет за собой неоправданное назначение препаратов железа, которые в данной ситуации не только не оказывают эффекта, но еще больше «перегружают» запасы железа в депо. следующие:
– низкий цветовой показатель;
– повышенное (реже нормальное) содержание железа в сыворотке;
– нормальная или сниженная железосвязывающая способность сыворотки;
– нормальное или повышенное содержание ферритина в сыворотке;
– повышенное количество сидеробластов в костном мозге;
– повышенная экскреция железа с мочой после введения десферала;
– отсутствие эффекта от препаратов железа.
Сидероахрестические анемии представляют собой гетерогенную группу и возникают в результате различных причин. Поэтому нозологический этап диагностического поиска при сидероахрестических анемиях должен проводиться с учетом как клинической ситуации, так и знания основных заболеваний и патологических процессов, сопровождающихся развитием данного анемического синдрома. Известны несколько форм сидероахрестических анемий:
– наследственные формы (аутосомные и рецессивные, чувствительные и рефрактерные к применению пиридоксина);
– связанные с дефицитом фермента гемсинтетазы (обеспечивающей включение железа в молекулу гема);
– связанные с нарушением синтеза гемоглобина из–за патологии его глобиновой части (талассемия). Это заболевание рассматривается обычно в группе гемолитических анемий;
– приобретенные формы (алкогольная интоксикация, хроническая свинцовая интоксикация, воздействие некоторых медикаментов, миелопролиферативные заболевания, кожная порфирия, идиопатические формы).
Клинические рекомендации ведения больных сидероахрестическими анемиями:
– коррекция основного патологического процесса (отмена подозреваемого медикамента, ЭДТА при свинцовой интоксикации и др.);
– назначение пиридоксина при некоторых формах (наследственных);
– назначение десфериоксиамина при высоком уровне сывороточного железа;
– трансфузии эритроцитов по строгим показаниям (выраженная анемия у больных с сопутствующей патологией);
– противопоказание к назначению препаратов железа.
Среди гипохромных анемий определенное место занимают анемии при различных воспалительных заболеваниях как инфекционного, так и неинфекционного происхождения. При всем многообразии патогенетических механизмов анемий в данных ситуациях одним из основных считается перераспределение железа в клетки макрофагальной системы, активирующейся при различных воспалительных (инфекционных и неинфекционных) или опухолевых процессах. Поскольку истинного дефицита железа при этих анемиях не наблюдается, более оправданно говорить о железоперераспределительных анемиях.
Критерии железоперераспределительных АН:
- умеренно гипохромный характер анемии;
- нормальное или умеренно сниженное содержание сывороточного железа;
- нормальная или сниженная железосвязывающая способность сыворотки;
- повышение содержания ферритина в сыворотке;
- повышение количества сидеробластов в костном мозге;
- клинико–лабораторные признаки активного процесса (воспалительного, опухолевого);
- отсутствие эффекта от препаратов железа.
Выделение данного патогенетического варианта и осведомленность о нем практических врачей имеет важное значение ввиду сходства железоперераспределительных анемий с ЖДА и некоторыми сидероахрестическими анемиями (табл. 2), хотя сущность и терапевтические подходы при этих анемиях различны.
Наиболее частыми инфекционно–воспалительными заболеваниями, при которых возникают железоперераспределительные анемии, являются активный туберкулез различной локализации, инфекционный эндокардит, нагноительные заболевания (абсцессы брюшной полости, легких, почек, эмпиема и др.), инфекции мочевыводящих путей, холангит. Среди неинфекционных заболеваний подобный вариант анемий может развиваться при ревматических заболеваниях (ревматоидный артрит и инфекционные артриты с высокой активностью), хронических гепатитах, опухолях различной локализации при отсутствии хронических и острых кровопотерь. Назначение препаратов железа, цианокобаламина в этих ситуациях обычно неэффективно и лишь затягивает своевременное выявление основной причины анемии и соответствующую терапию. Основным способом коррекции анемии у данной категории пациентов является лечение активного воспалительного процесса.
В12 – дефицитные и фолиеводефицитные анемии
В основе данного патогенетического варианта лежит дефицит витамина В12, реже – фолиевой кислоты, возникающий вследствие различных причин. В результате дефицита происходит нарушение синтеза ДНК в кроветворных клетках, развивается неэффективный мегалобластический эритропоэз (в норме существует только у плода) с продукцией нестойких мегалоцитов и макроцитов.
Критерии В12– дефицитной АН:
– высокий цветовой показатель;
– эритроциты с остатками ядер (тельца Жолли, кольца Кэбота);
– повышение содержания железа в сыворотке;
– мегалобластическое кроветворение в костном мозге;
– неврологические нарушения и психические расстройства.
На этапе синдромной диагностики основным методом является исследование костного мозга, при котором выявляется мегалобластический эритропоэз. Данное исследование должно проводиться до назначения цианокобаламина, который широко и часто необоснованно назначается по поводу неясных АН или различной неврологической симптоматики. При невозможности выполнить диагностическое исследование костного мозга (отказ больных и др.) допустимо пробное назначение цианокобаламина с последующим обязательным исследованием количества ретикулоцитов через 3–5 дней (не позже), приобретающим диагностическое значение. Если АН связана с дефицитом витамина В12, то под влиянием нескольких инъекций препарата происходит трансформация мегалобластического кроветворения в нормобластическое, что отражается в периферической крови значительным увеличением количества ретикулоцитов по сравнению с исходным (ретикулоцитарный криз).
Основными причинами развития В12–дефицитной анемии, на исключение которых должен ориентироваться врач на этапе нозологической диагностики, являются следующие:
– нарушение всасывания витамина В12 (атрофический гастрит, рак желудка, операция гастрэктомии, резекция тонкой кишки, наложение кишечных анастомозов с формированием «слепой петли», энтериты с нарушением всасывания, спру, целиакия, селективный дефект (аутосомно–рецессивный) всасывания в сочетании с протеинурией, проявляющийся в раннем детском возрасте (синдром Имерслунд);
– повышенная потребность в витамине В12 (инвазия широким лентецом, дивертикулез толстой кишки, дисбактериоз кишечника, быстрый рост у детей, гипертиреоз, хронические заболевания печени);
– нарушение транспорта витамина В12 (дефицит транскобаламина II (аутосомно–рециссивно наследуемый дефект, проявляющийся в раннем детском возрасте);
– нарушение использования при приеме некоторых медикаментов (ПАСК, неомицин, метформин);
– алиментарная недостаточность (редкая причина) главным образом в детском возрасте, при длительном парентеральном питании без дополнительного введения витаминов.
Фолиево–дефицитные АН по своим гематологическим признакам (макроцитоз, мегалобластический эритропоэз) напоминают В12– дефицитные АН, но встречаются значительно реже и имеют несколько иной спектр вызывающих эти АН заболеваний. Среди причин фолиеводефицитных анемий основными следует считать:
– алиментарную недостаточность (частая причина у пожилых);
– энтериты с нарушением всасывания;
– прием некоторых медикаментов, угнетающих синтез фолиевой кислоты (метотрексат, триамтерен, противосудорожные, барбитураты, метформин);
– хроническую алкогольную интоксикацию;
– повышенную потребность в фолиевой кислоте (злокачественные опухоли, гемолиз, эксфолиативный дерматит, беременность).
Алгоритм ведения больных с макроцитарной анемией неясного происхождения представлен на рисунке 3.
Рис. 3. Алгоритм ведения больных макроцитарной анемией неустановленной причины
Основным патогенетическим механизмом развития гемолитической АН (ГАН) является укорочение продолжительности жизни эритроцитов (в норме 100–120 дней) и их преждевременный распад под воздействием различных причин.
Основным патогенетическим механизмом развития гемолитической АН (ГАН) является укорочение продолжительности жизни эритроцитов (в норме 100–120 дней) и их преждевременный распад под воздействием различных причин.
Критериями ГАН являются следующие:
– нормальный цветовой показатель (низкий при талассемии);
– наличие в крови ядросодержащих эритроидных клеток (эритрокариоцитов);
– увеличение числа эритрокариоцитов в костном мозге (свыше 25%);
– повышение содержания непрямого билирубина в сыворотке с наличием желтухи или без таковой;
– повышение содержания железа в сыворотке;
– наличие в моче гемосидерина (при некоторых формах с внутрисосудистым гемолизом);
– повышение содержания свободного гемоглобина в плазме (при внутрисосудистом гемолизе);
– увеличение селезенки (при некоторых формах).
Большинство ГАН являются нормо– или гиперхромными за исключением ГАН, связанной с нарушением синтеза глобина (талассемия), которая является гипохромной.
Направление диагностического поиска на назологическом этапе определяется особенностями клинической ситуации (возраст больного, наличие и характер фоновой патологии, прием медикаментов, семейные случаи, острый или хронически протекающий гемолиз и т.д.). Следует различать наследственные и приобретенные ГАН.
Наследственные ГАН связаны с различными генетическими дефектами, в частности, с дефектом мембраны эритроцитов (наследственный микросфероцитоз, овалоцитоз), дефицитом некоторых ферментов в эритроцитах (глюкозо–6–фосфат–дегидрогеназа, пируваткиназа и др.), нарушением синтеза цепей глобина (талассемия), наличием нестабильных гемоглобинов.
Талассемию следует заподозрить у больных гипохромной анемией с нормальным или высоким содержанием сывороточного железа в сочетании с признаками гемолиза, а также при отсутствии эффекта от препаратов железа, нередко по ошибке назначаемых таким больным. Для подтверждения диагноза и определения формы талассемии необходимо электрофоретическое исследование гемоглобина.
Среди приобретенных ГАН наиболее распространенными являются аутоиммунные ГАН (симптоматические и идиопатические). Симптоматические аутоиммуные ГАН возникают на фоне лимфопролиферативных заболеваний (хронический лимфолейкоз, лимфогранулематоз и др.), системных васкулитов (системная красная волчанка, ревматоидный артрит), хронического активного гепатита, некоторых инфекций, в частности; вирусных, при приеме ряда медикаментов. Если причина аутоиммунного гемолиза не выявляется, то говорят об идиопатических ГАН. К приобретенным ГАН относятся болезнь Маркиафавы (перманентный внутрисосудистый гемолиз), микроангиопатические ГАН (гемолиз вследствие ДВС–синдрома на фоне различных заболеваний), механический гемолиз при протезированных сосудах и клапанах сердца, маршевой гемоглобинурии, ГАН при воздействии различных токсических веществ (уксусная кислота, мышьяк и др.).
Ведение больных аутоиммунными ГАН определяется вариантом ГАН (симптоматический или идиопатический) На рисунке 4 представлен алгоритм ведения больных аутоиммунной ГАН.
Рис. 4. Алгоритм лечения аутоиммунной гемолитической анемии
Анемии при костно–мозговой недостаточности
В основе данного патогенетического варианта АН лежит нарушение нормальной продукции эритроидных клеток в костном мозге. При этом часто одновременно с угнетением эритропоэза имеет место нарушение продукции клеток гранулоцитарного и тромбоцитарного ростков, что отражается на составе периферической крови (панцитопения) и служит ориентиром в распознавании возможного механизма развития АН.
В основе данного патогенетического варианта АН лежит нарушение нормальной продукции эритроидных клеток в костном мозге. При этом часто одновременно с угнетением эритропоэза имеет место нарушение продукции клеток гранулоцитарного и тромбоцитарного ростков, что отражается на составе периферической крови (панцитопения) и служит ориентиром в распознавании возможного механизма развития АН.
Критерии АН при костно–мозговой недостаточности:
– нормохромная (реже гиперхромная) АН;
– ретикулоцитопения (вплоть до полного отсутствия ретикулоцитов при некоторых формах);
– лейкопения за счет снижения содержания нейтрофильных гранулоцитов (гранулоцитопения);
– тромбоцитопения различной степени выраженности;
– лихорадка, инфекционные осложнения, язвенно–некротические поражения слизистых;
– изменения картины костно–мозгового кроветворения в соответствии с характером основного патологического процесса (замещение жировой тканью, инфильтрация бластными клетками и др.).
На рисунке 5. представлен диагностическаий алгоритм у больных с различными вариантами цитопенического синдрома (панцитопения, бицитопения). На рисунке 6 представлен алгоритм ведения больных с апластической анемией.
Рис. 5. Алгоритм диагностического поиска у больных панцитопенией
Рис. 6. Алгоритм ведения больных апластической анемией
Клинические рекомендации ведения больных апластической анемией:
- устранение выявленной причины (отмена лекарственного препарата, удаление тимомы, лечение вирусных инфекций и т.д.);
- HLA–типирование родных братьев и сестер больных с целью подбора донора костного мозга;
- трансфузии тромбоцитов при количестве тромбоцитов ниже 10х10 9 /л или при менее глубокой тромбоцитопении, но выраженном геморрагическом синдроме;
- трансфузии тромбоцитов от HLA–совместимых доноров при профузных кровотечениях;
- трансфузии эритроцитов при снижении Нв ниже 70 г/л или при менее глубокой анемии у пожилых и стариков;
- нецелесообразны трансфузии компонентов крови от родственников–потенциальных доноров костного мозга;
- эффективность антитимоцитарного глобулина и циклоспорина оценивается через 3–6 месяцев;
- назначение глюкокортикоидов в качестве монотерапии нецелесообразно;
- недоказанная эффективность рекомбинантных препаратов ростковых факторов (Г–КСФ, ГМ–КСФ, ИЛ–1, ИЛ–3);
- обеспечение условий, предупреждающих инфекционные осложнения.
Анемии с сочетанными патогенетическими механизмами
В клинической практике нередко встречаются АН, в развитии которых могут иметь значение два или более патогенетических механизма. Сочетанный патогенетический вариант может встречаться у больных пожилого и старческого возраста (например, железодефицитная анемия в сочетании с фолиеводефицитной анемией). В таких ситуациях оправдано назначение препаратов, содержащих железо и фолиевую кислоту.
источник