Злокачественная анемия, иначе анемия Аддисона-Бирмера, относительно редкое заболевание, обычно возникает у взрослых людей в возрасте 45-60 лет.
Что интересно, чаще встречается у лиц, имеющих 2-ую группу крови и голубые глаза. Принадлежит к группе мегалобластических анемий.
Причиной этого заболевания являются антитела, направленные против фактора Касла (IF – intrisic factor), который, связываясь с витамином В12 в желудке, обеспечивает ее транспортировку через стенку кишечника в кровь; и антитела, направленные против обкладочных клеток желудка, которые производят кислоту. Как правило, дефициту витамина В12 сопутствует диагноз воспаление слизистой оболочки желудка.
Другие причины, ведущие к дефициту витамина В12 это:
- неправильная диета (вегетарианство);
- алкоголизм;
- врожденный дефицит фактора Касла;
- состояние после резекции желудка – состояние после резекции тонкой кишки;
- болезнь Крона.
Появляются симптомы, присущие любой другой анемии, то есть:
- слабость и быстрая утомляемость;
- нарушение концентрации внимания;
- боль и головокружение;
- быстрый ритм сердца (при тяжелой форме заболевания);
- бледность кожи и слизистых оболочек.
Могут возникнуть также болезни, связанные с желудочно-кишечным трактом:
- признаки воспаления языка (темно-красный или очень бледный язык, жжение);
- воспаление полости рта: покраснение, болезненность, отек;
- потеря чувства вкуса;
- потеря аппетита;
- запор или диарея, тошнота.
Развиваются также неврологические симптомы:
- чувство онемения рук и ног;
- чувство «покалывания в конечностях»;
- ощущение прохождения тока через позвоночник при наклоне головы вперед;
- неустойчивая походка;
- потеря памяти и психические изменения, такие как депрессия, галлюцинации.
Чем больше времени прошло от момента появления неврологических симптомов до момента начала лечения, тем меньше вероятность выздоровления. Изменения, сохраняющиеся дольше, чем полгода, как правило, сохраняются на всю жизнь.
Заметив, что у пациента симптомы анемии, врач должен назначить ему анализ крови. В случае обнаружения снижения уровня гемоглобина и красных кровяных телец, оцениваются и другие параметры крови.
В случае мегалобластической анемии и злокачественной анемии, наблюдается повышенный размер эритроцитов (MCV → 110). Тогда вы должны выяснить причину неправильного метаболизма витаминов. В частности, оценить уровень кобаламина в крови: менее 130 пг/мл указывает на его недостаток.
Исследуется также содержание в крови и моче метилмалоновой кислоты. Она в увеличенном количестве образуется в случае недостатка витамина В12, поэтому её повышенное содержание подтверждает нарушение всасывания витамина. Когда уровень кобаламина уменьшается, рекомендуется исследование в направлении антител, атакующих фактор Касла. Когда результат отрицательный, необходимо выполнить тест Шиллинга.
О дефиците этого витамина свидетельствует также благоприятный ответ организма на лечение. Увеличение в крови количества молодых красных телец через 5-7 дней указывает на их восстановление. Злокачественная анемия эффективно обратима благодаря добавлению витамина В12. Обычно назначается 1000 мкг в сутки на 2 недели. После того, как симптомы анемии меняются, схему введения препарата изменяют и назначают прием препарата до конца жизни.
До времени открытия витамина В12 болезнь была смертельной и поэтому была названа злокачественной, сегодня это имя уже имеет только историческую ценность.
источник
Есть несколько видов патологий, которые связаны с дефицитом микроэлементов в организме человека. Одна из них — анемия Аддисона-Бирмера. Впервые ее описал Аддисон. Позже она нашла подтверждение у Бирмера.
Именно он изучил болезнь. Он же подробно описал ее клинически. Это не болезнь аддисона. И не болезнь бирмера. Впоследствии это состояние справедливо получило название по именам двух своих исследователей: Аддисона-Бирмера.
Болезнь, которую описали Томас Аддисон в 1855 году, а потом и Антон Бирмер в 1868 году, стала известна среди медиков как пернициозная анемия. Это болезнь гибельная, злокачественная. Долгие годы она считалась заболеванием неизлечимым, которое протекает неудержимо и тяжело.
Группа врачей тогда сделала великое открытие. И потому оно было удостоено Нобелевской премии. Они смогли вылечить малокровие у собак путем добавления в пищу сырой печени. А потом им удалось также выделить из печени фактор, который устраняет анемию. Они его назвали витамином В12 или внешним фактором Касла.
Анемия Аддисона-Бирмера развивается тогда, когда есть нехватка витамина В12 и фолиевой кислоты. Заболевание встречается в 30-50 случаях на 10 тысяч населения. Чаще подвергаются этому заболеванию женщины. Особенно в возрасте, превышающем 50 лет, риск развития болезни увеличивается. Есть предположение, что это имеет связь с менопаузой.
Сейчас достаточно ясен патогенез заболевания. Однако этиология остается только предположением.
Как правило, заболевают лица в возрасте свыше 40 лет. Для клинической картины болезни характерно наличие специфической триады нарушений в организме:
1)Нарушения со стороны пищеварительного тракта.
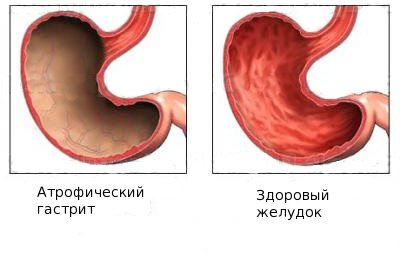
Гастрит по атрофическому типу протекает тяжело. Постепенно снижается функция железистого эпителия. Слизистая инфильтрируется. Она замещается клетками, которые не присущи данному органу. Происходит резкое сокращение выработки ферментов в крови. Выработка может вовсе прекратится.
2)Нарушения со стороны кроветворной системы.
Развивается мегалобластное кроветворение. Так образуются многие незрелые гранулоциты крови, которые не могут нормально выполнять свои функции. В этом течение анемии Аддисона-Бирмера напоминает злокачественные болезни крови.
3)Нарушения со стороны нервной системы.
Нет возможности усваиваться витамину В12 и фолиевой кислоте. Каждый из этих компонентов нужен для формирования клеток. При их участии происходит синтез ДНК и правильно образуется ядро клетки. Если этих компонентов недостаточно, то страдают первым делом гемопоэз и нервная ткань.
Ей способствует атрофия слизистой оболочки желудка. Это приводит к тому, что прекращается выработка пепсиногена, который обеспечивает доставку и всасывание цианкобаламина.
Отметим, что не во всех случаях атрофический гастрит приводит к тому, что получает развитие мегабластная анемия. Есть предположение, что развитие болезни – это следствие несколько факторов.
К нарушению усвоения В12 и фолиевой кислоты может привести обширное воспаление слизистой желудка и подвздошного отела кишечника. Или то, что они поражены злокачественными опухолями.
Пернициозная анемия в немалой степени – аутоиммунное заболевание. Ведь в сыворотке крови пациентов в 70-75% случаев обнаруживают антитела к внутренним клеткам желудка. Опыты над крысами показали, что подобные клетки являются причиной атрофии желудочной железистой ткани. Подобные антитела были обнаружены и в желудочном секрете.
Дополнительный фактор – наследственная склонность к заболеваниям поджелудочной железы.
Важен и образ жизни, который приводит к сбоям в иммунной системе. Скажем, эксперименты с жесткими диетами, резкий переход на вегетарианство, прием медицинских препаратов без контроля, нарушение дозировок при приеме лекарств.
Поражение кишечника паразитическими микроорганизмами – еще одна причина. А также в тот случай, когда патологическая кишечная микрофлора развивается сверх всякой меры.
Перечислим также отдельные факторы влияния.
- в северных районах такая патология встречается чаще;
- есть указания на то, что заболеваемость увеличивается у тех, кто работает со свинцом, а также у того, кто медленно травит свой организм окисью углерода;
- после операции по удалению желудка, когда тотально ликвидируют секреторную функцию. Анемия может развиться через 5-7 лет;
- есть информация о том, что мегабластная анемия развивается из-за токсического отравления у страдающих хроническим алкоголизмом.
Симптомы болезни развиваются незаметно. Уже за много лет до выраженной картины злокачественного малокровия можно обнаружить желудочную ахилию. Реже происходят изменения со стороны нервной системы.
В начале болезни появляется физическая и психическая слабость. Она нарастает. Больные жалуются на быстрое утомление, головокружение, головные боли, шум в ушах, «летающие мушки» в глазах, одышку. У них сердцебиение даже тогда, когда физическое напряжение маленькое. Беспокоит сонливость днем. А ночью – напротив, бессонница.
Затем присоединяются диспепсические явления. Скажем, анорексия, поносы. И больные отправляются в поликлинику к врачу, когда уже наступила значительная анемизация.
У других больных поначалу появляются боли и жжение в языке. Вот почему они идут к специалистам по болезням полости рта. В этих случаях достаточно осмотреть язык, чтобы обнаружить признаки типичного глоссита. Этого достаточно для того, чтобы поставить правильный диагноз. Диагностика подкрепляется анемичным видом больного и характерной картиной крови.
Классический симптом — глоссит Хантера — подтверждается тем, что на языке появляются ярко-красные участки воспаления. На них нельзя не обратить внимания. Ведь они очень чувствительны к приему пищи и лекарств.
Подобные изменения могут находиться на деснах, слизистой щек, мягком нёбе. Очень редко, но все-таки воспаления появляются на слизистой глотки и пищевода. Затем воспаления стихают, и сосочки языка атрофируются. Появляется «лакированный язык». Такое название язык получил из-за того, что он становится блестящим и гладким.
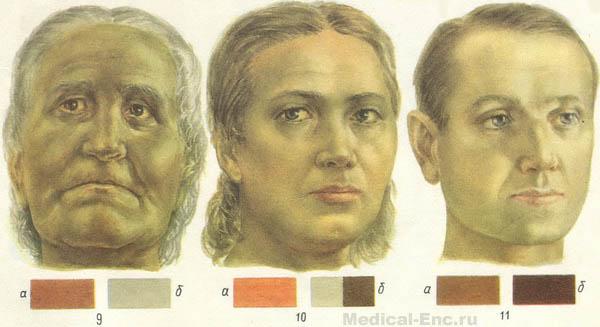
Во время обострения у больного необычный вид. У него кожа бледная, с лимонно-желтым оттенком. Нередко слизистые и покровы становятся желтушными. Изредка на лице наблюдается коричневая пигментация. Она имеет вид «бабочки» — на крыльях носа и над скуловыми костями. Лицо одутловатое. Довольно часто бывает отечность возле стоп и лодыжек.
Больные не бывают истощенными. Наоборот, они упитаны и склонны к ожирению. Печень в большинстве случаев увеличена. Иногда она достигает значительных размеров. Она нечувствительная, мягкой консистенции. У селезенки более плотная консистенция. Как правило, она пальпируется с трудом.
Возникающие симптомы анемии Аддисона-Бирмера можно разделить на проявления:
- СО СТОРОНЫ НЕРВНОЙ СИСТЕМЫ: нарушения регуляции движений, появление парестезии; боли в межреберье; изредка бывают поражения нерва зрительного и слухового; нарушение памяти.
- СО СТОРОНЫ ПИЩЕВАРИТЕЛЬНОГО ТРАКТА: глоссит характеризуется синдромом «лакированного языка» и болезненными ощущения в нем; тошнота, тяжесть в области эпигастрия, отвращения к пище, ухудшение вкусовых ощущений; печень увеличивается, реже – селезенка, появляется желтушность склер, слизистых оболочек;
- ВНЕШНИЕ ПРОЯВЛЕНИЯ: ноги и руки холодные, кожа бледная с желтоватым оттенком, формируется синдром анемии Аддисона-Бирмера – лицо восковой куклы; одутловатость лица, значительные отеки; вялость, сонливость.
- СО СТОРОНЫ СЕРДЦА: симптомы одышки, болей, дистрофических изменений в миокарде.
Чисто визуально можно выявить пигментные пятна на лице, руках и теле, бледные кожные покровы, желтушный оттенок склер. Характерная картина выявляется при осмотре ротовой полости.
При пальпации можно обнаружить маленькое увеличение печени. Она может выступать за край ребра. Проведение неврологических проб показывает, что есть изменения чувствительности в конечностях.
Главным признаком мегабластной анемии считается наличие гиперсегментарных нейтрофилов. У них 5 и более сегментов в ядре. У человека, если он здоров, таких клеток встречается в пределах 2%. У того, кто страдает злокачественной анемией, гиперсегментарных нейтрофилов более 5%.
Важно также исследовать костный мозг. В нем обнаруживается мегалобластный рост клеток. Клетки в своем развитии останавливаются. Они предшествуют эритроцитам. Их размеры аномально увеличены. Они деформировались. Можно заметить большую разницу в уровне развития ядра и цитоплазмы. Большинство незрелых и деформированных клеток эритроцитов (мегабластов) не выходит в кровоток, поскольку они разрушаются в костном мозге.
Инструментальная диагностика предусматривает исследование желудочного сока. После этого обычно выявляют, что кислотность понижена или полностью отсутствует. Зато много слизи, которая по составу похожа на кишечную. При эндоскопическом исследовании явно наблюдается обширная атрофия слизистой оболочки желудка. Ее нередко называют «перламутровыми бляшками».
В этом случае можно выявить первопричину и определить правильное лечение. Для этого нужно измерить концентрацию данных веществ в сыворотке крови. Норма фолиевой кислоты – 5-20 нг/мл, норма В12 – 150-900 нг/мл. Если показатели ниже, то налицо свидетельство того, что есть дефицит этих компонентов в организме.
Для проведения пробы больному вводят витамин В12 внутримышечно, а потом определяют, сколько его в моче. Малое количество – при В12-дефицитной анемии, максимальное – при фолиево-дефицитной.
Нередко возникает необходимость провести гистологическое исследование тканей, поскольку одной из причин, которые могут вызвать анемию Аддисона Бирмера, становятся злокачественные новообразования. Таким больным необходимо дополнительно проконсультироваться у узких специалистов: невролога, эндокринолога, кардиолога, иммунолога.
Среди тех, кому 60 лет и больше, частота заболевания составляет свыше 1%. При семейной предрасположенности к пернициозной анемии контингент больных моложе. Среди тех, кому доставляет страдания болезнь Аддисона женщин больше. Соотношение больных женщин и мужчин не изменяется. Оно постоянно составляет 10:7.
Для 65% пациентов основным фактором заболевания является образование антител против собственных клеток надпочечных желез. Преимущественно это характерно для женщин. Если поражения надпочечников врожденные, то часто обнаруживается и низкая активность щитовидной железы, молочница, недоразвитые половые органы, облысение, анемия, активный гепатит, витилиго.
В группу риска входят подростки, спортсмены, а также женщины при поздней беременности, у которых повышенная необходимость в витамине В12. Если взять детей, то у них патология получает развитие при наследственной предрасположенности к заболеванию.
Внешними факторами могут являться серьезное недоедание и вегетарианство матери, когда она вынашивает ребенка.
Витамин В12 синтезируется особым штаммом бактерий. Его всасывание происходит лишь тонком кишечнике. В его нижнем отделе.
У животных, которые питаются травой, а также у некоторых видов птиц в кишечнике есть бактерии, которые вырабатывают кобаламин. Вот почему они могут пополнять запасы вещества самостоятельно. В человеческом организме такие бактерии находятся лишь в толстой кишке. И витамин В12, синтезируемый ими, выходит вместе с каловыми массами.
Поэтому витамин В12 может поступать в организм человека лишь с продуктами животноводства. Он также есть в растительной пище, однако это неактивный его аналог. Большое содержание кобаламина в печени и почках. Чуть меньше — в морепродуктах и в мясе. Немного витамина содержится в молочных продуктах и в яйцах. Однако если их постоянно есть, то дефицита этого нутриента не будет.
Кобаламин накапливается в печени и других органах. Тем самым организм делает запасы. Они внушительны. Ведь их может хватить на два года даже в том случае, человек полностью откажется от продуктов животноводства.
Если анемия возникла во время беременности, то нехватка витамина В12 приводит к тому, что начинает отслаиваться плацента, наступают преждевременные роды. Если к плоду поступает мало кислорода, то это приводит к гипоксии, то есть к кислородному голоданию. А это влияет на рост и развитие ребенка.
Анемия может возникать, когда у организма повышенный расход витамина в период роста, большие силовые нагрузки, многоплодная беременность. Однако полноценное питание при условии, что нет других факторов, которые способствуют усугублению патологии, В12-дефицитную анемию устраняет.
Для профилактики анемии назначают фолиевую кислоту, но только определенным группам граждан. В частности, беременным женщинам – для того, чтобы предотвратить патологию спинного мозга плода. И кормящим мамам – тоже для того, чтобы правильно развивался ребенок. Пожилым людям – при некоторых формах анемии. Пациентам – в коматозном состоянии. Во всех остальных случаях в обычном рационе витамина вполне достаточно.
Сразу отметим, что лечение анемии Аддисона Бирмера имеет свои особенности. Лечение пернициозной анемии контролируют такие специалисты, как гематолог, гастроэнтеролог, невропатолог.
Суть основной терапии в том, чтобы восполнить дефицит витамина В12 в организме. Для этого его вводят под кожу. Параллельно идет лечение желудочно-кишечного тракта. Необходимо также нормализовать микрофлору. А в случае необходимости необходимо также устранить глистную инвазию.
При аутоиммунных патологиях одновременно с препаратами синтетического витамина нужно вводить глюкокортикостероиды. Они необходимы для того, чтобы нейтрализовать антитела к внутреннему фактору.
Нехватка фолиевой кислоты более благоприятна для организма в плане лечения, поскольку при ней не страдает секреторная функция желудка. И если ввести перорально терапевтические дозы препарата, то это быстро даст нужный эффект.
Фолиевая кислота – это отдельный препарат в форме таблеток. Она также может быть в виде раствора для инъекций. Бывает в составе комплексных витаминов.
Для тех, кто желает знать, как лечить заболевание, сообщаем, что при дефиците витамина В12 в организме использовать таблетки нет смысла. Ведь, если есть атрофический гастрит, то эффект от лечения становится нулевым. В лечении этого вида анемии необходимы внутримышечные или подкожные инъекции.
Лечение препаратами «Оксикобаламин» или «Цианокобаламин» в виде подкожных инъекций предусматривает два этапа — насыщение и поддержание.
Во время обострения каждый день больному вводят препарат. На дозировку и длительность курса влияют возраст и степени тяжести анемии. Как только показатели витамина В12 приходят в норму, необходимо провести поддерживающую терапию. Суть ее в том, чтобы вводить препарат раз в две недели.
Если анемия легкая или средней степени тяжести, то лечение можно отложить до полной диагностики. Ведь важно выявить причины дефицита. Если неврологические нарушения ярко выражены, и если есть значительные изменения картины крови, к лечению нужно приступать без промедления.
Нередко внешние признаки анемии Аддисона-Бирмера исчезают сразу же после начала лечения, то есть спустя считанные дни. Боли в языке и ротовой полости уходят. Прорезается аппетит. Организм не ощущает слабости. Восстанавливаются слух и зрение.
Всего через несколько суток количество мегабластов в костном мозге резко сокращается. Кроветворение восстанавливается, как правило, через 1-2 месяца. Симптомы тяжелых неврологических нарушений могут сохраняться нескольких месяцев. Но могут не исчезнуть вовсе.
Если лечение своевременное, то симптомы патологии постепенно устраняются. Покровы кожи приобретают естественный оттенок уже через пару недель. После того, как восстановлена норма эритроцитов, нет никаких проблем с пищеварением, нормализуется стул.
Постепенно сглаживаются неврологические расстройства. Чувствительность тканей нормализуется. Походка восстанавливается. Исчезают невропатия и провалы в памяти.
Если заболевание запущено, то атрофированные зрительные нервы, как и мышцы ног, к сожалению, не восстанавливаются. Очень редко, но бывает, что после выздоровления у пациентов появляется токсический зоб и микседема.
Для предупреждения развития заболевания необходимо правильно организовать рацион. В него обязательно должны быть включены продукты животноводства, в которых богатое содержание витамина В12. Нужно поменьше употреблять жирной пищи. Ведь она приводит к тому, что процессы кроветворения замедляются.
Злоупотребление препаратами от изжоги, которые снижают выработку соляной кислоты в желудочном соке, может привести к тому, что витамин будет разрушаться.
При хронических заболеваниях желудка и печени необходимо постоянно проводить анализ крови, чтобы знать, каково содержание витамина в организме. Человек в преклонном возрасте должен принимать витамин В12 в составе поливитаминных комплексов. Можно также для профилактики делать инъекции лекарственного препарата.
источник
Картина крови при anaemia perniciosa характерна. Число эритроцитов падает часто до очень низких цифр — до 1 млн. в 1 мм3, нередко еще ниже — до 800 000-600 000-500 000. Минимальные цифры отдельных наблюдений — 150 000 в 1 мм3. С другой стороны, в начале заболевания и во время ремиссий количество эритроцитов близко к нормальному. Следует отметить, что наблюдаются случаи с характерными для болезни Аддисон-Бирмера симптомами (явления фуникулярного миелоза) при количестве эритроцитов больше 4 млн. в 1 мм3 и гемоглобина выше 75%. Содержание гемоглобина падает в выраженных случаях до 30-20%, достигая у тяжелобольных цифр около 10%. Основной чертой малокровия Аддисон-Бирмера является то, что количество гемоглобина падает менее резко, чем количество эритроцитов. Таким образом, цветной показатель оказывается выше единицы. Анемия Бирмера является выраженно гиперхромной анемией. Степень гиперхромии, как правило, пропорциональна тяжести малокровия. При морфологическом исследовании крови бросается в глаза насыщенная окраска эритроцитов — морфологический субстрат указанной гиперхромии. Эта гиперхромия обычно ярко видна в окрашенных мазках.
В тяжелых случаях гиперхромия может быть очень выраженной и цветной показатель в отдельных случаях достигает 1,5 или даже 2, т. е. эритроциты при этом малокровии могут быть в 2 раза интенсивнее окрашены, чем нормальные. При успешном лечении во время ремиссии количество эритроцитов в периферической крови нарастает быстрее, чем гемоглобин, и цветной показатель благодаря этому падает до нормы и даже может быть временно ниже нормы, ниже единицы. Он может снизиться после кровотечений, при различных инфекционных заболеваниях, при недостаточном питании, в частности при алиментарной дистрофии.
Есть указания, что при малокровии Аддисон-Бирмера гемоглобин имеет пониженное сродство к кислороду, кровь при этом заболевании может связывать меньшие его количества.
Нормальный эритроцит в крови живет 110-120 дней. Значительное количество эритроцитов больного пернициозной анемией живет более короткое время: по наблюдениям Гальберга, продолжительность жизни их колеблется от 4 до 120 дней. Д. Н. Яновский говорит об усиленном распаде при анемии Бирмера эритроцитов-мегалоцитов. Процентное содержание ретикулоцитов обычно увеличено, но абсолютное их количество всегда уменьшено. При усиленной регенерации имеется большое количество ретикулоцитов. Их особенно много в начале ремиссии после введения камполона. Изучение морфологии эритроцитов дает представление не только о характере процесса, но и об его динамике, и о ходе эритропоэза.
Изменения эритроцитов обычно тем резче выражены, чем меньше число эритроцитов. В период ремиссии при количестве эритроцитов выше 4,5 млн., гемоглобина выше 90% морфологически красные кровяные тельца неотличимы от нормальных.
Количество лейкоцитов уменьшено до 2000-4000 в 1 мм3. Во время ремиссии число их увеличивается. При глистном малокровии и малокровии беременных наблюдаются относительно большие числа лейкоцитов.
Чем резче выражена анемия, тем, как правило, ниже количество лейкоцитов.
Наряду с лейкопенией определяется уменьшенное абсолютно и относительно количество нейтрофилов. Нейтрофилы обычно крупнее нормальных, ядро их имеет много сегментов, сдвиг ядерной формулы нейтрофилов вправо.
Иногда встречаются и единичные молодые клетки — миелоциты. Важно отметить, что при малокровии Аддисон-Бирмера, как правило, не наблюдается токсической зернистости нейтрофилов.
Количество лимфоцитов велико — до 40-50% и выше. Однако абсолютное их число обычно нормальное (около 1500 в 1 мм3).
Количество моноцитов или уменьшено (у более тяжело больных), или нормально. Наряду с ними в крови при более тяжелом состоянии больного появляются одноядерные атипичные клетки (гистиоциты), то более крупные с псевдоподиями, то более мелкие, по величине и общему виду напоминающие лимфоциты.
Количество эозинофилов обычно уменьшено. В тяжелых случаях они могут исчезнуть из периферической крови. Наличие или появление их служит хорошим прогностическим признаком.
Тромбоциты уменьшены в количестве, при истощении костного мозга они почти исчезают, что создает угрозу развития геморрагического диатеза. Среди тромбоцитов преобладают патологические формы с грубой зернистостью (постарение пластинок). Следует, однако, отметить, что явления геморрагического диатеза — петехиальные сыпи, различные кровотечения не свойственны этому заболеванию.
Систематическое исследование крови дает возможность регистрировать динамику процесса и прекрасно контролирует успех лечения. Данные гематологического исследования, занесенные в таблицу, — трудно заменимое подспорье при лечении больного анемией Аддисон-Бирмера.
Чрезвычайно интересны и показательны изменения состава лейкоцитов периферической крови при эффективной терапии. По Айзексу, в первые 7 дней после всасывания достаточного количества принятого соответствующего терапевтического вещества наступает четкий сдвиг влево лейкоцитарной формулы (по Шиллингу), в крови появляются молодые клетки нейтрофильного ряда.
Изучение клеточного состава костного мозга путем пункции чрезвычайно обогатило наше понимание состояния кровотворения при болезни Аддисон-Бирмера. Мы получили возможность изучать его в различные стадии заболевания, изучать влияние терапии на миелопоэз.
П. Шатилов исследовал состояние костномозгового кроветворения при пернициозной анемии на трупе. Он считал, что костный мозг при этом заболевании миелобластический. М. И. Аринкин, а за ним и все другие исследователи на основании прижизненного изучения костного мозга путем пункции показали, что он является мегалобластическим. В мазках пунктата эритропоэз преобладает над лейкопоэзом. До начала современной терапии он мог превышать последний в пять раз.
Итак, костный мозг при нелеченной болезни Аддисон-Бирмера является мегалобластическим. Нормобласты на высоте болезни в костном мозгу часто отсутствуют.
Мегалобластическое кроветворение возникает в условиях недостатка в организме витамина В12. При этом гемоцитобласт развивается в необычном направлении, и образуются особые клетки — мегалобласты различной степени зрелости. Из мегалобластов образуются особые формы эритроцитов, так называемые мегалоциты и частично макроциты.
Причиной анемии при болезни Аддисон-Бирмера является, по мнению Г. А. Алексеева, то обстоятельство, что мегалобластический эритропоэз совершается гораздо медленнее нормобластического, а образующиеся при этом эритроциты распадаются более интенсивно, чем нормальные.
Наряду с этим Д. Н. Яновский не считает возможным видеть основной причиной анемии своего рода «тупик кровотворения». Эритропоэз при болезни Аддисон-Бирмера совершается чрезвычайно интенсивно, а М. А. Чепелева обращает внимание на очень короткий срок жизни мегалобластов и тоже приходит к выводу о чрезвычайно высокой функциональной способности и деятельности мегалобластического костного мозга. Наконец, И. М. Менделеев на основании тщательного изучения кровотворения при ботриоцефальной анемии приходит к аналогичному выводу. Вопрос о причине анемии при мегалобластическом кроветворении, таким образом, окончательно еще не выяснен. Бесспорно, однако, что образующиеся эритроциты являются неполноценными и легко разрушаются.
Наряду с богатством костного мозга элементами мегалобластического ряда обращает на себя внимание выраженная гиперплазия в костном мозгу ретикуло-эндотелиальных клеток. М. И. Аринкин из 56 случаев отметил эту тенденцию в 47. Современные авторы также отмечают этот факт. Шартум-Ганзен в костном мозгу здоровых находил подобные клетки в среднем в количестве 0,21% от числа всех клеточных элементов (колебания от 0 до 1%). В случаях нелеченной пернициозной анемии процент ретикулярных клеток доходил до 9-13.
Требует разрешения вопрос об отношении мегалобластов к нормобластам, об отношении мегалобластического кровотворения к нормобластическому. Впервые описал мегалобласты Эрлих. Он считал, что нормобласты и мегалобласты представляют собой два принципиально различных вида эритробластов, что между ними не имеется никаких переходов, промежуточных форм.
В нормальном костном мозгу мегалобласты никогда не встречаются. Они свойственны только зародышу до IV месяца эмбриональной жизни и костному мозгу больного пернициозной анемией. Идентичность мегалобласта, наблюдаемого при злокачественном малокровии, и первичных клеток гемоглобинового ряда у эмбриона возможна, но не доказана.
А. А. Максимов считал, что наименование мегалобласт применимо только к клетке, описанной и так названной Эрлихом при anaemia perniciosa. А. А. Максимов категорически отрицал возможность наличия в физиологических условиях в костном мозгу мегалобластов. Мы считаем, что мегалобластическое кроветворение эмбриона и больного болезнью Аддисон-Бирмера не является идентичным.
Промегалобласт, мегалобласт — патологические формы зритропоэза, возникающие при недостатке в данном организме определенных веществ: витамина В12 и фолиевой кислоты.
М. И. Аринкин считает, что мегалобластический тип кровотворения связан с гиперплазией ретикулоэндотелия в костном мозгу. Школа Феррата, в частности Кинле, твердо придерживается этой точки зрения. Они считают доказанным, что свободная клетка костномозгового ретикулума развивается в промегалобласт и дальше по «эмбриональному» типу кровотворения. Кинле видит в крупных клетках с резко базофильной протоплазмой с нежно сетчатым ядром и ядрышками не проэритробласты, а промегалобласты. Фактически точки зрения М. И. Аринкина и школы Феррата полностью совпадают.
Д. Н. Яновский подчеркивает, что в костном мозгу имеется «значительное количество юных ретикулярных клеток со всеми переходами к мегалобластам». Ретикулярная ткань производит при данном заболевании не проэритробласты, а промегалобласты.
Наряду с резчайшим нарушением эритропоэза в костном мозгу обнаруживаются нарушения и лейкопоэза, и тромбоцитопоэза. Страдает гранулоцитопоэз. Находят патологические формы промиелоцитов, миелоцитов. Они отличаются большой величиной. Ядра и у этих клеток часто бывают многолопастными. Велики палочкоядерные нейтрофилы, в них нередки вакуоли.
Мегакариоциты велики, ядра их многолопастные.
Таким образом, при пернициозной анемии поражается и эритропоэз, и лейкопоэз, и тромбоцитопоэз. Это страдание всего костномозгового кровотворения — панмиелопатия.
Течение. Бирмер назвал это заболевание прогрессирующим злокачественным малокровием — Anaemia perniciosa progressiva. Без лечения оно через 2-3 года после начала кончалось смертью. До появления в терапии печенки только в отдельных редких случаях заболевание длилось 7-8 лет.
Болезни Аддисон-Бирмера свойственна волнообразность течения. Обострения сменяются ремиссиями то более длительными, то более короткими. Причины ремиссий и обострений не всегда могут быть выяснены. Улучшение состояния — ремиссия — наступает и спонтанно, и под влиянием различных терапевтических воздействий. До введения в лечение болезни Аддисон-Бирмера печенки и ее препаратов ремиссии наступали от применения мышьяка, переливания крови и т. п. Иногда они вызывались совершенно случайными причинами — гнойником на месте впрыскивания, острым инфекционным заболеванием и т. п. Ремиссии могут быть длительными, не дающими отчетливого ухудшения в течение года и больше. С прогрессированием болезни они наступают реже и более краткосрочны. Возвраты заболевания дают обострение всех кардинальных симптомов болезни Аддисон-Бирмера.
Современная терапия болезни Аддисон-Бирмера препаратами печени и желудка, фолиевой кислотой, витамином В12, не давая излечения, поразительно действует на основные клинические и гематологические проявления этого заболевания. Больные пернициозной анемией бывают практически здоровыми в течение долгих лет. Важно отметить, что после 1928 г., со времени повсеместного введения печеночной терапии, на секции почти не обнаруживают случаев анемии Аддисон-Бирмера.
Диагноз. Болезнь Аддисон-Бирмера принадлежит к тем болезням, которые в амбулатории и поликлинической практике часто не распознаются в течение долгого времени. Врачи не думают в подобных случаях о возможности малокровия, не делают исследования крови и очень часто ставят неверный диагноз. Чаще всего этих больных долго лечат от сердечно-сосудистых или почечных заболеваний. Между тем распознавание болезни Аддисон-Бирмера часто, возможно на основании только клинической картины даже без исследования крови.
Характерны следующие черты: медленно развивающееся заболевание без определенной внешней причины, малокровный вид без истощения, бледность с желтоватым оттенком покровов, наличие гентеровского языка, болезненность при надавливании на грудину, незначительное увеличение селезенки, явления фуникулярного миелоза, ахилия. Важно отметить насыщенный цвет кала и темный цвет мочи. Первыми проявлениями злокачественного малокровия, по некоторым авторам, бывают явления со стороны желудочно-кишечного канала в 31% случаев, явления со стороны нервной системы — в 26%, явления со стороны сердечно-сосудистой системы — в 10%, явления общей слабости в 33% случаев.
Со стороны крови характерно понижение количества эритроцитов, более значительное, чем гемоглобина, следовательно, высокий цветной показатель. Со стороны морфологии эритроцитов диагностически важна интенсивная окраска их и мегалобластов. Кроме того, важна лейкопения с относительным лимфоцитозом и наличием крупных нейтрофилов с большим количеством сегментов. Характерно понижение числа кровяных пластинок. Как правило, имеется своеобразная насыщенная окраска с оранжевым оттенком сыворотки крови.
источник
В периферической крови макроцитоз наиболее показательный элемент. Большинство эритроцитов крупных размеров (до 12 u и более), немного овальной формы, хорошо загруженные гемоглобином (без светлой центральной зоны); тем не менее существуют эритроциты и меньших размеров (менее 5 u), некоторые из них нерегулярной формы (пойкилоциты); также встречаются точечнобазофильные эритроциты, кольца Cabot.
Наличие анизоцитоза отмечает широкая кривая Price-Jones, верхушка которой сдвинута вправо; в принципе DEM (СДЭ) укладывается в пределы от 8 до 9 u, а иногда и более.
Соответственно повышаются показатели VEM (СОЭ) (95—110 u3, иногда более 140 u3) и НЕМ (33—38 пг, в отдельных случаях 50 пг.) В связи с макроцитозом число эритроцитов меньше соответственных показателей гемоглобина и гематокрита, при этом больные переносят относительно хорошо анемию, показатель которой равняется 1,5 мл Э/мм3. Число ретикулоцитов меньше нормы. Важным но не постоянным признаком для постановки диагноза составляет наличие в крови единичных мегалобластов.
Лейкоцитная картина характеризуется, вообще, умеренной лейкопенией (от 3000 до 5000 на мм3), сокращением численности гранулоцитов, которые крупные и проявляют тенденцию к гиперсегментированию (одновременно появляются молодые элементы — метамиэлоциты и миэлоциты). Численность тромбоцитов умеренно уменьшается (редко менее 50 тыс.), при этом отмечается анизоцитоз, в отдельных случаях с некоторым функциональным дефицитом.
В костном мозге обнаруживается (выраженная) гиперплазия предшественников эритроцитов и мегалобластические изменения во всех костномозговых рядах, морфологический характер, генез и последствия которых уже рассматривались при описании мегалобластоза. В некоторых тяжелых случаях обнаруживается наличие эктопических очагов кроветворения в печени и селезенке.
Среди прочих биологических постоянных бирмеровской болезни следует отметить: гипербилирубинемию (в основном костномозговой природы) — с увеличенным выделением с фекалиями билирубиновых телец (до 800 мг в сутки); рост показателя сывороточных ферментов — таких как лактикодегидрогеназа (изофермент эритроидной природы), малико-6-фосфоглюконат и 2-гидроксибутиратдегидрогеназа (за счет неэффективности эритропоэза и повышения их активности в мегалобластах); некоторые сдвиги в белковом обмене (увеличивается выделение с мочой аминокислот, растет РОЭ, уменьшается гаптоглобин (в связи с расплавлением крови), также в жировом обмене (при этом уменьшаются альфа- и растут бета-липопротеиды, сокращается поглощение кишечником жирных кислот); нарушение гемостаза (в принципе легкое, за счет тромбоцитопении и понижения активности протромбина).
Что касается обмена железа нередко обнаруживается наличие завышенного количества железа в крови с общей невысокой способностью связывания, одновременно понижение поглощения железа кишечником.
В процессе диагностирования представляют значение определения метаболизма витамина В12.
В сыворотке уровень витамина В12 (определяемый микробиологическом путем или способом радиоактивных изотопов) в отдельных случаях значительно меньше критического — 100 пг/мл.
Поглощаемость кишечником витамина В12 определяется реакцией Шиллинга, которая, судя по леченным нами больным, предоставляет существенную информацию. Эта реакция заключается в назначении внурть небольшого количества радиоактивного витамина (0,5 uCi), а спустя 2 ч с помощью внутримышечного инъецирования еще 1000 мкг витамина В12 (чтобы воспрепятствовать связыванию поглощаемого 60СоВ12 и одновременно способствовать его удалению). В подобных условиях за сутки у человека в норме выделяются с мочой 10% введенной в организм радиоактивности, в то время как у страдающих бирмеровской болезнью — менее 2%.
Однако заключение, по которому неполноценность поглощения обусловлена отсутствием внутреннего фактора требует подтверждения повторным испытанием (спустя 2 недели) при одновременном введении ВФ для поправки результата (при бирмеровской болезни). К ведущим факторам погрешности относятся почечная и сердечная недостаточность, инфекционные заболевания и пр.
На практике лишь в редких случаях оказывается необходимым определение активности внутреннего фактора в желудочном соке или исследование в сыворотке антител против внутреннего фактора (серологическим методом или путем радиоактивных изтотопов).
Косвенным методом выявления недостатка В12 является определение выделения с мочой метилмалоновой кислоты (норма 1—7 мг в сутки); при бирмеровской болезни этот показатель растет до нескольких десятков или даже сотен мг/сутки (в частности при формах болезни с невропатией).
Реакция на суппрессию включения дезоксиуридина (дУ), при дефиците В12 или фолиевой кислоты, основывается на факте включения меченного тимидина в эритробласты (или стимулированные лимфоциты), преимущественно по сравнению с дезоксиуридином (которого метилирование не преобразовывает в тимидин); откорригировать это положение возможно добавлением недостающего витамина (Killman).
В текущей клинической практике диагноз болезни Бирмера можно заподозрить по данным анамнеза и клинического обследования. Выявление признаков мегалобластической анемии и неподдающейся гистамину ахилии желудка по существу обеспечивают диагностирование, при этом подтверждение правильности определения дает наступление межприступного периода после назначения специфической терапии.
Реакция Шиллинга применяется для подтверждения отсутствия внутреннего фактора, в частности у леченных лиц или в случаях неполной симптоматологии. Определение витамина в крови (равно как и выделения АММ) можно применять лишь в сложных случаях (например при подозрительной нервной симптоматологии, без анемии), при этом сыворотку отбирать до начала лечения и сохранить в замороженном состоянии.
Дифференциальная диагностика рассматривается в общих сведениях о мегалобластической анемии.
источник
Существует несколько видов патологий, связанных с нехваткой микроэлементов в организме. Одна из них — анемия Аддисона Бирмера. Это злокачественное течение болезни, выражающееся анемия в дефиците витамина В12 и фолиевой кислоты. Заболевание, встречающееся в 30 – 50 случаях на 10000 населения, больше подвержены этому недугу женщины, причем, в возрасте старше 50 лет риск развития болезни возрастает (возможно это связано с менопаузой).
Впервые анемия Аддисона Бирмера развивается при дефиците витамина B12, она была описана в 1855 году Аддисоном, позднее подтвердилась Бирмером, который изучил болезнь и дал подробное клиническое описание. Впоследствии, это состояние получило название по именам своих исследователей. Долгое время считалась заболеванием неизлечимым, протекающим тяжело и неудержимо. В настоящее время достаточно ясен патогенез заболевания, но этиология в большей мере остается лишь предположением.
Анемия Аддисона — Бирмера характеризуется наличием специфической триады нарушений в организме:
- Тяжелое течение гастрита по атрофическому типу. Происходит постепенное снижение функции железистого эпителия, слизистая инфильтрируется, замещается несвойственными данному органу клетками, выработка ферментов в крови резко сокращается или прекращается вовсе.
- Невозможность усвояемости витамина В12 и фолиевой кислоты. Оба компонента необходимы для построения клеток, с их помощью синтезируется ДНК и правильно формируется ядро клетки. При недостатке и того, и другого страдают, прежде всего, гемопоэз и нервная ткань.
- Развитие мегалобластного кроветворения. Это образование множества незрелых гранулоцитов крови, не способных нормально выполнять свои функции. В этом течение анемии Аддисона-Бирмера схоже со злокачественными болезнями крови.
Основным фактором, ведущим к развитию заболевания, причины анемии Аддисона Бирмера является атрофия слизистой оболочки желудка, в результате прекращается секреция (выработка) пепсиногена. А роль пепсиногена в организме такова, что он обеспечивает транспорт и всасывание цианкобаламина. Однако далеко не всегда атрофический гастрит ведет к развитию мегабластной анемии. Вероятно, для развития болезни должны совпасть несколько факторов.
Усвоение В12 и фолиевой кислоты может нарушиться из-за обширного воспаления слизистой желудка и подвздошного отела кишечника или поражения их злокачественными опухолями.
Пернициозная анемия в, немалой степени, является аутоиммунным заболеванием, так в сыворотке крови пациентов в 70 -75% случаев выявлены антитела к внутренним клеткам желудка. При проведении опытов над крысами, выяснилось, что подобные клетки ведут к атрофии желудочной железистой ткани. Подобные антитела присутствуют и в желудочном секрете. Аутоиммунный ответ с высокой долей вероятности можно считать наследственным фактором, так как некоторое количество антител против париетальных клеток желудка, а так же клеток эндокринной системы обнаруживаются у здоровых родственников.
Дополнительным, но не менее важным фактором является наследственная склонность к заболеваниям поджелудочной железы.
Образ жизни, ведущий к сбоям в иммунной системе, например, экспериментирование с жесткими принципами диеты, резкий переход на вегетарианство, неконтролируемый прием медицинских препаратов, нарушение дозировок в приеме лекарств. Что важно, в послевоенные голодные годы заболеваемость пернициозной анемией не возрастала, а значит, недоедание количественное и качественное можно отнести лишь к сопутствующим причинам.
Поражение кишечника некоторыми паразитическими микроорганизмами и чрезмерное развитие патологической кишечной микрофлоры.
Существуют разрозненные факты по описанию случаев заболеваемости мегалобластной анемией. Например: в северных районах это патология встречается чаще; есть указания на увеличение заболеваемости у людей, чья работа связана со свинцом и возможностью медленного отравления окисью углерода; после операции по удалению желудка, когда происходит тотальная ликвидация секреторной функции, анемия способна развиться спустя 5-7 лет; есть сведения о развитии мегабластной анемии, как результате токсического отравления при хроническом алкоголизме.
Симптомы анемии Аддисона-Бирмера выглядит следующими образом, нарушается свертываемость крови, образуются эритроцитарные клетки аномальных размеров, с разросшейся цитоплазмой, а их ядра, содержат мелкие включения.
Из-за критической нехватки витамина В12 возникает дефект в метаболизме фолиевой кислоты, участвующей в синтезе ДНК. Как результат, нарушается деление клеток и понижается уровень эритроцитов на периферии. Таки же количественные и качественные деформации происходят и с тромбоцитами. Костный мозг изменяет окраску, приобретает насыщенный алый цвет, в нем преобладают мегабластные незрелые клетки, которые по типу развития напоминают злокачественное течение заболеваний крови.
Витамин В12 используется организмом не только для гемопоэза, но и для обеспечения нормальной работы нервной системы. При его недостатке наблюдается дистрофия в нервных окончаниях позвоночного столба.
Со стороны пищеварительной системы выявляется атрофия слизистой оболочки неба, глотки, пищевода, желудка и кишечника. Возможно образование полипов, небольшое увеличение печени. Клиника течения болезни анемии Аддисона-Бирмера проявляется постепенно: периодически возникает сильная слабость, хроническая усталость, усиливаются приступы головокружения, возникает шум в ушах.
Возникающие симптомы анемии Аддисона Бирмера можно разделить на проявления:
- со стороны нервной системы: нарушается регуляция движений, появляется парестезия; возникают боли в межреберье; иногда наблюдается поражение зрительного и слухового нерва; нарушение памяти.
- со стороны пищеварительного тракта: глоссит, характеризующийся синдромом «лакированного языка» и болезненные ощущения в языке; тошнота, тяжесть в области эпигастрия, формирование отвращения к пище, ухудшение вкусовых ощущений; увеличение печени, реже – селезенки, появление желтушности склер, слизистых оболочек;
- внешние проявления: холодные руки и ноги, бледная с желтоватым оттенком кожа, формируется характерный синдром анемии Аддисона-Бирмера – лицо восковой куклы; одутловатость лица, значительные отеки; вялость, сонливость.
- со стороны сердца: появление симптомов одышки, болей, дистрофических изменений в миокарде.
Диагностика анемии складывается из нескольких этапов.
Визуальный осмотр выявляет: бледные кожные покровы, желтушный оттенок склер, пигментные пятна на лице, руках и теле. Характерную картину дает осмотр ротовой полости, на начальной стадии заболевания язык болезненный, покрыт мелкими трещинками. В разгар болезни, язык приобретает алый цвет и отечность, выглядит, словно покрытый лаком. При проведении пальпации обнаруживается небольшое увеличение печени и выступление ее за край ребра. Селезенка увеличивается в размерах у небольшого количества пациентов. Проведение неврологических проб выявляет изменение чувствительности в конечностях.
При диагностике анемии Аддисона-Бирмера анализ крови играет ключевую роль. Проводится тщательное исследование периферической крови, где выявляется значительное повышение эритроцитарного объема крови, при этом количество ретикулоцитов резко снижено. Обнаруживается наличие гиперхромных эритроцитов. Главным признаком мегабластной анемии можно считать наличие гиперсегментарных нейтрофилов (имеющих пять и более сегментов в ядре). У человека относительно здорового таких клеток встречается в пределах 2%, у страдающих злокачественной анемией, количество гиперсегментарных нейтрофилов поднимается выше 5%.
Не менее важным является исследование костного мозга при анемии. В нем обнаруживается мегалобластный рост клеток – это остановившиеся в своем развитии клетки, предшествующие эритрацитам. Они аномально увеличены в размерах, деформированы, с заметной разницей в уровне развития ядра и цитоплазмы. Вообще, непродуктивный эритропоэз – характерная черта мегабластной анемии. Подавляющее число незрелых и деформированных клеток эритроцитов (мегабластов) разрушаются еще в костном мозге, не выходя в кровоток. При прогрессировании заболевания, количество ретикулоцитов продолжает падать, понижается количество тромбоцитов, при этом происходит их деформация.
Инструментальная диагностика включает в себя: исследование желудочного сока, где, как правило, выясняется снижение кислотности или полное ее отсутствие. Зато присутствует значительное количество слизи, схоже по составу с кишечной. Проводится эндоскопическое исследование, где явно наблюдается обширная атрофия слизистой оболочки желудка, часто называемая «перламутровыми бляшками», потеря секреторных клеток. К сожалению, даже в период ремиссии синтез пепсиногена не восстанавливается.
Часто проводят гистологическое исследование тканей, так как одной из причин, способных вызвать анемию Аддисона Бирмера, являются злокачественные новообразования.
Таким больным требуется дополнительная консультация узких специалистов: невролога, эндокринолога, кардиолога, иммунолога.
Обязательным методом диагностики является проведение пробы Шиллинга. Этот метод нацелен на разграничение фолиево-дефицитной анемии от В12-дефицитной анемии для того, чтобы выявить первопричину, и наметить правильное лечение. Для этого измеряют их концентрацию в сыворотке крови. Норма фолиевой кислоты – 5-20нг/мл, норма В12 – 150-900нг/мл. Показатели ниже этих рамок свидетельствуют о наличии дефицита этих компонентов в организме. Чтобы провести пробу, больному вводят витамин В12 внутримышечно, через достаточное время определяют его концентрацию в моче, малое количество при В12-дефицитной анемии, максимальное – при фолиево-дефицитной.
Дефицит фолиевой кислоты в организме встречается чаще в молодом возрасте и не имеет сопутствующими факторами атрофию секреторной функции желудка и наличие неврологических симптомов. Она благоприятно реагирует на введение фолиевой кислоты перорально и лучше поддается лечению. При обследовании пациентов с В12-дефицитной анемией важно установить первопричину заболевания.
Лечение анемии Аддисона Бирмера имеет свои особенности. Выбор лекарственного препарата зависит от причины заболевания. Фолиево-дефицитная анемия возникает из-за нарушения ее всасывания в кишечнике. Частой причиной этого вида анемии является хронический алкоголизм, причем особенно опасен он в период беременности.
Недостаток фолиевой кислоты более благоприятен для организма в плане лечения, так как при нем не страдает секреторная функция желудка, и введение перорально терапевтических доз препарата дает быстрый эффект.
Фолиевая кислота выпускается как отдельный препарат в форме таблеток или раствора для инъекций, так и в составе комплексных витаминов. Побочные эффекты при приеме фолиевой кислоты при лечении анемии возникают редко, но возможны аллергические реакции на внутримышечное введение препарата.

В случае с дефицитом витамина В12 в организме, применение таблетированных форм не обоснованно, так как наличие атрофического гастрита сводит подобное лечение к нулю. В лечении этого вида анемии применяются внутримышечные или подкожные инъекции цианокобаламина. Внутривенное введение препарата опасно. Цианокобаламин – это жидкость розоватого цвета, в ампулах по 1мл, иногда его применение может вызвать аллергическую сыпь. Лекарство вводят ежедневно в дозе до 500мгк, в течение 6 недель, дополнительно вводят фолиевую кислоту в дозе до 100мгк.
При легкой или средней степени тяжести анемии, лечение, возможно, отложить до окончания полной диагностики и выявления причин дефицита. При выраженных неврологических нарушениях и значительных изменениях картины крови лечение начинают немедленно.
Часто, внешние признаки анемии Аддисона-Бирмера исчезают уже в первые дни лечения. Стихают боли в языке и ротовой полости, появляется аппетит, проходит слабость, восстанавливается зрение и слух. Через несколько суток восстанавливается ретикулоцитоз, количество мегабластов в костном мозге резко сокращается. Восстановление кроветворения происходит обычно через 1 -2 месяца. Тяжелые неврологические нарушения могут сохранять свою симптоматику в течение нескольких месяцев, а могут полностью и не исчезнуть вовсе.
При тяжелой атрофии слизистой желудка и при В12-дефицитной анемии препараты, содержащие витамин В12 приходится принимать всю жизнь. Пациент должен знать, что отказ от поддерживающей терапии влечет за собой рецидив мегалобластной анемии. Как правило, переболевшие анемией Аддисона-Бирмера ставятся на диспансерный учет и находятся под регулярным наблюдением. Поддерживающие дозы вводятся короткими курсами по назначению врача и под постоянным контролем картины крови.
В целях профилактики анемии фолиевую кислоту назначают лишь определенным группам граждан. Например, беременным женщинам для предотвращения патологий спинного мозга у плода, кормящим мама, для правильного развития ребенка. Пожилым людям при некоторых формах анемии, а так же пациентам, находящимся в коматозном состоянии. Во всех остальных случаях, достаточно того количества, которое поступает с пищей в обычном рационе.
Витамин В12 в целях профилактики назначают лишь при возможном его дефиците, например, при строгом вегетарианстве или тотальном удалении желудка. Цианокобаламин имеет широкую репутацию общеукрепляющего препарата, что совершенно не доказано, но его часто назначают при общем истощении, утомляемости и повышенной усталости как тонизирующее средство. Учитывая необходимость витаминов группы В в регуляции работы нервной системы, возможно применение цианокоболамина для лечения воспаления тройничного нерва и прочих нейропатиях.
Лечение анемии Аддисона Бирмера любыми витаминными препаратами должно быть строго нацеленным. И только если есть подозрение на дефицит нескольких витаминных компонентов, можно принимать поливитаминные комплексы.
источник
Пернициозная анемия – нарушение красного ростка кроветворения, обусловленное недостатком в организме цианокобаламина (витамина В12). При В12-дефицитной анемии развивается циркуляторно-гипоксический (бледность, тахикардия, одышка), гастроэнтерологический (глоссит, стоматит, гепатомегалия, гастроэнтероколит) и неврологический синдромы (нарушение чувствительности, полиневриты, атаксия). Подтверждение пернициозной анемии производится по результатам лабораторных исследований (клинического и биохимического анализа крови, пунктата костного мозга). Лечение пернициозной анемии включает сбалансированную диету, внутримышечное введение цианокобаламина.
Пернициозная анемия – разновидность мегалобластной дефицитной анемии, развивающаяся при недостаточном эндогенном поступлении или усвоении в организме витамина В12. «Пернициозная» в переводе с латинского означает «опасная, гибельная»; в отечественной традиции такая анемия раньше называлась «злокачественным малокровием». В современной гематологии синонимами пернициозной анемии также служат В12-дефицитная анемия, болезнь Аддисона-Бирмера. Заболевание чаще возникает у лиц старше 40-50 лет, несколько чаще у женщин. Распространенность пернициозной анемии составляет 1%; вместе с тем, дефицитом витамина В12 страдает около 10% пожилых людей в возрасте старше 70 лет.
Ежесуточная потребность человека в витамине B12 равняется 1-5 мкг. Она удовлетворяется за счет поступления витамина с пищей (мясом, кисломолочными продуктами). В желудке под действием ферментов витамин В12 отделяется от пищевого белка, однако для усвоения и всасывания в кровь он должен соединиться с гликопротеином (фактором Касла) или другими связывающими факторами. Всасывание цианокобаламина в кровоток происходит в средней и нижней части подвздошной кишки. Последующий транспорт витамина В12 к тканям и гемопоэтическим клеткам осуществляется белками плазмы крови — транскобаламинами 1, 2, 3.
Развитие В12-дефицитной анемии может быть связано с двумя группами факторов: алиментарными и эндогенными. Алиментарные причины обусловлены недостаточным поступлением витамина В12 с пищей. Это может происходить при голодании, вегетарианстве и диетах с исключением животного белка.
Под эндогенными причинами подразумевается нарушение усвоения цианокобаламина вследствие дефицита внутреннего фактора Касла при его достаточном поступлении из вне. Такой механизм развития пернициозной анемии встречается при атрофическом гастрите, состоянии после гастрэктомии, образовании антител к внутреннему фактору Касла или париетальным клеткам желудка, врожденном отсутствии фактора.
Нарушение абсорбции цианокобаламина в кишечнике может отмечаться при энтерите, хроническом панкреатите, целиакии, болезни Крона, дивертикулах тонкого кишечника, опухолях тощей кишки (карциноме, лимфоме). Повышенное расходование цианокобаламина может быть связано с гельминтозами, в частности, дифиллоботриозом. Существуют генетические формы пернициозной анемии.
Всасывание витамина В12 нарушено у пациентов, перенесших резекцию тонкой кишки с наложением желудочно-кишечного анастомоза. Пернициозная анемия может быть ассоциирована с хроническим алкоголизмом, применением некоторых лекарственных средств (колхицина, неомицина, пероральных контрацептивов и др.). Поскольку в печени содержится достаточный резерв цианкобаламина (2,0-5,0 мг), пернициозная анемия развивается, как правило, только лишь спустя 4-6 лет после нарушения поступления или усвоения витамина В12.
В условиях недостаточности витамина В12 возникает дефицит его коферментных форм – метилкобаламина (участвует в нормальном протекании процессов эритропоэза) и 5-дезоксиаденозилкобаламина (участвует в метаболических процессах, протекающих в ЦНС и периферической нервной системе). Недостаток метилкобаламина нарушает синтез незаменимых аминокислот и нуклеиновых кислот, что приводит к расстройству образования и созревания эритроцитов (мегалобластному типу кроветворения). Они принимают форму мегалобластов и мегалоцитов, которые не выполняют кислородтранспортную функцию и быстро разрушаются. В связи с этим количество эритроцитов в периферической крови существенно сокращается, что приводит к развитию анемического синдрома.
С другой стороны, при дефиците кофермента 5-дезоксиаденозилкобаламина нарушается обмен жирных кислот, в результате чего накапливаются токсичные метилмалоновая и пропионовая кислоты, оказывающие непосредственное повреждающее действие на нейроны головного и спинного мозга. Кроме этого, нарушается синтез миелина, что сопровождается дегенерацией миелинового слоя нервных волокон – этим обусловлено поражение нервной системы при пернициозной анемии.
Тяжесть течения пернициозной анемии определяется выраженностью циркуляторно-гипоксического (анемического), гастроэнтерологического, неврологического и гематологического синдромов. Признаки анемического синдрома неспецифичны и являются отражением нарушения кислородтранспортной функции эритроцитов. Они представлены слабостью, снижением выносливости, тахикардией и ощущением сердцебиения, головокружением и одышкой при движении, субфебрилитетом. При аускультации сердца может выслушиваться шум «волчка» или систолические (анемические) шумы. Внешне отмечается бледность кожи с субиктеричным оттенком, одутловатость лица. Длительный «стаж» пернициозной анемии может приводить к развитию миокардиодистрофии и сердечной недостаточности.
Гастроэнтерологическими проявлениями В12-дефицитной анемии служат пониженный аппетит, неустойчивость стула, гепатомегалия (жировая дистрофия печени). Классический симптом, выявляемый при пернициозной анемии – «лакированный» язык малинового цвета. Характерны явления ангулярного стоматита и глоссита, жжение и болевые ощущения в языке. При проведении гастроскопии обнаруживаются атрофические изменения слизистой желудка, которые подтверждаются эндоскопической биопсией. Желудочная секреция резко снижается.
Неврологические проявления пернициозной анемии обусловлены поражением нейронов и проводящих путей. Больные указывают на онемение и скованность конечностей, мышечную слабость, нарушение походки. Возможно недержание мочи и кала, возникновение стойкого парапареза нижних конечностей. Осмотр невролога выявляет нарушение чувствительности (болевой, тактильной, вибрационной), повышение сухожильных рефлексов, симптомы Ромберга и Бабинского, признаки периферической полиневропатии и фуникулярного миелоза. При В12-дефицитной анемии могут развиваться психические нарушения – бессонница, депрессия, психозы, галлюцинации, деменция.
Кроме гематолога, к диагностике пернициозной анемии должны быть привлечены гастроэнтеролог и невролог. Дефицит витамина В12 (менее 100 пг/мл при норме 160-950 пг/мл) устанавливается при проведении биохимического исследования крови; возможно обнаружение Ат к париетальным клеткам желудка и к внутреннему фактору Касла. Для общего анализа крови типична панцитопения (лейкопения, анемия, тромбоцитопения). При микроскопии мазка периферической крови обнаруживаются мегалоциты, тельца Жолли и Кэбота. Исследование кала (копрограмма, анализ на яйца глистов) могут выявлять стеаторею, фрагменты или яйца широкого лентеца при дифиллоботриозе.
Проба Шиллинга позволяет определить нарушение всасывания цианокобаламина (по экскреции с мочой меченного радиоактивным изотопом витамина В12, принятого внутрь). Пункция костного мозга и результаты миелограммы отражают характерное для пернициозной анемии увеличение числа мегалобластов.
Для определения причин нарушения абсорбции витамина В12 в ЖКТ проводится ФГДС, рентгенография желудка, ирригография. В диагностике сопутствующих нарушений информативны ЭКГ, УЗИ органов брюшной полости, электроэнцефалография, МРТ головного мозга и др. В12-дефицитную анемию необходимо отличать от фолиеводефицитной, гемолитической и железодефицитной анемии.
Установление диагноза пернициозной анемии означает, что пациент будет нуждаться в пожизненном патогенетическом лечении витамином В12. Кроме этого, показано регулярное (каждые 5 лет) проведение гастроскопии для исключения развития рака желудка.
С целью восполнения дефицита цианокобаламина назначаются внутримышечные инъекции витамина В12. Требуется коррекция состояний, приведших к В12-дефицитной анемии (дегельминтизация, прием ферментных препаратов, хирургическое лечение), а при алиментарном характере заболевания — диета с повышенным содержанием животного белка. При нарушении выработки внутреннего фактора Касла назначаются глюкокортикоиды. К гемотрансфузиям прибегают только при анемии тяжелой степени или признаках анемической комы.
На фоне терапии пернициозной анемии показатели крови обычно нормализуются через 1,5-2 месяца. Дольше всего (до 6 мес.) сохраняются неврологические проявления, а при поздно начатом лечении они становятся необратимыми.
Первым шагом на пути предотвращения пернициозной анемии должно стать полноценное питание, обеспечивающее достаточное поступление в организм витамина В12 (употребление мяса, яиц, печени, рыбы, молочных продуктов, сои). Необходима своевременная терапия патологий ЖКТ, нарушающих усвоение витамина. После хирургических вмешательств (резекции желудка или кишечника) необходимо проведение поддерживающих курсов витаминотерапии.
Больные с В12-дефицитной анемией входят в группу риска по развитию диффузного токсического зоба и микседемы, а также рака желудка, поэтому нуждаются в наблюдении эндокринолога и гастроэнтеролога.
источник