Актиномикоз легких представляет собой микотическое поражение легочной ткани, вызванное лучистыми грибками Actinomicetes.
Актиномицеты постоянно находятся в ротовой полости и верхних дыхательных путях у здорового человека, но в обычных условиях болезнь не вызывают. Они распространены повсеместно, например, в почве их количество составляет около 65 % всех микроорганизмов. Считается, что лучистые грибки имеют свойства как грибов, так и микробов. Они быстро приспосабливаются к условиям окружающей среды, устойчивы к ультрафиолетовому облучению и умеренному температурному воздействию.
Актиномикоз является неконтагиозным заболеванием и развивается только при снижении общей резистентности. Этому способствуют:
- тяжелые ОРВИ;
- хронические заболевания респираторного тракта (абсцедирование легочной ткани, бронхоэктатическая болезнь или эмпиема плевры);
- туберкулез;
- сахарный диабет;
- нарушение целостности верхних дыхательных путей.
Проникновение возбудителя болезни в паренхиму легких может осуществляться аэрогенным путем, реже – через кровь или лимфу. В месте его внедрения образуется гранулема специфического характера. В патологическом очаге скапливаются клетки иммунной системы, происходит интенсивный фагоцитоз. Однако его процесс не завершается, и макрофаги погибают. Вокруг них создаются гранулемы второго и третьего порядка. Это приводит к облитерации мелких бронхов в зоне поражения и разрастанию соединительной ткани.
В клинической практике выделяют три основные формы актиномикоза:
- Бронхиальная.
- Бронхопульмональная.
- Плевропульмональная.
Любая из них может развиваться в результате первичной трансбронхиальной инвазии актиномицет или формироваться на фоне хронической патологии бронхолегочной системы (вторичный актиномикоз).
Виды первичного актиномикоза:
- бронхиальный (протекает в виде хронического бронхита);
- инфильтративно-легочный;
- солитарный (специфическая гранулема образуется на фоне обтурированного бронхиального сегмента);
- легочно-плевральный (поражает легкие, плевру и грудную стенку);
- долевой (поражается доля легкого);
- распространенный.
Данная патология имеет длительное течение с чередование периодов ремиссии и обострения.
При локализации патологического процесса в центральной части легкого клиническая картина является достаточно скудной:
- У таких лиц часто повторяются острые респираторные инфекции с сухим кашлем.
- Иногда при кашле отделяется мокрота с примесью крови.
Постепенно заболевание прогрессирует и появляется:
- субфебрильная температура;
- боль в грудной клетке, не имеющая четкой локализации;
- слабость;
- повышенная утомляемость;
- потеря массы тела;
- снижение аппетита.
Если актиномикомы располагаются субплеврально, то болезнь имеет более тяжелое течение:
- Боль в грудной клетке, усиливающаяся при кашле и глубоком дыхании, иногда становится мучительной.
- По вечерам температура тела достигает высоких цифр.
По мере прогрессирования болезни симптомы нарастают:
- кашель становится надсадным с отделением слизисто-гнойной мокроты;
- больные худеют (вплоть до кахексии);
- по ночам их беспокоят проливные поты;
- появляется выраженная бледность кожных покровов;
- половина грудной клетки на стороне поражения уменьшается в размерах и отстает в акте дыхания.
При длительном существовании специфические гранулемы могут нагнаиваться и абсцедироваться, что проявляется резким ухудшением самочувствия больных и гектической лихорадкой. Прорыв содержимого абсцесса может осуществляться в крупный бронх или полость плевры.
- В первом случае отходит большое количество мокроты с характерным запахом земли и привкусом меди.
- Во втором случае развивается пиопневмоторакс с колабированием части легкого.
С течением времени патологический процесс при актиномикозе способен распространяться на мягкие ткани грудной стенки, образуя там абсцессы и инфильтраты, а также грудину, ребра и позвонки. Нередко актиномикомы появляются и в других органах, чаще в сердце и головном мозге.
Поставить диагноз «актиномикоз» не так просто, как может показаться на первый взгляд. Врач может заподозрить его у больного на основании клинических проявлений и данных объективного обследования. Для подтверждения диагноза необходимы:
- результаты рентгенографии органов грудной клетки;
- выявление друз и мицелия актиномицет в мокроте, промывных водах бронхов или биопсийном материале.
Рентгенологические данные могут иметь определенные различия и зависят от формы и стадии болезни:
- При центральной локализации патологического процесса на рентгенограмме выявляются прикорневые инфильтраты разного размера.
- При субплевральных очагах выявляется только утолщение участка плевры.
- В стадии инфильтрации над поверхностью легких определяется снижение прозрачности легочного рисунка, затем плотность затенения возрастает, и становится виден инфильтрат неправильной формы с размытыми контурами и радиальной тяжистостью по периферии.
- Стадия абсцедирования характеризуется наличием очагов деструкции в пораженном легком с перифокальным воспалением и усилением легочного рисунка в здоровом легком.
- Нередко после прорыва абсцесса в паренхиме легких формируются плевролегочные полости с горизонтальным уровнем жидкости.
Нахождение мицелия актиномицет в мазках из гнойного отделяемого имеет большое значение для постановки диагноза, в том время как его выявление в мокроте не может подтвердить актиномикоз, так как в нее попадают и сапрофиты из ротовой полости.
Дифференциальная диагностика актиномикоза проводится с:
Лечение актиномикоза должно начинаться как можно раньше. Это поможет избежать деструктивных изменений легочной ткани (хронических абсцессов, кист, бронхоэктазов, плеврально-легочных полостей) и пневмофиброза.
Основными направлениями лечения актиномикоза легких являются:
- Полноценное и высококалорийное питание.
- Назначение специфических иммунологических препаратов – актинолизата и актиномицетной поливалентной вакцины.
- Антибактериальная терапия (для подавления бактериальной флоры).
- Санация трахебронхиального дерева.
- Дренирование гнойных очагов.
- Дезинтоксикационная терапия.
- Применение иммуномодуляторов.
- Физиотерапия.
- Хирургическое вмешательство (выполняется после стабилизации процесса с целью ликвидации остаточных явлений актиномикоза).
Прогноз относительно выздоровления у больных актиномикозом благоприятный при условии своевременного выявления болезни и адекватного лечения. После окончания курса лечебных мероприятий больные находятся на диспансерном наблюдении в течение 2 лет, а при сопутствующем туберкулезе или сахарном диабете еще более длительный период.
Применение современных методов лечения актиномикоза обеспечивает полное выздоровление пациента. Однако длительное течение болезни не проходит бесследно. У многих из них остаются необратимые изменения в легочной ткани, которые не всегда возможно удалить хирургическим путем.
Специалист клиники «Московский доктор» рассказывает об актиномикозе:
источник

Патогенез и патологическая анатомия. Заболевание возникает в результате экзогенного инфицирования и вследствие активизации эндогенной инфекции (сапрофитирующих в организме человека актиномицетов). Развитию болезни способствует понижение иммунологической резистентности на фоне хронических заболеваний, применения цитостатиков, глюкокортикостероидов и иных иммуносупрессоров, после беременности и родов, а также травматизация тканей.
Из очагов первичной локализации возбудители гематогенно или лимфогенно распространяются в различные органы, обусловливая возникновение метастатических очагов актиномикоза: В развитии болезни имеют значение специфическая сенсибилизация к актиномицетам и присоединение гноеродной флоры.
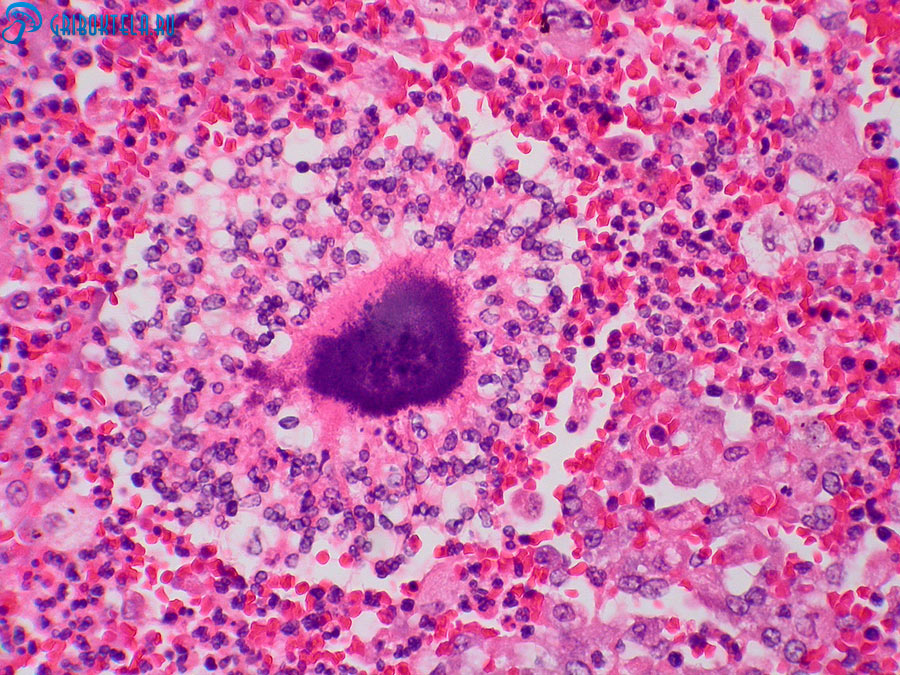
Патоморфологической основой актиномикоза является специфическая гранулема — актиномикома, начальная стадия которой формируется из молодой соединительной ткани и полинуклеаров. По мере развития в центральной части гранулемы возникает некроз, наблюдается фиброз окружающих тканей, появляются ксантомные клетки. Рубцовая ткань пронизана гнойниками и напоминает губку. В дальнейшем появляются эпителиоидные клетки, лимфоциты и плазмоциты, происходит гиалинизация рубцов. В центральной части актиномикомы можно обнаружить друзы актиномицетов окруженные лейкоцитами и подвергающиеся в дальнейшем фагоцитозу, кальцинозу или превращению в стекловидные шары.
Клиника. Единой классификации актиномикоза не создано. Инкубационный период болезни составляет от нескольких дней до ряда лет. Различают первичный и вторичный актиномикоз с локализацией процесса в легких (10-20 %), желудочно-кишечном тракте, мочеполовых органах, центральной нервной системе, костях, в коже или имеющие генерализованный характер.
В случае центральной локализации очага в легких (бронхопульмональная форма) клинические проявления могут быть нехарактерными и маловыраженными. По мере прогрессирования болезни появляются кашель, тупые боли в области груди, неправильная лихорадка, повышенная потливость. В дальнейшем выделяется слизисто-гнойная мокрота, часто с прожилками крови, содержащая плотные зерна — друзы актиномицетов.
При субплевральной локализации актиномикомы (плевропульмональная форма) клинические признаки появляются рано и выражены более ярко: отмечаются боли в груди соответственно локализации очага, чаще в боковых отделах и подлопаточной области, усиливающиеся при кашле и глубоком вдохе, а также при передвижении больного; характерны сухой мучительный кашель, неправильная лихорадка. При аускультации выявляются шум трения плевры, сухие и разнокалиберные влажные хрипы. По мере формирования абсцесса состояние больных ухудшается, они теряют массу тела. После прорыва абсцесса в просвет бронха выделяется обильная слизисто-кровянистая мокрота с плотными зернами-друзами. В случае прорыва абсцесса в плевральную полость развивается осумкованный плеврит.
Возможно поражение средостения с последующим распространением воспаления в забрюшинное пространство. Могут наблюдаться абсцессы в мягких тканях грудной клетки, остеолизис и периоститы ребер и позвонков с последующим образованием свищей, из которых выделяется густой гной с плотными зернами. Наблюдается гнойное поражение молочной железы, перикарда и сердца.
Рентгенологическое исследование в ранней стадии выявляет очаговые инфильтраты вокруг бронхов и сосудов, увеличение медиастинальных лимфатических узлов и содружественное поражение ребер или позвонков; характерно уплотнение плевры. Процесс может ограничиваться одним сегментом или захватывать целую долю.
Течение болезни длительное, при отсутствии лечения развиваются кахексия и анемизация больных.
Диагноз актиномикоза основан на выявлении характерных клинико-инструментальных признаков болезни и дополняется выявлением друз актиномицетов в мокроте или гнойном отделяемом из свищей при исследовании наливных препаратов и при окраске их по Цилю — Нильсену. Серологическая диагностика разработана недостаточно.
Дифференциальный диагноз проводят с туберкулезом легких, опухолями и иными пневмомикозами.
Профилактика не разработана.
Лечение. Основой терапии актиномикоза является иммуноантибиотикотерапия. Больным назначают актинолизат, поливалентную актиномицетную вакцину, вводимые внутрикожно или внутримышечно в постепенно возрастающих дозах на протяжении 1-3 месяцев в виде повторных курсов с интервалами 1 мес. Одновременно применяют сульфаниламидные препараты (сульфидин, сульфапиридин и др.), а в период обострения — антибиотики. Показаны гемотрансфузии, назначение биогенных стимуляторов. По показаниям применяют хирургическое лечение.
источник
Инфекционное хроническое заболевание актиномикоз легкого вызывает грибок Actinomyces. Он образован множественными нитями, между собой, объединенных в друзы. Характерны булавовидные утолщения. Проникает лучистый грибок в организм человека несколькими путями. В основном грибок оказывается в дыхательных путях с вдыхаемым воздухом, который, как правило, содержит растительную пыль, в которой находятся актиномицеты.
Бывает, что грибок находят в мазках, взятых из полости рта, и не только. Обнаруживается он и в полости кариозных зубов. Такие лучистые грибы, как актиномицеты, вполне способны поражать соседние органы, распространяясь постепенно и на рядом находящиеся здоровые ткани.
Грибок, непосредственно в легкие, может быть занесен током крови. Подобный вид продвижения инфекции носит название — милиарное обсеменение. Для сапрофитов свойственно метастазирование по кровеносным сосудам.
При актиномикозе, согласно статистике, ткани легкого повреждаются у одного из шести пациентов. От грибковой инфекции, как обычно, страдают нижние отделы легких. В процессе изучения характерных признаков течения заболевания была выявлена тенденция распространения инфекции, а именно, было выявлено, что актиномицеты из легких либо плевры способны проникать на кожные покровы грудной клетки и мышцы.
Заболевание, на начальных стадиях, имеет все признаки бронхита, наблюдается выделение малого количества слизистой или слизисто-гнойной мокроты. Также происходит усиление кашля при прогрессировании процесса на легочную ткань. Появляется одышка, повышается температура тела, происходит обильное потоотделение, количество выделяемой мокроты растет, к тому же, в грудной клетке усиливается при вдохе боль.
Легочная ткань в очагах инфильтрации нагнаивается, при этом появляются полости. Налицо — картина абсцесса легкого.
Втягивание в патологический процесс плевры вызывает у заболевшего жгучую боль. Далее наблюдается поражение стенки грудной клетки. Актиномикоз часто проявляется образованием под кожей инфильтратов сине-багрового цвета, довольно плотных, размягчающихся с возникновением гноящихся свищей, а также и разрушением ребер.
Над инфильтрированными участками легких, при физическом обследовании, отмечаются притупление перкуторного звука, дыхание ослаблено. Наблюдаются у больного сухие и влажные хрипы. В крови обнаруживают увеличение СОЭ и нейтрофильный лейкоцитоз. На фоне всех проявлений болезни происходит постепенное истощение организма. Гнойный процесс длительного характера оказывается причиной амилоидоза внутренних органов.
Специалисты при постановке диагноза сталкиваются с определенными трудностями. Это происходит в связи с отсутствием каких-либо отличительных признаков заболевания на первых порах. При легочном нагноении проводят лабораторное исследование, которое собственно и помогает выявить в мокроте друзы грибка.
При дифференциации с туберкулезом отличительным признаком актиномикоза является место сосредоточения инфекционного процесса. Как правило, грибками затронута одна сторона легкого, обычно нижняя доля. В мокроте пациента при этом не выявляется эластических волокон. В крови обнаруживается высокий лейкоцитоз.
Рентгенологическая картина малохарактерная в начальных стадиях заболевания, может рассматриваться, как хроническая пневмония или абсцесс. Предположить врачу наличие актиномикоза легких у больного помогут такие признаки, как изменение ребер в области инфильтрации, утолщение медиастинальной или костальной плевры, небольшие изменения со стороны бронхиального дерева. Эти же признаки дают повод провести целенаправленный диагностический поиск.
Довольно часто диагноз определяют гистологически, выполненяя резекции при подозрении на опухоль. Материал для исследования рекомендуется получать в анаэробных условиях.
Применяемые лабораторные тесты показывают воспалительный неспецифический характер заболевания. При формалиновой фиксации для распознавания видов внутри гранул используется иммунофлюоресценция.
Отметим, что диагностика, нуждается в комбинации определенных факторов, среди которых и выявление в гнойном материале пораженной ткани серных гранул, и высев культуры.
Гигиена полости рта должна носить обязательный и регулярный характер. Также важным аспектом является своевременное лечение зубов, воспалительных изменений слизистой оболочки полости рта и миндалин. Особой профилактики не существует. В очаге заболевания никаких особых мероприятий не проводят.
Эффективность лечения актиномикоза легких проявляется на первой стадии заболевания. Дальнейшие же перспективы болезни, на второй и третьей стадии, специалисты оценивают с осторожностью.
Из медикаментов рекомендуются пенициллины, также предлагается специфическая иммунотерапия. Больным назначают переливание крови, применяются высокие дозы йодистого калия. В некоторых случаях предлагается рентгенотерапия, а в случае необходимости и местное хирургическое вмешательство.
Лечение каждому заболевшему подбирают индивидуально. Выбор при актиномикозе такого препарата, как пенициллин, опирается больше на экстенсивном клиническом опыте, которому, без малого, свыше 50 лет.
В случае аллергии к пенициллинам используют: эритромицин, тетрациклин, клиндамицин, миноциклин. Данные препараты выступают как альтернативные средства.
Из последних антимикробных средств: цефтриаксон, имипенем/циластатин.
Кардинальное хирургическое вмешательство рекомендовано во время стабилизации процесса, при определении границ очага поражения, отрицательных результатов консервативного лечения, ликвидации остаточных явлений актиномикоза, мешающих полному излечению. К ним относятся кисты и бронхоэктазы. Больные после выздоровления не менее 2 лет должны наблюдаться диспансерно.
Нелеченый торакальный актиномикоз приводит, в конце концов, к фатальным последствиям. Напротив же, лечение приводит к благоприятному прогнозу в 90% случаев.
Больные, имевшие обширный торакальный или абдоминальный актиномикоз, несмотря на хирургическое вмешательство, не должны получать короткие курсы терапии. После операции, непрофессиональная антибактериальная терапия, может спровоцировать осложнения, как эмпиема и образование бронхоплевральных свищей.
При своевременной терапии прогноз актиномикоза легкого вполне благоприятный. Но, в случае прогрессирования в легких необратимых изменений, устранение лучисто-грибковой инфекции не свидетельствует о полной медицинской реабилитации.
источник
Актиномикозы и нокардиальные инфекции легких
Orhah Yildiz and Mehmet Doganay
Actinomycoses and Nocardia pulmonary infections
Current opinion in pulmonary medicine 2006, 12:228-234.
Легочный актиномиокоз и нокардиоз редко рассматривают в дифференциальной диагностике легочных заболеваний, поскольку спектр их клинических признаков подобен проявлениям других гранулематозов или новообразований, а также в связи с тем, что существует возможность сосуществования этих инфекций с другими патологическими процессами в легких. Даже среди опытных врачей, несмотря на знание об этих заболеваниях, случается задержка в их диагностики или происходит установление ошибочного диагноза, такого как туберкулез, легочный абсцесс или рак легкого [1]. В этой статье рассмотрены эпидемиология, клиника, диагностика и лечение этих заболеваний. Рост осведомленности врачей об этих инфекциях поможет улучшить их диагностику и предотвратить нежелательные осложнения, включая ненужное оперативные вмешательства с целью диагностики при персистирующих легочных поражениях.
Актиномикоз легких – редкое заболевание. Его обычно наблюдали как вторичную и локализованную инфекцию нередко с вовлечение легких, особенно при наличии резидуальных полостей или бронхоэктазов.
Члены рода Actinomyces – факультативные анаэробные грам-положительные, неспорообразующие прокариотические бактерии, относящиеся к семейству Actinomycaetaceae . Представители этого семейства являются комменсалам ротоглотки человека, желудочно-кишечного тракта и женских половых органов. Актиномикоз чаще всего вызывают такие виды как А ctinomyces israelii , другие встречаются значительно реже и включают комплекс A. naeslundii/viscosus , A. odontolyticus, A. meyeri и A. gerencseriae [1-3]. В зависимости от локализации поражения, большинство актиномических инфекций по сути своей являются полимикробными [4].
Актиномикоз – редкая инфекция, встречающаяся в год у одного из 300 000 человек и наблюдающаяся у людей всех возрастов [5,6]. Пик случаев заболевания приходится на средний возраст. Практически все исследования показывают, что мужчины болеют чаще, чем женщины в соотношении 3:1 [4,6,7]. Легочная форма актиномикоза составляет приблизительно 15% всех заболеваний, хотя иногда ее оценивают и свыше 50% [2,5,8]. Более высокая частота легочного актиномикоза описана у больных с предлежащими респираторными заболеваниями, такими как эмфизема, хронический бронхит, бронхоэктазы, но таких наблюдений немного [1,6]. Алкоголизм, плохая гигиена полости рта и ассоциированные заболевания зубов тоже повышают риск. Встречаемость всех форм актиномикоза в последние три четыре десятилетия падает, особенно в развитых странах. Проявления легочного актиномикоза также меняются. По сравнению с преантибиотической эрой появляются менее агрессивные случаи [1,2] .
Актиномикоз легких обыкновенно начинается, когда орофарингеальный секрет аспирируется в мелкие бронхи, вызывая ателектаз и пневмонит. Прямой путь распространения имеет место при заболеваниях головы, шеи и брюшной полости [7-10]. В эру до применения антибиотиков трансдиафрагмальный путь распространения инфекции из брюшной полости был важным путем распространения при торакальном актиномикозе, но в настоящее время вероятность этого крайне мала [1,6]. Развитие инфекции в результате отдаленного гематогенного распространения из шеи через средостение также случается очень редко [3,11,12]. Было установлено, что первоначально острое воспаление переходит в медленно протекающую хроническую стадию, которая приводит к локальному некрозу, фиброзу и обычно к образованию полости [13]. Гистопатологическое исследование определяет острое воспаление, окруженное фиброзной грануляционной тканью. Такой материал содержит «серные гранулы» (колонии микроорганизмов, формирующие аморфный центр, окруженный нитями), обычно включающие ассоциированные микоорганизмы, включая Actinobacillus actinomycetemcomitans , Haemophilus и Fusobacterium spp ., которые вероятно участвуют в патогенез заболевания [14].
Актиномикоз не имеет четкой связи с иммунодефицитными состояниями. Редкие случаи актиномикоза наблюдали у пациентов с ВИЧ-инфекций, острыми лейкозами на фоне химиотерапии, с трансплантациями почек и легких или на фоне использования стероидов [15-17].
В эру до антибиотиков актиномикотические процессы с вовлечением ребер, разрешением свищевых ходов через грудную клетку встречались часто. Эта форма заболевания среди случаев актиномикоза со временем уменьшалась [1,18]. Диагноз часто не устанавливается сравнительно долгое время. Актиномикоз легких обычно представлен как медленно прогрессирующая пневмония с лихорадкой, потерей веса, кашлем с мокротой, болями в грудной клетке [7-9]. Специфических рентгенологических проявлений нет, но предполагать актиномикоз можно при наличии легочными поражений, которые распространяются через грудную стенку и нередко с вовлечением плевры (плевральный выпот, эмпиема и плевральное утолщение), деструкцией смежных костей [19,20]. Клинические симптомы и рентгенологические признаки имитируют злокачественные опухоли и туберкулез. Присутствие на рентгенограммах воздуха внутри очага поражения может говорить о возможном неопухолевом процессе, таком как актиномикоз. Более чем в половине случаев обнаруживаются одна или несколько маленьких полостей [21]. Может быть кровохарканье, лимфоаденопатия, вовлечение сердца и средостения. По клиническим проявлениям нокардиоз может напоминать актиномикоз, но при этом в пораженных органах гранулы не образуются [22]. Туберкулез, эндемичные грибковые инфекции, криптококкоз, анаэробные легочные инфекции, бронхогеный рак, лимфома, мезотелиома, инфаркты легкого должны быть рассмотрены для дифференциальной диагностики легочного актиномикоза [1,5].
За исключением больных с классическими проявлениями с пенетрацией грудной клетки дренирующимися свищами диагноз актиномикоз легких предполагается редко [23]. В одной серии наблюдений, диагноз был заподозрен менее, чем у 7% больных, которые длительно страдали от этой инфекции [4]. Специфические серные гранулы при цитологическом исследовании обнаруживали в редких случаях [24]. Актиномицеты из откашливаемой мокроты или бронхоскопических аспиратов обычно не выделяются, в связи с тем, что эти образцы патматериала выращивают не в анаэробных условиях. Более того, в редких случаях актиномицеты можно увидеть в мокроте больных с карциномой, потому что эти микроорганизмы могут колонизировать некротические ткани. Это также может вести к диагностическим ошибкам. Игольная аспирация или трансбронхиальная биопсия и КТ, или аспирация под контролем УЗИ обычно позволяет успешно получить клинический материал для диагностики [25]. Во многих случаях диагноз устанавливали гистологически после выполнения резекции при подозрении на опухоль. Любой материал для исследования на актиномицеты должен был быть получен в анаэробных условиях. Возбудитель актиномикоза – неспорообразующие палочки (исключая A . meyeri ). Рост обычно начинает в течение 5-7 дней, но первичные изоляты получают только через 2-4 недели. Хотя они не нуждаются в специализированных средах, использование полуселективных сред может увеличить частоту выделения Actinomyces [26].
Основные лабораторные тесты отражают неспецифический воспалительный характер заболевания. Для идентификации видов внутри гранул при формалиновой фиксации тканей может быть использована иммунофлюоресценция. Диагностика, тем не менее, нуждается в комбинации ряда факторов, включая высев культуры и находку серных гранул в гнойном материале, полученном из пораженной ткани, корреляцию с клиническими и рентгенологическими проявлениями и ответом на антибактериальную терапию.
Нелеченый торакальный актиномикоз в конечном счете фатален, тогда как лечение может предотвращать развитие поздних осложнений, связанных с распространением п и процесса и приводит к выздоровлению почти в 90% случаев [4]. Выбор пенициллина при актиномикозе основан больше на экстенсивном клиническом опыте в течение более чем 50 лет, чем на рандомизированных контролируемых исследованиях [1]. Хотя терапия должна быть индивидуальной, изначально вводят 18-24 миллиона единиц пенициллина в день внутривенно в течение 2-6 недель, с последующей пероральной терапией пенициллином или амоксициллином в течение 6-12 месяцев. Тетрациклины (особенно у пациентов с аллергией на пенцициллин), эритромицин (особенно у беременных женщин), хломафеникол и клиндамицин могут выступать как альтернативные средства [1,8,27].
Роль хирургических вмешательств часто противоречива. Некоторыми авторами доложены впечатляющие результаты антимикробной терапии у больных с распространенным заболеванием. Хотя хирургическое дренирование абсцессов и эмпиемы также, как и иссечение свищевых ходов часто является полезным, вскоре после операции должна быть проведена соответствующая антибактериальная терапия для предотвращения возможных осложнений или распространения заболевания. Чрезкожный дренаж абсцессов в комбинация с медикаментозной терапией является другой опцией [29].
Недавно некоторые исследователи пролечили распространенный торакальный актиномикозов относительно короткими курсами антибактериальной терапии [7,30,31,32]. Kinnear и MacFarlane [7] описали 19 пациетов, при которых торакальный актиномикоз был вылечен антибактериальной терапией в среднем за 6 недель (от 1 недели до 6 месяцев). Хирургическая резекция была проведена у 7 пациентов. Hsieh et al . [32] успешно вылечили торакальный актиномикоз у 16 пациентов за две недели внутривенной пенициллинотерапии с последующими 3 месяцами пероральной терапии пенициллином. Больные, которые имели обширный торакальный или абдоминальный актиномикоз не должны получать короткие курсы терапии, несмотря на хирургическое лечение. Неадекватная антибактериальная терапия после операции может привести к осложнениями, таким как формирование бронхоплевральных свищей и эмпиема.
Легочная инфекция, вызываемая Nocardia , редкая, но серьезная, которая обнаруживается главным образом у пациентов с иммуносупрессией. Даже когда клиническое подозрение на нокардиоз велико, заболевание часто путают с другими нагноительными заболеваниями легких и опухолями.
Nocardia относится к аэробным актиномицетам ответственным за локальные и диссеминированные инфекции. Nocardia s pp . – аэробные ветвящиеся филаментозные грам-положительные слабокислотоустойчивые бактерии, которые существуют как почвенные сапрофиты. Члены комплекса N . asteroids гетерогенная группа организмов, Наиболее часто вызывают нокардиоз у людей [33,34,35]. Другие виды, которые могут вызывать легочную или диссеминированную инфекцию, включают N . farcinica , N . nova , N . otitidiscaviarum , N . transvalensis и N . brasiliensis [33,34,35,36-38].
Nocardia spp . – нередкий почвенный микроорганизм, который часто инфицирует больных с предлежащей иммунной недостаточностью, заболеваниями легких или наличием в анамнезе травмы или хирургической операции [38]. Наиболее частый путь для попадания в организм аэрозольный, легкие – наиболее частое место инфекции. Так как Nocardia spp . не является частью нашей нормальной микрофлоры и является редким лабораторным контаминантом, то выделение Nocardia из ткани или стерильных в норме жидкостей организма игнорироваться не должно [39,40].
Ранние исследования предполагали, что в США в год регистрируется 500-1000 случаев нокардиоза [41]. В течение последнего десятилетия отмечено увлечение числа наблюдений нокардиоза у больных с выраженной иммуносупрессией. Многие из них известны как экстремально чувствительные к развитию нокардиоза. Нокардиоз наблюдается во всем мире, во всех возрастных группах и расах и в 2-3 раза чаще встречается у мужчин, чем у женщин [42,43,44]. Поражение легких является основным клиническим проявлением (более, чем 40% доложенных случаев) и почти в 90% случаев, вызывается N . asteroids [33,45-47, 48] Большинство штаммов в нашей серии наблюдений, тем не менее, было вида N . farcinica (60%) [42]. Известно, что N . farcinica самый вирулентный штамм Nocardia spp . [44] Недавно во Франции было доложено увеличение выделения вида N . farcinica и предполагается, что это связано с учащением случав ВИЧ-инфекции. Они также обнаружили у этих больных более высокий уровень смертности [49].
Большинство случаев инфекции является результатом вдыхания бацилл; легкие – обычно первичное место заболевания. Легочные поражения характеризуются в основном некротическими абцессами, которые не хорошо инкапсулированы и поэтому легко распространяются и видны ветвящиеся четковидные, филаментозные бактерии, подобные тем, которыенаблюдают в мазках из культуры. Гранулемобразование происходит нечасто и в отличие от актиномикотических поражений фиброз редок. Серные гранулы, как при актиномикозе, при нокардиальных висцеральных поражениях не определяются [50].
Клеточно-опосредованпый иммунитет играет важную роль в защите от нокардиоза и предполагается, что иммуноскомпрометированные пациенты подвержены этой инфекции. Важность антиген-специфических Т-лимфоцитов иммунной функции доказано увеличением чувствительности к нокардиальной инфекции атимического клона мышей и способности Т-лимфоцитов, полученных от иммунизированных N . asteroids кроликов, усиливать фагоцитоз и ингибировать рост этих микроорганизмов макрофагами [50,51].
Нокардиоз обычно возникает у больных, которые имеют любые повреждения местной легочной защиты или системную иммуносупрессию. Нокардиоз особенно часто случается у больных с лейкемией, лимфомами, трансплантациями органов, СПИДом и длительной кортикостероидной или цитотоксичной терапией [33,34,35,42,43,44-47,48,50], хотя в некоторых случаях предрасполагающих факторов вовсе не находят [39,52,53]. В наших наблюдениях четыре (44,4%) больных не имели явных предрасполагающих факторов [42,54].
Возбудитель вызывает острую, часто некротическую пневмонию, обычно ассоциированную с образованием полости. Другие проявления заболевания могут включать медленно увеличивающиеся легочные узлы или пневмонию, сочетающуюся эмпиемой. У больных с образованием полостей отмечается медленно прогрессирующая лихорадка, озноб, продуктивный кашель, потливость, потеря веса, анорексия, одышкя и кровохарканье [55,56]. Рентгенологические проявления включают узлы, ретикулонодулярные или диффузные легочные инфильтраты, единичные или множественные абсцессы, и области уплотнения с кавитацией и без нее, которые часто граничат с плевральной полостью [42]. В связи со склонностью к гематогенной диссеминации, Nocardia нередко вызывает метастатические распространение, чаще в мозг (примерно 33% всех наблюдений). Инвазия в грудную стенку может встречаться, но нечасто [15,55-57].
Клинические и рентгенологические проявления легочного нокардиоза неспецифичны и могут быть ошибочны для различных бактериальных инфекций легких, включая актиномикоз и туберкулез, так же как и грибковые инфекции и новообразования. Настороженность к возможности нокардиоза позволяет ускорить постановку диагноза, особенно у больных с иммуносупрессией. Нокардиоз может быть быстро диагностирован после исследования мокроты, плевральной жидкости, бронхиального лаважа или чрезкожного легочного аспирата с окраской по Граму и выделения кислотоустойчивых бактерий. При окраске по Граму четко видно ветвящиеся грам-положительные бациллы неотличимые от Actinonyces , но они являются кислотоустойчивыми бактериями, тогда как Actinomyces нет. Nocardia spp . Неприхотливы, растут в аэробных условиях в течение от 48 часов до нескольких недель и должны быть инкубированы от 4-6 недель. Исследование антимикробной чувствительности является полезным для терапии, но результаты этих исследований должны быть интерпритированы с осторожностью [55,56]. Национальный комитет по клиническим лабораторным стандартам США не так давно одобрил метод для определения антимикробной чувствительности аэробных актиномицетов, включая бульоны для микроразведений [59]. Е-тест ( AB — biodisk , Solna , Sweden ) и BACTEC радиометрический метод коррелируют с бульонами для микроразведений и могут быть более полезным при рутинной клинической лабораторной диагностике [59,60].
Большая часть штаммов Nocardia чувствительная к сульфаниламидам и к триметоприму-сульфаметокзазолу in vitro . Резистенция наиболее часта, тем не менее, среди N . farcinica и N . otitiddiscaviarium изоляты [48,49,61,62]. В наших наблюдениях, три из 10 изолятов были чувствительны к триметоприму-сульфаметокзазолу и все шесть N . farcinica были резистентны к этому препарату in vitro [42]. Клинический опыт показывает, что для успешной терапии необходимо использование антимикробных препаратов в комбинации с соответствующим хирургическим лечением (дренажем). Сульфаниламиды, такие как триметоприм-сульфаметокзазол, остаются препаратами первой линии для лечения,. Рекомендуемая доза триметоприма-сульфаметокзазола 5-10 мг/кг (триметприм) и 25-50 мг/кг (сульфаметоксазол) за два приема в день [61]. Путь введения определяется общим клиническим статусом больного. Парентеральная терапия может быть дана в начале и изменена на пероральный прием после 3-6 недель, в зависимости от клинического ответа. Клиническое улучшение обычно отмечается в течение 7-10 дней после начала терапии [38].
Другие парентеральные препараты, имеющие активность против Nocardia включают: амикацин, карбапенемы и третье-поколение цефалоспоринов; каждый из этих препаратов может быть использоваться как часть комбинированной терапии у тяжелых больных. Сульфаниламиды, миноциклин и ко-амоксиклав эффективны против N . farcinica и могут применяться перорально. Карбапенемы и третье поколение цефалоспоринов могут быть использованы как альтернативная терапия у тяжелых больных и при токсичных реакциях или у больных с иммуносупрессией [33,42,63,64]. Амикацин показал синнергическую активность в случаях, когда он используется с другими антимикробными средствами, особенно карбапенемами, цефалоспоринами 3-го поколения и триметопримом-сульфаметокзазолом [42,44,47,65]. Новейшие антимикробные средства многообещающи. Все Nocardia spp . показали чувствительность in vitro к линезолиду [42,66]. С учетом случаев высокой гематологической токсичности линезолида после 4 недель терапии, использование линезолида в лечении нокардиоза не представляется целесообразным [67,68].
У иммунокомпетентных больных с легочными поражениями длительность терапии составляет минимум 6 месяцев. Терапия должна быть продлена до 12 месяцев при поражениях головного мозга и составляет год и более при СПИДе или у других иммунокомпрометированных больных [39,42,44,46,55,56]. У этих больных в течение длительного времени может также проводится низкодозная базисная супрессивная терапия. У больных с легочным абсцессом, эмпиемой и подкожными абсцессами, как правило, должно быть проведено хирургическое дренирование. Общая смертность у больных с легочным нокардиозом находится в пределах 15-30%, включая лиц с иммунодефицитами [33,35,42,47,67]. В случаях перехода в хроническое течение больные с острым заболеванием прогноз ухудшается.
Нокардиоз и актиномикоз легких – хронические гранулематозные инфекции, вызываемые грам-положительными бациллами порядка Actinomycetales . Рентгенологические проявления этих инфекций полиморфны. Наличие плевральных поражений при хронических легочных процессах может являться диагностическим ключом. Возможность диагностики и лечения актиномикоза без оперативного вмешательства иногда проблематично. Лечение актиномикоза обычно простое, требующее длительного введения пенициллина в высоких дозах. Однако в последнее время короткие курсы лечения были представлены как успешные. Нокардиоз легких наиболее часто развивается у иммунокомпрометированных больных и частота случаев этой инфекции возрастает. Для начала соответствующей терапией имеет значение раннее распознавание. Карбапенемы используют в качетве альтернативного лечения у тяжелых больных, а сульфаниламиды – при менее серьезных инфекциях.
1 . Russo TA. Agents of actinomycosis. In: Mandell GL, Bennet JE, Dolin R,editors. Principles and practice of infectious diseases. 6th ed. Philadelphia:Churchill Livingstone; 2005. pp. 2924–2934.
2. Mabeza GF, Macfarlane J. Pulmonary actinomycosis. Eur Respir J 2003;21:545–551.
3. Rose HD, Varkey B, Kutty CP. Thoracic actinomycosis caused by Actinomyces myeri. Am Rev Respir Dis 1982; 125:251–254.
4. Weese WC, Smith IM. A study of 57 cases of actinomycosis over a 36-year period. A diagnostic ‘failure’ with good prognosis after treatment. Arch Intern Med 1975; 135:1562–1568.
5. Lerner PI. Agents of actinomycosis. In: Gorbach SL, Bartlett JG, Blacklow NR, editors. Infectious diseases. 2nd ed. Philadelphia: W.B. Saunders Company; 1998. pp. 1973–1980.
6 . Bennhoff DF. Actinomycosis: diagnostic and therapeutic considerations and a review of 32 cases. Laryngoscope 1984; 94:1198–1217.
7 Kinnear W, Macfarlane J. A survey of thoracic actinomycosis. Resp Med 1990; 84:57–59.
8. Bates M, Cruickshank G. Thoracic actinomycosis. Thorax 1957; 12:99–123.
9. Heffner JE. Pleuropulmonary manifestations of actinomycosis and noardiosis. Semin Respir Infect 1988; 3:352–361.
10. Schaal KP, Lee H. Actinomycete infections in humans: a review. Gene 1992; 115:201–211.
11. Apothloz C, Regamey C. Disseminated infection due to Actinomyces myeri: case report and review. Clin Infect Dis 1995; 22:621–625.
12. Hachitanda Y, Nakagawara A, Ikeda K. An unusual wall tumour due to actinomycosis in a child. Paediatr Radiol 1989; 20:96.
13 . Brown JR. Human actinomycosis. A study of 181 subjects. Human Pathol 1973; 4:319–330.
14 . Read RC. Nocardiosis and actinomycosis. Medicine 2005; 33:114– 115.
This is a clinically oriented review
15. Takeda H, Mitsuhashi Y, Kondo S. Cutaneous disseminated actinomycosis in a patient with acute lymphocytic leukemia. J Dermatol 1998; 25: 37–40.
16. Chen CY, Chen YC, Tang JL, et al. Splenic actinomycotic abscess in a patient with acute myeloid leukemia. Ann Hematol 2002; 81:532–534.
17. Ossorio MA, Fields CL, Byrd RP Jr, Roy TM. Thoracic actinomycosis and human immunodeficiency virus infection. South Med J 1997; 90: 1136–1138.
18. Slade PR, Slesser BV, Southgate J. Thoracic actinomycosis. Thorax 1973; 28:73–85.
19. Kwong JS, Muller NL, Godwin JD, et al. Thoracic actinomycosis: CT findings in eight patients. Radiology 1992; 183:189–192.
20. Kobashi Y, Yoshida K, Miyashita N, et al. Thoracic actinomycosis with mainly pleural involvement. J Infect Chemother 2004; 10:172–177.
A case of thoracic actinomycosis suspected to have spread from the lung to the chest wall was discussed in this study.
21. Flynn MW, Felson B. The roentgen manifestations of thoracic actinomycosis. Am J Roentgenol Radium Ther Nucl Med 1970; 110:707–716.
22. Robboy SJ, Vickery AL Jr. Tinctorial and morphologic properties distinguishing actinomycosis and nocardiosis. N Engl J Med 1970; 282:593– 596.
23. Perez-Castrillon JL, Gonzalez-Castaneda C, del Campo-Matias F, et al. Empyema necessitatis due to Actinomyces odontolyticus. Chest 1997; 11:1144.
24. Lazzari G, Vineis C, Cugini A. Cytologic diagnosis of primary pulmonary actinomycosis: report of two cases. Acta Cytol 1981; 25:299–301.
25 . Pauker SG, Kopelman RI. Clinical problem-solving. A rewarding pursuit of certainty. N Engl J Med 1993; 329:1103–1107.
26. Lewis R, McKenzie D, Bagg J, Dickie A. Experience with a novel selective medium for isolation of Actinomyces spp. from medical and dental specimens. J Clin Microbiol 1995; 33:1613–1616.
27. Martin MV. The use of oral amoxycillin for the treatment of actinomycosis. A clinical and in vitro study. Br Dent J 1984; 156:252–254.
28 . Wohlgemuth SD, Gaddy MC. Surgical implications of actinomycosis. South Med J 1986; 79:1574–1578.
29. Goldwag S, Abbitt PL, Watts B. Case report: percutaneous drainage of periappendiceal actinomycosis. Clin Radiol 1991; 44:422–424.
30. Choi J, Koh WJ, Kim TS, et al. Optimal duration of IV and oral antibiotics in the treatment of thoracic actinomycosis. Chest 2005; 128:2211– 2217.
This study showed that the traditional recommendation of intravenous antibiotic therapy for 2–6 weeks followed by oral antibiotic therapy for 6–12 months is not always necessary for all thoracic actinomycosis patients.
31. Sudhakar SS, Ross JJ. Short-term treatment of actinomycosis: two cases and a review. Clin Infect Dis 2004; 38:444–447.
This report describes cases of oesophageal and of cervicofacial actinomycosis treated successfully with short-term antibiotic therapy and reviews the literature.
32. Hsieh MJ, Liu HP, Chang JP, Chang CH. Thoracic actinomycosis. Chest 1993; 104:366–370.
33. Hui CH, Au VW, Rowland K, et al. Pulmonary nocardiosis re-visited: experience of 35 patients at diagnosis. Respir Med 2003; 97:709–717.
34. Kageyama A, Yazawa K, Ishikawa J, et al. Nocardial infections in Japan from 1992 to 2001, including the first report of infection by Nocardia transvalensis. Eur J Epidemiol 2004; 19:383–389.
This paper provides detailed information about the aetiological agents, clinical presentation and underlying condition in 303 patients with nocardiosis.
35. Queipo-Zaragoza JA, Broseta-Rico E, Alapont-Alacreu JM, et al. Nocardial infection in immunosuppressed kidney transplant recipients. Scand J Urol Nephrol 2004; 38:168–173.
This study showed that nocardiosis is associated with significant morbidity and mortality in kidney transplant patients receiving immunosuppressive therapy.
36. Dikensoy O, Filiz A, Bayram N, et al. First report of pulmonary Nocardia otitidiscaviarum infection in an immunocompetent patient from Turkey. Int J Clin Pract 2004; 58:210–213.
37. Kiska DL, Hicks K, Pettit DJ. Identification of medically relevant Nocardia species with an abbreviated battery of tests. J Clin Microbiol 2002; 40:1346– 1351.
38. McNeil MM, Brown JM. The medically important aerobic actinomycetes: epidemiology and microbiology. Clin Microbiol Rev 1994; 7:357–417.
39 . Burgert SJ. Nocardiosis: a clinical review. Infect Dis Clin Pract 1999; 8: 27–32.
40. Saubolle MA. Aerobic actinomycetes. In: McClatchey KD, editor. Clinical laboratory medicine. 2nd ed. Philadelphia: Lippincott Williams & Wilkins; 2002. pp. 1201–1220.
41. Beaman BL, Burnside J, Edwards B, Causey W. Nocardial infections in the United States, 1972–1974. J Infect Dis 1976; 134:286–289.
42.Yildiz O, Alp E, Tokgoz B, et al. Nocardiosis in a teaching hospital in the Central Anatolia region of Turkey: treatment and outcome. Clin Microbiol Infect 2005; 11:495–499.
This paper provides detailed information about predisposing factors, clinical features, radiological findings, antimicrobial susceptibility patterns, treatments, duration of treatments and outcomes of the patients with nocardiosis. The use of imipenem or meropenem in combination with amikacin is suggested for initial therapy of serious nocardial infections.
43.Matulionyte R, Rohner P, Uckay I, et al. Secular trends of nocardia infection over 15 years in a tertiary care hospital. J Clin Pathol 2004; 57:807–812.
This is a review of the epidemiology, clinical, and microbiological characteristics, treatment, and outcome of nocardial infections diagnosed in 20 patients at the Geneva University Hospitals, Switzerland over a 15-year period. The authors emphasized that the drug susceptibility testing should be performed due to increasing resistance to TMP-SMX.
44 . Lerner PI. Nocardiosis. Clin Infect Dis 1996; 22:891–903.
45. Roberts SA, Franklin JC, Mijch A, Speiman D. Nocardia infection in heart– lung transplant recipients at Alfred Hospital, Melbourne, Australia, 1989– 1998. Clin Infect Dis 2000; 31:968–972.
46. Uttamchandani RB, Daikos GL, Reyes RR, et al. Nocardiosis in 30 patients with advanced human immunodeficiency virus infection: clinical features and outcome. Clin Infect Dis 1994; 18:348–353.
47. Menendez R, Cordero PJ, Santos M, et al. Pulmonary infection with Nocardia species: a report of 10 cases and review. Eur Respir J 1997; 10:1542–1546.
48.Mootsikapun P, Intarapoka B, Liawnoraset W. Nocardiosis in Srinagarind Hospital, Thailand: review of 70 cases from 1996–2001. Int J Infect Dis 2005; 9:154–158.
This retrospective study reported the clinical manifestations, underlying diseases, radiologic findings, antimicrobial susceptibility and treatment of nocardial infection. The authors emphasize that drug susceptibility testing should be performed due to increasing resistance to TMP-SMX.
49. Boiron P, Provost F, Chevrier G, Dupont B. Review of nocardial infections in France 1987 to 1990. Eur J Clin Microbiol Infect Dis 1992; 11:709–714.
50. Beaman BL, Beaman L. Nocardia species: host-parasite relationships. Clin Microbiol Rev 1994; 7:213–264.
51. Black CM, Beaman BL, Donovan RM, Goldstein E. Effect of virulent and less virulent strains of Nocardia asteroides on acid-phosphatase activity in alveolar and peritoneal macrophages maintained in vitro. J Infect Dis 1983; 148:117– 124.
52. Saubolle MA, Sussland D. Nocardiosis: review of clinical and laboratory experience. J Clin Microbiol 2003; 41:4497–4501.
53. Fleetwood IG, Embil JM, Ross IB. Nocardia asteroides cerebral abscess in immunocompetent hosts: report of three cases and review of surgical recommendations. Surg Neurol 2000; 53:605–610.
54. Alp E, Yildiz O, Aygen B, et al. Disseminated nocardiosis due to unusual species: two case report. Scand J Infect Dis (in press).
55 . Bach MC. Nocardia. In: Gorbach SL, Bartlett JG, Blacklow NR, editors. Infectious diseases. 2nd ed. Philadelphia: W.B. Saunders Company; 1998. pp. 1969–1973.
56. Sorrell TC, Mitchell DH, Iredell JR. Nocardia species. In: Mandell GL, Bennet JE, Dolin R, editors. Principles and practice of infectious diseases. 6th ed. Philadelphia: Churchill Livingstone; 2005. pp. 2916–2924.
57. Conant EF, Wechsler RJ. Actinomycosis and nocardiosis of the lung. J Thorac Imaging 1992; 7:75–84.
58. National Committee for Clinical Laboratory Standards. Susceptibility testing of mycobacteria, Nocardia, and other aerobic actinomycetes: tentative standard M24-T2. 2nd ed. Wayne: NCCLS; 2000.
59. Biehle JR, Cavalieri SJ, Saubolle MA, Getsinger LJ. Comparative evaluation of the E test for susceptibility testing of Nocardia species. Diagn Microbiol Infect Dis 1994; 19:101–110.
60. Ambaye A, Kohner PC, Wollan PC, et al. Comparison of agar dilution, broth microdilution, disk diffusion, E-test, and BACTEC radiometric methods for antimicrobial susceptibility testing of clinical isolates of the Nocardia asteroids complex. J Clin Microbiol 1997; 35:847–852.
61. Wallace RJ, Septimus EJ, Williams TW, et al. Use of trimethoprim-sulfamethoxazole for treatment of infections due to Nocardia. Rev Infect Dis 1982; 4:315–325.
62. Hitti W, Wolff M. Two cases of multidrug-resistant Nocardia farcinica infection in immunosuppressed patients and implications for empiric therapy. Eur J Clin Microbiol Infect Dis 2005; 24:142–144.
This paper shows two cases of multidrug-resistant Nocardia farcinica infection that occurred in immunocompromised patients. The use of imipenem in combination with amikacin is suggested for initial therapy of serious Nocardia infections.
63. Gombert ME. Susceptibility of Nocardia asteroides to various antibiotics, including newer beta-lactams, trimethoprim-sulfamethoxazole, amikacin, and N-formimidoyl thienamycin. Antimicrob Agents Chemother 1982; 21:1011– 1012.
64. Gutmann L, Goldstein FW, Kitzis MD, et a l. Susceptibility of Nocardia asteroides to 46 antibiotics, including 22 beta-lactams. Antimicrob Agents Chemother 1983; 23:248–251.
65. Goldstein FW, Hauteford B, Acar JF. Amikacin-containing regimens for treatment of Nocardiosis in immunocompromised patients. Eur J Clin Microbiol Infect Dis 1987; 6:198–200.
66. Moylett EH, Pacheco SE, Brown-Elliott BA, et al. Clinical experience with Linezolid for the treatment of Nocardia infection. Clin Infect Dis 2003; 36:313–318.
67. Lederman ER, Crum NF. A case series and focused review of nocardiosis: clinical and microbiologic aspects. Medicine 2004; 83:300–313.
In this paper, the aetiological agents, clinical presentation and current treatment options of nocardiosis are discussed.
68. Corti ME, Villafane-Fioti MF. Nocardiosis: a review. Int J Infect Dis 2003; 7:243–250.
источник
Актиномикоз заболевание, имеющее инфекционную природу. Возбудителями болезни являются лучистые грибы актиномицеты. Если они проникают в организм человека, у последнего на коже появляются нагноения (абсцессы), выпуклые круглые гранулемы и свищи. В данной статье мы расскажем, что такое актиномикоз, о причинах его возникновения и возможных факторах риска.
Возбудитель актиномикоза — микроорганизмы рода Actinomyces. В окружающей среде они встречаются в загрязненной почве, застарелом сене/соломе или растениях. В организм человека лучистые грибы могут попасть одним из следующих способов:
- с некачественной или плохо обработанной термически пищей;
- при вдыхании;
- через небольшие раны и повреждения на коже.
После попадания в организм актиномицеты далеко не всегда вызывают воспаление. В большинстве случаев они остаются на слизистой оболочки ротовой полости или глаз и питаются отмершими клетками. К актиномицету приводят предшествующие воспалительные процессы в органах дыхания, ротовой полости или ЖКТ.
Заражение кожи может быть первичным или вторичным. В первом случае актиномицеты проникают в организм через раны и другие повреждения. При вторичном инфицировании заражение кожи происходит от миндалин, молочной железы, лимфатических узлов и т.п.
Заболевание может развиваться на любом участке кожи или внутренних тканей. В зависимости от этого выделяют несколько типов заболевания:
- актиномикоз кожи. Грибы проникают под кожу через различные повреждения и вызывают выраженные изменения покровов. Внешние изменения, происходящие с эпидермисом, заметны невооруженным глазом: тело покрывается выпуклыми узелками, которые затем становятся глубоко залегающими инфильтратами. По мере развития болезни последние образовывают свищ и вскрываются. Чаще всего происходит поражение шейно-лицевой области. В этом случае патогенные микроорганизмы поражают подкожно-жировой слой, кожа становится синевато-красной, плотной и блестящей. Со временем свищи размягчаются, из них выделяется жидкий гной. Актиномикоз кожи становится хроническим, поражает внутренние органы, может привести к летальному исходу;
- актиномикоз полости рта. Это хроническое заболевание, поражающее преимущественно людей среднего и старшего возраста. Причиной часто становятся первичные патологии, ослабляющие местный иммунитет. К ним относятся кариес, зубной камень, налет, болезни десен, актиномикоз миндалин. Поражение происходит в том случае, если слизистая оболочка ротовой полости нарушается. В этом случае актиномицеты внедряются в ткани и провоцируют актиномицет челюстно-лицевой полости. Воспалительный процесс распространяется на костную ткань, и она начинает отмирать. Симптомы болезни развиваются постепенно: вначале гранулемы находятся глубоко в слизистой оболочке, затем в полости рта появляются гноящиеся фистулы. Далее возникают признаки интоксикации: незначительное повышение температуры, общая слабость, головная боль;
- актиномикоз легких. Поражает нижнюю часть легких. Клиническое течение и симптомы схожи с пневмонией. У человека наблюдается выраженная гипертермия (повышение температуры тела), влажный кашель с кровью, упадок сил, усиленное потоотделение. Дыхание заболевшего человека становится тяжелым, при прослушке врачи обнаруживают хрип. В дальнейшем актиномикоз легких прогрессирует, поэтому лечение рекомендуется начинать еще на 1-ой стадии болезни;
- актиномикоз печени. Поражение данного органа является вторичным. В первую очередь актиномицеты проникают в кишечник, аппендикс и прямую кишку. После этого по венам микроорганизмы достигают печени и вызывают ее поражение. Очаги поражения выглядят как серовато-белые массы и внешне напоминают метастазы раковых опухолей. Сопутствующие симптомы: сильная лихорадка, потливость, головная боль, истощение. При диагностике наблюдается увеличение печени.
Специалисты рекомендуют обращаться в больницу при первых признаках болезни. Так вы сможете облегчить течение актиномикоза и предотвратить тяжелые последствия.
Самый распространенный метод диагностики грибковых заболеваний — микроскопическое исследование соскоба или слизистого отделяемого. Однако в случае актиномикоза применение этого способа не всегда оправдано, так как актиномицеты встречаются в организме здоровых людей. Для обследования берут отделяемое из свищей при поражении кожи. Если в больницу поступает пациент с инфицированием внутренних органов, диагноз ставится с помощью пункции, которая проводится через кожу.
После первичной диагностики врачи выявляют вид актиномицетов. Для этого проводится специальная процедура — реакция иммунофлуоресценции (РИФ). Проходит все в несколько этапов:
- Делается соскоб биологического материала с мочеполового тракта, после чего подготавливается мазок. В отдельных случаях исследуется слизистое отделяемое или кровь пациента.
- Мазок обрабатывается специальными антителами, которые помогают обнаружить антиген.
- Если антигены в мазке присутствуют, антитела связываются с ними. Это дает специфическое свечение, которое выявляется через люминесцентный микроскоп. Как только данное свечение обнаружено, врач становит диагноз «актиномикоз».
Преимущество РИФ — высокая скорость исследования. К недостаткам относится относительная неточность (80%), поэтому одной реакции иммунофлуоресценции недостаточно. Для окончательного подтверждения диагноза назначается бактериологический посев. Микроорганизмы, взятые из биологического материала, помещаются в специальную среду. В течение 2-х недель наблюдается скорость роста колоний актиномицетов и их чувствительность к антибиотикам. Окончательные результаты обычно готовы через 14 дней.
Лечить актиномикоз необходимо комплексно. Процесс включает в себя прием этиотропных антибиотиков, иммуномодуляторов и других препаратов. В запущенных случаях допустимо хирургическое вмешательство. При терапии актиномикоза соблюдаются следующие принципы:
- при назначении этиотропных препаратов учитывается чувствительность лучистого грибка и бактериальной флоры, которая присоединилась в процессе болезни. Если антибиотики назначаются без учета данных факторов, бактерии приобретают резистентность (устойчивость) к прописанным препаратам. Естественная микрофлора подавляется, из-за чего иммунитет больного ослабляется еще сильнее;
- введение антибактериальных препаратов должно быть парентеральным. Это способ, при котором желудочно-кишечный тракт минуется, что выгодно отличает такое использование лекарств от их традиционного применения. Делается это с помощью инъекции или ингаляции. При запущенном и тяжелом течении заболевания применяется комбинация из разных препаратов;
- дополнительный аспект при лечении актиномикоза — иммунотерапия. Данный терапевтический метод помогает увеличить эффективность от использования антибиотиков и снизить выраженность побочных эффектов. В процессе иммунотерапии применяется Актинолизат — культуральная жидкость самолизирующихся (растворяющихся) актиномицетов. Применяется непосредственно при лечении актиномикоза и считается одним из наиболее эффективных лекарственных средств.
В процессе лечения рекомендуется принимать продукты, богатые йодом: морскую капусту, морепродукты, репчатый лук, говядину и йодированную соль. Для поддержания иммунитета подойдут природные антибиотики: лук, чеснок, мед, мята, розмарин. Также можно применять луковый сок местно для смазывания свищей.
Для борьбы с лучистым грибком и бактериями применяются лекарственные препараты тетрациклинового ряда, бензилпенициллин, фторхинолы и макролиды. Подбор соответствующего средства определяется видом актиномикоза и разнообразными факторами. Препараты для борьбы с болезнью:
- актиномикоз лицевой и шейной зоны лечится Флемоклавом или Амоксиклавом в сочетании с пенициллинами. Врач назначает 2,4 г средства 3 раза в день. Курс лечения — до 7 дней, после чего доза уменьшается в 2 раза. С новой дозировкой препараты нужно принимать еще 1 неделю. Если патология затрагивает область груди и легких, терапевтический курс составляет не менее 3-х недель;
- для повышения клеточного иммунитета применяется Актинолизат. После его введения выраженность воспалительной реакции уменьшается, а защитные силы организма становятся значительно выше. Актинолизат вводится в организм больного внутримышечно 3 раза в неделю. Допустимая доза — 3 миллилитра. Курс лечения определяется состоянием пациента и может составлять 10, 20 или 25 инъекций. При необходимости терапевтический курс повторяется через месяц;
- в качестве вспомогательных препаратов врачи прописывают витаминные комплексы, растворы для дезинтоксикации, калия йодид;
- для нейтрализации аллергических реакций назначаются Супрастин, Тавегил, Диазолин и другие антигистаминные (противоаллергические) препараты;
- стимуляция иммунного ответа проводится с помощью инъекций экстракта алоэ или аутогемотерапии — подкожное введение собственной крови пациента, предварительно взятое из вены. Курс — 4 процедуры. Проводится 1 раз в неделю;
- свищевые ходы промываются антисептическими растворами. Также применяются местные препараты (крема и мази) содержащие противогрибковые и антибактериальные действующие компоненты. Для быстрого заживления ран в послеоперационный период назначаются: Винилин, Метилурацил, Солкосерил. Бактерицидными свойствами обладает и лампа, используемая для кварцевания. Рекомендуется применять данный метод в период острого воспаления;
- скопление отмерших клеток, крови и лимфы устраняется электрофорезом с применением Лидазы и Йода. Для усиления эффекта рекомендовано воздействие ультразвука. Врач назначает курс из 25 ежедневных процедур.
Хирургическое лечение проводится наряду с консервативной терапией. Помощь хирурга заключается во вскрытии абсцессов и флегмон с дальнейшим промыванием и откачиванием гнойного содержимого. В запущенных случаях применяется иссечение спаек.
источник