Адреногенитальный синдром – наследственное заболевание. У больного нарушается образование кортизола и альдостерона надпочечниками. Это происходит из-за дефекта ферментов, участвующих в синтезе стероидных гормонов.
Некоторые типы болезни имеют выраженные признаки с рождения, а в других случаях имеются скрытые гены, которые проявляются при стрессовых ситуациях в подростковом периоде или детородном. Провокаторами могут быть травмы, радиация, стресс, отравления, тяжелые инфекции, физические перенапряжение. Чтобы заболевание проявилось, необходимо его наличие у обоих родителей. Причем один из них может быть болен, а другой – носитель.
Генетическая аномалия нарушает образование гормонов надпочечников. На это реагирует гипофиз выработкой адренокортикотропного гормона (АКТГ). Результатом является увеличение надпочечных желез. Возникает такое состояние, как врожденная гиперплазия надпочечников (собственно, это и есть название адреногенитального синдрома).
При этом производство мужских половых гормонов при гиперплазии возрастает. Мужские гормоны в организме женщин вырабатывают только надпочечники. Их избыток вызывает маскулинизацию. У мальчиков основная часть андрогенов продуцируется яичками, но они атрофируются при заболевании. Повышенное содержание гормонов стимулирует раннее половое созревание и отставание в росте.
Первые признаки неправильного строения половых органов часто видны на УЗИ даже до рождения ребенка. У новорожденных девочек увеличен клитор, бывает даже полностью сформированный половой член. Влагалище и матка присутствуют, но они бывают не до конца развитыми. У мальчиков обнаруживают увеличение мошонки и полового члена. Дети могут родиться с темной кожей из-за усиленного синтеза пигмента кожи.
Недостаток кортизола проявляется низким артериальным давлением, учащенным сердцебиением. При стрессовой ситуации может возникать адреналовый криз с шоковым состоянием. Дефицит альдостерона вызывает тяжелое обезвоживание.
Формы врожденной патологии – вирильная, сольтеряющая и неклассическая.
Методы диагностики: УЗИ, анализ амниотической жидкости или после 21 недели берут кровь плода (из пуповины под контролем УЗИ); После родов назначается обследование: проба с АКТГ, анализ крови, мочи. Для молодых женщин с нетипичным течением гиперплазии учитывают данные, полученные при: рентгенографии костей кисти; УЗИ яичников; измерении температуры в прямой кишке на протяжении цикла (базальной).
Беременной женщине назначается гормональная терапия, и девочки рождаются с нормально сформированными половыми признаками. Последствия для мамы: повышается давление, нарастают отеки, прибавляется масса тела, возможен поздний токсикоз. После рождения при наличии аномалий строения половых органов показана их хирургическая коррекция. При недостатке кортизола и альдостерона назначается заместительная терапия Гидрокортизоном и Кортинеффом. Эндокринолог наблюдает на протяжении всей жизни за больными.
При скрытом течении болезни у женщин гормоны не назначают. Если планируется зачатие, то необходимо применение Гидрокортизона до полного восстановления овуляции. Для предупреждения выкидыша гормональная терапия продолжается до 12 недели, ее дополняют эстрогенами, прогестероном. При расстройствах менструального цикла, угревой сыпи, усиленном оволосении назначают комбинированные препараты с эстрогенами, антиандрогенами, ОК.
Если родился ребенок, обладая внешними чертами мальчика, но является девочкой с выраженной аномалией развития половых органов, в таких случаях могут быть два варианта – хирургическая коррекция, заместительная терапия и помощь психотерапевта, либо сохраняют документально мужской пол, а матку удаляют.
Читайте подробнее в нашей статье об адреногенитальном синдроме, методах его профилактики.
Это заболевание относится к наследственным. У больного нарушается образование кортизола и альдостерона надпочечниками. Это происходит из-за дефекта ферментов, участвующих в синтезе стероидных гормонов.
Некоторые типы болезни имеют выраженные признаки с рождения, а в других случаях имеются скрытые, «молчащие» гены, которые проявляются при стрессовых ситуациях в подростковом периоде или детородном. Провокаторами могут быть травмы, радиация, стресс, отравления, тяжелые инфекции, физические перенапряжение. Ранее эти формы патологии считали приобретенными, а затем нашли дефектные гены, полученные от родителей. Причины мутаций остались пока неисследованными.
Так как ген, отвечающий за адреногенитальный синдром, является рецессивным (подавленным), то для того, чтобы заболевания проявилось, необходимо его наличие у обоих родителей. Причем один из них может быть болен, а у другого обнаруживается носительство гена.
А здесь подробнее о болезни и синдроме Иценко-Кушинга.
Генетическая аномалия нарушает образование гормонов надпочечников. На это реагирует гипофиз выработкой адренокортикотропного гормона (АКТГ). Это соединение в норме стимулирует синтез стероидов. Результатом активации является увеличение надпочечных желез.
Даже большие надпочечники не способны образовывать кортизол и альдостерон, так как имеется разрыв ферментативной цепи. Возникает такое состояние, как врожденная гиперплазия надпочечников. Именно так эндокринологи формулируют диагноз адреногенитального синдрома.
Путь наследования врожденной гиперплазии надпочечников. Патологический ген обозначен черным кружочком
Если стероидные гормоны не могут образоваться, то производство мужских половых гормонов (андрогенов) при гиперплазии возрастает. Все предшественники кортизола и альдостерона используются надпочечниками для синтеза андрогенов.
Мужские гормоны в организме женщин вырабатывают только надпочечники. Их избыток вызывает маскулинизацию, то есть приобретение половых признаков мужчины. Это проявляется очень ярко еще и потому, что андрогены имеют свойство подавлять действие женских (эстрогенов).
У мальчиков основная часть андрогенов продуцируется яичками, но так как надпочечниковые гормоны имеются в крови в избытке, то собственные железы теряют активность. Яички атрофируются. Повышенное содержание гормонов стимулирует раннее половое созревание и отставание в росте, так как удлинение костей скелета прекращается с наступлением половой зрелости.
Раннее половое созревание мальчика
Первые признаки неправильного строения половых органов часто видны на УЗИ даже до рождения ребенка. У новорожденных девочек увеличен клитор, бывает даже полностью сформированный половой член. Влагалище и матка присутствуют, но они бывают не до конца развитыми. У мальчиков обнаруживают увеличение мошонки и полового члена.
Так как в еще в период внутриутробного развития образуется много АКТГ и меланоцитстимулирующего гормона, то дети могут родиться с темной кожей из-за усиленного синтеза пигмента кожи.
Недостаток кортизола проявляется низким артериальным давлением, учащенным сердцебиением. При стрессовой ситуации может возникать адреналовый криз с шоковым состоянием. Дефицит альдостерона вызывает тяжелое обезвоживание – понос, рвота, судорожный синдром. Они могут иметь катастрофические последствия для младенца.
Симптоматика гиперплазии надпочечников связана с дефектами разных видов ферментов. Наиболее типичными являются три формы вирильная, сольтеряющая и неклассическая.
Преобладают нарушения развития половых органов. У девочек:
- увеличен клитор, похожий на половой член;
- углублен вход во влагалище;
- половые губы больше нормы;
- матка и придатки сформированы.
У мальчиков увеличен пенис, кожа мошонки имеет темную пигментацию. У детей половое созревание начинается с семи лет. Девочки широкоплечие, с узким тазом, укороченными и массивными конечностями. У них низкий голос, кадык на шее, молочные железы не растут. У мальчиков рано появляются грубые волосы на подбородке и верхней губе, ломается голос.
Проявления болезни начинают обнаруживаться с первых недель жизни. У девочек половые органы формируются по мужскому типу, а у мальчиков увеличиваются пенис и мошонка. Из-за грубого нарушения образованная стероидных гормонов развивается тяжелая рвота, понос, судороги, темнеет кожа. Прогрессирующее обезвоживание ведет к смерти при отсутствии своевременной заместительной терапии.
Через 2-3 дня от начала клинического проявления заболевания появляются симптомы дегидратации и развития метаболического ацидоза
Выявляют в молодом возрасте. Половые органы соответствуют полу, но бывает увеличение клитора и пениса. Основные нарушения встречаются у женщин – уменьшаются или прекращаются месячные после стресса, травмы, аборта, выкидыша. Наступление первой менструации может быть только к 15 годам, цикл удлинен (более 30-40 дней).
Кожа склонна к повышенной жирности и образованию угрей, имеется повышенное оволосение. При обследовании обнаруживают гиперплазию коркового слоя надпочечников.
На фото девушка с поздним началом заболевания
Также имеются и варианты неклассического течения адреногенитального синдрома – с высоким давлением крови, с лихорадкой, липидный (ожирение, нарушен холестериновый обмен), с гирсутизмом (усиленный рост волос на теле и лице, по средней линии живота, около сосков).
Чем раньше возникают признаки адреногенитального синдрома, тем меньше шансов на то, что у женщины может произойти зачатие и нормальное вынашивание плода. Стойкое бесплодие характерно для вирилизирующей и сольтеряющей формы, а при неклассическом варианте беременность наступает, но возрастает риск выкидышей.
Адреналовый криз у младенцев проявляется тяжелой рвотой, поносом, срыгиванием, неуправляемым падением давления, частым сердцебиением. Ребенок быстро теряет массу тела, впадает в бессознательное состояние. Ему требуется экстренная госпитализация для спасения жизни.
Смотрите на видео о развитии андрогении:
При обследовании беременных о возможности гиперплазии надпочечников может свидетельствовать аномальное формирование половых органов плода. Это можно увидеть на втором скрининговом акушерском УЗИ. В таких случаях рекомендуется дополнительное обследование для выявления патологии еще до родов. Проводят анализ амниотической жидкости или после 21 недели берут кровь плода (из пуповины под контролем УЗИ).
После родов назначается обследование:
- проба с АКТГ – нет повышения содержания кортизола после его введения;
- анализ крови – снижен натрий, повышен калий, 17 ОН-прогестерон в 5-7 раз и более, андростендион (предшественник стероидов), ренин (при сольтеряющей форме);
- анализ мочи – высокая концентрация 17-кетостероидов, после приема преднизолона снижается наполовину.
Анализ амниотической жидкости
Для молодых женщин с нетипичным течением гиперплазии учитывают данные, полученные при:
- рентгенографии костей кисти (раннее завершение роста);
- УЗИ яичников – фолликулы, не достигающие овуляции;
- измерении температуры в прямой кишке на протяжении цикла (базальной) – отсутствие изменений, характерных для овуляции.
В некоторых случаях лечение гиперплазии начинается еще до родов. Беременной женщине назначается гормональная терапия и девочки рождаются с нормально сформированными половыми признаками. Этот метод не безопасен для матери, так как у нее повышается давление, нарастают отеки, прибавляется масса тела. Такие изменения могут привести к позднему токсикозу или усугубить его течение.
При недостатке кортизола и альдостерона назначается заместительная терапия Гидрокортизоном и Кортинеффом. Важен постоянный контроль и коррекции дозы при любых сопутствующих заболеваниях или стрессах, так как возможен адреналовый криз. За пациентами с адреногенитальным синдромом ведется наблюдение эндокринолога на протяжении всей жизни.
При скрытом течении болезни у женщин гормоны не назначают, если она не планирует беременность, а месячные сохраняют относительную ритмичность. Если же пациентка стремится к рождению ребенка, то необходимо применение Гидрокортизона до полного восстановления овуляции. Для предупреждения выкидыша гормональная терапия продолжается до 12 недели, ее дополняют эстрогенами, а в более поздних сроках – прогестероном.
При расстройствах менструального цикла, угревой сыпи, усиленном оволосении назначают комбинированные препараты с эстрогенами, антиандрогенами, противозачаточные последнего поколения (Клайра, Логест, Мерсилон). Через полгода проявляется терапевтический эффект, но по окончанию их применения таблеток симптомы вновь возвращаются.
Особая ситуация возникает, если диагноз до родов не поставлен, а ребенок, обладая внешними чертами мальчика, является девочкой с выраженной аномалией развития половых органов. В таких случаях могут быть два варианта дальнейших действий – хирургическая коррекция, заместительная терапия и помощь психотерапевта, либо сохраняют документально мужской пол, а матку удаляют.
Смотрите на видео об адреногенитальном синдроме:
При наличии в роду случаев подобных болезней обязательно назначается консультация медицинского генетика молодым людям, которые планируют ребенка. Даже обычный тест с АКТГ позволяет выявить скрытые варианты патологии или носительство гена. При наступившей беременности показано генетическое исследование клеток зародыша или амниотических вод. На пятые сутки жизни проводят анализ на уровень 17-гидропрогестерона.
Чем раньше болезнь обнаружена, тем больше шансов на ее успешную коррекцию.
А здесь подробнее о недостаточности гипофиза.
Адреногенитальный синдром характеризуется ферментной аномалией наследственного происхождения. Нарушается образование кортизола и альдостерона, а андрогены синтезируются в избыточном количестве. Девочки рождаются с признаками мужских половых органов, по мере роста их телосложение и внешние черты становятся мужеподобными. При сольтеряющей форме отмечается обезвоживание.
При первом проявлении болезни у молодых женщин преобладают нарушения менструального цикла, бесплодие. Для обнаружения патологии применяется дородовая диагностика, скрининг новорожденных. Лечение заключается в заместительной терапии гормонами, оперативной коррекции половых органов.
К сожалению, болезни надпочечников не всегда определяются своевременно. Чаще их обнаруживают как врожденные у детей. Причины могут быть и в гиперфункции органа. Симптомы у женщин, мужчин в целом схожи. Помогут выявить болезни анализы.
Многие путают болезнь и синдром Иценко-Кушинга, а ведь причины у них отличные, лечение также. Симптомы проявляются внешне, перебоями в работе всех органов. Диагностика комплексная, прогноз не всегда благоприятный, даже у детей.
Преимущественно недостаточность гипофиза возникает у пожилых, но бывает врожденная или приобретенная у детей, послеродовая. Также выделяют тотальную, парциальную, первичную и вторичную. Диагностика синдрома гипопитуитарима включает анализ на гормоны, МРТ, КТ, рентген и прочие. Лечение — восстановление функции гормонами.
Опасная острая надпочечниковая недостаточность может возникнуть в любом возрасте. Причины синдрома — недостаток гормон. Симптомы острой формы нарастают мгновенно Проводится экспресс-диагностика, пациента госпитализирую для лечения.
Возникает хроническая надпочечниковая недостаточность при длительном течении заболевания, поражении вирусами, грибками. Первичная возникает у детей и взрослых, есть вторичная и третичная. Симптомы изначально скрыты. Осложнения тяжелые без лечения. Диагностика комплексная
источник
Адреногенитальный синдром – основные симптомы:
- Рвота
- Понос
- Пониженное артериальное давление
- Перебои в работе сердца
- Оволосение по мужскому типу
- Атрофия молочных желез
- Небольшой рост
- Развитая мускулатура
- Мужеподобное телосложение
- Увеличение клитора
- Короткие руки
- Атлетическое телосложение
- Короткие ноги
- Низкий голос
- Гиперпигментация половых органов
- Гиперпигментация ореол сосков
- Крупное тело
- Аномалии в развитии половых органов
- Мужские черты лица у женщин
- Плечи шире таза
Адреногенитальный синдром — это генетическая патология коры надпочечников (желез внутренней секреции, которые располагаются около почек), при которой происходит нехватка ферментов во время синтеза гормонов. Количество андрогенов увеличивается, что вызывает развитие вирилизации.
- Этиология
- Классификация
- Симптоматика
- Диагностика
- Лечение
- Возможные осложнения
- Профилактика
Адреногенитальный синдром у мальчиков и у девочек встречается в равной степени, но специфической профилактики не существует. Лечение врач назначает после диагностики, однако, полное устранение болезни невозможно.
Причины развития данной патологии зависят от того, врожденный развивающийся адреногенитальный синдром или же приобретенный.
Врожденный появляется из-за повреждения гена, который отвечает за выработку гормонов коры надпочечников. Дети наследуют такое заболевание по аутосомно-рецессивному типу. Другими словами, если только один родитель является носителем патологии, тогда адреногенитальный синдром у девочек или мальчиков не проявится. В случае когда и папа, и мама ‒ носители, тогда риск появления заболевания у ребенка равен 25%. Если болен один родитель, а второй ‒ носитель, тогда в 75% случаев родится больной малыш.
Приобретенный вид может развиться при доброкачественном образовании (андростерома), которое имеет тенденцию к перерождению в злокачественное. Такая опухоль может появиться в любом возрасте.
При диагностировании патологии, в 95% случаев выявляется врожденная форма, и только в 5% ‒ приобретенная.
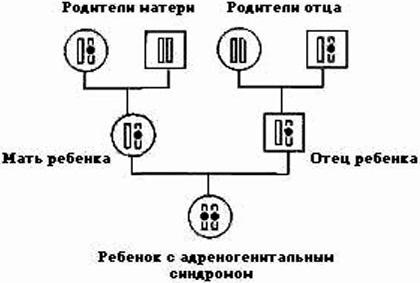
В медицине адреногенитальный синдром имеет классификацию, которая подразделяет его на три формы развития.
Итак, формы развивающегося адреногенитального синдрома следующие:
- Адреногенитальный выявленный синдром – сольтеряющая форма. Эту форму патологии можно выявить уже в течение первого года жизни малыша. У девочек наружные половые органы имеют мужское строение, а внутренние ‒ женское. Иногда определение пола сильно затруднено слишком выраженными изменениями. Говоря о мальчиках, у них увеличен половой член и наблюдается сильная пигментация мошонки. Нарушения в работе коры надпочечников приводят к возникновению тошноты, рвоты, диареи. Также может появиться сильная пигментация кожного покрова и начаться судороги.
- Адреногенитальный синдром – вирильная форма. Однако ее могут называть и по-другому ‒ адреногенитальный развивающийся синдром, классическая форма. Все визуальные признаки такие же, как и при сольтеряющей форме, но нет сбоя в работе коры надпочечников.
- Постпубертатная (неклассическая) форма. Для нее не характерны изменения строения наружных половых органов, но нет нарушений в работе коры надпочечников. Ее часто диагностируют у женщин, которые не могут забеременеть или жалуются на скудные выделения при месячных.
Различные формы развивающегося адреногенитального синдрома проявляют характерные признаки.
Необходимо сказать, что адреногенитальный синдром проявляет симптомы уже сразу после родов. Например, адреногенитальный синдром, выявленный у новорожденных, будет проявляться в виде большого веса и роста ребенка. Примерно к двенадцати годам рост останавливается, поэтому такие больные всегда имеет низкий рост. К тому же строение их тела больше схоже с мужским: у них крупное тело, короткие руки и ноги, а плечи шире таза.
При вирильной форме вырабатывается большое количество андрогенов. Нарушения в строении тела начинают развиваться еще в пубертатном периоде. В зависимости от времени появления вирилизации появляются совершенно различные симптомы. Например, у женщины могут расти волосы на лице, как у мужчин. Они будут такие же жесткие и черные. Клитор слишком увеличен, также наблюдаются аномалии в развитии половых органов. У таких пациенток мужские черты лица, телосложение, тембр голоса и хорошо развита мускулатура. У них часто наблюдается гиперпигментация половых органов и ореол около сосков.
Сольтеряющая форма появляется, когда возникает нехватка синтеза гормона альдостерона, ведь он нужен, чтобы соль через почки вернулась в кровоток. Это состояние проявляется такими симптомами, как сильная диарея и рвота, которые не связаны с приемами пищи, снижение показателей кровяного давления. Из-за этого в организме нарушается водно-солевой баланс, происходят сбои в работе сердца вплоть до летального исхода. Такой адреногенитальный развивающийся синдром у новорожденных считается самым опасным для жизни.
Постпубертатная (приобретенная) форма возникает из-за новообразования в коре надпочечников. Признаки этой формы таковы: атрофия молочных желез, редкие выделения при месячных, гипоплазия матки, увеличенный клитор. Появляется у девушек, уже живущих половой жизнью. У большинства представительниц женского пола такая форма вызывает бесплодие. У некоторых все же получается забеременеть, однако, в десять недель происходит самопроизвольный выкидыш.
Необходимо отметить, что адреногенитальный синдром, возникший у детей, точнее, у девочек, проявляет себя определенными признаками, а именно: наличие жестких и черных волос на лице и теле, понижение тембра голоса. Молочные железы, матка и половые губы недоразвитые. Первые месячные начинаются в 16 лет. Они могут быть нерегулярными и с задержками.
В редких случаях врачи выявляют гипертоническую форму болезни. В организме женщины обнаруживают много мужского гормона андрогена, постоянно присутствует высокое кровяное давление. В дальнейшем может случиться кровоизлияние в головной мозг. Также нарушается зрение, происходят сбои в работе сердечно-сосудистой системы.
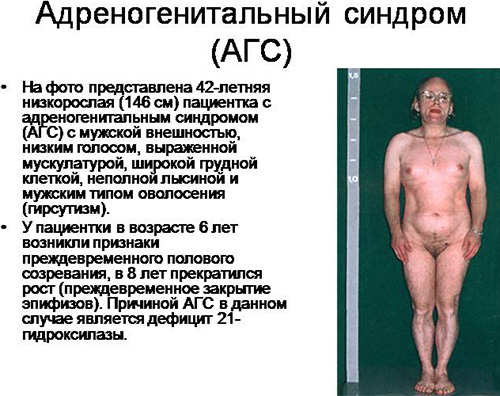
Диагностика развивающегося адреногенитального синдрома включает в себя следующие мероприятия:
- сбор анамнеза пациента и изучение жалоб;
- визуальный осмотр больного, при этом четко видна сильная пигментация кожного покрова, высокое кровяное давление, а также пациент имеет низкий рост, чрезмерный волосяной покров и измененное строение наружных половых органов;
- гормональные исследования – делается проба с дексаметазоном, чтобы определить 17-КС в крови до приема лекарственного препарата (глюкокортикоидов) и после приема;
- анализ на адреногенитальный развивающийся синдром – данное исследование является генетическим, оно может указать на риск развития патологии, а при положительном результате исследования можно начать своевременное лечение, то есть прогрессирование процесса будет приостановлено;
- определяется уровень тестостерона;
- ультразвуковое исследование;
- рентген;
- компьютерная томография;
- магнитно-резонансная томография.
Несколько тяжелее диагностировать патологический процесс, когда адреногенитальный синдром развивается у взрослых женщин параллельно с поликистозом яичников, поскольку эта патология провоцирует избыток выработки андрогенов.
Чтобы подтвердить диагноз, понадобится консультация гинеколога, эндокринолога, генетика, кардиолога и дерматовенеролога.
Лечение адреногенитального синдрома проводится с помощью комплексных мероприятий.
Врач может назначить следующие препараты:
- практически всегда назначают Дексаметазон;
- минералокортикоиды (при сольтеряющей форме).
Некоторым пациенткам проводится операция по пластике влагалища, а также полное или частичное удаление увеличенного клитора.
Основными осложнениями при данной патологии являются:
- бесплодие женщины;
- возникновение психологических проблем.
Пациентка может впасть в депрессию. Ее поведение становится агрессивным, появляются наклонности к суициду.
Так как адреногенитальный синдром имеет патогенез врожденный, то определенных профилактических мер нет.
Но будущие родители все же должны соблюдать некоторые правила:
- серьезно подходить к вопросу зачатия;
- во время вынашивания малыша избегать воздействия на организм негативных факторов;
- вовремя проконсультироваться с медицинским генетиком.
Другими словами, самой хорошей профилактикой является медико-генетическое консультирование. Полностью излечить данный патологический процесс у женщин или мужчин невозможно.
Если Вы считаете, что у вас Адреногенитальный синдром и характерные для этого заболевания симптомы, то вам могут помочь врачи: эндокринолог, гинеколог, генетик.
источник
Недуг представляет собой наследственное заболевание надпочечников, которое вызывает нарушение стероидогенеза. Гиперплазия парного органа является самой часто встречающейся патологией. Описываемая болезнь в медицинских кругах известна как синдром Крука-Апёра-Галле. Она связана с повышенным синтезом стероидных мужских половых гормонов и снижением уровня альдостерона и гидрокортизона. Причиной отклонения является врожденная дисфункция коры надпочечников (ВДКН).
Последствия недуга для маленьких деток представляют большую опасность, так как кора надпочечников производит большое количество гормонов, принимающих участие в регуляции большей части систем в организме. Теперь вы знаете ответ на вопрос: адреногенитальный синдром у мальчиков, что это такое.
Каждая разновидность недуга тесно связана с генетическими мутациями: чаще всего аномалия передается по наследственной линии от отца и матери к малышу. Реже встречаются ситуации, в которых тип наследования при АГС (адреногенитальный синдром) спорадический. Тип передачи аутосомно-рецессивный, каждый родитель является носителем опасного гена. Стоит отметить, что встречаются ситуации, при которых у абсолютно нормальной и здоровой семьи рождается кроха, пораженный данной болезнью.
Рассмотрим подробнее закономерности, которые оказывают воздействие на вероятность появления заболевания у крохи:
- мать и отец здоровы, но являются носителями гена, вызывающего липоидную гиперплазию надпочечников. В такой ситуации есть риск появления врожденной гиперплазии коры надпочечников у ребенка;
- если при обследовании, у одного из партнеров был выявлен недуг, а генетика второго партнера абсолютно нормальная. При таком раскладе, все дети этой пары будут здоровыми, но станут носителями патологии;
- если один из родителей имеет адреногенетический синдром, а второй является его носителем. У половины детей такой пары будут наблюдаться отклонения, а другая будет носителем мутации;
- если болеют оба родители, то все их дети также будут страдать от данной болезни.
Чаще всего тип наследования адреногенитального синдрома является врожденным.
Признаки описываемой проблемы можно выявить сразу после родов. Крохи с АГС отличаются от других слишком увеличенной массой тела и довольно крупным ростом. Их тело кажется вытянутым. В некоторых случаях рост ребенка в 11– 12 лет может резко прекратиться, и он останется таким на всю жизнь. У девочек заболевание вызывает изменения вульвы. Клитор приобретает членообразный внешний вид. Внутренние органы продолжают нормально развиваться, хотя со временем может произойти их атрофия. Несмотря на все это месячные либо нарушены, либо полностью отсутствуют. Грудь также может прекратить свое развитие. Маскулинизация сопровождается обильным оволосением малышек.
- Классическая. Вульва у малышек сформирована по гетеросексуальному типу: клитор увеличен, а половые губы имеют вид мошонки. При достижении возраста двух лет, у малышей обоих полов начинают возникать признаки полового созревания: появление волос в подмышечных впадинах и паху, изменение тембра голоса, появление округлостей на бедрах и груди, акне.
- Сольтеряющая. В дополнении к описанным выше симптомам добавляются признаки надпочечной недостаточности. Причем происходит это уже в первые несколько дней после появления крохи на свет. При сольтеряющей форме адреногенитального синдрома появляются такие симптомы как рвота, жидкий стул, маленькие пациенты быстро теряют вес, происходит снижение артериального давление и учащение количества сердечных сокращений. В результате может произойти остановка работы сердечной мышцы по причине слишком большого количества калия в крови.
- Постпубертатная. Признаки, характерные для полового созревания, появляются на третьем году жизни. У малышек нарушается менструальная функция, а на яичниках появляются кисты.
Узнав об основных симптомах адреногенитального синдрома, родители смогут своевременно выявить патологию и обратиться за помощью к специалистам.
До 96% всех отклонений происходит из-за вирилизирующей формы ВГКН, которая характеризуется дефектом 21-гидроксилазы, принимающей участие в синтезе стероидных гормонов. Если продуцирование гидрокортизона нарушено, это приводит к гиперразвитию коры надпочечников. У пациентов появляется ложная аномалия развития наружных половых органов. К примеру, у девочек наблюдаются признаки гермафродизма при рождении, а у мальчиков слишком рано начинает расти борода, усы, становится низким тембр голоса. Описанные отклонения свойственны классической форме адреногенитального синдрома. При полной блокаде фермента 21-гидроксилазы наступает нарушение процесса синтеза кортизола и альдостерона. При снижении последнего наблюдается потеря воды и натрия. Проявляется в виде избыточного количества стероидных мужских половых гормонов и надпочечниковой недостаточности. Данная картина характерная для сольтеряющей формы. Есть и неклассическая форма, для которой свойственны нарушения месячных в подростковом возрасте.
Как уже говорилось выше, андрогенитальный синдром имеет три формы.
- Сольтеряющая – характеризуется тяжелым течением и может проявиться уже в первых год жизни малыша. У него будут наблюдаться грубые нарушения в анатомии наружных половых органов. 21-гидроксилаза имеет активность не более 1%. Болезнь сопровождается судорогами, пигментацией кожных покровов, рвотой. Если не начать лечения, детки умирают в раннем возрасте.
- Верильная (классическая) течение не такое тяжелое, как у предыдущего варианта. Также наблюдаются изменения в строении гениталий. 21-гидроксилаза имеет активность 1–5%. Признаки надпочечниковой недостаточности у пациентов отсутствуют.
- Неклассическая (постпубертантная) – одна из самых благоприятных форм АГС. Ее признаки проявляются в период полового созревания и в репродуктивном возрасте. Гениталии имеют нормальный внешний вид. 21-гидроксилаза имеет активность 20-30%. В большинстве случаев, диагноз выявляется при возникновении проблем с зачатием.
Болезнь может привести к обезвоживанию организма. Это связано с тем, что при данном недуге перестает продуцироваться вещество, которое отвечает за сохранение жидкости в теле. Одним из главных осложнений при данном заболевании является развитие бесплодия. При своевременном лечении можно улучшить детородную функцию и предотвратить развитие бесплодия. Для этого назначается препарат «Простатилен АЦ». Он реализуется в виде ректальных суппозиторий и предназначен для поддержания мужского здоровья. Лекарство оказывает противовоспалительный эффект, устраняет болезненные ощущения, препятствует образованию тромбов и нормализует выработку секрета простаты. Препарат улучшает качество спермы, повышает уровень тестостерона в крови и нормализует сексуальную функцию. Осложнения при данном недуге заключаются в прогрессирующей надпочечниковой недостаточности. В связи с этим крайне важно своевременно обнаружить заболевание для его дальнейшего лечения.
Как и для любого заболевания, для выявления АГС необходимо провести исследование, назначенное лечащим врачом. Специалист в первую очередь назначает сдачу биохимического анализа крови. Опираясь на него, доктор сможет установить в норме ли гормональный фон пациента. Далее представлено фото врожденного адреногенитального синдрома. Очень важно выявить патологию на первых стадиях ее развития. После родов наружные половые органы мальчика нужно тщательно проверить: яички должны быть опущены в мошонку. Если присутствуют какие-либо отклонения, пациента должен осмотреть специалист по эндокринологии. Он назначает анализ для выявления полового хроматина. Дополнительно назначается ультразвуковое исследование, в некоторых случаях может потребоваться рентген. Малышу во сне измеряют базальную температуру тела.
Для выявления степени риска рождения неполноценных детей у родителей при планировании беременности берут кровь для проведения проб с адренокортикотропным гормоном. С их помощью лаборанты могут выявить наличие или отсутствие гетерозиготного носительства. Для проведения диагностики адреногенитального синдрома назначается анализ крови на определение кариотипа и выявления 17-OH-прогестерона. При выявлении болезни на ранних этапах риск развития осложнений минимален.
Большую помощь для своевременного определения патологии оказывает сбор семейного анамнеза. При помощи опроса становится ясно, имела ли место быть гибель детей в поколении из-за АГС. Если крохе поставлен страшный диагноз, необходимо уточнить у матери, принимала ли она во время вынашивания плода прогестерон или стероидные мужские половые гормоны. В подавляющем большинстве случаев недуг у маленьких пациентов диагностируется в возрасте 4-5 лет. Это связано с тем, что именно в этот период у мальчиков начинают появляться вторичные половые признаки. Если диагностика была проведена слишком поздно, а также если мальчик не получал своевременной гормональной терапии, возможен летальный исход в период от рождения и до одной недели жизни.
Сразу же после появления малыша на свет проводится скрининг. Если были выявлены какие-либо нарушения, проводится повторное обследование. После того как доктор выявил проблему и установил, что она носит врожденный характер может назначаться терапия. Как правило, начинают ее с назначения гормональных препаратов. Если заболевание приобретенное, то вначале необходимо устранить причины адреногенитального синдрома.
Лечение может быть медикаментозным или хирургическим, в зависимости от конкретного случая каждого пациента. Первый метод заключается в приеме таблеток, дополнительно может назначаться внутривенное введение натрия хлорида и глюкозы. Из гормонов назначаются такие лекарственные препараты, как флудрокортизон и преднизалон. Не стоит пытаться заниматься самолечением, правильную терапию может назначить только врач. При несоблюдении рекомендация по применению тех или иных медикаментов могут возникнуть побочные действия, которые нанесут вред организму.
При хирургическом лечении проводят операцию. Малышкам 4–6 лет проводят коррекцию вульвы. Критериями успешного оперативного лечения является:
- нормализация процесса роста ребенка;
- нормализация АД;
- нормализация уровня электролитов в крови.
Для устранения андреногенетического синдрома необходимо восполнить дефицит глюкокортикоидов. Выбор плана лечения зависит от симптомов, формы недуга и степень его выраженности. Назначается прием глюкокортикоидов и иных препаратов, в зависимости от анамнеза. Женщины могут значительно снизить риск развития болезни у ребенка. Для этого ей необходимо соблюдать следующие правила:
- проводить своевременное лечение хронических заболеваний;
- заниматься планированием периода беременности, а не обращаться в женскую консультацию уже по факту;
- не принимать лекарственных препаратов, не назначенных врачом, особенно актуально данное правило в первом триместре, так как именно в этот период происходит закладка органов у плода;
- если в роду у одного из супругов была мутация генов, необходимо пройти консультацию у генетика.
При сольтеряющей форме в профилактических целях надпочечниковой недостаточности больному периодические увеличивают дозу кортизона в несколько раз. Если у него развилось необходимое состояние, препарат вводят через капельницу.
В ситуации, если аномалия гениталий отсутствует, справиться с АГС помогут следующие рецепты.
- Настойка из трав. Возьмите засушенные цветки ландыша, полынь, чистотел и лапчатку гусиную по 1 столовой ложке. Залейте смесь кипятком и дайте настояться 2-3 часа. Употреблять внутрь 2 раза в день.
- Для улучшения гормонального фона проводиться гирудотерапия (лечение пиявками). В слюне этих кольчатых червей находятся ферменты, они активно стимулируют синтез недостающих гормонов в человеческом организме.
- Полезны следующие продукты: тыквенные семечки, молоко, отдельного внимания заслуживает чеснок, овсянка, миндаль, нежирная говядина.
Узнав о том, как улучшить состояние при АГС сольтеряющей форме, рассмотрим подробнее мероприятия, которые помогут предотвратить развитие патологии.
Как таковых препаратов, предупреждающих развитие дисфункции коры надпочечников, не существует. Все, что могут сделать родители, чтобы обезопасить семью от страшной болезни, это пройти своевременную генетическую консультацию. Для выявления отклонений в организме назначаются специальные анализы. Не помешает посещение эндокринолога, если в семье были случаи болезней эндокринологической системы. Генетика адреногенитального синдрома выявляется уже после рождения малыша. Для ее обнаружения нужно провести полное обследование крохи, это позволит быть уверенным в состоянии его здоровья. Чтобы обезопасить развитие недуга у себя, нужно на постоянной основе проходить осмотр у врача.
Если дефективность обнаружена вовремя и была выбрана оптимальная терапия, прогноз может быть благоприятным. Благодаря развитию медицины сегодня можно провести пластические операции, после которых пациент сможет вести нормальную половую жизнь. Прием гормональных препаратов нормализует месячные и способствует феминизации груди.
Из материалов данной статьи вы узнали о патологии, характеризующейся дисфункцией коры надпочечников. Если родители имеют в анамнезе данные отклонения, во время планирования беременности им необходимо пройти полное обследование у генетиков.
Далее представлен информативный ролик на тему адреногенитальный синдром у мужчин.
источник
Развитие адреногенитального синдрома у детей обусловлено генетически – заболеть им в течение жизни невозможно, его можно только унаследовать от родителей.
Известны случаи, когда у пары, в которой один из родителей страдает этой патологией, рождаются здоровые дети, но по статистике, риск унаследовать болезнь достигает 75 %.
Ярко выраженная симптоматика чаще всего проявляется у девочек, поэтому у них выявить АГС легче. У мальчиков обычно внешние признаки заболевания более завуалированы.
Адреногенитальный синдром новорожденных — это наследственное заболевание, обусловленное генетически детерминированным снижением активности ферментов, участвующих в стероидогенезе.
Причины адреногенитального синдрома, осложненного синдромом потери соли, чаще всего связаны с выраженным наследственным недостатком 21 -гидроксилазы.
Клиника адреногенитального синдрома у детей начинает проявляться уже на 1-2-й неделе жизни: у ребенка наблюдаются упорные срыгивания, прогрессирующее снижение массы тела.
Затем со 2-3-й недели вследствие увеличивающейся потери натрия почками, срыгивания учащаются, появляются рвота, иногда — «фонтаном», признаки эксикоза (сухая кожа и слизистые оболочки, западение большого родничка, глаз, заострение черт лица, землистый оттенок кожи).
Ребенок становится вялым, плохо сосет, у него снижается тонус мышц. Характерным симптомом адреногенитального синдрома является появление одышки.
Нередко новорожденные, особенно мальчики, поступают в клинику с симптомами тяжелого шока и токсикоза. Без лечения больные умирают от сосудистого коллапса.
Вследствие гиперкалиемии возможна внезапная смерть ребенка без явных признаков дегидратации и коллапса.
У новорожденных девочек отмечают увеличенный клитор и губомошоночное сращение; внутренние половые органы сформированы по женскому типу (псевдогермафродитизм). У мальчиков патология гениталий не выявляется.
Лечение адреногенитального синдрома заключается в заместительной терапии глюко-кортикоидами для подавления секреции АКТГ и гиперпродукции андрогенов, применении минералокортикоидов (флудрокортизон по 0,01-0,1 мг/сут.) для снижения уровня ренина в крови.
Из глюко-кортикоидов при выраженной надпочечниковой недостаточности назначают гидрокортизона гемисукцинат по 15-20 мг/(кг • сут.) или преднизолон по 2-10 мг/(кг•сут.).
В дальнейшем больного с врожденным адреногенитальным синдромом переводят на прием кортизона внутрь.
Суточную дозу подбирают индивидуально, обычно она не превышает 25-50 мг/сут. в 3-4 приема (половину дают на ночь). При выраженном синдроме потери соли вводят 0,5% масляный раствор ДОКСА по 0,5-1 мг/(кг•сут.) внутримышечно 1 раз в день.
При остром кризе потери соли проводят регидратационную терапию (5% раствор глюкозы, реополиглюкин, производные гидроксиэтилкрахмала), борьбу с ацидозом (4% раствор натрия гидрокарбоната по 2-2,5 мл/кг, под контролем КОС, кокарбоксилаза — 50-100 мг) и гиперкалиемией (10% раствор кальция глюконата в дозе 1 мл/год жизни, 10% раствор глюкозы с инсулином), вводят изотонический раствор натрия хлорида.
Соблюдая рекомендации по лечению адреногенитального синдрома, контролем адекватности терапии служит нормализация экскреции 17-КС с мочой и электролитного состава крови.
Адреногенитальный синдром (синонимы: АГС, врожденная дисфункция коры надпочечников или врожденная надпочечниковая гиперплазия) представляет собой заболевание, в основе которого лежит наследственное нарушение биосинтеза стероидных гормонов.
Надпочечники представляют собой парные органы, которые находятся на верхних полюсах почек. Каждую железу покрывает плотная оболочка (капсула), которая проникает внутрь и делит орган на два слоя: корковое вещество (наружный слой) и мозговое вещество (внутренний слой). Корковое вещество синтезирует кортикостероиды:
- глюкокортикоиды (кортикостерон, кортизон) – регулируют все обменные процессы;
- минералокортикоиды (альдостерон) – регулирует калиево-натриевый баланс;
- половые гормоны.
Мозговое вещество отвечает за выработку катехоламинов (адреналин и норадреналин). Адреналин увеличивает частоту и силу сердечных сокращений. Норадреналин поддерживает тонус сосудов.
Возникновение врожденной надпочечниковой гиперплазии связано с угнетением продукции (выработки) одних кортикостероидных гормонов при одновременной активации выработки других. Это происходит из-за нехватки того или иного фермента, который участвует в стероидогенезе (продуцировании кортикостероидов). Основной патогенетический механизм АГС – врожденный дефицит фермента С 21-гидроксилазы.
В зависимости от степени дефицита фермента развивается недостаточность альдостерона и кортизола.
Нехватка последнего по типу отрицательной обратной связи стимулирует выработку адренокортикотропного гормона (АКТГ), который воздействует на кору надпочечников и приводит к ее гиперплазии.
В результате этого кортикостероиды синтезируются выше нормы, т. е. стероидогенез сдвигается в сторону избыточности андрогенов.
В механизме развития заболевания лежит избыточная выработка одних кортикостероидных гормонов при снижении продукции других
В организме развивается гиперандрогения надпочечникового происхождения. Повышенная выработка андрогенов оказывает вирилизирующее (лат. «вирилис» – мужской, «вирилизация» – маскулинизация) действие на ребенка еще во внутриутробном периоде.
Впоследствии развивается классическая (врожденная) форма заболевания. Клинические проявления зависят от степени активности мутированного гена СУР21-В.
При полном отсутствии активности формируется сольтеряющая форма синдрома, при которой нарушается выработка и минералокортикоидов, и глюкокортикоидов.
Распространенность АГС варьируется среди различных национальностей. Среди европеоидов классические варианты врожденной надпочечниковой гиперплазии составляют один случай на 14000 новорожденных детей (1 к 9800 – в Швеции, 1 к 11000 – в США).
В Японии заболеваемость составляет 1 случай на 18000 новорожденных. Среди изолированных популяций распространенность АГС превышает средние показатели в 5–10 раз.
Так, у эскимосов Аляски распространенность классических вариантов заболевания составляет примерно один случай на 282 новорожденного.
Врожденная надпочечниковая гиперплазия очень разнообразна по клиническим проявлениям. Выделяют две классические формы заболевания:
- сольтеряющая;
- простая вирильная форма.
Для сольтеряющей формы характерно полное отсутствие фермента, что проявляется в виде нарушения солевого обмена (недостаточность минералокортикоидов). В патологический процесс вовлекается ренинальдостероновая система.
Симптомы появляются в первые дни после рождения младенца.
Адреногенитальный синдром у новорожденных по типу надпочечниковой недостаточности (нехватка альдостерона и кортизона) сопровождается следующими признаками:
- срыгивания;
- рвота;
- плохое периферическое кровообращение;
- снижение массы;
- сонливость.
Обезвоживание организма вызывает жажду, из-за чего наблюдается активное сосание. Перечисленные симптомы возникают на второй–третьей неделе после рождения. О дефиците глюкокортикоидов свидетельствует прогрессирующая гиперпигментация.
Надпочечниковая недостаточность сопровождается признаками обезвоживания и недостаточности кровообращения
В биохимическом анализе крови присутствуют гипонатриемия (недостаток натрия), гиперкалиемия (избыток калия), ацидоз («закисление» организма).
При избытке андрогенов с ранних стадий внутриутробного развития у новорожденных девочек отмечается женский псевдогермафродизм.
Изменения варьируются от обычной гипертрофии клитора до полной вирилизации наружных половых органов (пенисообразный клитор с вытягиванием уретрального отверстия на головку).
У мальчиков наблюдается увеличение пениса с гиперпигментацией мошонки. При отсутствии адекватного лечения в постнатальном периоде вирилизация быстро прогрессирует.
Зоны роста костей закрываются раньше времени, из-за чего взрослые пациенты отличаются низкорослостью.
У девочек отсутствие лечения приводит к первичной аменорее, связанной с угнетением гипофизарно-яичниковой системы гиперпродукцией мужских половых гормонов.
Вирильная форма характеризуется прогрессирующей маскулинизацией, быстрым формированием органов, повышенным выделением гормонов коры надпочечников.
У родившихся девочек с кариотипом 46,ХХ присутствует маскулинизация различной выраженности – от умеренно гипертрофированного клитора до абсолютного сращивания губных складок с образованием пениса и мошонки.
Внутренняя половая система сформирована без особенностей – по женскому типу.
У мальчиков вирильный АГС сразу после появления на свет обычно не диагностируется, так как гениталии визуально обычные. Диагноз ставят на пятом-седьмом году жизни при появлении признаков раннего полового созревания. Выделяют также неклассическую (позднюю) форму дефицита 21-гидроксилазы, которая обусловлена снижением активности фермента на 40–80% по сравнению с нормальными показателями.
Клинически заболевание проявляется в подростковом возрасте
У девочек присутствует умеренное увеличение клитора, уменьшение размеров матки, раннее формирование груди, преждевременное закрытие зон роста скелета, нарушения менструации, гирсутизм (рост волос по мужскому типу). Первая менструация случается в 15–16 лет, далее цикл сбивается, имеется тенденция к олигоменорее (большие промежутки между месячными).
Влияние мужских гормонов сказывается на комплекции: больше мужские пропорции туловища, размашистые плечи, суженый таз, укороченные конечности. Нередко у пациенток в дальнейшем развивается бесплодие, часто беременность прерывается на ранних сроках. У мальчиков признаком избыточности андрогенов является раннее закрытие зон роста костей, уменьшение яичек.
У всех детей независимо от пола наиболее частый симптом неклассической формы АГС – преждевременное лобковое и подмышечное оволосение. Латентно протекающая врожденная надпочечниковая гиперплазия не имеет клинических признаков, однако в крови можно обнаружить умеренно повышенный уровень предшественников кортизола. Далеко не все авторы выделяют такое состояние в отдельную форму заболевания.
Ведущее место в диагностике заболевания отводится гормональным анализам. Для определения генезиса андрогенов гормональные тесты проводятся до и после дексаметазоновой пробы. Понижение уровня ДГЭА и ДГЭАС в крови после приема специальных средств, затормаживающих экскрецию АКТГ, свидетельствует о надпочечниковом происхождении мужских гормонов.
Исследование крови на гормоны – основной метод диагностики
При сольтеряющей форме болезни наблюдается повышение уровня ренина в плазме, что отражает недостаток альдостерона и обезвоживание. При классической форме вместе с этим увеличивается уровень АКТГ.
При поздних формах заболевания устанавливают в семейном анамнезе случаи сбоев цикла у родственниц по обеим линиям.
На запущенные формы указывают типичные признаки: преждевременное оволосение у девочек по мужскому типу, поздние месячные, «спортивное» телосложение и др.
С помощью УЗИ яичников можно установить ановуляцию (отсутствие овуляции): присутствие фолликулов разной степени зрелости, но не достигших преовуляторного диаметра. У девочек наблюдается базальная температура с растянувшейся первой фазой и короткой второй. Это указывает на недостаточность желтого тела. Также отмечается андрогенный тип мазков из влагалища.
АГС, наряду с галактоземией, относится к заболеваниям, подлежащим просеивающей диагностике у новорожденных, однако это не совсем оправдано. Ранний неонатальный скрининг не помогает корректировке нарушений у девочек. Лучше проводить пренатальную диагностику и пренатальное лечение недостаточности фермента в семьях, где оба родителя гетерозиготные и уже имеют больное потомство.
Это позволяет принять решение в отношении сохранения беременности. В случае сохранения проводится внутриутробная терапия гормонами, что избавляет девочку от необходимости корректировать половые органы хирургическим путем.
Исследование мочи для выявления сольтеряющей формы заболевания
У мальчиков своевременно диагностируют сольтеряющую форму, выявление которой в постнатальном периоде нередко задерживается.
Дифференциальная диагностика адреногенитального синдрома проводится с андрогенпродуцирующими опухолями надпочечников и половых желез, идиопатическим ранним половым созреванием у мальчиков. Сольтеряющую форму следует отличать от редких вариантов врожденной дисфункции коры надпочечников, псевдогиперальдостеронизма и некоторых других нарушений.
При классической форме детям назначаются Гидрокортизон в таблетках (суточная доза 15–20 мг/м2 поверхности тела) или Преднизолон в дозировке 5мг/м2.
Суточную дозировку разбивают на два приема: треть дозы утром и две трети перед сном. Это позволяет максимально подавить выработку АКТГ гипофизом.
При неполноценной второй фазе цикла требуется стимуляция овуляции с пятого по девятый день цикла, что значительно повышает шансы на беременность.
Если беременность наступила, прием глюкокортикостероидов следует продолжить во избежание самопроизвольного выкидыша. При сольтеряющем АГС назначают флудрокортизон (от 50 до 200 мкг/сутки).
Если имеются тяжелые сопутствующие болезни или проведена операция, дозу глюкокортикоидов увеличивают.
При запоздалой постановке диагноза вирильной формы АГС у пациентов с генетически женским полом проводят хирургическое вмешательство, направленное на пластику наружных половых органов.
Неклассическая форма заболевания требует лечения только при выраженных внешних проблемах (угри, гирсутизм) или снижении фертильности. В этом случае назначают 0,25-0,5 мг дексаметазона или до 5 мг преднизолона перед сном.
Гормонотерапия занимает основное место в лечении
Угри и гирсутизм эффективно корректируются с помощью антиандрогенов (ципротерон) вместе с эстрогенами (в составе средств оральной контрацепции). Антиандрогенным действием обладает спиронолактон. Препарат принимают по 25 мг два раза в сутки. Использование спиронолактона в течение полугода снижает уровень тестостерона на 80%.
Гипертрихоз уменьшают также синтетические прогестины, однако женщинам с врожденной надпочечниковой гиперплазией длительно применять их не следует (в соответствии с рекомендациями врачей, подавление гонадотропинов нежелательно при угнетенной функции яичников). Мужчины с неклассическим типом заболевания лечение не проходят.
При классической форме прогноз зависит от своевременной постановки диагноза (предотвращение выраженных нарушений строения наружных половых органов у девочек), качества назначенного лечения и своевременности проведения хирургического вмешательства на гениталиях. Сохранение гиперандрогении или перенасыщенность кортикостероидами приводят к тому, что пациенты остаются низкого роста.
Это вкупе с косметическими дефектами значительно нарушает психосоциальную адаптацию. При адекватном и своевременном лечении у женщин с классической формой АГС возможно благополучное наступление и вынашивание беременности.
Светлана:
Дочери поставили диагноз ВДКН. Сейчас ей три года. Заместительная терапия – постоянный и важнейший этап в лечении. Пока все антропометрические критерии в норме. Эндокринолог говорит, что дозу гормонов пока повышать не стоит, а при стрессовых ситуациях сказал вводить гидрокортизон внутримышечно.
Мария:
У ребенка еще внутриутробно диагностировали АГС, лечение начали вовремя. Сразу после рождения обратились в платную клинику, сделали операцию, принимаем теперь назначенные препараты. Врачи говорят, все будет в норме, беременность в дальнейшем возможна.
Адреногенитальный синдром у детей вызывается генным нарушением, которое передается по наследству от родителей. В первую очередь это заметно по функциям надпочечников, а также по состоянию половых органов. Особенно это проявляется у женщин, так как в организме начинают преобладать мужские гормоны.
Встречается несколько разновидностей данного синдрома. Чаще всего, в 90% случаев, его вызывает недостаточное количество ферментов 21 гидроксилазы.
- Первая форма является вирилизирующей. При ней сильно увеличены половые признаки. В особенности это заметно у лиц женского пола, когда начинаются развиваться половые органы после рождения. Внутренняя структура остается нормальной, не внешне заметно увеличение клитора, который может принять вид пениса.
- Вторая форма, в которой может проходить болезнь, это сольтеряющая. Здесь проявляется недостаток альдостерона. Почки не возвращают соль в кровоток, что вызывает серьезные последствия, вплоть до смертельного исхода.
- Третьей формой является врожденная, при которой недостаток гидроксила проявляется сразу после рождения. Адреногенитальный синдром у недоношенных новорожденных проявляется, если рецессивные гены были у обоих родителей.
Адреногенитальный синдром у мальчиков и девочек передается генетически по аутосомно-рецессивному виду. Это означает, что за одно поколение накапливаются больные, которые передают болезнь детям. У предков мог быть ряд отклонений в данной области, которые приводят к более яркому проявлению у ребенка.
Только одна хромосома может содержать ген с данным синдромом. Он может быть нормальным или мутантным. У ребенка он становится мутантным, что и приводит к болезни.
Если мутантный ген только у одного из родителей, то ребенок может быть вполне здоровым, так как наличие лишь одного такого гена не приводит к проявлению болезни и человек может считаться вполне здоровым.
Для выявления болезни у новорожденных используется несколько диагностических методов. В первую очередь это можно определить визуально, так как наблюдается явное отклонение в строении наружных половых органов. Неправильная форма и увеличение размеров говорит о большой вероятности заболевания.
Если в анализе крови обнаруживается слишком высокое содержание 17-ОН-прогестерона, то это также говорит о наличии синдрома, причем определить это можно буквально с первых дней жизни.
Уже на 2 день можно проводить скрининг тесты и если прогестерон будет превышать норму в несколько раз, то можно диагностировать адреногенитальный синдром.
Если синдром сопряжен с потерей соли, то характерными его проявлениями станут гипохлоремия, гипонатриемия, а также гиперкалиемия. С мочой повышается экскреция 17-кетостероидов.
Существует также несколько инструментальных методов выявления болезни. Адреногенитальный синдром у девочки может проявляться в обнаружении матки и яичников в раннем возрасте. Также может быть увеличение костного возраста по рентгенограмме. Он заметно выше фактического возраста ребенка.
Во время первого года жизни ребенка дифференциальная диагностика проводится с ложной формой гермафродитизма. Чтобы более точно определить диагноз, специалисты обращают внимание на кариотипирование и 17-он-прогестерон. Это помогает выделить синдром на фоне других болезней, на которые возникли подозрения у ребенка.
За первичные и вторичные половые признаки отвечают гормоны, часть которых вырабатывается в надпочечниках. Существует врожденное заболевание, характеризующееся дисфункцией этих желез внутренней секреции и чрезмерным выделением андрогенов. Избыток мужских половых гормонов в организме приводит к существенным изменениям строения тела.
Рассматриваемая патология возникает вследствие врожденной генетической мутации, передающейся по наследству. Она диагностируется редко, частота встречаемости адреногенитального синдрома составляет 1 случай на 5000-6500.
Изменение генетического кода провоцирует увеличение размеров и ухудшение работы коры надпочечников. Снижается выработка особых ферментов, которые участвуют в продуцировании кортизола и альдостерона.
Их дефицит приводит к увеличению концентрации мужских половых гормонов.
В зависимости от степени разрастания надпочечниковой коры и выраженности симптомов описываемая болезнь существует в нескольких вариациях. Формы адреногенитального синдрома:
- сольтеряющая;
- вирильная (простая);
- постпубертатная (неклассическая, атипичная).
Самый распространенный вид патологии, который диагностируется у новорожденных или детей первого года жизни. При сольтеряющей форме адреногенитального синдрома характерно нарушение гормонального баланса и недостаточность функции коры надпочечников.
Данный тип заболевания сопровождается слишком низкой концентрацией альдостерона. Он необходим для поддержания водно-солевого баланса в организме. Указанный адреногенитальный синдром провоцирует нарушение сердечной деятельности и скачки артериального давления.
Это происходит на фоне скопления солей в почках.
Простой или классический вариант течения патологии не сопровождается явлениями надпочечниковой недостаточности. Описываемый адреногенитальный синдром (АГС вирильной формы) приводит только к изменениям наружных половых органов. Этот вид болезни тоже диагностируется в раннем возрасте или сразу после родов. Внутри репродуктивная система остается нормальной.
Рассматриваемый тип заболевания еще называют атипичным, приобретенным и неклассическим. Такой адреногенитальный синдром встречается только у женщин, которые ведут активную половую жизнь.
Причиной развития патологии может стать как врожденная мутация генов, так и опухоль коры надпочечников. Данная болезнь часто сопровождается бесплодием, поэтому без адекватной терапии адреногенитальный синдром и беременность – несовместимые понятия.
Даже при успешном зачатии высок риск невынашивания, плод гибнет еще на ранних сроках (7-10 недель).
Клиническая картина описываемой генетической аномалии соответствует возрасту и форме заболевания. Адреногенитальный синдром у новорожденных иногда определить не удается, из-за чего пол младенца могут идентифицировать неправильно. Специфические признаки патологии становятся заметны с 2-4 лет, в некоторых случаях она проявляется позже, в подростковом периоде или зрелости.
При сольтеряющей форме болезни наблюдаются симптомы нарушения водно-солевого баланса:
- диарея;
- сильная рвота;
- пониженное артериальное давление;
- судороги;
- тахикардия;
- потеря веса.
Простой адреногенитальный синдром у детей мужского пола имеет следующие признаки:
- увеличенный пенис;
- избыточная пигментация кожи мошонки;
- темный эпидермис вокруг ануса.
Новорожденным мальчикам редко ставится указанный диагноз, потому что клиническая картина в раннем возрасте выражена слабо. Позднее (с 2-х лет) адреногенитальный синдром более заметен:
- рост волос на теле, включая половые органы;
- низкий, грубоватый голос;
- гормональные прыщи (вульгарные угри);
- маскулинизация;
- ускорение формирования костей;
- низкорослость.
Определить рассматриваемую болезнь у младенцев женского пола проще, она сопровождается такими симптомами:
- гипертрофированный клитор, внешне очень похожий на пенис;
- большие половые губы, выглядят, как мошонка;
- вагина и уретра объединены в урогенитальный синус.
На фоне представленных признаков новорожденных девочек иногда принимают за мальчиков и воспитывают в соответствии с неправильно установленным полом.
Из-за этого в школьном или подростковом возрасте у таких детей часто появляются психологические проблемы. Внутри репродуктивная система девочки полностью соответствует женскому генотипу, поэтому и ощущает она себя женщиной.
У ребенка начинаются внутренние противоречия и сложности с адаптацией в обществе.
После 2-х лет врожденный адреногенитальный синдром характеризуется следующими признаками:
- преждевременный рост волос на лобке и подмышками;
- короткие ноги и руки;
- мускулистость;
- появление волос на лице (к 8-ми годам);
- мужское телосложение (широкие плечи, узкий таз);
- отсутствие роста молочных желез;
- низкий рост и массивное туловище;
- грубый голос;
- угревая болезнь;
- позднее начало менструаций (не раньше 15-16 лет);
- нестабильный цикл, частые задержки месячных;
- аменорея или олигоменорея;
- бесплодие;
- скачки артериального давления;
- избыточная пигментация эпидермиса.
Выявить гиперплазию и дисфункцию коры надпочечников помогают инструментальные и лабораторные исследования. Чтобы диагностировать адреногенитальный врожденный синдром у младенцев, выполняется тщательный осмотр половых органов и компьютерная томография (либо УЗИ). Аппаратное обследование позволяет обнаружить яичники и матку у девочек с мужскими половыми органами.
Для подтверждения предполагаемого диагноза осуществляется лабораторный анализ на адреногенитальный синдром. Он включает исследование мочи и крови на содержание гормонов:
- 17-ОН-прогестерона;
- альдостерона;
- кортизола;
- 17-кетостероидов.
- биохимия;
- клинический анализ крови;
- общее исследование мочи.
Избавиться от рассмотренной генетической патологии нельзя, но ее клинические проявления можно устранить. Адреногенитальный синдром – клинические рекомендации:
- Пожизненный прием гормональных препаратов. Для нормализации работы коры надпочечников и контроля эндокринного баланса придется постоянно пить глюкокортикоиды. Предпочтительный вариант – Дексаметазон. Дозировка рассчитывается индивидуально и составляет от 0,05 до 0,25 мг в день. При сольтеряющей форме болезни важно принимать минералкортикоиды, чтобы поддерживать водно-солевой баланс.
- Коррекция внешнего вида. Пациенткам с описываемым диагнозом рекомендуется пластика влагалища, клиторэктомия и другие хирургические вмешательства, обеспечивающие придание половым органам правильной формы и соответствующего размера.
- Регулярные консультации с психологом (по требованию). Некоторым больным необходима помощь в социальной адаптации и принятии себя как полноценного человека.
- Стимуляция овуляции. Женщинам, желающим забеременеть, требуется пройти курс специальных медикаментов, обеспечивающих корректировку менструального цикла и подавление выработки андрогенов. Глюкокортикоиды принимаются весь период вынашивания.
Адреногенитальный синдром, или врожденная гиперплазия коры надпочечников, — это генетически обусловленное наследственное аутосомно-рецессивное эндокринное заболевание, возникающие в результате нарушения синтеза в организме альдостерона, кортизола и андрогенов.
Путь наследования врожденной гиперплазии надпочечников. Патологический ген обозначен черным кружочком
В большинстве случаев (более 95%) причиной нарушения синтеза в организме альдостерона, кортизола и андрогенов является дефицит 21-гидроксилазы. Данный фермент является предшественником в цепочке образования этих гормонов.
Схема синтеза гормонов надпочечников. 21-гидроксилаза обозначается как CYP-21.
В результате недостатка данного фермента в организме возникает дефицит альдостерона и кортизола.
Для того, чтобы компенсировать недостаток этих гормонов, начинает активно синтезироваться адренокортикотропный гормон (стимулятор). Действует он на всю кору надпочечника, однако т.к.
дефицит CYP-21 не устранен, синтез идет по 3-му пути: образование андрогенов (21-гидроксилаза независимый путь).
Результатом таких нарушений является:
- Снижение уровня альдостерона и кортизола.
- Избыток андрогенов и тестостерона.
Существует 3 клинических варианта течения врожденной гиперплазии надпочечников (в основе лежит степень недостаточности 21-гидроксилазы):
- Сольтеряющая форма — характеризуется практически полным отсутствием синтеза данного фермента.
- Типичная вирильная форма — частичная недостаточность фермента.
- Нетипичная (поздняя) форма.
Данная форма адреногенитального синдрома ярче проявляется у девочек. Это связано с тем, что из-за дефицита 21-гидроксилазы возникает избыток андрогенов при нормальном уровне альдостерона и кортизола.
В результате этого у девочек начинается процесс вирилизации (омужествления). Происходит это в эмбриональном периоде на 24-25 неделе.
Поэтому первые признаки простой формы адреногенитального синдрома у новорожденных девочек можно заметить уже сразу после родов. К таковым относят:
- гипертрофию клитора;
- наличие сращения больших половых губ (мошоночный шов);
- урогенитальный синус.
Степень выраженности надпочечниковой гиперандрогении разнообразна от небольшого увеличения клитора до полного формирования наружных мужских половых органов (ложный гермафродитизм).
При несвоевременной постановке диагноза врожденной гиперплазии надпочечников процессы вирилизации продолжаются:
- Отмечается раннее закрытие зон роста. Итог — низкорослость.
- Избыточное оволосение по мужскому типу, причем возможно его появление уже в 2-3 года.
- Формирование мужеподобной фигуры (узкий таз, широкие плечи).
- Аменорея.
- Бесплодие.
Гипертрихоз у женщин с адреногенитальном синдромом может возникнуть в области подбородка, а также бывает избыточное оволосение верхней губы, белой линии живота, бедер, ягодиц.
Адреногенитальный синдром у мальчиков имеет не столь выраженную клиническую картину. При рождении не наблюдается никаких аномалий развития. Внешние и внутренние половые органы сформированы правильно.
Первыми симптомами тревоги могут стать раннее появление вторичных половых признаков (увеличение в размерах пениса, появление оволосения). Начинается ложное преждевременное половое созревание.
Возраст 3-4 года, иногда возможно и раньше. Зоны костного роста так же, как и у девочек, закрываются рано: к 9-10 годам.
Репродуктивная функция чаще всего сохранена, однако возможно развитие олиго- или азооспермии.
Эта форма является наиболее жизнеугрожающей из всех вариантов течения врожденной гиперплазии надпочечников, т.к. при отсутствии своевременной постановки диагноза и адекватного лечения ребенок гибнет в течение первого месяца жизни.
В патогенезе заболевания лежит полное отсутствие фермента 21-гидроксилазы, в результате чего развивается недостаточность альдостерона и кортизола. Итог — отсутствие нормальной реабсорбции в канальцах почек, избыточное мочевыделение.
Первые симптомы тревоги могут появиться на 2-й неделе жизни ребенка. Это может быть вялость, сонливость, адинамия в поведении. Обильное мочевыделение, срыгивание, рвота. Снижение аппетита.
Через 2-3 дня от начала клинического проявления заболевания появляются симптомы дегидратации и развития метаболического ацидоза
Гибель наступает от развития острой надпочечниковой недостаточности и шока.
Наиболее распространенная форма адреногенитального синдрома. Клиническая картина весьма скудная. До начала полового созревания часто наблюдается полное отсутствие симптомов. Иногда отмечают:
- некоторое ускорение роста;
- костный возраст опережает биологический;
- у девочек — небольшое увеличение клитора;
- у мальчиков — рост полового члена без увеличения размеров яичек.
В период полового созревания проявляются следующие симптомы:
- относительно раннее начало: для девочек 8-9 лет, для мальчиков 9-10 лет;
- появление угревой болезни;
- гирсутизм (рост волос по мужскому типу) у девочек;
- нарушение менструальной функции;
- поликистоз яичников;
- бесплодие;
- невынашивание беременности.
Для диагностики адреногенитального синдрома проводится ряд исследований и анализов.
Начинается исследование со сбора анамнеза (были ли случаи возникновения данного заболевания у родителей, родственников, братьев, сестер).
Далее производится внешний осмотр. При этом оценивается фигура, рост, состояние внешних и внутренних половых органов, степень оволосения.
Шкала измерения избыточного оволосения у женщин. По результатам визуального осмотра каждой области присваивается определенное количество баллов в зависимости от степени развития волосяного покрова. Сумма баллов более 8 считается патологией.
Для подтверждения адреногенитального синдрома проводится ряд анализов на гормоны. К таковым относится анализ на 17-гидроксипрогестерон. Повышение уровня данного гормона выше 15 нмоль/л является диагностическим критерием врожденной гиперплазии надпочечников.
Для диагностики сольтеряющей формы проводится исследование уровня ренина в крови.
Лечение адреногенитального синдрома пожизненное. Цель — проведение заместительной терапии. Обычно используется гидрокортизон или преднизолон. Дозировки подбираются врачом индивидуально.
При возникновении сольтеряющей формы, кроме глюкокортикостероидов, назначаются и аналоги минералокортикоидных гормонов (флудрокортизон).
Данный препарат назначается в неонатальном периоде с последующим снижением дозы и полной отменой препарата
Кроме консервативного лечения, иногда применяют и хирургическое. Чаще всего это коррекция наружных половых органов у девочек — удаление увеличенного клитора, коррекция урогенитального синуса, формирование влагалища.
При своевременно начатом лечении прогноз относительно жизни таких пациентов благоприятный. Так как ранняя заместительная терапия позволяет стимулировать правильное развитие половых органов как у мальчиков, так и у девочек, благоприятен прогноз и в отношении сохранения репродуктивной функции.
Адреногенитальный синдром — это группа наследственных и приобретенных заболеваний, главным признаком которых является мутация в определенном гене. Данные нарушения проявляются в чрезмерном выделении гормонов коры надпочечников.
Данному заболеванию предрасположены как мальчики, так и девочки, причем в равной степени. Адреногенитальный синдром у новорожденных встречается довольно часто. Вероятность появления ферментативного дефекта составляет порядка 1:14000. Несвоевременная диагностика адреногенитального синдрома, неправильная терапия могут привести к достаточно тяжелым последствиям:
- Ошибке в выборе половой принадлежности, связанной с выраженной вирилизацией наружных гениталий у девочки;
- Нарушению роста и последующего полового созревания;
- Бесплодию;
- Смерти ребенка от сольтеряющих кризов.
Адреногенитальный синдром встречается в трех формах:
- Вирильная, нарушения при которой начинаются у плода еще в период беременности. Проявляется в том, что рождающиеся девочки имеют признаки, указывающие на ложный женский гермафродитизм, а мальчики – большой половой член. Адреногенитальный синдром у детей в данной форме выражается:
- В сильной пигментации кожи в области наружных половых органов, около анального отверстия и вокруг сосков;
- Преждевременном половом созревании (первые признаки появляются уже в возрасте 2 – 4 лет);
- Низкорослости.
- Сольтеряющая. Данная форма характеризуется следующими признаками:
- Обильная рвота, которая не связана с приемами пищи;
- Жидкий стул;
- Пониженное артериальное давление.
В результате у больного наблюдается нарушение уровня водно-солевого баланса, работы сердца и последующая гибель ребенка.
Т.е. каждая форма имеет свои симптомы адреногенитального синдрома.
Адреногенитальный синдром у новорожденных возникает по различным причинам. Каждая из них имеет свои отличительные особенности и зависит от формы заболевания.
Наиболее распространенной является дефицит ферментов, которые участвуют в синтезе гормонов надпочечников — 21-гидроксилазы, реже 11-гидроксилазы и 3-бета-ол-дегидрогеназы и других. В результате синтезируется недостаточное количество кортизола и альдостерона. Эти вещества относятся к стероидным гормонам коры надпочечников.
Кортизол отвечает за защиту организма от проникновения различного рода инфекций и стресса. Альдостерон отвечает за нормальный уровень кровяного давления и работу почек.
Недостаток этих гормонов приводит к повышенной секреции адренокортикотропного гормона, способствующего гиперплазии коры надпочечников и развитию данного заболевания.
Т.к. данное заболевание носит врожденный характер, обусловленный мутацией определенных генов, то единственным профилактическим методом при адреногенитальном синдроме можно назвать медико-генетические консультации.
Адреногенитальный синдром у детей может быть выявлен на ранней стадии протекания заболевания.
Связано это с тем, что всем родившимся малышам в роддоме на четвертые сутки проводят неонатальный скрининг – капельку крови из пятки новорожденного наносят на тест-полоску.
При положительной реакции ребенка отправляют в эндокринологический диспансер для повторного обследования. При подтверждении диагноза сразу назначается соответствующее лечение.
Диагностика адреногенитального синдрома проводится достаточно просто. Однако на практике согласно статистических данных данная патология выявляется на поздних стадиях развития заболевания.
В настоящее время диагностика данного заболевания включает следующие этапы:
- Проводится сбор данных семейного анамнеза. Это позволяет узнать были ли в роду случаи гибели грудных детей, связанные с адреногенитальным синдромом.
- При выявлении у новорожденного патологии в области развития половых органов, у матери выясняют, принимала ли она во время беременности андрогены или прогестерон.
- Проводится обязательное общее клиническое обследование. На данном этапе выявляются симптомы, характерные для адреногенитального синдрома.
- Делаются рентгеновские снимки кистей рук для определения костного возраста.
- Проводится ультразвуковое обследование. У девочек – УЗИ матки и придатков, у мальчиков – мошонки. А также обязательно проводится УЗИ органов в области забрюшинного пространства.
- Проводится обследование у генетиков для определения набора хромосом, полового хроматина.
- Компьютерная томография головного мозга и электрокардиограмма.
- Сдаются анализы:
- Мочи на повышенное выделение 17-кетостероидов;
- Крови на уровень гормонов;
- Крови на уровень калия, натрия, хлоридов;
- Биохимический анализ крови.
- Проводятся осмотры у врачей-специалистов. Гинеколог, эндокринолог, уролог, онколог, дерматовенеролог, детский кардиолог и окулист должны дать свои заключения.
Лечение адреногенитального синдрома проводится двумя способами – медикаментозным и хирургическим.
Медикаментозный способ зависит от формы заболевания. Так при вирильной форме он заключается в восполнении недостатка глюкокортикостероидных гормонов.
Доза препарата (преднизолона) строго индивидуальна и определяется по следующим параметрам – возраст пациента, степень вирилизации. Обычно полученное количество препарата (4 – 10 мг) принимается в три приема в течение дня.
Это позволяет подавить избыточную секрецию андрогенов без каких-либо побочных действий.
Лечение адреногенитального синдрома при сольтеряющей форме проводится аналогично острой надпочечниковой недостаточности. В данном случае применяется капельное введение изотонических растворов хлорида натрия и глюкозы.
Также используется парентеральное введение препаратов гидрокортизона. Количество данного препарата составляет порядка 10 – 15 мг/кг в сутки, которое распределяется равномерно. По мере стабилизации состояния уколы гидрокортизона заменяются на таблетки.
Иногда, при необходимости, может быть добавлен минералокортикоид.
Хирургическое вмешательство требуется в случае поздней диагностики заболевания, если симптомы адреногенитального синдрома не ярко выражены. Тогда девочкам в возрасте 4 – 6 лет проводят коррекцию наружных половых органов.
Лечение можно считать эффективным, если темпы роста ребенка, артериальное давление, уровень электролитов в сыворотке крови нормализовались.
При вирильной и сольтеряющей формах своевременная диагностика, правильное лечение, возможное хирургическое вмешательство дают благоприятный прогноз.
Пациенты с адреногенитальным синдромом на протяжении всей жизни должны наблюдаться у эндокринолога, гинеколога или уролога. Однако при правильном лечении они сохраняют трудоспособность.
Адреногенитальный синдром – наследственное заболевание. У больного нарушается образование кортизола и альдостерона надпочечниками. Это происходит из-за дефекта ферментов, участвующих в синтезе стероидных гормонов.
Некоторые типы болезни имеют выраженные признаки с рождения, а в других случаях имеются скрытые гены, которые проявляются при стрессовых ситуациях в подростковом периоде или детородном.
Провокаторами могут быть травмы, радиация, стресс, отравления, тяжелые инфекции, физические перенапряжение. Чтобы заболевание проявилось, необходимо его наличие у обоих родителей.
Причем один из них может быть болен, а другой – носитель.
Генетическая аномалия нарушает образование гормонов надпочечников. На это реагирует гипофиз выработкой адренокортикотропного гормона (АКТГ). Результатом является увеличение надпочечных желез. Возникает такое состояние, как врожденная гиперплазия надпочечников (собственно, это и есть название адреногенитального синдрома).
При этом производство мужских половых гормонов при гиперплазии возрастает. Мужские гормоны в организме женщин вырабатывают только надпочечники. Их избыток вызывает маскулинизацию.
У мальчиков основная часть андрогенов продуцируется яичками, но они атрофируются при заболевании.
Повышенное содержание гормонов стимулирует раннее половое созревание и отставание в росте.
Первые признаки неправильного строения половых органов часто видны на УЗИ даже до рождения ребенка. У новорожденных девочек увеличен клитор, бывает даже полностью сформированный половой член.
Влагалище и матка присутствуют, но они бывают не до конца развитыми. У мальчиков обнаруживают увеличение мошонки и полового члена. Дети могут родиться с темной кожей из-за усиленного синтеза пигмента кожи.
Недостаток кортизола проявляется низким артериальным давлением, учащенным сердцебиением. При стрессовой ситуации может возникать адреналовый криз с шоковым состоянием. Дефицит альдостерона вызывает тяжелое обезвоживание.
Формы врожденной патологии – вирильная, сольтеряющая и неклассическая.
Методы диагностики: УЗИ, анализ амниотической жидкости или после 21 недели берут кровь плода (из пуповины под контролем УЗИ); После родов назначается обследование: проба с АКТГ, анализ крови, мочи. Для молодых женщин с нетипичным течением гиперплазии учитывают данные, полученные при: рентгенографии костей кисти; УЗИ яичников; измерении температуры в прямой кишке на протяжении цикла (базальной).
Беременной женщине назначается гормональная терапия, и девочки рождаются с нормально сформированными половыми признаками. Последствия для мамы: повышается давление, нарастают отеки, прибавляется масса тела, возможен поздний токсикоз.
После рождения при наличии аномалий строения половых органов показана их хирургическая коррекция. При недостатке кортизола и альдостерона назначается заместительная терапия Гидрокортизоном и Кортинеффом.
Эндокринолог наблюдает на протяжении всей жизни за больными.
При скрытом течении болезни у женщин гормоны не назначают. Если планируется зачатие, то необходимо применение Гидрокортизона до полного восстановления овуляции.
Для предупреждения выкидыша гормональная терапия продолжается до 12 недели, ее дополняют эстрогенами, прогестероном.
При расстройствах менструального цикла, угревой сыпи, усиленном оволосении назначают комбинированные препараты с эстрогенами, антиандрогенами, ОК.
Если родился ребенок, обладая внешними чертами мальчика, но является девочкой с выраженной аномалией развития половых органов, в таких случаях могут быть два варианта – хирургическая коррекция, заместительная терапия и помощь психотерапевта, либо сохраняют документально мужской пол, а матку удаляют.
Читайте подробнее в нашей статье об адреногенитальном синдроме, методах его профилактики.
Это заболевание относится к наследственным. У больного нарушается образование кортизола и альдостерона надпочечниками. Это происходит из-за дефекта ферментов, участвующих в синтезе стероидных гормонов.
Некоторые типы болезни имеют выраженные признаки с рождения, а в других случаях имеются скрытые, «молчащие» гены, которые проявляются при стрессовых ситуациях в подростковом периоде или детородном.
Провокаторами могут быть травмы, радиация, стресс, отравления, тяжелые инфекции, физические перенапряжение. Ранее эти формы патологии считали приобретенными, а затем нашли дефектные гены, полученные от родителей.
Причины мутаций остались пока неисследованными.
Так как ген, отвечающий за адреногенитальный синдром, является рецессивным (подавленным), то для того, чтобы заболевания проявилось, необходимо его наличие у обоих родителей. Причем один из них может быть болен, а у другого обнаруживается носительство гена.
Рекомендуем прочитать статью о болезнях надпочечников. Из нее вы узнаете о том, какие могут быть болезни надпочечников, их гиперфункция и гипофункция, причинах болезней надпочечников, а также о симптомах у детей, женщин и мужчин.
А здесь подробнее о болезни и синдроме Иценко-Кушинга.
Генетическая аномалия нарушает образование гормонов надпочечников. На это реагирует гипофиз выработкой адренокортикотропного гормона (АКТГ). Это соединение в норме стимулирует синтез стероидов. Результатом активации является увеличение надпочечных желез.
Даже большие надпочечники не способны образовывать кортизол и альдостерон, так как имеется разрыв ферментативной цепи. Возникает такое состояние, как врожденная гиперплазия надпочечников. Именно так эндокринологи формулируют диагноз адреногенитального синдрома.
Путь наследования врожденной гиперплазии надпочечников. Патологический ген обозначен черным кружочком
Если стероидные гормоны не могут образоваться, то производство мужских половых гормонов (андрогенов) при гиперплазии возрастает. Все предшественники кортизола и альдостерона используются надпочечниками для синтеза андрогенов.
Мужские гормоны в организме женщин вырабатывают только надпочечники. Их избыток вызывает маскулинизацию, то есть приобретение половых признаков мужчины. Это проявляется очень ярко еще и потому, что андрогены имеют свойство подавлять действие женских (эстрогенов).
У мальчиков основная часть андрогенов продуцируется яичками, но так как надпочечниковые гормоны имеются в крови в избытке, то собственные железы теряют активность. Яички атрофируются. Повышенное содержание гормонов стимулирует раннее половое созревание и отставание в росте, так как удлинение костей скелета прекращается с наступлением половой зрелости.
Раннее половое созревание мальчика
Первые признаки неправильного строения половых органов часто видны на УЗИ даже до рождения ребенка. У новорожденных девочек увеличен клитор, бывает даже полностью сформированный половой член. Влагалище и матка присутствуют, но они бывают не до конца развитыми. У мальчиков обнаруживают увеличение мошонки и полового члена.
Так как в еще в период внутриутробного развития образуется много АКТГ и меланоцитстимулирующего гормона, то дети могут родиться с темной кожей из-за усиленного синтеза пигмента кожи.
Недостаток кортизола проявляется низким артериальным давлением, учащенным сердцебиением. При стрессовой ситуации может возникать адреналовый криз с шоковым состоянием. Дефицит альдостерона вызывает тяжелое обезвоживание – понос, рвота, судорожный синдром. Они могут иметь катастрофические последствия для младенца.
Симптоматика гиперплазии надпочечников связана с дефектами разных видов ферментов. Наиболее типичными являются три формы вирильная, сольтеряющая и неклассическая.
Преобладают нарушения развития половых органов. У девочек:
- увеличен клитор, похожий на половой член;
- углублен вход во влагалище;
- половые губы больше нормы;
- матка и придатки сформированы.
У мальчиков увеличен пенис, кожа мошонки имеет темную пигментацию. У детей половое созревание начинается с семи лет. Девочки широкоплечие, с узким тазом, укороченными и массивными конечностями. У них низкий голос, кадык на шее, молочные железы не растут. У мальчиков рано появляются грубые волосы на подбородке и верхней губе, ломается голос.
Проявления болезни начинают обнаруживаться с первых недель жизни. У девочек половые органы формируются по мужскому типу, а у мальчиков увеличиваются пенис и мошонка. Из-за грубого нарушения образованная стероидных гормонов развивается тяжелая рвота, понос, судороги, темнеет кожа. Прогрессирующее обезвоживание ведет к смерти при отсутствии своевременной заместительной терапии.
Через 2-3 дня от начала клинического проявления заболевания появляются симптомы дегидратации и развития метаболического ацидоза
Выявляют в молодом возрасте. Половые органы соответствуют полу, но бывает увеличение клитора и пениса. Основные нарушения встречаются у женщин – уменьшаются или прекращаются месячные после стресса, травмы, аборта, выкидыша. Наступление первой менструации может быть только к 15 годам, цикл удлинен (более 30-40 дней).
Кожа склонна к повышенной жирности и образованию угрей, имеется повышенное оволосение. При обследовании обнаруживают гиперплазию коркового слоя надпочечников.
На фото девушка с поздним началом заболевания
Также имеются и варианты неклассического течения адреногенитального синдрома – с высоким давлением крови, с лихорадкой, липидный (ожирение, нарушен холестериновый обмен), с гирсутизмом (усиленный рост волос на теле и лице, по средней линии живота, около сосков).
Чем раньше возникают признаки адреногенитального синдрома, тем меньше шансов на то, что у женщины может произойти зачатие и нормальное вынашивание плода. Стойкое бесплодие характерно для вирилизирующей и сольтеряющей формы, а при неклассическом варианте беременность наступает, но возрастает риск выкидышей.
Любой стрессовый фактор может спровоцировать наступление острой надпочечниковой недостаточности. При сольтеряющей форме это возможно уже на второй неделе жизни.
Адреналовый криз у младенцев проявляется тяжелой рвотой, поносом, срыгиванием, неуправляемым падением давления, частым сердцебиением. Ребенок быстро теряет массу тела, впадает в бессознательное состояние. Ему требуется экстренная госпитализация для спасения жизни.
Смотрите на видео о развитии андрогении:
При обследовании беременных о возможности гиперплазии надпочечников может свидетельствовать аномальное формирование половых органов плода. Это можно увидеть на втором скрининговом акушерском УЗИ.
В таких случаях рекомендуется дополнительное обследование для выявления патологии еще до родов. Проводят анализ амниотической жидкости или после 21 недели берут кровь плода (из пуповины под контролем УЗИ).
После родов назначается обследование:
- проба с АКТГ – нет повышения содержания кортизола после его введения;
- анализ крови – снижен натрий, повышен калий, 17 ОН-прогестерон в 5-7 раз и более, андростендион (предшественник стероидов), ренин (при сольтеряющей форме);
- анализ мочи – высокая концентрация 17-кетостероидов, после приема преднизолона снижается наполовину.
Анализ амниотической жидкости
Для молодых женщин с нетипичным течением гиперплазии учитывают данные, полученные при:
- рентгенографии костей кисти (раннее завершение роста);
- УЗИ яичников – фолликулы, не достигающие овуляции;
- измерении температуры в прямой кишке на протяжении цикла (базальной) – отсутствие изменений, характерных для овуляции.
В некоторых случаях лечение гиперплазии начинается еще до родов. Беременной женщине назначается гормональная терапия и девочки рождаются с нормально сформированными половыми признаками. Этот метод не безопасен для матери, так как у нее повышается давление, нарастают отеки, прибавляется масса тела. Такие изменения могут привести к позднему токсикозу или усугубить его течение.
После рождения при наличии аномалий строения половых органов показана их хирургическая коррекция. Эту операцию необходимо провести как можно раньше.
При недостатке кортизола и альдостерона назначается заместительная терапия Гидрокортизоном и Кортинеффом. Важен постоянный контроль и коррекции дозы при любых сопутствующих заболеваниях или стрессах, так как возможен адреналовый криз. За пациентами с адреногенитальным синдромом ведется наблюдение эндокринолога на протяжении всей жизни.
При скрытом течении болезни у женщин гормоны не назначают, если она не планирует беременность, а месячные сохраняют относительную ритмичность.
Если же пациентка стремится к рождению ребенка, то необходимо применение Гидрокортизона до полного восстановления овуляции.
Для предупреждения выкидыша гормональная терапия продолжается до 12 недели, ее дополняют эстрогенами, а в более поздних сроках – прогестероном.
При расстройствах менструального цикла, угревой сыпи, усиленном оволосении назначают комбинированные препараты с эстрогенами, антиандрогенами, противозачаточные последнего поколения (Клайра, Логест, Мерсилон). Через полгода проявляется терапевтический эффект, но по окончанию их применения таблеток симптомы вновь возвращаются.
Особая ситуация возникает, если диагноз до родов не поставлен, а ребенок, обладая внешними чертами мальчика, является девочкой с выраженной аномалией развития половых органов. В таких случаях могут быть два варианта дальнейших действий – хирургическая коррекция, заместительная терапия и помощь психотерапевта, либо сохраняют документально мужской пол, а матку удаляют.
Смотрите на видео об адреногенитальном синдроме:
При наличии в роду случаев подобных болезней обязательно назначается консультация медицинского генетика молодым людям, которые планируют ребенка.
Даже обычный тест с АКТГ позволяет выявить скрытые варианты патологии или носительство гена. При наступившей беременности показано генетическое исследование клеток зародыша или амниотических вод.
На пятые сутки жизни проводят анализ на уровень 17-гидропрогестерона.
Чем раньше болезнь обнаружена, тем больше шансов на ее успешную коррекцию.
Рекомендуем прочитать статью об острой надпочечниковой недостаточности. Из нее вы узнаете о причинах синдрома острой надпочечниковой недостаточности, видах криза и симптомах острой надпочечниковой недостаточности.
А здесь подробнее о недостаточности гипофиза.
Адреногенитальный синдром характеризуется ферментной аномалией наследственного происхождения. Нарушается образование кортизола и альдостерона, а андрогены синтезируются в избыточном количестве. Девочки рождаются с признаками мужских половых органов, по мере роста их телосложение и внешние черты становятся мужеподобными. При сольтеряющей форме отмечается обезвоживание.
При первом проявлении болезни у молодых женщин преобладают нарушения менструального цикла, бесплодие. Для обнаружения патологии применяется дородовая диагностика, скрининг новорожденных. Лечение заключается в заместительной терапии гормонами, оперативной коррекции половых органов.
источник







