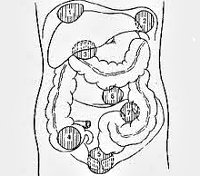
Абсцесс брюшной полости – это неспецифический воспалительный процесс, при котором между внутренними органами формируется полость, заполненная гнойным содержимым. Стенками образования могут выступать анатомические углубления, «карманы», листки сальника или связок. Заболевание обычно сопровождается интоксикацией организма и выраженным болевым синдромом.
Клиническая картина болезни зависит от локализации, вида и давности абсцесса. Характер и интенсивность жалоб также напрямую связаны с общим состоянием организма человека, болевым порогом. Встречаются случаи, когда пациента беспокоят лишь незначительные боли в животе и субфебрильная лихорадка.
-
волнообразная лихорадка от 37,5 °C до 39-40 °C с ознобом и потливостью;
- учащенное сердцебиение (тахикардия) на фоне гипертермии;
- общая интоксикация (головная боль, тошнота, ухудшение аппетита, слабость);
- бледность или мраморность кожных покровов;
- боли в животе различной интенсивности и локализации, которые могут распространяться на грудную клетку, поясничную область;
- локальное напряжение мышц передней брюшной стенки.
Возможно присоединение признаков пареза кишечника: запоры, сильное вздутие живота, рвота. В клиническом анализе крови обнаруживаются изменения, характерные для острого воспалительного процесса: повышенные значения СОЭ, лейкоцитоз с нейтрофилезом.
Особенность клинической картины абсцесса также зависит от его локализации:
- Поддиафрагмальный абсцесс. Чаще всего образуется после оперативных вмешательств на брюшной полости, в результате травм. Типичная локализация – справа, в области печени. При таком расположении боли возникают в правом подреберье и могут иррадиировать в грудную клетку, правое надплечье, усиливаться во время ходьбы, при кашле.
-
Печеночные абсцессы. Зачастую имеют множественный характер, развиваются на фоне ранений, инфекций желчевыводящих путей. Болезненные ощущения локализуются в области правого подреберья, реже – в эпигастральной области, характерна постоянная тошнота. Быстрая ходьба, резкие наклоны вперед могут усиливать болевой синдром.
- Аппендикулярный абсцесс. Появляется на фоне воспалительного инфильтрата вокруг измененного аппендикса. На первых стадиях характерно уменьшение болей в подвздошной области, снижение температуры тела. Спустя 6-7 суток симптомы возвращаются с новой силой, и пальпируется болезненное неплотное образование.
- Абсцесс Дугласова кармана. Характеризуется скоплением гноя в позадиматочном пространстве в результате воспалительных заболеваний матки, яичников, маточных труб или аппендикулярного отростка. Кроме сильных болей внизу живота женщину могут беспокоить частые позывы на мочеиспускание, акт дефекации, чувство распирания в этой области, диарея.
-
Межкишечные абсцессы. Появляются за счет скопления гноя между петлями тонкой, толстой кишки; чаще всего множественные. Пациента беспокоят постоянные ноющие или острые боли в животе без точной локализации, тошнота, рвота. Парез кишечника сопровождается метеоризмом, запорами, асимметрией живота.
Полости с гноем в области поджелудочной железы, селезенки встречаются реже и имеют сходные признаки с острым воспалением этих органов (деструктивный панкреатит, спленит).
К формированию абсцессов в брюшной полости может привести:
- хирургическое вмешательство с несоблюдением правил антисептики, «забытый» инструментарий, салфетки;
- ножевые, тупые травмы живота, огнестрельные ранения;
- острый холецистит, деструктивный панкреатит, перфоративная язва 12-перстной кишки или желудка;
- острый флегмонозный аппендицит, воспаление придатков матки;
- разлитой перитонит.
В формировании гнойных полостей большую роль играет микробная инфекция, некрозы тканей, несколько меньшую – паразитарные инвазии.
При появлении характерных для гнойного воспаления жалоб следует обратиться к терапевту, который после осмотра и опроса должен перенаправить пациента к соответствующему специалисту. Это может быть врач- хирург или врач-гинеколог. В случае острого развития симптомов или резкого ухудшения состояния, рекомендуется вызвать бригаду скорой медицинской помощи, которая доставит больного в специализированное отделение.
Для подтверждения диагноза, а также для поиска его причины могут быть назначены такие исследования:
-
Ультразвуковая диагностика органов брюшной полости. Методика отлично подходит для поиска осумкованного гноя в области печени, селезенки, под диафрагмой, в Дугласовом пространстве. УЗИ также может помочь определить причину болезни (острый аппендицит или панкреатит, гнойный сальпингоофорит и т.д.).
- Компьютерная томография. Исследование назначается в случае малоинформативности УЗИ, для обследования труднодоступных зон. КТ позволяет выявить не только локализацию образования, но и количество абсцессов, их размеры.
- Обзорная рентгенография брюшной полости. Методика позволяет отличить поддиафрагмальный абсцесс от печеночного или межкишечного. Полости с гноем выявляются в виде округлых образований с уровнем жидкости.
-
Клинический, биохимический анализы крови, исследование крови на стерильность. В пользу воспалительного процесса говорит высокий лейкоцитоз с нейтрофильным сдвигом формулы, высокие значения СОЭ, повышение печеночных ферментов, появление С-реактивного белка, прокальцитонина.
- Диагностическая лапароскопия. Исследование брюшной полости выполняется через прокол в стенке живота с помощью специальной аппаратуры – эндоскопа. При необходимости такая диагностика может закончиться полноценной операцией.
Основной метод лечения сформировавшихся в брюшной полости абсцессов – хирургический. В обязательном порядке назначается один или несколько антибактериальных препаратов с широким спектром воздействия. При необходимости используют антипаразитарные средства, ингибиторы протеолитических ферментов, человеческие иммуноглобулины.
При поддиафрагмальных, подпеченочных и при межкишечных абсцессах дренирование осуществляется через переднюю брюшную стенку под контролем УЗИ. Если гной скопился в малом тазу, то доступ происходит через прямую кишку или позадиматочное пространство.
При неэффективности предыдущего метода, в случае труднодоступного расположения абсцесса выполняется общий доступ путем срединного разреза. В обязательном порядке в брюшной полости оставляют дренажи для дальнейшего оттока гноя, регулярного промывания растворами антисептика.
Ингибиторы протеолиза («Гордокс», «Контрикал») помогают остановить процессы распада ткани, а также улучшают проникновение антибактериальных препаратов в место воспаления. При недостаточном ответе пациента на системную противомикробную терапию к лечению добавляют иммуноглобулины, которые содержат антитела против большого количества микроорганизмов.
При отсутствии должного лечения возрастает риск развития таких осложнений:
- Разлитой перитонит вследствие разрыва капсулы абсцесса. Проявляется острой болью, ухудшением состояния, появлением сильного напряжения мышц брюшного пресса, тахикардией, лихорадкой.
- Сепсис – системная ответная реакция организма на гнойное воспаление. Характеризуется выраженной интоксикацией, образованием некрозов во внутренних органах и полиорганной недостаточностью.
В случае проведения оперативного вмешательства, аспирации гноя и назначения адекватной антибактериальной терапии, прогноз заболевания является благоприятным — возможно полное излечение.
источник
ЛИГ часто наблюдают у пациентов, инфицированных ВИЧ, и у больных, получающих длительную иммуносупрессивную терапию в качестве профилактики отторжения трансплантата или в рамках лечения аутоиммунных заболеваний или системных заболеваний соединительной ткани.
Используют все диагностические возможности, описанные выше (см. врезку 20-1), однако у данной категории пациентов часто возникают редкие оппортунистические инфекции. Кроме того, ВИЧ-инфицированные и пациенты, получающие иммуносупрессивную терапию, более подвержены развитию некоторых злокачественных новообразований, при которых также может возникать ЛНГ. Наиболее распространённые диагнозы представлены во врезке 20-3. Большинство инфекционных заболеваний, такие, как токсоплазмоз головного мозга, пневмоцистный или криптококковый менингит, имеют характерную клиническую картину, позволяющую сразу выставить диагноз. Другие заболевания, первым симптомом которых часто становится ЛНГ, обсуждены ниже.
Пиогенные абсцессы могут формироваться в любом месте. При СПИДе они нередко имеют необычную локализацию, например в простате или в придаточных пазухах носа. При объективном осмотре и в ходе диагностики следует исключать эти причины.
Инфекция Mycobacterium tuberculosis, как правило, манифестирует лихорадкой в сочетании с кашлем и потерей массы тела. На рентгенограмме органов грудной клетки обнаруживают инфильтраты в лёгочной ткани. Чаще наблюдают внелёгочное поражение, однако на рентгенограмме менее выражен фиброз и каверни- зация по сравнению с больными с нормальным уровнем иммунитета. Посев мокроты нередко отрицателен.
Mycobacterium avium-intracellulare — частая причина ЛНГ на тяжёлых стадиях СПИДа, которую обнаруживают у 10—20% больных. Воротами инфекции становится ЖКТ. Возбудитель диссеминирует по кровеносному руслу и обнаруживается в печени, костном мозге и лимфатических узлах. Клиническую картину характеризуют колебания температуры и ознобы. Диагностика основана на результатах специального посева крови, посева кала, костного мозга и биопсии печени.
Неходжкинская лимфома также нередко становится причиной ЛНГ на поздних стадиях СПИДа. Лимфома может формироваться в любом месте. У пациентов со СПИДом, как правило, обнаруживают обширное увеличение лимфатических узлов, что затрудняет диагностику только на основании клинической картины. Для подтверждения диагноза необходима биопсия увеличенных узлов, КТ органов брюшной полости и биопсия костного мозга.
Стойкая лихорадка неясного генеза возникает на поздней стадии СПИДа и может сохраняться в течение нескольких месяцев. Часто проводят попытки лечения инфекции Mycobacterium avium-intracellulare и пиогенных инфекций, которые обычно не дают результата, поэтому назначают симптоматическую терапию нестероидными и стероидными препаратами.
Врезка 20-3. Причины лихорадки неясного генеза на фоне ВИЧ-инфекции или у пациентов с иммуносупрессией
Бактериальные инфекции Пиогенная бактериальная инфекция (образование абсцесса)
Mycobacterium tuberculosis Mycobacterium avium-intracellulare Другие атипичные микобактерии Г рибковые инфекции Candida Cryptococcus Aspergillus Протозойные Токсоплазмоз ГТневмоцистная инфекция Злокачественные заболевания Лимфома Саркома Капоши Эпителиальные опухоли Стойкая лихорадка неясного генеза
Пациент, 65 лет, бизнесмен, обратился с жалобами на ознобы в течение 6 нед, потерю массы тела и слабость. Его жена умерла 5 лет назад, он долго пребывал в тяжёлой депрессии и нередко в большом количестве употреблял алкоголь. В течение многих лет пациент страдает запорами, по поводу которых регулярно принимает слабительные. По совету своего лечащего врача он поехал на восстановительный отдых в южную Италию, где у него однократно возникла боль в левой подвздошной области и диарея с незначительной примесью крови в кале. В течение 5 дней он получал антибиотики широкого спектра действия, и симптомы исчезли через 3 дня. Рецидивов диареи не было. Через
две недели после возвращения он почувствовал себя плохо, стала подниматься температура, появился дискомфорт в верхних отделах живота.
При осмотре: лёгкая анемия, температура 38,4 °С. Данные обследования живота в пределах нормы, за исключением лёгкой болезненности нисходящей ободочной кишки.
При обследовании: гемоглобин 102 г/л; средний объём эритроцитов 100 фл; средняя концентрация гемоглобина в эритроците 31 пкг; лейкоциты 10,4х109/л (80% нейтрофилов, 17% лимфоцитов, 3% эозинофилов); СОЭ 72 мм/ч; на рентгенограмме органов грудной клетки определяется незначительный выпот в плевральной полости справа и фиброз в верхних отделах слева. При микроскопии мочи: следы белка, в остальном — в пределах нормы. Серологические анализы на сальмонеллу отрицательны, за исключением анализа на антиген Н Salmonella typhi, положительный 1/10 при двух измерениях с интервалом 10 дней.
• Каков наиболее вероятный диагноз?
• Какие исследования дадут больше всего информации для диагностики?
• Каков ваш план неотложного лечения?
У данного больного был приступ диареи, купированный антибиотиками широкого спектра действия до начала нынешнего заболевания. Очень велика вероятность, что его нынешнее состояние связано с этим фактом. Нет объективных признаков скопления гноя в животе или полости таза, однако не исключена возможность абсцесса печени или подциафрагмально- го абсцесса. Первый вариант вероятнее, так как предшествующее заболевание быстро исчезло и вряд ли у пациента в это время произошла перфорация полого органа. Абсцесс печени чаще развивается у пожилых ослабленных пациентов, поэтому нередко он протекает с минимальными местными симптомами. Небольшой выпот в правой плевральной полости также подтверждает этот диагноз. После частичного лечения инфекции может возникать незначительный нейтрофильный лейкоцитоз.
Не исключено также скрытое злокачественное новообразование, и в первую очередь необходимо исключать поражение желудка, печени и кишечника. У европейцев рак печени практически всегда возникает на фоне цирроза печени. Его предшествующее заболевание трудно объяснить злокачественной патологией; продолжительность симптомов составляет всего лишь 6 нед, признаки метастазирования отсутствуют.
На рентгенограмме грудной клетки обнаружен фиброз в верхних отделах, однако этого слишком мало, чтобы предполагать у пациента туберкулёз лёгких. При туберкулёзе кишечника, вызвавшем диарею, не было бы реакции на антибиотики широкого спектра действия. Возможно поражение забрюшинных лимфоузлов, но это не объясняет предшествующего приступа диареи.
Длительность заболевания слишком велика для брюшного тифа. Серологические данные соответствуют иммунизации, но не инфекции. Высокая интермиттирующая лихорадка и ознобы не типичны для бруцеллёза. Лимфома с поражением забрюшинных лимфатических узлов может давать лихорадку, однако заболевание слишком непродолжительно и предшествующий приступ диареи этот диагноз также не объясняет. Несмотря на отсутствие признаков поражения печени, у пациента может быть цирроз печени в связи со злоупотреблением алкоголя, что становится причиной лёгкой лихорадки или может осложняться грамотрицательной септицемией.
Для обследования большое значение имеет УЗИ печени, так как оно может продемонстрировать дефект наполнения при абсцессе печени. При его обнаружении КТ позволяет дифференцировать абсцесс и опухоль. Следует выполнить посевы крови. Если УЗИ печени не даст результатов, целесообразно проведение рентгенологических исследований с пассажем бария и ирригоскопии для исключения рака желудка и кишечника. Высокая активность щелочной фосфатазы печёночного происхождения в сочетании с низкой концентрацией альбумина характерна для диффузного поражения печени. При обнаружении патологии печени рассматривают возможность тонкоигольной аспирации для бактериологического и цитологического исследования.
Если все эти обследования не дают результатов, оценивают целесообразность лапаротомии. До постановки диагноза лечение не проводят. В настоящее время назначают лишь симптоматическую терапию.
У данного больного был пиогенный абсцесс печени после приступа дивертикулита. При УЗИ печени обнаружен дефект наполнения, после аспирации которого и назначения антибиотиков широкого спектра действия пациент выздоровел.
источник
| Информация о документе | |
| Дата добавления: | |
| Размер: | |
| Доступные форматы для скачивания: |
ХИРУРГИЧЕСКАЯ ИНФЕКЦИЯ КОЖИ И МЯГКИХ ТКАНЕЙ У ВИЧ-ИНФИЦИРОВАННЫХ
И.М. ДИЗЕНГОФ, Н.Н. ХАЧАТРЯН, Г.Г. СМИРНОВ, Л.И. ЛАЗУТКИНА
В группе социально значимых болезней одно из ведущих мест занимает ВИЧ/СПИД, эпидемия которого началась в нашей стране с 1996 года среди молодёжи — потребителей инъекционных наркотических средств. В результате пандемии ВИЧ-инфекции в мире она как причина смерти занимает 3-е место после ОРВИ и туберкулёза. ВИЧ СПИД имеет 100%-ную летальность, входит в число заболеваний при которых отсутствуют надёжные средства лечения. Разработанная антиретровирусная терапия лишь продлевает жизнь больного при условии пожизненного лечения.
Пандемия ВИЧ-инфекции продолжает нарастать, по расчётным данным WHO UNAIDS (2006), на конец 2005 года с ВИЧ жило около 40 млн человек. Социально-экономические сдвиги последних десятилетий обусловили стремительный рост наркомании в России. Число наркоманов превысило 4 млн, большая часть из них — молодые люди в возрасте 14-30 лет.
Эпидемия наркомании вызвала рост инфекций, передаваемых парентеральным путём: так, среди выявленных в России ВИЧ-инфицированных, 90% составляют потребители наркотических средств.
По информации Федерального центра по профилактике и борьбе со СПИДом, каждый сотый россиянин в возрасте от 18 до 24 лет ВИЧ инфицирован. Ежедневно регистрируется примерно 100 новых случаев ВИЧ-инфекции. В настоящее время центр располагает данными о 387 тыс. ВИЧ-инфицированных гражданах России. Большинство же экспертов склоняются к тому, что сейчас в России с ней живут 1-1,5 млн человек. Как отмечает В.В. Покровский, если в России инфицировано порядка 1 млн. человек, то при средней продолжительности жизни заражённых 10-12 лет и с учётом того, что эпидемия началась около 5-6 лет назад, к 2010 году могут умереть от СПИДа порядка 1 млн человек.
Лечение и обследование ВИЧ-положительных больных с острой хирургической патологией в целом является актуальной и недостаточно изученной проблемой, которая пока не стала предметом широкого обсуждения медицинской общественности.
В связи с продолжающейся во всём мире эпидемией ВИЧ-инфекции растёт число ВИЧ-позитивных пациентов, обращающихся за помощью к хирургам. Так, у 25% ВИЧ-инфицированных лиц в течение жизни возникают показания к оперативному лечению. Частично это обусловлено тем, что 74% из них принимали наркотики, болынинство — внутривенно, что способствует развитию постинъекционных
осложнений, особенно на фоне иммунодефицита.
В современной литературе проблема хирургической инфекции кожи и мягких тканей у ВИЧ-положительных рассматривается недостаточно. Статьи, посвященные этому вопросу, единичны, и, по сути, пока отражают лишь этап накопления материала без его подробного анализа.
Возраст пациентов с ГЗМТ и сопутствующей ВИЧ-инфекцией от 18 до 35 лет, мужчин — 63%, женщин — 37% (под наблюдением находилось 270 пациентов). Больные поступают с флегмонами различных локализаций, нагноившимися гематомами, абсцессами, тромбофлебитами. Эти заболевания часто осложняются сепсисом, инфекционным эндокардитом. Рекомендуется обращать внимание на локализацию гнойных процессов, которые возникают в местах введения наркотиков без соблюдения правил асептики и антисептики.
Очень серьёзная проблема возникает при локализации процесса в паховой области, так как наркоманы «со стажем» из-за отсутствия периферических вен начинают вводить препараты в сосуды бедренного треугольника, где возникают аневризмы, пульсирующие гематомы.
Велик удельный вес постинъекционных осложнений, что с одной стороны связано с имеющимся иммунодефицитом, а с другой — с большим количеством внутривенных наркоманов среди ВИЧ-инфицированных. Основной причиной развития флегмон и абсцессов является попадание нестерильного раствора наркотического препарата
В паравазальную клетчатку. В 78,8% используются подкожные вены плеча и предплечья, что приводит к формированию тромбофлебитов (25,9%), Флегмон и абсцессов в зонах введения препаратов (64,1%). Наибольший эффект комфорта наркоманы получают после внутривенного введения препарата.
Когда все гнойные очаги санированы, а явления интоксикации сохраняются, необходимо выполнение УЗИ сердца для выявления септического эндокардита. Чаще всего вегетации выявляются на клапанах правых отделов сердца. Частым и очень тяжёлым осложнением в этой группе больных является ангиогенный сепсис. Особенностью течения гнойных процессов у ВИЧ-инфицированных больных является медленное заживление ран после вскрытия гнойных очагов, частое появление новых гнойников без явной воспалительной реакции.
В изученных работах не затронуты микробиология гнойных процессов, частота их развития в этой группе больных, связь со степенью иммунодефицита.
Частично эти вопросы освещаются в статьях Т.Н. Булискерия т Г.Г. Смирнова с соавторами, под наблюдением которых находилось 140 пациентов с ГЗМТ. Так, например, указывается, что среди ВИЧ-инфицированных, принимающих внутривенно наркотики, 43,6% нуждаются в оперативном лечении по поводу постинъекционных абсцессов и флегмон. Распространённость постинъекционых осложнений (абсцессов, флегмон, нагноившихся гематом) среди ВИЧ-инфицированных значительно выше. Выявлено, что у всех ВИЧ-инфицированных больных, независимо от характера хирургической инфекции, отмечается замедленная динамика регресса основных клинических симптомов послеоперационного периода по сравнению с больными, не отягощенными ВИЧ-инфекцией. Продолжительность лихорадки, гнойного отделяемого, сроков очищения раны и койко-день находятся в прямой связи со стадией ВИЧ-инфекции. Так же были проведены иммунологические исследования. Однако микрофлора и чувствительность её к антибиотикам не изучались.
В конце 2006 года Е.Н. Бычковым публикуется работа о применении новых методов лечения бактериальных инфекций у ВИЧ-инфицированных потребителях героина. Автор обращает внимание на связь парентерального использования наркотиков с распространением ВИЧ-инфекции. Основным наркотиком для российских потребителей является героин, основной путь его введения парентеральный. Далее указывается, что на фоне роста числа ВИЧ-инфицированных особое значение приобрела проблема лечения у них различных сопутствующих заболеваний, в том числе инфекций кожи и мягких тканей. Частое парентеральное применение наркотиков ВИЧ-инФицицированными пациентами приводит к развитию у них различны гнойно-воспалительных заболеваний. Вновь проводятся иммунологические исследования, однако микробиологические вопросы не попали в поле зрения автора.
В главе «ВИЧ-инфекция в хирургии» фундаментального руководства «Хирургические инфекции» (под редакцией И.А. Ерюхина, Б.Р. Шляпникова) рассматриваются кожные поражения у больных ВИЧ-инфекцией. Они встречаются очень часто, регистрируются у 90% больных в разные периоды болезни и могут быть вызваны самыми разными агентами, причём у 41% больных имеются признаки поражений, локализующиеся в области головы и шеи. Среди бактериальных инфекций наиболее часто регистрируются поражения, вызванные S.aureus: фолликулит, импетиго, буллёзный импетиго, фурункулы, карбункулы, а также абсцессы, чаще связаные с венозным катетером, либо наблюдающиеся у лиц, вводящих внутривенно психоактивные вещества, которые, кроме антибактериального, требуют оперативного лечения. При развитии гангренозной эктимы (без сепсиса) на месте эрозий и язв, вызванных Р.аеruginoza, также требуется хирургическое вмешательство, поскольку антибактериальная терапия при этой форме синегнойной инфекции почти не даёт эффекта.
В последние годы появляется всё больше сообщений о развитии у больных ВИЧ-инфекцией бациллярного ангиоматоза (генерализованная форма болезни кошачьих царапин), вызываемого рохалимиями из рода бартонелл: R.henselae и R.quintana. При гистологическом исследовании выявляется выраженная дольчатая пролиферация капилляров с большим скоплением эндотелиальных клеток. Процесс может затронуть глубокие мягкие ткани и даже кости.
Иногда больные могут обратиться за хирургической помощью для устранения косметических дефектов, которые могут быть связаны с контагиозным моллюском, излюбленной локализацией которого является лицо. Серьёзные косметические дефекты и дефекты, вызывающие тяжёлые страдания, по поводу которых больные могут обращаться за хирургической помощью, могут быть связаны с различными грибковыми поражениями, например, с криптококкозом (особенно при его сочетании с контагиозным моллюском), или гистоплазмозом, при котором на коже лица появляются пятна, папулы, узлы, пустулы вегетирующие бляшки с распространением на слизистую оболочку полости рта и образованием хронических изъязвлений. Аналогичные изменения могут развиваться и при других системных микозах. Так автором наблюдался спонтанный абсцесс ягодицы, вызванный Candida, у ВИЧ-инфицированного ребёнка.
Генитальные бородавки — остроконечные кондиломы (вызываемые вирусом папилломы человека) — характерны для инфицированных ВИЧ, особенно заразившихся половым путём. Иссечение кондилом у больных ВИЧ-инфекцией — лишь временная мера, так как рецидивы почти неминуемы.
В монографии «Инфекции в хирургии. Фармакотерапия и профилактика» рассматривается проблема инфекций на фоне иммуносупрессии, в том числе при СПИДе. Указывается, что увеличение количества пациентов с ВИЧ-инфекцией способствует росту числа с инфекций. Заболевания при иммуносупрессии имеют ряд особеностей. Во-первых, пациенты подвержены высокому риску инвазии оппортунистической инфекцией. Во-вторых, летальность у таких больных очень высока и достигает 45%. Болезнь склонна к затяжному тяжёлому течению. ВИЧ-инфекция, вызывая нарушение клеточного звена иммунитета (Т-лимфоцитов или мононуклеарных макрофагов) предрасполагает к инфицированию вирусами, грибками, атипичными микобактериями.
В результате изучения единичных работ, посвященных проблеме хирургической инфекции кожи и мягких тканей у ВИЧ-инфицированных, становится очевидным, что течение этих заболеваний имеет ряд особенностей, которые связаны в первую очередь с имеющимся у пациентов иммунодефицитом, что обуславливает необычный спектр возбудителей инфекций кожи и мягких тканей (вирусы, грибы). Однако гнойные заболевания кожи и мягких тканей, требующие операции и антимикробной терапии, вызываются лишь некоторыми из них.
Нарушения иммунитета разной степени удлиняют течение послеоперационного периода, репаративных процессов, длительности очищения гнойной раны и продолжительности лихорадочного периода. Следовательно, увеличиваются сроки госпитализации, а результаты лечения ухудшаются. Высок риск гнойно-септических осложнений. Обширные гнойные процессы на фоне резкого ослабления защитных сил организма быстро приводят к сепсису и нередко к летальному исходу.
Таким образом, очевидно, что существуют клинические особенности течения гнойной инфекции мягких тканей у ВИЧ-инфицированных пациентов. В то же время ни один из источников полностью не посвящен особенностям гнойных заболеваний кожи и мягких тканей у ВИЧ-инфицированных. Специальной литературы по этому вопросу нет. Источники единичны. Количество пациентов с гнойными заболеваниями мягких тканей и сопутствующей ВИЧ-инфекцией увеличивается лавинообразно соответственно распространению эпидемии в нашей стране и необходимость в создании целостной картины этой проблемы существует.
источник
Абсцесс брюшной полости – это ограниченный гнойник в брюшной полости, заключенный в пиогенную капсулу. Особенности клиники зависят от локализации и величины гнойного очага; общими проявлениями абсцесса брюшной полости служат боль и локальное напряжение мышц живота, лихорадка, кишечная непроходимость, тошнота и др. Диагностика абсцесса включает обзорную рентгенографию органов брюшной полости, УЗИ и КТ брюшной полости. Лечение заключается во вскрытии, дренировании и санации гнойника; массивной антибактериальной терапии.
В широком смысле к абсцессам брюшной полости в абдоминальной хирургии относят внутрибрюшинные (интраперитонеальные), забрюшинные (ретроперитонеальные) и интраорганные (внутриорганные) абсцессы. Внутрибрюшинные и забрюшинные гнойники, как правило, располагаются в области анатомических каналов, карманов, сумок брюшной полости и клеточных пространствах ретроперитонеальной клетчатки. Внутриорганные абсцессы брюшной полости чаще образуются в паренхиме печени, поджелудочной железы или стенках органов.
Пластические свойства брюшины, а также наличие сращений между ее париетальным листком, сальником и органами, способствуют отграничению воспаления и формированию своеобразной пиогенной капсулы, препятствующей распространению гнойного процесса. Поэтому абсцесс брюшной полости еще называют «отграниченным перитонитом».
В 75% случаев абсцессы располагаются внутри- или забрюшинно; в 25% — внутриорганно. Пиогенная флора абсцессов чаще полимикробная, сочетающая аэробные (кишечную палочку, протей, стафилококки, стрептококки и др.) и анаэробные (клостридии, бактероиды, фузобактерии) микробные ассоциации. Причины абсцесса:
- Перитонит. В большинстве случаев формирование абсцессов брюшной полости связано с вторичным перитонитом, развивающимся вследствие попадания в свободную брюшную полость кишечного содержимого при перфоративном аппендиците; крови, выпота и гноя при дренировании гематом, несостоятельности анастомозов, послеоперационном панкреонекрозе, травмах и т. д. Типичными местами локализации служат большой сальник, брыжейка, малый таз, поясничная область, поддиафрагмальное пространство, поверхность или толща тканей паренхиматозных органов.
- Инфекционные процессы в малом тазу. Причиной абсцесса могут выступать гнойные воспаления женских гениталий – острый сальпингит, аднексит, параметрит, пиовар, пиосальпинкс, тубоовариальный абсцесс.
- Заболевания органов ЖКТ. Встречаются абсцессы брюшной полости, обусловленные панкреатитом: в этом случае их развитие связно с действием ферментов поджелудочной железы на окружающую клетчатку, вызывающим выраженную воспалительную реакцию. В некоторых случаях абсцесс брюшной полости развивается как осложнение острого холецистита или прободения язвы желудка и 12-перстной кишки, болезни Крона.
- Инфекции забрюшинного пространства. Псоас-абсцесс может являться следствием остеомиелита позвоночника, туберкулезного спондилита, паранефрита.
По ведущему этиофактору различают микробные (бактериальные), паразитарные и некротические (абактериальные) абсцессы брюшной полости.
В соответствии с патогенетическим механизмом выделяют посттравматические, послеоперационные, перфоративные и метастатические гнойники.
По расположению относительно брюшины абсцессы делятся на забрюшинные, внутрибрюшинные и сочетанные; по количеству гнойников — одиночные или множественные.
По локализации встречаются:
- поддиафрагмальные,
- межкишечные,
- аппендикулярные,
- тазовые (абсцессы дугласова пространства),
- пристеночные
- внутриорганные абсцессы (внутрибрыжеечные, абсцессы поджелудочной железы, печени, селезенки).
В начале заболевания при любом виде абсцесса брюшной полости превалирует общая симптоматика: интоксикация, интермиттирующая (перемежающаяся) лихорадка с гектической температурой, ознобами, тахикардией. Часто отмечается тошнота, нарушение аппетита, рвота; развивается паралитическая кишечная непроходимость, определяется выраженная болезненность в зоне гнойника, напряжение брюшных мышц. Симптом напряжения мышц живота наиболее выражен при абсцессах, локализующихся в мезогастрии; гнойники поддиафрагмальной локализации, как правило, протекают со стертой местной симптоматикой. При поддиафрагмальных абсцессах может беспокоить боль в подреберье на вдохе с иррадиацией в плечо и лопатку, кашель, одышка.
Симптомы тазовых абсцессов включают абдоминальные боли, учащение мочеиспускания, понос и тенезмы вследствие рефлекторного раздражения мочевого пузыря и кишечника. Для забрюшинных абсцессов характерна локализация боли в нижних отделах спины; при этом интенсивность боли усиливается при сгибании нижней конечности в тазобедренном суставе. Выраженность симптоматики связана с величиной и локализацией гнойника, а также с интенсивностью проводимой противомикробной терапии.
Обычно при первичном осмотре абдоминальный хирург обращает внимание на вынужденное положение пациента, которое он принимает для облегчения своего состояния: лежа на боку или спине, полусидя, согнувшись и т. д. Язык сухой, обложен сероватым налетом, живот незначительно вздут. Пальпация живота обнаруживает болезненность в отделах, соответствующих локализации гнойного образования (в подреберье, глубине таза и др.). Наличие поддиафрагмального абсцесса характеризуется асимметрией грудной клетки, выпячиваем межреберий и нижних ребер. В общем анализе крови обнаруживаются лейкоцитоз, нейтрофилез, ускорение СОЭ.
Решающая роль в диагностике абсцесса брюшной полости отводится рентгенологическому обследованию. Как правили, обзорная рентгенография брюшной полости позволяет выявить дополнительное образование с уровнем жидкости. При контрастном исследовании ЖКТ (рентгенографии пищевода и желудка, ирригоскопии, фистулографии) определяется оттеснение желудка или петель кишечника инфильтратом. При несостоятельности послеоперационных швов контрастное вещество поступает из кишечника в полость абсцесса. УЗИ брюшной полости наиболее информативно при абсцессе верхних ее отделов. При сложностях дифференциальной диагностики показано проведение КТ, диагностической лапароскопии.
Хирургическое лечение проводится под прикрытием антибактериальной терапии (аминогликозидов, цефалоспоринов, фторхинолонов, производных имидазола) для подавления аэробной и анаэробной микрофлоры. Принципы оперативного лечения всех видов абсцессов заключаются во вскрытии и дренировании, проведении адекватной санации. Доступ определяется локализацией гнойника: поддиафрагмальные абсцессы вскрывают внебрюшинно или чрезбрюшинно; абсцессы дугласова пространства – трансректально или трансвагинально; псоас-абсцесса – из люмботомического доступа и т. д.
При наличии множественных абсцессов выполняется широкое вскрытие брюшной полости. После операции оставляют дренаж для активной аспирации и промывания. Небольшие одиночные поддиафрагмальные абсцессы могут быть дренированы чрезкожно под ультразвуковым наведением. Однако при неполной эвакуации гноя велика вероятность рецидива гнойника или его развития в другом месте субдиафрагмального пространства.
При одиночном абсцессе прогноз чаще благоприятный. Осложнениями абсцесса может явиться прорыв гноя в свободную плевральную или брюшную полость, перитонит, сепсис. Профилактика требует своевременного устранения острой хирургической патологии, гастроэнтерологических заболеваний, воспалительных процессов со стороны женской половой сферы, адекватного ведения послеоперационного периода после вмешательств на органах брюшной полости.
источник
Осложнения ВИЧ-инфекции — вторичные заболевания, развивающиеся на фоне иммунодефицита. Механизм их возникновения связан либо с угнетением клеточного и гуморального иммунитета (инфекционные болезни и опухоли), либо с прямым воздействием вируса иммунодефицита человека (например, некоторые неврологические нарушения).

Примерно у 65% больных ВИЧ-инфекцией диагностируют туберкулёз как впервые возникшее заболевание, у остальных пациентов обнаруживают реактивацию процесса. ВИЧ существенно влияет на состояние иммунной системы (и на иммуно-реактивность) при туберкулёзе, нарушает дифференцировку макрофагов и препятствует образованию специфической гранулёмы. В то время как на ранних стадиях ВИЧ-инфекции морфология специфического воспаления существенно не меняется, на стадии СПИДа гранулёмы просто не формируются. Особенность туберкулёза лёгких у больных ВИЧ-инфекцией — тяжёлое течение заболевания с поражением бронхов и образованием свищей плевры, перикарда и лимфатических узлов. Как правило, в 75-100% случаев у больных ВИЧ-инфекцией возникает лёгочная форма туберкулёза, однако, по мере нарастания иммунодефицита, у 25-70% пациентов отмечают диссеминацию и развитие внелёгочных форм заболевания. Туберкулёз — одна из основных причин смерти пациентов (на стадии СПИДа) в Украине. Процессы, происходящие в лёгких больных СПИДом людей, — формирование корневой аденопатии и милиарных высыпаний; возникновение преимущественно интерстициальных изменений и образование плеврального выпота. При этом отмечают снижение количества случаев, сопровождающихся распадом лёгочной ткани, а следовательно, и числа больных, в мокроте которых при микроскопии и посеве обнаруживают микобактерии туберкулёза. Весьма характерным считают частое развитие туберкулёзной микобактериемии у больных СПИДом, как правило осложнённой септическим шоком и нарушением функций различных органов. Нередко наблюдают поражение лимфатических узлов (особенно шейных), костей, ЦНС, мозговых оболочек и органов пищеварительной системы: описаны абсцессы простаты и печени. Примерно у 60-80% ВИЧ-инфицированных пациентов туберкулёз протекает только с поражением лёгких, у 30-40% выявляют изменения других органов.
Группу возбудителей «нетуберкулёзных» микобактериозов составляют представители различных видов микобактерии (свыше сорока). Заболевания у человека вызывают восемнадцать разновидностей микобактерии. четыре вида микроорганизмов обладают сравнительно высокой патогенностью для людей, а четырнадцать видов относят к условно-патогенным. Атипичный микобактериоз, вызванный М. avium (входят в состав комплекса М. avium complex — MAC), — суперинфекция. составляющая группу СПИД-ассоциированных оппортунистических инфекций. До пандемии ВИЧ-инфекции атипичный микобактериоз диагностировали крайне редко, как правило, у лиц с выраженной иммуносупрессией (например, при трансплантации органов и тканей, после длительной кортикостероидной терапии, у онкологических больных). У пациентов, страдающих ВИЧ-инфекцией, иногда развивается диссеминированная форма МАС-инфекции. В терминальной стадии регистрируют локализованную или генерализованную формы заболевания. При локализованной МАС-инфекции обнаруживают абсцессы кожи и поражения лимфатических узлов, а при генерализованной — общеинтоксикационный и желудочно-кишечный синдромы, а также синдром экстрабилиарной обструкции. Признаки общеинтоксикационного синдрома — лихорадка, астенизация, снижение массы тела, тяжёлая анемия, лейкопения, повышение активности аланиновои трансаминазы в сыворотке крови. При желудочно-кишечном синдроме возникает хроническая диарея, боли в животе: отмечают гепатоспленомегалию, мезаденит и синдром мальабсорбции. Экстрабилиарная обструкция обусловлена перипортальным и перипанкреатическим лимфаденитом, приводящим к билиарному блоку и токсическому гепатиту. Основой диагностики атипичных микобактериозов считают выделение гемокультуры микобактерии.
Ранее возбудителя этого заболевания относили к простейшим, но генетический и биохимический анализ P. carinii показал его таксономическую принадлежность к дрожжевым грибам. Существуют три морфологические формы P. carinii — спорозоит (внутрицистное тельце диаметром 1-2 мкм). трофозоит (вегетативная форма), циста с толстой стенкой диаметром 7-10 мкм (состоит из восьми грушевидных спорозоитов).
В природе пневмоцисты обнаруживают у крыс, мышей, собак, кошек, свиней, кроликов и других млекопитающих, но заражение человека возможно только при контакте с человеком. Инфицирование происходит воздушно-капельным, аэрогенным, ингаляционным и трансплацентарным путём (редко). Пневмоцисты обладают высокой тропностью к лёгочной ткани, поэтому даже в фатальных случаях патологический процесс редко выходит за пределы лёгких (это связывают с крайне низкой вирулентностью возбудителя). Микроорганизмы прикрепляются к пневмоцитам, вызывая их десквамацию. Основные клинические признаки пневмоцистоза — интерстициальная пневмония и реактивный альвеолит. Симптомы неспецифичны. Продолжительность инкубационного периода пневмоцистной пневмонии варьирует от 8-10 дней до 5 нед. Начало заболевания невозможно отличить от банальных инфекций респираторного тракта. Клинические симптомы у больных СПИДом развиваются медленнее, чем у пациентов с гемобластозами. Одышка возникает очень быстро (частота дыхательных движений до 30-50 в минуту) и сопровождается сухим или влажным кашлем со скудной, вязкой (иногда пенистой) мокротой, цианозом, повышением температуры тела. Плевральные боли и кровохарканье возникают редко. При аускультации выслушивают жёсткое или ослабленное дыхание (локально или над всей поверхностью лёгких), сухие хрипы. По мере прогрессирования пневмонии могут нарастать симптомы дыхательной и сердечно-сосудистой недостаточности. Рентгенологическая картина в начале неспецифическая, затем обнаруживают прикорневое снижение пневматизации лёгочной ткани и усиление интерстициального рисунка. Более чем в половине случаев визуализируют билатеральные облаковидные инфильтраты (симптом «бабочки»), а в разгаре заболевания — обильные очаговые тени («ватное» лёгкое). В начале заболевания нормальную рентгенологическую картину обнаруживают у трети пациентов. Раннее вовлечение ацинусов создает на рентгенограммах картину так называемой воздушной бронхограммы (нередко ошибочно связывают с интерстициальным поражением). Однако в дальнейшем на рентгенограммах определяют преимущественно паренхиматозную природу пневмонии. В 10-30% случаев отмечают асимметричные, как правило, верхнедолевые инфильтраты. При проведении КТ обнаруживают периферические инфильтраты (иногда с очагами распада), снижение прозрачности («матовое стекло») и эмфизематозные участки. Пневмоторакс — наиболее часто возникающее осложнение.
При исследовании крови определяют гипохромную анемию, лейкоцитоз (до 50х10 9 /л) и эозинофилию. При проведении биохимического анализа крови обнаруживают повышение активности ЛДГ до 700-800 МЕ/л. Определение РаО2 позволяет выявить артериальную гипоксемию. Обнаружение антител к P. carinii — неспецифичный тест; культуральные методы отсутствуют. Поэтому диагноз ставят на основании прямой морфологической визуализации пневмоцист в биологическом материале с помощью различных методов (иммунофлюоресценция, методы окрашивания образцов Романовского-Гимзы и Грама, использование реактива Шиффа и др.), а также проводят ПЦР-диагностику.
Открытую биопсию лёгкого выполняют при прогрессирующем течении заболевания. Макроскопически во время операции лёгкое больного выглядит увеличенным, уплотнённым, консистенция его напоминает резину; отмечают буллёзные и эмфизематозные изменения, обнаруживают полости распада. Интраальвеолярный пенистый экссудат, диффузные альвеолярные повреждения, эпителиоидные гранулёмы, десквамативный интерстициальный пневмонит, интерстициальные лимфоидные инфильтраты — гистологические изменения в ткани лёгкого при пневмоцистной пневмонии. Выживаемость больных СПИДом при развитии пневмоцистной пневмонии не превышает 55%. Прогноз значительно ухудшается, если лечение начинают на фоне острой дыхательной недостаточности, тяжёлой гипоксии или при лейкопении. Летальность вследствие пневмонии и острой дыхательной недостаточности у больных СПИДом составляет, по разным данным, от 52,5 до 100%, а при осуществлении ИВЛ — 58-100%.
Цитомегаловирусная инфекция, как правило, протекает латентно. Однако иногда диагностируют клинически выраженные формы заболевания, обусловленные первичным инфицированием цитомегаловирусом, а также реинфекцией или реактивацией вируса в заражённом организме. Генерализованная цитомегаловирусная инфекци, сопровождающаяся возникновением клинических симптомов, занимает важное место в структуре оппортунистических заболеваний ВИЧ-инфицированных пациентов. Данную патологию регистрируют у 20-40% больных СПИДом, не принимающих антиретровирусные препараты. Цитомегаловирусная инфекция — непосредственная причина смерти 10-20% ВИЧ-инфицированных пациентов. Вероятность возникновения и тяжесть течения цитомегаловирусной инфекции связывают со степенью иммуносупрессии. Если количество СД4+-лимфоцитов в крови составляет 100-200 клеток в 1 мкл, то манифестную цитомегаловирусную инфекцию диагностируют у 1,5% ВИЧ-инфицированных людей. При уменьшении числа СД4+-лимфоцитов до 50-100 клеток в 1 мкл вероятность развития цитомегаловирусной инфекции увеличивается почти в четыре раза. При тотальном исчезновении СД4+-лимфоцитов (менее 50 клеток в 1 мкл) заболевание регистрируют практически у половины инфицированных пациентов.
Если содержание СД4+-лимфоцитов в крови достаточно велико (более 200 клеток в 1 мкл), то манифестацию цитомегаловирусной инфекции отмечают редко. Данное заболевание, как правило, развивается постепенно, при этом обнаруживают симптомы-предвестники. предшествующие формированию выраженных органных нарушений. У взрослых отмечают длительную волнообразную лихорадку неправильного типа с подъёмами температуры тела выше 38,5 °С. слабость, быструю утомляемость, потерю аппетита, существенное снижение веса; реже — потливость (преимущественно по ночам), артралгии или миалгии. При поражении лёгких указанные симптомы дополняет постепенно усиливающийся сухой или со скудной мокротой кашель. При вскрытии умерших пациентов, страдавших цитомегаловирусным поражением органов дыхания, нередко обнаруживают фиброателектаз лёгких с кистами и инкапсулированными абсцессами. Наиболее тяжёлый признак цитомегаловирусной инфекции — ретинит (диагностируют у 25-30% пациентов). Больные жалуются на плавающие пятна перед глазами, затем происходит снижение остроты зрения. Потеря зрения необратима, поскольку данный процесс развивается в результате воспаления и некроза сетчатки. При офтальмоскопии на сетчатке обнаруживают экссудаты и периваскулярные инфильтраты. При цитомегаловирусном эзофагите у больного при глотании возникает боль за грудиной. При эндоскопии в типичном случае визуализируют обширную поверхностную язву слизистой оболочки пищевода или желудка. Гистологические методы позволяют обнаружить клетки цитомегалии в биоптате: с помощью метода ПЦР можно определить ДНК вируса. Цитомегаловирусная инфекция может поражать различные органы пищеварительной системы, но чаще всего развивается колит. Пациента беспокоят боли в животе, жидкий стул, похудание и потеря аппетита. Перфорация кишки — наиболее грозное осложнение. Как возможные клинические симптомы цитомегаловирусной инфекции диагностируют также восходящий миелит и полиневропатию (подострого течения): энцефалит, характеризующийся деменцией; цитомегаловирусный гепатит с одновременным поражением жёлчных путей и развитием склерозирующего холангита; адреналит. проявляющийся резкой слабостью и снижением артеирального давления. Иногда возникает эпидидимит, цервицит. панкреатит.
Специфическое поражение сосудов преимущественно микроциркуляторного русла и сосудов мелкого калибра — морфологическая особенность патологического процесса при цитомегаловирусной инфекции. Для постановки клинического диагноза цитомегаловирусной инфекции необходимо проводить лабораторные исследования. Как показали исследования, наличие в крови больного антител класса IgM (или высоких титров антител класса IgG), a также присутствие вирионов в слюне, моче, сперме и вагинальном секрете недостаточно ни для установления факта активной репликации вируса, ни для подтверждения диагноза манифестной цитомегаловирусной инфекции. Обнаружение вируса (его антигенов или ДНК) в крови имеет диагностическое значение. Достоверным критерием высокой активности цитомегаловируса, доказывающим его этиологическую роль в развитии тех или иных клинических симптомов, служит титр ДНК цитомегаловируса. При повышении концентрации ДНК вируса в плазме в 10 раз вероятность развития цитомегаловирусного заболевания возрастает в три раза. Определение высокой концентрации ДНК вируса в лейкоцитах крови и плазме требует безотлагательного начала этиотропной терапии.

Токсоплазмоз — заболевание, вызываемое Т. gondii, чаще всего возникающее у ВИЧ-инфицированных пациентов на фоне СПИДа. Попадание токсоплазм в организм человека приводит к формированию объёмных образований в ЦНС (в 50-60% случаев) и развитию первичных эпилептических припадков (в 28% случаев). Токсоплазма — внутриклеточный паразит; заражение человека происходит при употреблении в пищу продуктов (мясо и овощи), содержащих ооцисты или тканевые цисты. Полагают, что развитие токсоплазмоза — реактивация латентной инфекции, поскольку при наличии в сыворотке крови антител к токсоплазме вероятность возникновения токсоплазмоза увеличивается в десять раз. Однако примерно у 5% ВИЧ-инфицированных пациентов на момент постановки диагноза токсоплазмоза антитела к Т. gondii отсутствуют. Заражение обычно происходит в детском возрасте. Цисты представляют собой очаги тлеющей инфекции, обострение или рецидив которых может наступить через несколько лет или даже десятилетий после инфицирования ВИЧ. В форме цист токсоплазмы сохраняются до 10-15 лет. преимущественно в тканях головного мозга и органа зрения, а также во внутренних органах. Патоморфологические изменения при токсоплазмозе имеют фазовый характер. В паразитемической фазе токсоплазмы поступают в регионарные лимфатические узлы, затем проникают в кровеносное русло и распространяются по органам и тканям. Во второй фазе происходит фиксация токсоплазмы в висцеральных органах, приводящая к развитию некротических и воспалительных изменений и образованию мелких гранулём. В течение третьей (заключительной) стадии токсоплазмы формируют в тканях истинные цисты; воспалительная реакция исчезает, очаги некроза подвергаются обызвествлению. Хотя токсоплазмы могут поражать все органы и ткани, но, как правило, у ВИЧ-инфицированных пациентов регистрируют церебральную форму заболевания. Отмечают лихорадку, головные боли, возникновение в 90% случаев разнообразной очаговой неврологической симптоматики (гемипарез, афазия, психические и некоторые другие нарушения). При отсутствии адекватного лечения наблюдают спутанность сознания, оглушённость, сопор и кому в результате отёка головного мозга. При выполнении МРТ или КТ с контрастированием обнаруживают множественные очаги с кольцевидным усилением и перифокальным отёком, реже — единичный очаг. Дифференциальный диагноз проводят с лимфомой головного мозга, опухолями другой этиологии, СПИД-дементным синдромом, мультифокальной лейкоэнцефалопатией и туберкулёмами. Почти в каждом случае диагностируют преимущественное поражение определённых органов и систем. Иногда токсоплазмоз протекает без формирования объёмных образований в головном мозге (по типу герпетического энцефалита или менингоэнцефалита). Внемозговые локализации токсоплазмоза (например, интерстициальная пневмония, миокардит, хориоретинит и поражение органов пищеварительной системы) у больных СПИДом регистрируют в 1,5-2% случаев. Максимальное количество очагов внемозговых локализаций обнаруживают при исследовании зрительного аппарата глаза (примерно в 50% случаев). Диссеминацня (по меньшей мере две локализации) происходит в 11,5% случаев. Диагностировать токсоплазмоз крайне сложно. Ликвор при спинномозговой пункции может быть интактным. Диагноз ставят на основании клинической картины, данных МРТ или КТ, а также при наличии антител к токсоплазме в сыворотке крови. Биопсию головного мозга выполняют при невозможности правильно установить диагноз. При биопсии в поражённых участках наблюдают воспаление с зоной некроза, расположенной в центре.
Саркома Капоши — многоочаговая сосудистая опухоль, поражающая кожу, слизистые оболочки и внутренние органы. Развитие саркомы Капоши связывают с вирусом герпеса человека 8-го типа, который впервые обнаружили в коже больного с этой опухолью. В отличие от эндемического и классического вариантов заболевания, эпидемическую форму саркомы регистрируют только у ВИЧ-инфицированных пациентов (преимущественно у гомосексуалистов). В патогенезе саркомы Капоши ведущую роль отводят не злокачественному перерождению клеток, а нарушению продукции цитокинов, контролирующих клеточную пролиферацию. Инвазивный рост для данной опухоли нехарактерен.
При гистологическом исследовании саркомы Капоши обнаруживают усиленную пролиферацию веретенообразных клеток, сходных с эндотелиальными и гладкомышечными клетками сосудов. Саркома у ВИЧ-инфицированных пациентов протекает неодинаково. У одних больных диагностируют лёгкую форму заболевания, у других — более тяжёлую. Клинические признаки саркомы Капоши разнообразны. Чаще всего развиваются поражения кожи, лимфатических узлов, органов пищеварительной системы и лёгких. Разрастание опухоли может приводить к лимфатическому отёку окружающих тканей. В 80% случаев поражение внутренних органов сочетается с вовлечением в патологический процесс кожи. На начальных стадиях заболевания на коже или слизистой оболочке формируются небольшие возвышающиеся красно-лиловые узлы, нередко возникающие на месте травмы. Вокруг узловых элементов иногда обнаруживают мелкие тёмные пятна или желтоватый ободок (напоминают синяки). Диагноз саркомы Капоши ставят с учётом гистологических данных. При биопсии поражённых участков отмечают пролиферацию веретенообразных клеток, диапедез эритроцитов; обнаруживают содержащие гемосидерин макрофаги, а также воспалительные инфильтраты. Одышка — первый признак поражения лёгких при саркоме Капоши. иногда наблюдают кровохарканье. На рентгенограммах грудной клетки определяют двусторонние затемнения в нижних долях лёгких, сливающиеся с границами средостения и контуром диафрагмы; нередко обнаруживают увеличение прикорневых лимфатических узлов. Саркому Капоши следует дифференцировать с лимфомами и микобактериальной инфекцией, протекающей с поражением кожи. У 50% больных диагностируют поражение органов пищеварительной системы, а в тяжёлых случаях возникает кишечная непроходимость или кровотечение. Вовлечение в патологический процесс жёлчных путей приводит к развитию механической желтухи.
Смерть больных ВИЧ-инфекцией наступает либо от прогрессирования вторичных заболеваний, либо от любых других сопутствующих заболеваний, не связанных с ВИЧ. Генерализованный туберкулёз — основная причина гибели больных СПИДом. Кроме того, причиной смерти считают лёгочную патологию (с последующим развитием дыхательной недостаточности) и манифестную цитомегаловирусную инфекцию. В последнее время регистрируют увеличение летальности вследствие цирроза печени, обусловленного развитием вирусного гепатита С на фоне хронической алкогольной интоксикации. Прогрессирование хронического гепатита в цирроз у таких пациентов происходит в течение 2-3 лет.
источник
Тонкая серозная оболочка — брюшина, — которая в том или ином виде располагается на большей части органов, имеет специфические защитные свойства. Так, например, при возникновении воспаления она может отграничивать пораженную область, формируя абсцесс брюшной полости. На медицинском сленге это называется «припаивание», то есть образование спаек между соседними органами таким образом, чтобы получилось замкнутое пространство.
Абсцесс брюшной полости – это гнойное воспаление органа или его части, с дальнейшим расплавлением тканей, образование полости и капсулы вокруг нее. Он может сформироваться абсолютно в любом «этаже» брюшной полости и сопровождаться явлениями интоксикации, лихорадки и сепсиса.
Кром этого, у пациента будут превалировать болевые ощущения, наблюдаться дефанс мышц живота, возможна тошнота и рвота. Иногда, в сложных случаях, спайки вызывают кишечную непроходимость.
Абсцесс брюшной полости, что не удивительно, образуется после хирургических вмешательств и трактуется как осложнение этого вида лечения. Ввиду роста количества проводимых ежегодно операций, число подобных осложнений тоже прогрессивно увеличивается. Большую роль в этом играет снижение иммунитета и повсеместное применение антибиотиков, формирующее у микроорганизмов устойчивость и затрудняющее послеоперационную профилактику осложнений.
Согласно заключениям статистов, у одного процента хирургических пациентов развивается послеоперационный абсцесс. Эта цифра выше, если вмешательство было экстренным и времени на предоперационную подготовку не было.
Основной фактор риска, из-за которого может возникнуть абсцесс брюшной полости, — это, конечно, полостное оперативное вмешательство. Чаще всего он возникает после лечения заболеваний поджелудочной железы, желчного пузыря, сшивания петель кишечника.
Появление воспаления связано с попаданием содержимого кишечника на брюшину, а также обсеменения ее в условиях операционной. Оно может быть вызвано и тупой травмой живота. В месте сдавления образуется асептическое воспаление, к которому позже присоединяется вторичная флора.
Более чем в половине случаев абсцесс располагается либо за париетальным (пристеночным) листком брюшины, либо между ее париетальным и висцеральным листками.
Абсцесс брюшной полости (МКБ 10 — К65) может появиться в результате травм живота, например, длительных сдавлений или ударов, инфекционных заболеваний кишечной трубки (иерситеоз, сальмонелез, брюшной тиф), развития воспалительных процессов в органах или на слизистых, а так же после перфорации язвы желудка или кишечника.
Выделяют три основные причины:
- Наличие вторичного перитонита из-за разрыва аппендикса, несостоятельности кишечных анастомозов после полостных операций, некроза головки поджелудочной железы, травмы живота.
- Гнойное воспаление тазовых органов, например, сальпингит, параметрит, пиосальпинкс, тубоовариальный абсцесс и другие.
- Острое воспаление поджелудочной железы и желчного пузыря, неспецифический язвенный колит.
Помимо вышеперечисленного, иногда причиной абсцесса может быть воспаление околопочечной клетчатки, остеомиелит поясничного отдела позвоночника, туберкулезный спондилит. Чаще всего в очаге воспаления высеивают стафилококков, стрептококков, клостридий и ишерихий, то есть ту флору, которая и в норме может встречаться в кишечнике.
Абсцесс после операции брюшной полости появляется вследствие чрезмерной реакции иммунной системы на вмешательство во внутреннюю среду или на размножение микроорганизмов. Возбудитель может проникнуть в брюшную полость и с током крови или лимфы, а так же просочиться через стенку кишечника. Кроме того, всегда есть риск занести инфекцию с руками хирурга, инструментарием или материалами во время операции. Еще одним фактором выступают органы, сообщающиеся с внешней средой, такие как маточные трубы или кишечник.
Нельзя исключать появление воспалительных инфильтратов после проникающего ранения брюшной полости, перфорации язв и расхождении швов после хирургического лечения.
Брюшина реагирует на появление раздражающего фактора (воспаления) стереотипно, а именно, она вырабатывает на своей поверхности фибрин, который склеивает участки слизистой между собой и отграничивает таким образом очаг от здоровых тканей. Если в результате действия гноя эта защита разрушается, то воспалительный детрит затекает в карманы и отлогие места живота. При развитии такого сценария говорят уже о сепсисе.
Что происходит с человеком, когда у него формируется абсцесс брюшной полости? Симптомы схожи с любым воспалительным заболеванием:
- Высокая, внезапно начавшаяся лихорадка сопровождающаяся ознобом и обильным потом.
- Тянущие боли в животе, которые усиливаются при дотрагивании или надавливании.
- Учащенное мочеиспускание, так как брюшина натягивается и это раздражает барорецепторы стенки мочевого пузыря.
- Нарушения стула в виде запора.
- Тошнота и рвота на высоте лихорадки.
Кроме того, у пациента может быть учащенное сердцебиение. Оно возникает по двум причинам: высокая температура и интоксикация. А так же патогномоничным симптомом является напряжение мышц пресса. Это защитный рефлекс, который не позволяет еще больше травмировать воспаленную область.
Если абсцесс расположен непосредственно под диафрагмой, то помимо общих симптомов будут такие, которые укажут на эту особенность. Первым отличием будет то, что боль локализуется в подреберной области, усиливается во время вдоха и иррадиирует в лопаточную область. Второе отличие – это изменение походки. Человек начинает невольно беречь больную сторону и наклоняется к ней, чтобы уменьшить напряжение мышц.
Абсцесс брюшной полости (МКБ 10 – К65) может остаться не диагностированным, если развивается на фоне других тяжелых состояний, либо пациент не обращается за помощью. Но следует помнить, что в результате такого халатного поведения могут развиться угрожающие жизни состояния, такие как сепсис и разлитой перитонит.
Поддиафрагмальные абсцессы способны расплавлять диафрагму и прорываться в плевральную полость, образуя там спайки. Такой сценарий может даже привести к повреждению легкого. Поэтому, если после операции или травмы у вас поднялась температура или возникли болевые ощущения, не ждите, что все само пройдет. В таком вопросе лишняя проверка не помешает.
Послеоперационный абсцесс брюшной полости в условиях стационара выявить достаточно легко. Самыми информативными методами являются рентген, УЗИ, КТ и МРТ органов груди и живота. Помимо этого, можно женщинам сделать пункцию свода влагалища, чтобы проверить, есть ли гнойные затеки в отлогих местах.
Кроме того, не стоит забывать и о лабораторной диагностике. В общем анализе крови будет наблюдаться резкое повышение скорости оседания эритроцитов (СОЭ), лейкоцитарная формула будет иметь резкий сдвиг влево, возможно даже до юных форм, а абсолютное число лейкоцитов повысится за счет нейтрофилов.
Эталоном в диагностике абсцессов остается ультразвуковое исследование брюшной полости. Существуют четкие признаки, которые указывают на наличие воспалительного инфильтрата:
- образование имеет четкие контуры и плотную капсулу;
- внутри его находится жидкость;
- содержимое неоднородное по структуре и разделяется на слои;
- над жидкостью есть газ.
Основным методом лечения абсцессов, конечно же, остается оперативное вмешательство. Необходимо дренировать гнойник, промыть полость антисептиком и раствором антибиотиков. Консервативное лечение не дает никакой гарантии того, что воспаление утихнет, а жидкость внутри абсцесса самостоятельно эвакуируется.
Конечно, после того как очаг будет удален, пациенту обязательно назначают противомикробную терапию антибиотиками широкого спектра. Как правило, врач выписывает одновременно два препарата, имеющих различный механизм действия и эффективно уничтожающих разных представителей микробной флоры.
Обязательно стоит предупредить больного о возможных последствиях данного лечения, таких как рвота, отсутствие аппетита, воспаление сосочкового слоя языка, головные боли и учащенное мочеиспускание. Да и самому врачу стоит о них помнить и не добавлять их к клинической картине заболевания.
Абсцесс брюшной полости (код по МКБ 10 – К65) — достаточно серьезное осложнение, поэтому врачам и пациентам стоит озаботиться профилактикой этого состояния. Необходимо адекватно и в полном объеме лечить воспалительные заболевания любых органов брюшной полости, обязательно проводить пред- и постоперационную подготовку больных, а так же хорошо стерилизовать инструментарий и руки хирурга.
При подозрении на аппендицит или в случае внезапного подъема температуры не стоит ждать знака свыше, а необходимо немедленно обратиться к врачу за консультацией. Это может спасти вам жизнь и здоровье.
Смертность от абсцесса брюшной полости достигает сорока процентов. Все зависит от того, насколько распространен процесс, где он располагается и какое заболевание его вызвало. Но при своевременно обращении в больницу вероятность неблагоприятного исхода снижается.
источник
 волнообразная лихорадка от 37,5 °C до 39-40 °C с ознобом и потливостью;
волнообразная лихорадка от 37,5 °C до 39-40 °C с ознобом и потливостью; Печеночные абсцессы. Зачастую имеют множественный характер, развиваются на фоне ранений, инфекций желчевыводящих путей. Болезненные ощущения локализуются в области правого подреберья, реже – в эпигастральной области, характерна постоянная тошнота. Быстрая ходьба, резкие наклоны вперед могут усиливать болевой синдром.
Печеночные абсцессы. Зачастую имеют множественный характер, развиваются на фоне ранений, инфекций желчевыводящих путей. Болезненные ощущения локализуются в области правого подреберья, реже – в эпигастральной области, характерна постоянная тошнота. Быстрая ходьба, резкие наклоны вперед могут усиливать болевой синдром.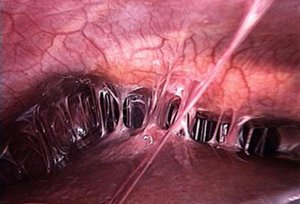 Межкишечные абсцессы. Появляются за счет скопления гноя между петлями тонкой, толстой кишки; чаще всего множественные. Пациента беспокоят постоянные ноющие или острые боли в животе без точной локализации, тошнота, рвота. Парез кишечника сопровождается метеоризмом, запорами, асимметрией живота.
Межкишечные абсцессы. Появляются за счет скопления гноя между петлями тонкой, толстой кишки; чаще всего множественные. Пациента беспокоят постоянные ноющие или острые боли в животе без точной локализации, тошнота, рвота. Парез кишечника сопровождается метеоризмом, запорами, асимметрией живота.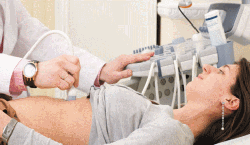 Ультразвуковая диагностика органов брюшной полости. Методика отлично подходит для поиска осумкованного гноя в области печени, селезенки, под диафрагмой, в Дугласовом пространстве. УЗИ также может помочь определить причину болезни (острый аппендицит или панкреатит, гнойный сальпингоофорит и т.д.).
Ультразвуковая диагностика органов брюшной полости. Методика отлично подходит для поиска осумкованного гноя в области печени, селезенки, под диафрагмой, в Дугласовом пространстве. УЗИ также может помочь определить причину болезни (острый аппендицит или панкреатит, гнойный сальпингоофорит и т.д.).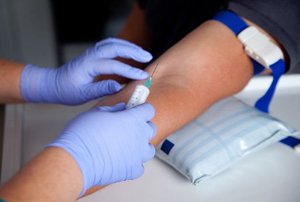 Клинический, биохимический анализы крови, исследование крови на стерильность. В пользу воспалительного процесса говорит высокий лейкоцитоз с нейтрофильным сдвигом формулы, высокие значения СОЭ, повышение печеночных ферментов, появление С-реактивного белка, прокальцитонина.
Клинический, биохимический анализы крови, исследование крови на стерильность. В пользу воспалительного процесса говорит высокий лейкоцитоз с нейтрофильным сдвигом формулы, высокие значения СОЭ, повышение печеночных ферментов, появление С-реактивного белка, прокальцитонина.