Абсцессы брюшной полости, возникающие в послеоперационном периоде, продолжают оставаться актуальной проблемой в абдоминальной хирургии.
Частота таких гнойных осложнений как подпеченочный и межкишечный абсцессы после холецистэктомии по данным ряда авторов колеблется от 0,2 до 2,5 %.
Литературные данные свидетельствуют о сохраняющейся высокой летальности (20,7% — 58,2%) при послеоперационных абсцессах брюшной полости и гнойниках малого таза, что заставляет искать новые пути лечения гнойных осложнений послеоперационного периода.
Неинвазивность ультразвукового исследования сделала его методом выбора для контроля пункций и аспираций жидкостных образований брюшной полости.
Применение цветного допплеровского картирования позволяет дифференцировать сосудистые структуры и тем самым избегать возможных осложнений. Таким образом, показания к миниинвазивным вмешательствам постоянно расширяются.
Использование миниинвазивных вмешательств позволяет сократить число открытых операций по поводу ограниченных жидкостных образований брюшной полости.
С расширением спектра задач, решаемых с помощью ультразвуковых методик, возникла необходимость разработки диагностических критериев и алгоритмов использования, различных миниинвазивных технологий в лечении осложнений операций на органах брюшной полости.
Нами проведен ретроспективный анализ 28 историй болезни пациентов, находившихся на лечении в хирургических клиниках Саратовского государственного медицинского университета с послеоперационными абсцессами брюшной полости.
Больные по локализации абсцессов распределились следующим образом: 19 больных с подпеченочным абсцессом, 5 больных с поддиафрагмальным абсцессом, из них у 4 пациентов абсцесс локализовался справа, а у 1 — слева, 2 больных с абсцессами малого таза, 2 больных с межкишечными абсцессами.
У 22 больных абсцессы развились после выполненной холецистэктомии: 10 — после лапароскопической, у 12 — открытым способом. У остальных шестерых больных абсцессы развились после следующих операций: после ампутации матки — 1, после аппендэктомии — 2, после резекции желудка — 2, после правосторонней гемиколэктомии — 1.
18 пациентам нами были выполнены миниинвазивные вмешательства (группа сравнения). 10 пациентам была выполнена пункция и дренирование абсцессов брюшной полости под контролем УЗИ, и у 8 пациентов выполнялась, лапароскопическое дренирование абсцессов брюшной полости. Пункция и дренирование абсцессов проводилось по следующей методике: при УЗИ в брюшной полости выявлялось патологическое жидкостное образование, и определяли оптимальную траекторию пункционного канала, чтобы избежать повреждения расположенных рядом полых органов и крупных кровеносных сосудов, с использованием цветного доплеровского картирования. Затем производилось дренирование либо стилет-катетером с помощью набора Ившина, либо по методике Сельдингера — двойной пункционной иглой G18-20, дренажем типа «свиной хвост» F9-F12, с помощью рентгенконтрастного проводника. Содержимое абсцессов отправлялось на бактериологическое исследование. Эффективность лечения оценивали при динамическом УЗИ и фистулографии. В 8 наблюдениях для диагностики и лечения послеоперационных абсцессов мы применили лапароскопические вмешательства. Операция состояла из следующих этапов: обзорная лапароскопия, вскрытие полости абсцесса, санации гнойной полости и дренирование гнойника. Наличие выраженных воспалительно-инфильтративных изменений вокруг подпеченочного абсцесса вынудило в 2 наблюдениях выполнить конверсию и закончить операцию из лапаротомного доступа.
И 10 пациентам (контрольная группа) была выполнена либо релапаротомия, либо конверсия, либо лапаротомия после проведенных ранее лапароскопических операций, вскрытие и дренирование абсцесса брюшной полости. Пациенты в этих группах были соотносимы по полу, возрасту и сопутствующим заболеваниям (преобладали ИБС и артериальная гипертония). В обеих группах большую часть составили больные пожилого и старческого возраста от 45% до 54%.
У больных с выявляемыми в послеоперационном периоде гипертермией и ограниченными жидкостными образованиями брюшной полости при УЗИ, и без признаков разлитого перитонита мы придерживались следующего алгоритма. Алгоритм заключается в последовательных этапах, где каждый последующий выполняется при неэффективности предыдущего:
1. Диагностическая тонкоигольная пункция, с биохимическим и бактериологическим исследованием полученной жидкости, в случае выявления признаков инфицирования, в полость вводятся растворы антибиотиков и антисептиков.
2. Чрескожное дренирование под контролем УЗИ.
3. Лапароскопия, санация гнойника и наружное дренирование.
4. Релапаротомия (либо конверсия, либо лапаротомия после перенесенной лапароскопической операции).
Выполнение миниинвазивных вмешательств позволило в более ранние сроки активизировать больных. Уменьшился срок пребывания в стационаре: у больных из контрольной группы средний послеоперационный койко-день составил 20,4, а у пациентов, которым были выполнены миниинвазивные вмешательства, средний послеоперационный койко-день снизился до 15,6.
Так же следует отметить меньшее количество местных гнойных осложнений, так в группе больных, которым выполнялись миниивазивные вмешательства, осложнений не было, а у больных, которым были выполнены открытые вмешательства, нагноение послеоперационного шва возникло в 6 случаях из 12, а у одного больного течение послеоперационного периода осложнилось подкожной эвентрацией. В группе больных, перенесших релапаротомию, отмечен 1 летальный исход, в результате тромбоэмболии легочной артерии в раннем послеоперационном периоде.
Таким образом, считаем эффективным предложенный алгоритм действий при выявлении ограниченных скоплений жидкости в брюшной полости в послеоперационном периоде. Миниинвазивные вмешательства, можно считать методом выбора в лечении послеоперационных абсцессов брюшной полости.
источник
ПЕРВЫЙ ОПЫТ ПРИМЕНЕНИЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ В КОМПЛЕКСНОМ МАЛОИНВАЗИВНОМ ЛЕЧЕНИЕ АБСЦЕССОВ БРЮШНОЙ ПОЛОСТИ
Абсцессы брюшной полости остаются важной проблемой абдоминальной хирургии. Как осложнение послеоперационного периода они встречаются с частотой 0,1-1,8% случаев [1, 2, 3]. При ургентной патологии, послеоперационный период осложняется отграниченными гнойными очагами брюшной полости в 20-25% [4]. Отграниченные гнойные осложнения брюшной полости становятся причиной повторных хирургических вмешательств в 19-28,5% случаев [5, 6]. Хирургический метод лечения абсцессов брюшной полости направлен на устранение очага инфекции при минимальной травматизации окружающих тканей. Именно малоинвазивные интервенционные методики под УЗ- и КТ-контролем, на современном этапе, становятся операцией выбора при отграниченных очагах брюшной полости. Существует множество методик, описывающих различные способы санации гнойных очагов брюшной полости после транскутанных дренирований. Однако в 5-8% случаев положительного эффекта от лечения достичь не удаётся [7, 8].
Фотодинамическая терапия (ФДТ) является разновидностью химиотерапии, основанной на фотохимической реакции, катализатором которой является кислород, активированный фотосенсибилизатором (ФС) и воздействием лазерного излучения [9]. В 1897 году Оскар Рааб, студент Мюнхенского университета, обнаружил, что низкие концентрации акридинового оранжевого и других красителей, инертных в темноте, приводят к быстрой гибели микроорганизмов при облучении обычным солнечным светом. В 1900 году он опубликовал первое подробное описание эффекта химической фотосенсибилизации и фотодеструкции живых клеток. В 1903 году в Германии, профессором Мюнхенского университета Германом фон Таппейнером ( Herman von Tappeiner ) и его коллегами, был проведен первый сеанс фотодинамической терапии. Тогда же был введен и термин «фотодинамическое действие», используемый по настоящее время. В 1990 году Z . Malik с соавторами в своем обзоре сообщил о бактерицидном действии ФДТ на микроорганизмы и дрожжевые грибки. A . Minnock с соавторами показал, что большинство грамнегативных и грампозитивных бактерий может быть успешно фотоинактивировано с применением водорастворимых фталоцианинов. В настоящее время установлена возможность фотоинактивации безоболочечных вирусов с применением такого простого фотосенсибилизатора, как метиленовый синий. Достаточно эффективно подвергаются фотодинамической инактивации грибы, в том числе в форме спор.
В настоящее время антимикробная фотодинамическая терапия (АФДТ) использует опыт, накопленный при ФДТ опухолей. До сих пор наиболее активно исследуемой областью АФДТ являются исследования in vitro межклеточного взаимодействия активизированного фотосенсибилизатора и возбудителя инфекционного заболевания. Исследованы практически все фотосенсибилизаторы и красители, все источники света и большинство возбудителей инфекционных заболеваний
Цель исследования: улучшить результаты малоинвазивного хирургического лечения больных с абсцессами брюшной полости, путём разработки комплексного метода лечения в основе которого лежит фотодинамический эффект.
Материалы и методы: проанализированы результаты лечения 20 больных с абсцессами брюшной полости. 8 из них составили основную группу, которым применялась фотодинамическая терапия; 12 – контрольную, которым применялось стандартное промывание растворами антисептиков. В условиях хирургического отделения БУЗ ВО ВГКБСМП №10 по разработанной нами методике было проведено лечение 8 больных (3 мужчин и 5 женщин, возраст от 28 до 67 лет); 4 больных с абсцессами брюшной полости после деструктивных форм панкреатита, 3 – аппендикулярный инфильтрат с абсцедированием, 1 – послеоперационный абсцесс брюшной полости после лапароскопической аппендектомии, 1 – поддиафрагмальный абсцесс после разлитого гнойного перитонита.
Всем больным после верификации диагноза «абсцесс брюшной полости» производилась пункция и дренирование гнойного очага под УЗ-контролем с постановкой дренажа 10-12 Fr . Содержимое активно аспирировалось шприцом. Полость абсцесса промывалась физиологическим раствором. После промывания в полость вводился фотосенсибилизатор, после чего дренаж перекрывался. Затем через установочную канюлю, введённую в дренаж герметично проводилось фторопластовое оптическое волокно, с помощью которого на заполненную ФС полость воздействовали лазерным излучением. Источник излучения: аппарат лазерный терапевтический «Мустанг 2000». Длинна волны составляла 665 10 нм, мощность 50 мВт, максимальная плотность мощности на торце волокна 40 Вт/см 2 . Длительность сеанса облучения составляла 30 мин. После проведённого сеанса ФДТ дренаж оставлялся на отток. В дальнейшем осуществлялась ежедневная перевязка с промыванием полости абсцесса 0,05% раствором хлоргекседина биглюконата. Всем больным проводилась системная антибиотикотерапия. Группа препаратов подбиралась в зависимости от основного заболевания и длительности лечения до постановки диагноза «Абсцесс брюшной полости». При необходимости коррекция антибиотикотерапии осуществлялась после получения результатов бактериологических посевов.
Результаты: Для оценки применяемой методики проводился контроль следующих параметров: сроки нормализации количества лейкоцитов, лейкоцитарный индекс интоксикации (ЛИИ), результаты бактериологических посевов. Результаты сравнивались с аналогичными показателями, полученными при малоинвазивном лечении абсцессов брюшной полости с использованием пункционно-дренирующей методики под УЗ-контролем и дальнейшим ежедневным промыванием полости 0,05% раствором хлоргекседина биглюконата. В контрольную группу вошло 12 пациентов с абсцессами брюшной полости различной этиологии.
У всех больных удалось достичь выздоровления, используя малоинвазивные интервенционные вмешательства. Нормализации уровня лейкоцитов в крови и снижение ЛИИ ниже 4 наблюдалась на 4 сутки у 7 из 8 пролеченных больных основной группы. В контрольной группе данных показателей удалось достичь к 7-8 суткам. Лишь у пациентки с поддиафрагмальным абсцессом после перенесённого разлитого гнойного перитонита снижение лабораторных показателей произошло на 10 сутки, что скорее всего является следствием более тяжёлого общего состояния пациентки и истощением иммунной системы организма. Отрицательные бактериологические посевы в основной группе были получены на 5-6 сутки после дренирования и сеанса ФДТ у 100% пациентов. У пациентов контрольной группы на 7-9 сутки. Следует также отметить, что купирование болевого синдрома произошло на 2-3 сутки у всех пациентов основной группы; снижение гипертермии — на 31 сутки у 7 из 8 больных (кроме пациентки с поддиафрагмальным абсцессом, у которой явления субфебрилитета наблюдались в течение 11 дней). В контрольной группе нормализация температуры и стихание болевого синдрома произошло на 4-6 сутки после оперативного лечения.
Заключение: Можно сделать предварительный вывод о положительных результатах применения метода комплексного лечения пациентов с абсцессами брюшной полости различного генеза, в основе которого лежит фотодинамическая терапия. Использование данного метода позволило ограничиться применением малоинвазивных пункционно-дренирующих вмешательств, не прибегая к конверсии. Фотодинамическая терапия может быть использована в первые сутки после дренирования гнойника, не дожидаясь результатов посева и чувствительности к антисептикам, т.к. вырабатываемый в процессе фотохимической реакции синглетный кислород способен воздействовать на большинство известных микробов (бактерий, грибов). Благодаря ускорению некролитической фазы процесса и стимуляции грануляции уже к 2-3 суткам наблюдается улучшение общего состояния больных, которые субъективно отмечают купирование болевого синдрома и гипертермии. Предполагаемый эффект воздействия антимикробной фотодинамической терапии нельзя недооценивать. Быстрое распространение антибиотикорезистентных микроорганизмов позволяет предположить, что скоро все антибиотики окажутся бесполезными перед лицом ранее хорошо поддававшихся лечению бактериальных инфекций, в случае чего будет необходима альтернатива.
Считаем целесообразным продолжить использования данного метода комплексного малоинвазивного лечения пациентов с абсцессами брюшной полости для накопления результатов и проведения их сравнительного анализа.
Жебровский ВВ. Ранние и поздние послеоперационные осложнения в хирургии органов брюшной полости. Симферополь. : КГМУ; 2000. 688 с.
Bufolari A, Giustozzi G, Moggi L Postoperative intraabdominal abscesses: percutaneous versus surgical treatment. Acta Chir. Belg 1996;5:197-200.
Kumar RR, Kim JT, Haukoos JS, Macias LH, Dixon MR, Stamos MJ, Konyalian VR. Factors affecting the successful management of intra-abdominal abscesses with antibiotics and the need for percutaneous drainage. Dis Colon Rectum. 2006 Feb;49(2):183-9. DOI:10.1007/s10350-005-0274-7.
Ильюшонок ВВ, Шулейко АЧ, Шкурин СВ. Малоинвазивные вмешательства под УЗ-контролем в лечении абсцессов брюшной полости и печени. Хирургия. Восточная Европа. 2012;3:58-59.
Артюсов ВП, Артюсов ОВ. Анализ причин релапаротомий. Здравоохранение Чувашии. 2008;1:12-14.
Барсуков КН, Рычагов ГП. Абсцессы брюшной полости как причина послеоперационного перитонита. Хирургия Восточная Европа. 2012;3:22-24.
Малоштан АВ. Пункция парапанкреатических скоплений жидкости в комплексе лечения инфицированного панкреонекроза. Клиническая хирургия. 2008;4-5:52-52.
Демьянова ВН, Суздальцев ИВ, Пыхтин ЮЮ, Пустий С А, Панченко АС. Сравнительная оценка и клиническая эффективность различных способов санаций внутрибрюшных абсцессов. Медицинский вестник Северного Кавказа 2016;11/1:87-89. DOI :10.14300/ mnnc 2016.11005. Dem ’ yanova VN , Suzdal ’ tsev IV , Pykhtin JuJu , Pustiy SA , Panchenko AS . Comparative evaluation and clinical effecyiveness of various methods of intra-abdominal abscesses sanation. Medical news of North Caucasus 2016;11 1:87-89. DOI :10.14300/ mnnc 2016.11005 (in Russian).
Гейниц АВ, Сорокатый АЕ, Ягудаев ДМ, Трухманов РС. Фотодинамическая терапия. История создания метода и её механизмы. Лазерная медицина. 2007;11/3:42-46. Geinitz AV, Sorokaty AE, Yagudajev DM, Trukhmanov RS. Photodynamic therapy. The history and mechanisms of its action. Laser medicine. 2007; 11/3: 42-46. (in Russian).
Lipson RL, Baldes EJ, Olsen AM . Hematoporphyrin derivative: a new aid of endoscopic detection of malignant disease. J. Thorac. Cardiovasc. Surg. 1961;42:623–629.
Русин ВИ. Возможности применения фотодинамической терапии в хирургии. Новостихирургии . 2010;2:109-114. Rusin VI. Possibilities of application of photodynamic therapy in surgery. News surgery. 2010;2:109-114.
Пантелеев ВС, Нартайлаков МА, Грицаенко ГА, Баязитова ГР, Соколов ВП. Фотодинамическая терапия в комплексном лечении больных гнойным холангитом. Анналы хирургической гепатологии. 2010;15/2:53-57. Panteleev VS, Nartailakov MA, Sokolov VP, Gritsaenko GA, Bajazitova GR. Photodynamic therapy in complex treatment of patients with purulent cholangitis. The annals of surgical Hepatology. 2010;15/2:53-57. ( in Russian) .
источник
Наиболее трудными для диагностики и грозными по своим последствиям являются абсцессы брюшной полости.
При подозрении на развитие абсцессов брюшной полости необходимо тщательное динамическое УЗИ. По нашему мнению диагностика остаточных скоплений выпота, гнойников брюшной полости должна быть следствием активного и целенаправленного поиска, а не случайной находкой.
Необходимо сделать правилом проведение УЗИ на 3 4 сутки после операций, произведенных по поводу деструктивного аппендицита, осложненного диффузным или разлитым перитонитом, а так же, после операций по поводу острого аппендицита с атипичным расположением червеобразного отростка.
Такая диагностическая тактика позволяет выявлять и устранять пункционным способом ограниченные скопления жидкости в брюшной полости до развития абсцессов.
В ультразвуковом изображении жидкостные скопления имеют вид объемных эхонегативных или гипоэхогенных образований различной формы. При скоплении жидкости под диафрагмой или в подпеченочном пространстве скопления жидкости выглядят в виде серповидных или овальных образований (рисунок 15). При этом обычно бывает реактивный выпот в плевральном синусе (рисунок 16). Не менее важным диагностическим признаком служит уменьшение подвижности диафрагмы на стороне поражения.
Аналогичные скопления выпота в полости малого таза визуализируются либо в виде анэхогенной полоски жидкости различной толщи ны, либо в виде округлого гипоэхогенного образования, которое может выглядеть неоднородным, в связи с присутствием сгустков фибрина и гноя.
Скопления жидкости в межкишечных пространствах определяются как объемные, полиморфные, не имеющие четких контуров гипоэхогенные образования, отличить которые от содержимого в просвете прилежащих петель кишки помогает отсутствие перистальтических движений и перемещения в них содержимого (рисунок 17).
При трансформации скоплений жидкости в абсцессы, в их окружности происходит формирование различной степени плотности и толщины пиогенной капсулы.
Оптимальным вариантом устранения патологических скоплений жидкости, а также дренирования абсцессов брюшной полости является их пункция и дренирование под контролем ультразвука.
Подготовка к проведению чрескожного вмешательства предусматривает четкую локализацию полостного образования, определение кратчайшего пути к нему, на котором не должны находиться свободные плевральные синусы, кровеносные сосуды, по возможности паренхиматозные органы и кишечные петли.
При ограниченных жидкостных скоплениях бывает достаточно пункционного метода. Под ультразвуковым наведением производится пункция полостного образования, аспирация его содержимого, промывание полости антисептическим растворами (диоксидин, хлоргексидин) с аспирацией промывных вод. В последующем осуществляется динамический ультразвуковой контроль. Порой требуется 2-3 пункции, производимые через два-три дня до полного спадения стенок полости.
Для дренирования рецидивирующих внутрибрюшных жидкостных скоплений и сформированных абсцессов требуется использовать специальные стилет — катетеры, пункции под контролем УЗИ троакаром с последующим проведением через его просвет в полость абсцесса дренажной трубки. Может быть использован метод введения катетера по Сельдингеру. При необходимости длительного дренирования целесообразно использовать двухпросветные дренажи, что позволяет обеспечить проточно-аспирационное лечение по Н.Н.Каншину.
При наличии многокамерных полостных образований необходимо проведение фистулографии, для уточнения взаимоотношений этих полостей, наличия или отсутствия сообшения между ними. В последних случаях, для обеспечения адекватного дренирования необходимо введение дополнительных дренажей.
Примером успешного использования описанного пункционного метода лечения остаточных гнойников может служить следующее наблюдение.
Больная Д. 52 лет доставлена в клинику 13.10-97. через 7 дней от начала заболевания. При поступлении в стационар клиническая картина распространенного перитонита, полиорганной недостаточности. После предоперационной подготовки произведена средняя срединная лапаротомия. Диагностирован острый гангренозный перфоративный аппендицит, разлитой гнойный перитонит, множественные абсцессы брюшной полости (межкишечные, поддиафрагмальные, подпеченочный, тазовый). Произведена аппендэктомия, промывание брюшной полости с частичным удалением массивных фибринозных наложений, назоинтестинальная интубация. Операционная рана ушита редкими лавсановыми швами через все слои брюшной стенки, завязанными на «бантики» Произведено наружное дренирование грудного лимфатического протока.
В послеоперационном периоде проводилась массивная этиотропная антибактериальная терапия со сменой препаратов через 5-6 суток (цефалоспорины 111 поколения/метронидазол; амикацин/метронидазол; карбапенемы). С интервалом в сутки произведено 4 ревизии и санации брюшной полости. Интенсивная детоксикационная терапия включала лимфосорбцию (3-3,5 л/сут), УФО крови. Были обеспечены парентеральное питание, постоянная декомпрессия и лаваж тонкой кишки, санационные бронхоскопии, ГБО.
Состояние больной оставалось крайне тяжелым, сохранялись проявления печеной, почечной, дыхательной и сердечной недостаточности После прекращения хирургических санаций брюшной полости ежедневно производилось динамическое УЗИ. На 3 сутки после последней ревизии и санации брюшной полости обнаружено скопление жидкости в правом поддиафрагмальном пространстве и двухсторонний плеврит. Под контролем УЗИ выполнены плевральные пункции с удалением серозного транссудата. При пункции поддиафрагмального пространства получено 18 мл сливкообразного гноя. С интервалом 2 суток, с учетом результатов УЗИ, трижды производились пункции поддиафрагмального пространства с аспирацией содержимого и промыванием полости диоксидином.
Постепенно состояние больной улучшилось. Операционная рана зажила первичным натяжением. Выписана на амбулаторное лечение по поводу пролежня в области крестца.
В заключение следует отметить, что УЗИ не может решить всех проблемы диагностики острого аппендицита и его осложнений. Нужно помнить о том. что, как и при других методах исследования, при УЗИ можно получить как ложноположительные, так и ложноотрицательные данные. Только тщательная оценка всей совокупности данных анамнеза, физикального обследования, лабораторных данных, порой результатов нескольких инструментальных исследований выполненных неоднократно, позволяет прийти к правильному диагнозу.
И все же, на пути этих кропотливых исканий иногда не хватает малой толики, нюанса, «изюминки». Иногда этой «изюминкой» может стать неприметная, но очень важная деталь, выявленная при ультразвуковом исследовании, выполненным опытным исследователем.
Д.Г. Кригер, А.В.Федоров, П.К.Воскресенский, А.Ф.Дронов
источник
Абсцесс брюшной полости – это ограниченный гнойник в брюшной полости, заключенный в пиогенную капсулу. Особенности клиники зависят от локализации и величины гнойного очага; общими проявлениями абсцесса брюшной полости служат боль и локальное напряжение мышц живота, лихорадка, кишечная непроходимость, тошнота и др. Диагностика абсцесса включает обзорную рентгенографию органов брюшной полости, УЗИ и КТ брюшной полости. Лечение заключается во вскрытии, дренировании и санации гнойника; массивной антибактериальной терапии.
В широком смысле к абсцессам брюшной полости в абдоминальной хирургии относят внутрибрюшинные (интраперитонеальные), забрюшинные (ретроперитонеальные) и интраорганные (внутриорганные) абсцессы. Внутрибрюшинные и забрюшинные гнойники, как правило, располагаются в области анатомических каналов, карманов, сумок брюшной полости и клеточных пространствах ретроперитонеальной клетчатки. Внутриорганные абсцессы брюшной полости чаще образуются в паренхиме печени, поджелудочной железы или стенках органов.
Пластические свойства брюшины, а также наличие сращений между ее париетальным листком, сальником и органами, способствуют отграничению воспаления и формированию своеобразной пиогенной капсулы, препятствующей распространению гнойного процесса. Поэтому абсцесс брюшной полости еще называют «отграниченным перитонитом».
В 75% случаев абсцессы располагаются внутри- или забрюшинно; в 25% — внутриорганно. Пиогенная флора абсцессов чаще полимикробная, сочетающая аэробные (кишечную палочку, протей, стафилококки, стрептококки и др.) и анаэробные (клостридии, бактероиды, фузобактерии) микробные ассоциации. Причины абсцесса:
- Перитонит. В большинстве случаев формирование абсцессов брюшной полости связано с вторичным перитонитом, развивающимся вследствие попадания в свободную брюшную полость кишечного содержимого при перфоративном аппендиците; крови, выпота и гноя при дренировании гематом, несостоятельности анастомозов, послеоперационном панкреонекрозе, травмах и т. д. Типичными местами локализации служат большой сальник, брыжейка, малый таз, поясничная область, поддиафрагмальное пространство, поверхность или толща тканей паренхиматозных органов.
- Инфекционные процессы в малом тазу. Причиной абсцесса могут выступать гнойные воспаления женских гениталий – острый сальпингит, аднексит, параметрит, пиовар, пиосальпинкс, тубоовариальный абсцесс.
- Заболевания органов ЖКТ. Встречаются абсцессы брюшной полости, обусловленные панкреатитом: в этом случае их развитие связно с действием ферментов поджелудочной железы на окружающую клетчатку, вызывающим выраженную воспалительную реакцию. В некоторых случаях абсцесс брюшной полости развивается как осложнение острого холецистита или прободения язвы желудка и 12-перстной кишки, болезни Крона.
- Инфекции забрюшинного пространства. Псоас-абсцесс может являться следствием остеомиелита позвоночника, туберкулезного спондилита, паранефрита.
По ведущему этиофактору различают микробные (бактериальные), паразитарные и некротические (абактериальные) абсцессы брюшной полости.
В соответствии с патогенетическим механизмом выделяют посттравматические, послеоперационные, перфоративные и метастатические гнойники.
По расположению относительно брюшины абсцессы делятся на забрюшинные, внутрибрюшинные и сочетанные; по количеству гнойников — одиночные или множественные.
По локализации встречаются:
- поддиафрагмальные,
- межкишечные,
- аппендикулярные,
- тазовые (абсцессы дугласова пространства),
- пристеночные
- внутриорганные абсцессы (внутрибрыжеечные, абсцессы поджелудочной железы, печени, селезенки).
В начале заболевания при любом виде абсцесса брюшной полости превалирует общая симптоматика: интоксикация, интермиттирующая (перемежающаяся) лихорадка с гектической температурой, ознобами, тахикардией. Часто отмечается тошнота, нарушение аппетита, рвота; развивается паралитическая кишечная непроходимость, определяется выраженная болезненность в зоне гнойника, напряжение брюшных мышц. Симптом напряжения мышц живота наиболее выражен при абсцессах, локализующихся в мезогастрии; гнойники поддиафрагмальной локализации, как правило, протекают со стертой местной симптоматикой. При поддиафрагмальных абсцессах может беспокоить боль в подреберье на вдохе с иррадиацией в плечо и лопатку, кашель, одышка.
Симптомы тазовых абсцессов включают абдоминальные боли, учащение мочеиспускания, понос и тенезмы вследствие рефлекторного раздражения мочевого пузыря и кишечника. Для забрюшинных абсцессов характерна локализация боли в нижних отделах спины; при этом интенсивность боли усиливается при сгибании нижней конечности в тазобедренном суставе. Выраженность симптоматики связана с величиной и локализацией гнойника, а также с интенсивностью проводимой противомикробной терапии.
Обычно при первичном осмотре абдоминальный хирург обращает внимание на вынужденное положение пациента, которое он принимает для облегчения своего состояния: лежа на боку или спине, полусидя, согнувшись и т. д. Язык сухой, обложен сероватым налетом, живот незначительно вздут. Пальпация живота обнаруживает болезненность в отделах, соответствующих локализации гнойного образования (в подреберье, глубине таза и др.). Наличие поддиафрагмального абсцесса характеризуется асимметрией грудной клетки, выпячиваем межреберий и нижних ребер. В общем анализе крови обнаруживаются лейкоцитоз, нейтрофилез, ускорение СОЭ.
Решающая роль в диагностике абсцесса брюшной полости отводится рентгенологическому обследованию. Как правили, обзорная рентгенография брюшной полости позволяет выявить дополнительное образование с уровнем жидкости. При контрастном исследовании ЖКТ (рентгенографии пищевода и желудка, ирригоскопии, фистулографии) определяется оттеснение желудка или петель кишечника инфильтратом. При несостоятельности послеоперационных швов контрастное вещество поступает из кишечника в полость абсцесса. УЗИ брюшной полости наиболее информативно при абсцессе верхних ее отделов. При сложностях дифференциальной диагностики показано проведение КТ, диагностической лапароскопии.
Хирургическое лечение проводится под прикрытием антибактериальной терапии (аминогликозидов, цефалоспоринов, фторхинолонов, производных имидазола) для подавления аэробной и анаэробной микрофлоры. Принципы оперативного лечения всех видов абсцессов заключаются во вскрытии и дренировании, проведении адекватной санации. Доступ определяется локализацией гнойника: поддиафрагмальные абсцессы вскрывают внебрюшинно или чрезбрюшинно; абсцессы дугласова пространства – трансректально или трансвагинально; псоас-абсцесса – из люмботомического доступа и т. д.
При наличии множественных абсцессов выполняется широкое вскрытие брюшной полости. После операции оставляют дренаж для активной аспирации и промывания. Небольшие одиночные поддиафрагмальные абсцессы могут быть дренированы чрезкожно под ультразвуковым наведением. Однако при неполной эвакуации гноя велика вероятность рецидива гнойника или его развития в другом месте субдиафрагмального пространства.
При одиночном абсцессе прогноз чаще благоприятный. Осложнениями абсцесса может явиться прорыв гноя в свободную плевральную или брюшную полость, перитонит, сепсис. Профилактика требует своевременного устранения острой хирургической патологии, гастроэнтерологических заболеваний, воспалительных процессов со стороны женской половой сферы, адекватного ведения послеоперационного периода после вмешательств на органах брюшной полости.
источник
Абсцесс брюшной полости – это неспецифический воспалительный процесс, при котором между внутренними органами формируется полость, заполненная гнойным содержимым. Стенками образования могут выступать анатомические углубления, «карманы», листки сальника или связок. Заболевание обычно сопровождается интоксикацией организма и выраженным болевым синдромом.
Клиническая картина болезни зависит от локализации, вида и давности абсцесса. Характер и интенсивность жалоб также напрямую связаны с общим состоянием организма человека, болевым порогом. Встречаются случаи, когда пациента беспокоят лишь незначительные боли в животе и субфебрильная лихорадка.
-
волнообразная лихорадка от 37,5 °C до 39-40 °C с ознобом и потливостью;
- учащенное сердцебиение (тахикардия) на фоне гипертермии;
- общая интоксикация (головная боль, тошнота, ухудшение аппетита, слабость);
- бледность или мраморность кожных покровов;
- боли в животе различной интенсивности и локализации, которые могут распространяться на грудную клетку, поясничную область;
- локальное напряжение мышц передней брюшной стенки.
Возможно присоединение признаков пареза кишечника: запоры, сильное вздутие живота, рвота. В клиническом анализе крови обнаруживаются изменения, характерные для острого воспалительного процесса: повышенные значения СОЭ, лейкоцитоз с нейтрофилезом.
Особенность клинической картины абсцесса также зависит от его локализации:
- Поддиафрагмальный абсцесс. Чаще всего образуется после оперативных вмешательств на брюшной полости, в результате травм. Типичная локализация – справа, в области печени. При таком расположении боли возникают в правом подреберье и могут иррадиировать в грудную клетку, правое надплечье, усиливаться во время ходьбы, при кашле.
-
Печеночные абсцессы. Зачастую имеют множественный характер, развиваются на фоне ранений, инфекций желчевыводящих путей. Болезненные ощущения локализуются в области правого подреберья, реже – в эпигастральной области, характерна постоянная тошнота. Быстрая ходьба, резкие наклоны вперед могут усиливать болевой синдром.
- Аппендикулярный абсцесс. Появляется на фоне воспалительного инфильтрата вокруг измененного аппендикса. На первых стадиях характерно уменьшение болей в подвздошной области, снижение температуры тела. Спустя 6-7 суток симптомы возвращаются с новой силой, и пальпируется болезненное неплотное образование.
- Абсцесс Дугласова кармана. Характеризуется скоплением гноя в позадиматочном пространстве в результате воспалительных заболеваний матки, яичников, маточных труб или аппендикулярного отростка. Кроме сильных болей внизу живота женщину могут беспокоить частые позывы на мочеиспускание, акт дефекации, чувство распирания в этой области, диарея.
-
Межкишечные абсцессы. Появляются за счет скопления гноя между петлями тонкой, толстой кишки; чаще всего множественные. Пациента беспокоят постоянные ноющие или острые боли в животе без точной локализации, тошнота, рвота. Парез кишечника сопровождается метеоризмом, запорами, асимметрией живота.
Полости с гноем в области поджелудочной железы, селезенки встречаются реже и имеют сходные признаки с острым воспалением этих органов (деструктивный панкреатит, спленит).
К формированию абсцессов в брюшной полости может привести:
- хирургическое вмешательство с несоблюдением правил антисептики, «забытый» инструментарий, салфетки;
- ножевые, тупые травмы живота, огнестрельные ранения;
- острый холецистит, деструктивный панкреатит, перфоративная язва 12-перстной кишки или желудка;
- острый флегмонозный аппендицит, воспаление придатков матки;
- разлитой перитонит.
В формировании гнойных полостей большую роль играет микробная инфекция, некрозы тканей, несколько меньшую – паразитарные инвазии.
При появлении характерных для гнойного воспаления жалоб следует обратиться к терапевту, который после осмотра и опроса должен перенаправить пациента к соответствующему специалисту. Это может быть врач- хирург или врач-гинеколог. В случае острого развития симптомов или резкого ухудшения состояния, рекомендуется вызвать бригаду скорой медицинской помощи, которая доставит больного в специализированное отделение.
Для подтверждения диагноза, а также для поиска его причины могут быть назначены такие исследования:
-
Ультразвуковая диагностика органов брюшной полости. Методика отлично подходит для поиска осумкованного гноя в области печени, селезенки, под диафрагмой, в Дугласовом пространстве. УЗИ также может помочь определить причину болезни (острый аппендицит или панкреатит, гнойный сальпингоофорит и т.д.).
- Компьютерная томография. Исследование назначается в случае малоинформативности УЗИ, для обследования труднодоступных зон. КТ позволяет выявить не только локализацию образования, но и количество абсцессов, их размеры.
- Обзорная рентгенография брюшной полости. Методика позволяет отличить поддиафрагмальный абсцесс от печеночного или межкишечного. Полости с гноем выявляются в виде округлых образований с уровнем жидкости.
-
Клинический, биохимический анализы крови, исследование крови на стерильность. В пользу воспалительного процесса говорит высокий лейкоцитоз с нейтрофильным сдвигом формулы, высокие значения СОЭ, повышение печеночных ферментов, появление С-реактивного белка, прокальцитонина.
- Диагностическая лапароскопия. Исследование брюшной полости выполняется через прокол в стенке живота с помощью специальной аппаратуры – эндоскопа. При необходимости такая диагностика может закончиться полноценной операцией.
Основной метод лечения сформировавшихся в брюшной полости абсцессов – хирургический. В обязательном порядке назначается один или несколько антибактериальных препаратов с широким спектром воздействия. При необходимости используют антипаразитарные средства, ингибиторы протеолитических ферментов, человеческие иммуноглобулины.
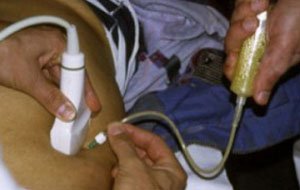
При поддиафрагмальных, подпеченочных и при межкишечных абсцессах дренирование осуществляется через переднюю брюшную стенку под контролем УЗИ. Если гной скопился в малом тазу, то доступ происходит через прямую кишку или позадиматочное пространство.
При неэффективности предыдущего метода, в случае труднодоступного расположения абсцесса выполняется общий доступ путем срединного разреза. В обязательном порядке в брюшной полости оставляют дренажи для дальнейшего оттока гноя, регулярного промывания растворами антисептика.
Ингибиторы протеолиза («Гордокс», «Контрикал») помогают остановить процессы распада ткани, а также улучшают проникновение антибактериальных препаратов в место воспаления. При недостаточном ответе пациента на системную противомикробную терапию к лечению добавляют иммуноглобулины, которые содержат антитела против большого количества микроорганизмов.
При отсутствии должного лечения возрастает риск развития таких осложнений:
- Разлитой перитонит вследствие разрыва капсулы абсцесса. Проявляется острой болью, ухудшением состояния, появлением сильного напряжения мышц брюшного пресса, тахикардией, лихорадкой.
- Сепсис – системная ответная реакция организма на гнойное воспаление. Характеризуется выраженной интоксикацией, образованием некрозов во внутренних органах и полиорганной недостаточностью.
В случае проведения оперативного вмешательства, аспирации гноя и назначения адекватной антибактериальной терапии, прогноз заболевания является благоприятным — возможно полное излечение.
источник
Абсцессом брюшной полости является воспаление органов брюшной полости гнойного характера с дальнейшим их расплавлением и образованием в них гнойной полости различного размера с наличием пиогенной капсулы. Он может сформироваться в любой части брюшной полости с формированием целого ряда клинических синдромов: септического, интоксикационного, лихорадочного.

Количество проводимых хирургических вмешательств на органах брюшной полости постоянно растет. Это, применение огромного числа самых разнообразных антибиотиков, а также сильное ослабление иммунной системы организма вследствие быстрой урбанизации приводит к частому развитию послеоперационных абсцессов брюшной полости. По статистике, послеоперационный осложнения в виде образования абсцессов развиваются у 0,8% пациентов после плановых полостных оперативных вмешательств и у 1,5% — после экстренных операций.

Как правило, абсцессы брюшной полости развиваются после получения различных травм, перенесения инфекционных заболеваний ЖКТ, воспалительных процессов в органах, которые находятся в брюшной полости, а также вследствие перфорации дефекта при язве желудка или двенадцатиперстной кишки.
- Следствие вторичного перитонита, (перфоративный аппендицит; несостоятельность анастомозов после полостных операций, панкреонекроз после операции, травматические повреждения) и т. д.
- Воспаления внутренних женских половых органов гнойного характера (сальпингиты, воспаление придатков яичников, гнойные параметриты, пиосальпинксы, тубоовариальные абсцессы).
- Острый панкреатит и холецистит, неспецифический язвенный колит.
Остеомиелит позвоночника, спондилит туберкулезной этиологии, воспаление околопочечной клетчатки.
Основными возбудителями абсцессов являются аэробная (Escherichia coli, протеи, Staphylococcus и Streptococcus и др.) и анаэробная (Clostridium, Bacteroides fragilis, Fusobacteriales) бактериальная флора.

Очень часто абсцессы органов брюшной полости развиваются вследствие хирургических вмешательств на органах брюшной полости (чаще всего, после операций на желчных путях поджелудочной железы, кишечнике). Бывают случаи, когда брюшина инфицируется уже после проведения вмешательства, особенно, при несостоятельности анастомоза.
В 70% случаев абсцесс развивается в внутрибрюшинно или в забрюшинной области, в 30% он локализуется внутри какого-либо органа.

Абсцесс брюшной полости развивается вследствие гиперреактивности иммунной системы при активном росте и размножении стрептококковой и стафилококковой флоры, а также кишечной палочки (аппендикулярный абсцесс). Возбудители проникают в брюшную полость лимфогенным или гематогенным путем, а также контактно через фаллопиевые трубы, когда происходит деструктивное воспаление органов или органа, ранение, перфорация, несостоятельность швов, которые были наложены в процессе хирургического вмешательства.
Основным отличием абсцесса брюшной полости является тот факт, что очаг воспаления четко ограничивается от здоровых тканей, которые его окружают. Если пиогенная оболочка разрушается, развивается сепсис и гнойные затеки. Гнойники могут быть как одиночными, так и многочисленными.

Первые признаки абсцесса брюшной полости варьируются, но в большинстве случаев у пациентов наблюдаются:
- Резкая лихорадка, озноб, которое сопровождается слабо выраженными тянущими ощущениями в области живота, которые усиливаются при пальпации.
- Частые позывы к мочеиспусканию (так как брюшная полость находится недалеко от мочевого пузыря.
- Запоры.
- Тошнота, которая может сопровождаться рвотой.
Также другими объективными симптомами абсцесса брюшной полости являются:
- Тахикардия, повышенное артериальное давление.
- Напряжение мышц передней стенки живота.
Если абсцесс поддиафрагмальный, то среди основных симптомов также присутствуют:
- Болевые ощущения в районе подреберья, которые могут усиливаться во время вдоха и иррадиировать в лопатку.
- Изменением в ходьбе пациента, он начинает наклонять туловище в сторону дискомфорта.
- Высокая температура тела.

Если не диагностировать абсцесс брюшной полости вовремя и не начать правильное лечение, могут возникнуть достаточно серьезные последствия:
Именно поэтому, если вы почувствовали какой-либо дискомфорт или боль в области живота, необходимо сразу же обратиться за помощью к гастроэнтерологу или терапевту.

Основными методами диагностики являются:
- Рентген органов грудной и брюшной полости.
- Ультразвуковое исследование.
- КТ и МРТ как вспомогательные методы диагностики.
- Взятие пункции из заднего свода влагалища или передней стенки прямой кишки (если существует подозрение на развитие абсцесса дугласовой зоны).

Если диагностировать абсцесс не удается из-за отсутствия каких-либо симптомов, на могут быть назначены анализы, в том числе и общий анализ крови. При этом заболевании у пациента практически всегда наблюдается лейкоцитоз, иногда нейтрофиллез (резкий сдвиг лейкоцитарной формулы влево), а также увеличение СОЭ.

С помощью рентгена органов грудной полости можно заметить, что на пораженной стороне купол диафрагмы высоко стоит. В плевральной зоне можно увидеть реактивный выпот. При поддиафрагмальном абсцессе на рентгенологических снимках можно заметить газовый пузырь и уровень жидкости под ним.
«Золотым» стандартом диагностики абсцессов брюшной полости различной локализации является ультразвуковое исследование. УЗИ-признаками являются: четко очерченное жидкостное образование в капсуле, содержимое которого неоднородное и имеет вид нитевидной структуры или эхогенной взвеси. Имеет место так называемый эффект реверберации из-за газов, когда многократные отражения звука постепенно уменьшают его интенсивность.
Лечение заключается в проведении хирургической операции, целью которой является устранение гнойника и дренирование с помощью катетера.
Медикаментозное лечение не дает возможности вылечить абсцесс брюшной полости, но с помощью различных антибиотиков можно ограничить распространение инфекции. Именно поэтому врачи назначают их пациентам до и после хирургического вмешательства. Преимущественно используют препараты, которые способны подавить развитие кишечной микрофлоры. В некоторых случаях также рекомендованы антибиотики, которые проявляют активность по отношению к анаэробным бактериям, в том числе и к Pseudormonas.
Метронидазол. Эффективное противомикробное и противопротозойное средство. В лекарстве находится активное вещество метронидазол. Он способен восстанавливать 5-нитрогруппу внутриклеточными протеинами у простейших и анаэробных бактерий. После восстановления данная нитрогруппа взаимодействует с ДНК бактерий, вследствие чего происходит угнетение синтеза нуклеиновых кислот возбудителей и они погибают.
Метронидазол эффективен в борьбе с амебами, трихомонадами, бактероидами, пептококками, фузобактериями, эубактериями, пептострептококками и клостридиями.
Метронидазол обладает высокой абсорбцией и эффективно проникает в пораженные ткани и органы. Дозировка является индивидуальной и устанавливается лечащим врачом в зависимости от состояния пациента. Больным с непереносимостью метронидазола, эпилепсией в анамнезе, заболеваниями центральной и периферической нервной системы, лейкопенией, неправильной работой печени использовать препарат запрещено. Также нельзя назначать во время беременности.
В некоторых случаях применение средства может вызывать: рвоту, анорексию, диарею, глоссит, панкреатит, мигрени, вертиго, депрессию, аллергию, дизурию, полиурию, кандидоз, частое мочеиспускание, лейкопению.
Профилактические меры основываются на адекватном и своевременном лечении различных заболеваний органов, которые находятся в брюшной полости. Также очень важно вовремя поставить правильный диагноз при остром аппендиците и сделать операцию по его удалению.

источник
Малые инвазивные вмешательства при интрапаренхиматозных и межпетельных абсцессах брюшной полости УЗИ в лечении абсцессов паренхиматозных органов
В детской хирургической клинике МОНИКИ разработана и внедрена методика лечения абсцессов брюшной полости у детей путем чрескожных пункций и дренирований под контролем УЗИ. Лечению с помощью этих методов подвергались абсцессы паренхиматозных органов и различных отделов брюшной полости и забрюшинного пространства, а также мягких тканей передней брюшной стенки (табл. 6.5).
Метод был использован нами у 34 детей с 50 абсцессами, в возрасте от 3 нед до 15 лет. По локализации абсцессы, подвергшиеся чрескожным пункциям и дренированиям, распределились следующим образом: 27 абсцессов печени; 8 — око- лопеченочных (подпеченочные и надпеченочные, расположенные над V сегментом печени); 7 — подциафрагмальных; 4 — полости таза; 2 — забрюшинного пространства и по 1 — селезенки и передней брюшной стенки. При пункции абсцесса передней брюшной стенки использовался ультразвуковой контроль, так как гнойник был двухкамерным, а также для исключения проникновения в брюшную полость.
Частота применения чрескожных пункций и дренирований
| Локализация абсцессов | Количество абсцессов | Проведено пункций | Проведено дренирований |
| Печень | 27 | 10 | 21 |
| Около печени | 8 | 2 | 8 |
| Под диафрагмой | 7 | 2 | 7 |
| Полость таза | 4 | 5 | |
| Забрюшинное пространство | 2 | 3 | |
| Передняя брюшная стенка | 1 | 1 | |
| Селезенка | 1 | 1 | |
| Всего. | 50 | 15 | 45 |
У 22 человек с помощью чрескожных пункций или дренирования было санировано по одному абсцессу; у 10 — по два; у 1 ребенка — три и у 1 — пять абсцессов. Только при использовании чрескожных пункций было излечено 10 абсцессов и 40 — посредством чрескожного дренирования. Всего у детей этой группы было произведено 15 пункций и 45 дренирований; т.е. 9 абсцессов было излечено после однократно проведенной чрескожной пункции и 1 — после двукратной; в 36 случаях чрескожное дренирование было использовано однократно; повторное дренирование в 3 наблюдениях проводили дважды и в 1 — трижды; у 4 детей дренированию предшествовали чрескожные пункции.
Повторные дренирования проводились для замены дренажа на более толстый и. в случаях выпадения дренажа из полости.
Минимальный диаметр пунктированного абсцесса — 1,3 см, максимальный — 10 см. Максимальный объем гноя, удаленного одномоментно, — 380 мл (из 2 забрюшинных абсцессов у одного ребенка в возрасте 2 мес).
Показаниями для применения чрескожных пункций и дренирований под контролем УЗИ являются:
- наличие у больного абсцессов паренхиматозных органов (печени, селезенки), абсцессов брюшной полости, прилежащих к передней, боковой стенкам живота или к прямой кишке (поддиафрагмальные, подпеченочные, латеральных каналов, забрюшинные, полости малого таза);
- достоверная визуализация абсцесса при эхографии;
- диаметр абсцесса более 15 мм;
- абсцессы паренхиматозных органов должны находиться в стадии деструктивных изменений, т.е. являться вполне сформированными полостными образованиями.
Большой объем абсцессов, множество их у одного больного, внутриполостные перегородки, неизвестная этиология абсцес-
сов паренхиматозных органов, маленький возраст пациентов (вплоть до новорожденное™) и тяжелое состояние не являются противопоказанием для чрескожных инвазивных вмешательств. При сочетании внутриорганно расположенных абсцессов с разлитым гнойным перитонитом чрескожное дренирование может быть использовано как самостоятельный метод лечения перед лапаротомией для санации других отделов брюшной полости.
Основным показателем для решения вопроса о проведении чрескожнои пункции или дренирования для нас являлся размер абсцесса. Если один из трех размеров не превышал 3—3,5 см, для санации гнойника назначали чрескожную пункцию, однако эти показатели не являлись абсолютными. Во внимание принимались возраст ребенка, его общее состояние, а также вязкость гноя и степень опорожнения полости через иглу при проведении чрескожнои пункции.
Предоперационная подготовка сводилась к очистительной клизме, детоксикационной инфузионной терапии и устранению грубых метаболических нарушений. Подготовка занимала, как правило, не более суток. Средний срок от установления диагноза до проведения чрескожнои пункции или дренирования в нашей клинике составил 1—2 дня. Для абсолютного большинства наблюдений это явилось дооперационным кой- ко-днем.
Чрескожные пункции и чрескожные дренирования производились в операционной под внутривенным наркозом. При дренировании абсцессов печени, поддиафрагмальных и крупных подпеченочных абсцессов проводили интубацию трахеи с использованием миорелаксантов. Устранение дыхательных движений в момент продвижения иглы дало возможность сократить время пункции, увеличивало точность попадания и позволяло избежать травмирования плевральных синусов. Особенно важно это было у детей младшего возраста, так как дыхательная экскурсия у них дает значительное смещение печени.
Манипуляции проводились хирургом и врачом ультразвуковой диагностики. Для пункций использовался линейный биопсийный датчик частотой 3,5 МГц с направителем. У новорожденных детей пунктирование проводилось методом «свободной руки» под визуальным контролем с использованием секторного датчика с частотой 7,5 МГц. Для пункций применяли иглы эхотипа фирмы «COOK» (Дания) длиной 15—20 см с внутренним диаметром 1,05—1,5 мм или иглы аналогичных параметров многоразового использования. Для дренирования — наборы для одномоментного проведения катетера на пункци- онной игле с мандреном, дренажи типа «свиного хвоста» фирмы «COOK», силиконовые дренажи с внутренним диаметром 2—3 мм. Для абсцессов с неоднородным по структуре, густым за счет преобладания тканевого детрита, фибрина содержимым
выбирали более толстые иглы и дренажи. Мелкие абсцессы с однородным, анэхогенным содержимым пунктировались иглами диаметром 1,05 мм.
После укладки на операционный стол операционное поле обрабатывалось стандартно, затем спиртовой раствор йода смывался 70 % спиртом. Пункционный датчик и часть провода помещались в длинный стерильный полиэтиленовый пакет. Таким образом достигалась абсолютная стерильность всех контактирующих поверхностей. Внутренняя часть пакета смачивалась спиртом или стерильным гелем.
Кожа рассекалась скальпелем на 0,3 см. Далее под постоянным УЗ-контролем пункционная игла плавно проводилась до границы образования на фоне отключенного дыхания. Ввод иглы в полость производился штыкообразным движением, при этом пунктирующий ощущал эффект «провала» иглы.
Первоначально все гнойные полости пунктировались иглой с мандреном. После получения гноя, забора анализов для посева гнойное содержимое отсасывалось через иглу полностью. Полость промывали раствором антисептиков или изотоническим раствором хлорвда натрия до чистых вод объемами, не превышающими эвакуированных, чтобы не повредить пи- огенную капсулу. Отмывание гноя производилось через иглу, так как, изменяя угол наклона и глубину проникновения, мы получали доступ практически во все отделы полости, что особенно важно при наличии внутриполостных перегородок. Изменить же положение дренажа очень трудно. При отмывании гноя через дренаж осуществляется санация полости лишь в небольшом радиусе дренажа, не достигая периферии по всей окружности.
Все эти манипуляции производили под постоянным УЗ- контролем. Обязательным условием являлась визуализация конца иглы в каждый момент времени.
Если диаметр абсцесса не превышал 3 см, после отмывания гноя в полость вводили раствор антибиотиков широкого спектра действия из расчета на массу тела ребенка, затем иглу удаляли. Крупные, расположенные поверхностно абсцессы брюшной полости дренировали металлическим троакаром после рассечения кожи, затем в его просвет вводили силиконовый дренаж. Приводим клинический пример.
Больной Г., 9 лет, поступил в ДХО МОНИКИ 6.11.96 г. с диагнозом: состояние после удаления гангренозно-перфоративного аппендицита (22.10.96 г.), перитонита. Абсцесс брюшной полости?
При поступлении жалобы на боли в правом подреберье. Температура тела 38,3 °С. Живот вздут, болезненный при пальпации в правой половине. В клиническом анализе крови л. 23 • 10″/л, СОЭ 48 мм/ч, выражен сдвиг формулы крови влево. При УЗИ выявлено незначительное увеличение печени за счет правой доли. В VI сегменте печени и подпеченочно лоцируются 2 прилежащих друг к другу образования,
Рис. 6.11. Сканограммы. Абсцессы VI сегмента печени и подпеченоч- ный абсцесс с разделительной перегородкой у больного Г. а — до лечения; б — после пункции обоих абсцессов. Остаточная сухая по- низкой эхогенности, мелкоячеистой структуры, размерами 4,5×5,0x4,5 см и 2,5×4,5×4 см. Между ними лоцировалась соединительнотканная перегородка (рис. 6.11, а). По другим органам без патологии.
Дано заключение о наличии двух абсцессов — VI сегмента печени и подпеченочного.
В этот же день в операционной под внутривенным наркозом в положении на спине у реберной дуги произведена пункция одноразовым дренажным набором фирмы «COOK» сначала абсцесса печени, а затем из того же доступа — подпеченочного абсцесса. Под визуальным контролем перегородка, разделявшая 2 образования, была разрушена иглой. Из обеих полостей эвакуировано 60,0 мл гноя. Полость промыта до чистых вод. Установлен один дренаж типа свиной хвост. В посевах выделена культура E.coli. Осложнений не было.
При контрольном УЗИ через 4 сут лоцировалась остаточная сухая полость с включениями газа диаметром 17 мм и дренаж в ней (рис. 6.11, б). Температура тела нормализовалась через 2 сут после дренирования, а лейкоцитоз и СОЭ нормализовались к 14-му дню. На 6-е сутки полностью прекратилось отделяемое из дренажа и на 7-е сутки он был удален.
По Сельдингеру дренировались абсцессы печени, расположенные на небольшой глубине, а также локализовавшиеся пристеночно в брюшной полости. При этом через просвет иглы, находящейся в полости абсцесса, вводили проводник. Пункционная игла удалялась. По проводнику после последовательного расширения раневого канала вращательным движением в полость вводили дренаж, проводник удалялся и для уточнения положения дренажа под контролем УЗИ вводилось немного жидкости. Дренирование по Сельдингеру использовалось нами при отсутствии одноразовых наборов для одномоментного дренирования.
Интрапаренхиматозные абсцессы и абсцессы малого таза, прилежащие к прямой кишке, дренировались одномоментно дренажными наборами фирмы «COOK». При этом существенно сокращалось время манипуляции, уменьшалась травмати- зация паренхимы печени. После отмывания гноя через иглу в полость вводили небольшое количество антисептического раствора и игла удалялась. Дренаж фиксировался к коже в положении, при котором отток жидкости из полости был максимальным. Подключалась активная аспирация при помощи отсасывающего приспособления типа гармошки. Полость промывали ежедневно растворами антисептиков. Мы не практиковали постановки двух дренажей.
Нами разработана и внедрена методика двухступенчатого дренирования абсцессов, которая заключается в дренировании уже санированной через иглу до чистых вод гнойной полости. Метод оказался весьма эффективным. Мы считаем, что дренирование уже санированной через иглу полости абсцесса позволяет использовать дренажи меньшего диаметра, что умень
шает риск кровотечения, а также избежать постановки второго дренажа в крупные абсцессы для проточного промывания, сократить срок дренирования.
Контрольные УЗИ осуществляли через 30 мин после чрескожной пункции или дренирования для исключения кровотечения; на следующие сутки — для исключения кровотечения и подтекания жидкости в брюшную полость. В дальнейшем УЗИ проводили ежедневно до стойкой положительной динамики, перед удалением дренажа и перед выпиской.
Дренирование и антибиотикотерапия считались адекватными, если в течение 2—3 сут с момента чрескожной пункции или дренирования полость значительно сокращалась в размерах и содержала незначительное количество жидкости. В клиническом статусе отмечались улучшение состояния больного, отсутствие жалоб, нормализация температуры тела и снижение уровня лейкоцитов.
Дренаж удалялся после нормализации температуры тела, клинического анализа крови, при отсутствии отделяемого при промывании, отсутствии визуализации полости абсцесса при УЗИ.
Приводим наблюдение.
Больной Д., 9 лет, поступил в отделение детской хирургии МОНИКИ 18.08.97 г. с диагнозом: состояние после лапаротомии 15.06.97 г., абсцесс брюшной полости? Из анамнеза известно, что 08.06 мальчик перенес автодорожную травму, а через 7 сут был оперирован в областном стационаре по поводу динамической кишечной непроходимости. Операция закончена наложением подвесной энте- ростомы. В послеоперационном периоде развились септические осложнения. Больной высоко лихорадил, в клиническом анализе крови были выражены изменения воспалительного характера. При рентгенографии органов брюшной полости 15.08 (через 2 мес от начала заболевания) по месту жительства заподозрен абсцесс в поддиафраг- мальном пространстве слева. Ребенок переведен на долечивание в МОНИКИ.
При поступлении мальчик «загружен», кожные покровы землистого цвета, выражен эксикоз. Предъявляет жалобы на боли в пояснице слева тянущего характера. Температура тела 39 °С. ЧСС 104 уд/ мин. Живот несколько вздут, при пальпации болезненный в левой поясничной области. Пальпируются увеличенные печень и селезенка. НЬ — 72 г/л, эр. — 3 • 1012/л, л. — 13,8 • 109/л, СОЭ 40 мм/ч. В посевах крови выделен Str. viridans. В биохимическом анализе крови и клиническом анализе мочи отклонений не обнаружено.
При экстренном УЗИ в отделении 18.08 отмечено увеличение селезенки — длина ее 14,5 см, эхогенность паренхимы повышена. В средних отделах селезенки лоцируется округлое образование 4,2×3,5 см с нечетким, неровным контуром. Содержимое неоднородно — гипоэхогенная центральная часть и гиперэхогенная периферия. Содержания газа в абсцессе не отмечено (рис. 6.12, а).
Заключение: спленомегалия, абсцесс селезенки. Гепатомегалия. Произведена разметка абсцесса на кожу для дренирования под кон-
Рис. 6.12. Сканограммы. Абсцесс селезенки у больного Д. а — до лечения; б — после пункции и дренирования. Полость абсцесса исчезла.
тролем УЗИ. 19.08 под наркозом выполнена чрескожная пункция образования — получен гной. Эвакуировано 35 мл густого гноя. Полость промыта до чистых вод. Абсцесс дренирован. Осложнений не было. В посевах гноя выделен Str viridans.
При контрольном исследовании 21.08 (через 2 сут после дренирования) отмечалась выраженная положительная динамика. Лоцировал- ся дренаж и небольшая зона неоднородности вокруг. Полость абсцесса не определялась (рис. 6.12, б).
При динамическом УЗ-наблюдении отмечено, что пристеночные абсцессы брюшной полости уменьшаются в размерах вплоть до полного исчезновения быстрее, чем в случаях их интрапаренхиматозной локализации, когда остаточные полости, как правило, небольшого диаметра, могут сохраняться длительно, до 1,5 мес.
Перед удалением дренажей из полостей, расположенных внутрипеченочно, в случаях появления желчи по дренажу, выполнялась фистулография для определения истинных размеров остаточной полости, исключения затекания контрастного вещества за ее пределы, а также сообщения с желчными протоками. Помимо этого, контрастное вещество оказывало склеро- зирующее действие на остаточную полость.
Отдаленные результаты были прослежены нами у 9 детей „ через 2—6 мес после чрескожного дренирования крупных абсцессов печени с целью выявить сонографические изменения печеночной ткани. У 5 из них обнаружено очаговое повышение эхогенности в месте располагавшихся ранее абсцессов, но выраженное незначительно. Из структурных изменений отмечено некоторое обеднение печеночного рисунка в зонах «интереса». Скорее всего, это связано с развитием фиброза. Каких-либо отклонений в биохимических анализах крови в отдаленные сроки не выявлено.
Анализируя собственный опыт лечения 50 паренхиматозных абсцессов у 34 детей, можно говорить об успешном применении разработанной нами методики чрескожных пункций и . дренирований абсцессов под ультразвуковым контролем. Осложнений, связанных с проведением манипуляций, не было ни в одном наблюдении. Повторных лапаротомий для санации у- абсцессов не потребовалось ни в одном случае. Повторные ! дренирования проводились в связи с неэффективностью дренирования крупного абсцесса из-за малого диаметра дренажа в 2 наблюдениях, и в 2 случаях — из-за выпадения дренажа из
- полости при промывании.
Мы имели опыт проведения диагностической лапароскопии у 3 больных с уже дренированными абсцессами печени (V, VI,
- VII сегментов). У 2 больных с сепсисом и множественными абсцессами печени лапароскопия проводилась с целью исклю- ‘ чения микроабсцедирования паренхиматозных органов брюш- «ной полости и нагноения асцитической жидкости и у одного больного — с целью обнаружить причину продолжающегося перитонита (была выявлена несостоятельность культи черве- ‘ образного отростка). Во время осмотра печени отмечено, что поверхность ее не изменена, несмотря на неглубокое расположение абсцессов, и выявить точную их бывшую локализацию ;;м при визуальном осмотре затруднительно. Кроме того, в месте прохождения дренажа формировались рыхлые спайки между
брюшной стенкой и капсулой печени, способствуя ограничению воспалительного процесса.
Метод дренирования абсцессов паренхиматозных органов брюшной полости при лапароскопическом контроле является более сложным и, на наш взгляд, не вполне оправданным.
источник
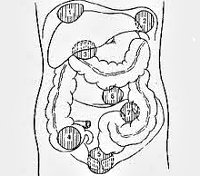


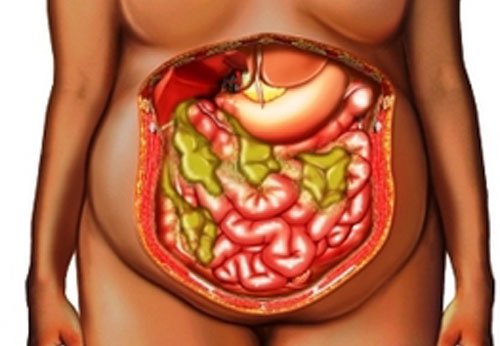
 волнообразная лихорадка от 37,5 °C до 39-40 °C с ознобом и потливостью;
волнообразная лихорадка от 37,5 °C до 39-40 °C с ознобом и потливостью; Печеночные абсцессы. Зачастую имеют множественный характер, развиваются на фоне ранений, инфекций желчевыводящих путей. Болезненные ощущения локализуются в области правого подреберья, реже – в эпигастральной области, характерна постоянная тошнота. Быстрая ходьба, резкие наклоны вперед могут усиливать болевой синдром.
Печеночные абсцессы. Зачастую имеют множественный характер, развиваются на фоне ранений, инфекций желчевыводящих путей. Болезненные ощущения локализуются в области правого подреберья, реже – в эпигастральной области, характерна постоянная тошнота. Быстрая ходьба, резкие наклоны вперед могут усиливать болевой синдром. Межкишечные абсцессы. Появляются за счет скопления гноя между петлями тонкой, толстой кишки; чаще всего множественные. Пациента беспокоят постоянные ноющие или острые боли в животе без точной локализации, тошнота, рвота. Парез кишечника сопровождается метеоризмом, запорами, асимметрией живота.
Межкишечные абсцессы. Появляются за счет скопления гноя между петлями тонкой, толстой кишки; чаще всего множественные. Пациента беспокоят постоянные ноющие или острые боли в животе без точной локализации, тошнота, рвота. Парез кишечника сопровождается метеоризмом, запорами, асимметрией живота.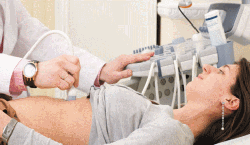 Ультразвуковая диагностика органов брюшной полости. Методика отлично подходит для поиска осумкованного гноя в области печени, селезенки, под диафрагмой, в Дугласовом пространстве. УЗИ также может помочь определить причину болезни (острый аппендицит или панкреатит, гнойный сальпингоофорит и т.д.).
Ультразвуковая диагностика органов брюшной полости. Методика отлично подходит для поиска осумкованного гноя в области печени, селезенки, под диафрагмой, в Дугласовом пространстве. УЗИ также может помочь определить причину болезни (острый аппендицит или панкреатит, гнойный сальпингоофорит и т.д.). Клинический, биохимический анализы крови, исследование крови на стерильность. В пользу воспалительного процесса говорит высокий лейкоцитоз с нейтрофильным сдвигом формулы, высокие значения СОЭ, повышение печеночных ферментов, появление С-реактивного белка, прокальцитонина.
Клинический, биохимический анализы крови, исследование крови на стерильность. В пользу воспалительного процесса говорит высокий лейкоцитоз с нейтрофильным сдвигом формулы, высокие значения СОЭ, повышение печеночных ферментов, появление С-реактивного белка, прокальцитонина.