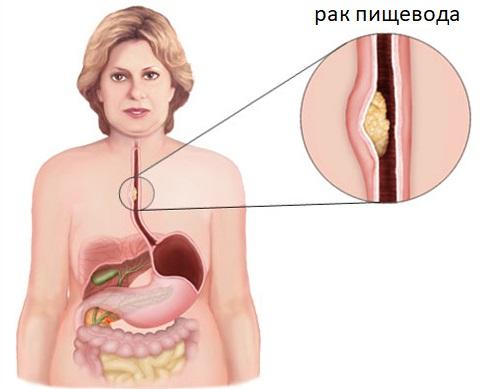
Рак пищевода – это рак, который возникает в пищеводе – длинной полой трубке, которая идет от горла к животу. Пищевод помогает перемещать пищу, которую вы глотаете из задней части горла, в желудок для переваривания.
Рак пищевода обычно начинается в клетках, которые выстилают внутреннюю часть пищевода. Опухоль может возникнуть где угодно вдоль пищевода.
Рак пищевода является шестой по распространенности причиной смерти от рака во всем мире. Показатели заболеваемости различаются в разных географических регионах. В некоторых регионах существует более высокий уровень случаев рака пищевода может быть связан с употреблением табака и алкоголя или с особыми привычками питания и ожирением.
Мужчины заболевают раком пищевода гораздо чаще женщин: на одну заболевшую женщину приходится шесть больных мужчин. Огромное значение имеет пожилой возраст; рак пищевода лишь в исключительных случаях наблюдается раньше 40 лет, обычно болезнь возникает в возрасте от 50 до 60 лет. Наследственность играет роль предрасполагающего фактора, но гораздо большее значение имеют экзогенные влияния: горячая, раздражающая пища, алкоголь, табак и т. п.
Чаще всего рак пищевода бывает первичным, реже он распространяется с соседних органов (из желудка, гортани). Метастазы из более отдаленных мест являются исключительной редкостью. Анатомически следует различать две формы: твердую (скирозную), которая встречается чаще всего, и мягкую (вегетативную), имеющую наклонность к изъязвлению или к усиленному разрастанию. Над опухолью обычно образуется маловыраженное циркулярное расширение пищевода.
По гистологическому строению рак пищевода — это чаще всего плоскоэпителиальный рак, имеющий по своему характеру доброкачественное течение; он растет медленно, не дает той типичной кахексии, которая быстро появляется при раке желудка; при нем отдаленные метастазы появляются относительно редко.

Тяжесть ракового поражения пищевода главным образом заключается в том, что он быстро суживает просвет пищевода, дает его стриктуру, которая может через 3-4 месяца полностью обтурировать пищевод. Зависит это от циркулярного расположения лимфатических сосудов, по которым идет рост опухоли. Таким образом, главным моментом, определяющим положение подобных больных, являются угроза голодной смерти и обеднение организма жидкостью.

Дисфагия, или затруднение при прохождении пищи, является основным симптомом рака пищевода. Чтобы оценить его важность, достаточно указать, что в 85% всех сужений пищевода причиной является рак, поэтому всякое медленно развивающееся затруднение при прохождении пищи в возрасте после 45 лет всегда заставляет подозревать его.
Раковая дисфагия начинается постепенно, но она медленно и верно прогрессирует. Сначала больной чувствует затруднение при прохождении твердой пищи (сухой хлеб, куски мяса), ему приходится есть медленнее и, прежде чем проглотить, долго и старательно пережевывать пищу; затем становится трудно есть кашицеобразные и полужидкие блюда, и больной переходит на жидкую пищу. Наконец, при полной обтурации пищевода по нему перестает проходить и жидкость. Однако нужно иметь в виду, что состояние установившейся дисфагии может временно прерываться периодами улучшения вследствие или распада опухоли, или прекращений сопутствующего опухоли спазма, или затихания воспалительных явлений, возникших вокруг рака. Этот симптом особенно тягостен для больных, потому что они обыкновенно сохраняют хороший аппетит в противоположность больным раком желудка, у которых он рано пропадает.
Затруднение при прохождении пищи обыкновенно прогрессирует при раке пищевода. Рано или поздно появляется второй признак — срыгивание или настоящие пищеводные рвоты. Еще до появления срыгивания больные часто жалуются на обильное слюнотечение (в результате пищеводно-слюнного рефлекса). Эти слюнотечения бывают настолько велики, что слюна, накапливающаяся в изобилии над опухолью, стенозирующей пищевод, служит первым поводом для появления срыгивания густыми, слизистыми массами, к которым иногда примешиваются прожилки крови. В дальнейшем (с прогрессированием стеноза) эти срыгивания наступают вскоре после глотания, а затем несколько позже. Срыгиваемые массы содержат непереваренные куски проглоченной пищи, несвернувшееся молоко, и все это перемешано с большим количеством густой слизи.
Третьим признаком являются боли — загрудинные и подложечные. Они не являются постоянными симптомами рака пищевода, однако наблюдаются нередко в результате сдавления растущей опухолью разнообразных и многочисленных нервов, проходящих вблизи пищевода. Их локализация разнообразна: то спереди за грудиной, то сзади между лопатками, то на шее, между ребрами и под ложечкой. Иногда они симулируют стенокардические приступы.
При раке пищевода не нужно забывать и о других компрессионных симптомах, возникающих вследствие роста опухоли и распространения ее на органы грудной полости. Ларингоскопия нередко обнаруживает парез голосовых связок, особенно левой, даже тогда, когда нет изменений со стороны голоса больного. Это — признак сдавления возвратного нерва, который чаще наблюдается при аневризме дуги аорты. В некоторых случаях сужение зрачка, уменьшение глазной щели, ретракция глазного яблока и аномалия потоотделения на одной стороне лица и шеи заставляют подозревать сдавление симпатического нерва.
Появление одышки и судорожного кашля объясняется ростом опухоли по направлению к трахее и бронхам; иногда констатируются стенотическое дыхание и ослабление дыхательного шума. Одним из тяжелых осложнений является образование пищеводно-бронхиального или трахеального свища, когда пищевод сообщается с дыхательными путями и в выделяемой мокроте появляются пищевые массы. Такой свищ легко диагностируется на рентгеновском экране или появлением в мокроте проглоченной больным подкрашенной жидкости. Эти свищи обыкновенно скоро ведут к аспирационной пневмонии и легочной гангрене. Другим тяжелейшим осложнением рака пищевода являются прорастание опухолью аорты и возможность смертельного артериального кровотечения.
Как последствие вторичной инфекции могут возникнуть околопищеводные нагноения, влекущие за собой целый ряд тяжелых осложнений: абсцессы в средостение, перикардиты, гнойные плевриты и пневмотораксы, легочные абсцессы и пр. Отдаленные метастазы при раке пищевода обыкновенно редки, самым излюбленным их местом являются печень и желудок. Похудание и истощение таких больных — это следствие хронического голодания, а не раковой кахексии, которая является столь характерной для рака желудка.
источник
С раком пищевода сталкивается семь процентов всех больных онкологией, что говорит о большой распространенности этого заболевания среди других злокачественных болезней. Что такое онкология пищевода необходимо знать каждому, кто попадает в группу риска, поскольку только своевременная диагностика и терапия могут избавить пациента от онкологического процесса и продлить ему жизнь.
Развитие злокачественного новообразования в пищеводе происходит в слизистом слое, патология возникает в результате малигнизации нормальных эпителиальных клеток пищевода. В основном данное заболевание локализуется в среднем или нижнем отделе органа, и опасно тем, что может произойти сужение просвета пищевода, но это зависит от размера опухоли. Наиболее часто патология возникает у мужчин в возрасте старше шестидесяти лет. Злокачественное новообразование пищевода может пускать метастазы не только в ближние, но и в дальние органы.
Точные причины возникновения рака пищевода и желудка неизвестны, но специалисты выделяют некоторые факторы, способные провоцировать раковую опухоль в пищеводе:
- Генетическая предрасположенность. Ученым удалось установить взаимосвязь онкологии пищевода с генной аномалией (мутирует ген p53). Во время этого в организме начинается выработка патологического белка, не способного защищать кишечник и пищевод от патологических клеток. Рак чаще всего поражает людей, у родственников которых уже были онкологические заболевания пищеварительной системы.
- ВПЧ. Очень часто во время постановки диагноза в крови пациента обнаруживают вирус папилломы человека, что приводит ученых к мысли о его причастии к злокачественному перерождению клеток.
- Повреждения пищевода. Травмы, которые возникли из-за проглатывания твердой еды или посторонних предметов могут спровоцировать мутацию клеток.
- Термические или химические ожоги. Повреждения пищевода горячей пищей или жидкостью, паром или химическими веществами негативно влияют на структуру клеток. Ожог щелочью может малигнизировать спустя несколько лет.
- Вредные продукты питания. Человек, постоянно употребляющий в пищу острое и маринады, продукты с нитратами, а также пренебрегающий свежими овощами и фруктами рискует столкнуться с онкологией.
- Алкоголизм. Спиртные напитки способствуют обжиганию и истончению слизистой оболочки, а также разрушению ее верхнего слоя.
- Курение. Канцерогены, содержащиеся в табачном дыму, способствуют негативным изменениям эпителиальных клеток. Доказано, что курильщики сталкиваются с раком в четыре раза чаще некурящих людей. Опасным также является пассивное курение.
- Авитаминоз. Дефицит в организме витаминов A, B и E становится причиной потери слизистой тканью защитных свойств.
- Ожирение. Из-за лишнего веса в брюшине повышается давление, что приводит к рефлюксу. Пища из желудка забрасывается в пищевод и приводит к тому, что состояние слизистой ухудшается, возникает такое воспалительное заболевание как эзофагит.
Чаще совокупность факторов провоцирует опухоль стенок пищевода.
Классификация может зависеть от формы роста новообразования, морфологического строения опухоли, ее локализации. Классификация рака пищевода в зависимости от особенностей роста:
- Экзофитная опухоль – происходит рост новообразования внутрь просвета органа и возвышение ее над слизистой оболочкой;
- Эндофитная опухоль – возникновение новообразования в подслизистом слое или внутри тканей;
- Смешанный тип опухоли – новообразование затрагивает все слои стенок пищевода, изъязвляется и быстро распадается.
В зависимости от морфологического строения клеток онкология пищевода делится на:
- Аденокарциному. Данный тип является очень редким, новообразование формируется из железистых клеток, которые продуцируют слизь. Это тяжелая форма рака, которая чаще локализуется около желудка.
- Плоскоклеточный рак пищевода. Распространенная форма онкопатологии, берущая свое начало в клетках плоского эпителия.
К наиболее редким видам рака относятся саркома, лимфома, хорионкарцинома и меланома. Плоскоклеточная карцинома делится на:
- поверхностную, имеющую наиболее благоприятный прогноз и имеющую вид бляшек или эрозий;
- глубоко-инвазивную, захватывающую глубоко лежащие ткани, имеющую форму гриба или углубленной язвы.
Очень редко патология растет в форме полипа, чаще рак опоясывает орган изнутри, вследствие чего наблюдается сужение просвета пищевода, формирующее основную клиническую картину болезни. Установлено, что у пациентов женского пола плоскоклеточный тип рака чаще возникает внизу органа и переходит в верхние отделы, тогда как у мужчин опухоль возникает на грани с желудком.
Плоскоклеточный тип онкологического процесса также разделяется на:
- Плоскоклеточный неороговевающий рак пищевода. Орган практически теряет свою функцию из-за того что его просвет сильно сужается. Человеку трудно глотать пищу и слюну, также он периодически срыгивает.
- Плоскоклеточный ороговевающий рак пищевода. Изменяется поверхность слизистой оболочки, она становится ороговевшей и пересушенной. Размер новообразования быстро увеличивается, но так как в нем медленно образуются сосуды, происходит нарушение питания опухоли и ее частичный некроз.
При дифференцированном раке строение клеток опухоли похожее на здоровые ткани, умеренно дифференцированный плоскоклеточный рак пищевода носит среднюю степень злокачественности, при недифференцированном раке врачу трудно определить, из каких клеток он произошел и какой имеет прогноз.
Онкологический процесс может приостановиться на 1-вой стадии и не развиваться, но потом опухоль начинает стремительный рост.
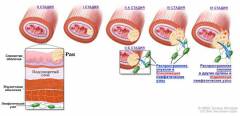
Всего существует четыре стадии рака пищевода:
- Опухоль первой стадии локализуется в верхних слизистых оболочках и подслизистом слое, но не прорастает в мышечную ткань, из которой образован пищевод. Метастазирование на этом этапе отсутствует, а просвет органа не сужается.
- Когда речь идет о второй стадии, то подразумевается прорастание новообразования в мышечный слой. При этом происходит незначительное сужение просвета, но это еще не сопровождается нарушением процесса глотания. Опухоль может незначительно инфильтровать за пределы органа, но это не проявляется выраженной симптоматикой. На второй стадии может быть наличие метастазов в ближайших лимфоузлах, но опухоли в них единичны.
- На третьей стадии развития новообразование прорастает все слои пищевода. Иногда может поражаться клетчатка и серозная оболочка органа. В соседние органы опухоль еще не прорастает, но при обследовании выявляется множественное поражение лимфатических узлов.
- При онкологии 4-й стадии возникает яркая симптоматика, поскольку происходит прорастание новообразования сквозь орган. Опухоль пищевода 4 стадии пускает метастазы в отдаленные органы, просвет настолько сужается, что больной уже не может проглотить даже слюну.
Так как первые две стадии могут протекать бессимптомно, только полное обследование больного дает врачу возможность определить стадию протекания болезни.
Сразу после возникновения рака пищевода симптомы отсутствуют, поэтому заболевание очень редко диагностируется на ранних стадиях. В процессе роста опухоли пищевода возникает проявление дисфагии (затрудненного глотания), которая набирает выраженность в соответствии с увеличением опухоли. Незадолго до ее возникновения у человека могут появиться первые признаки рака пищевода:
- За грудиной начинает царапать;
- Возникает несильный, но навязчивый кашель;
- Человеку кажется, что в пищеводе что-то застряло;
- Во время глотания возникают незначительные болезненные ощущения.
Когда опухоль пищевода начинает понемногу перекрывать просвет, больному становится трудно проглатывать, плохо пережеванные кусочки еды, пища словно образовывает комок в пораженном отделе или прилипает к стенкам органа, но это ощущение проходит после того, как человек попьет. Чуть позже возникает следующий признак онкологии пищевода – становится трудно проглатывать хорошо прожеванную пищу. Человек начинает питаться полужидкими блюдами – пюре, киселями и т.д. Через какое-то время первые симптомы рака пищевода отступают, что говорит о распаде опухоли.
Несколько позже симптомы возобновляются, проявления болезни уже более выражены, кроме проблем с принятием пищи возникают сильные боли за грудной клеткой, которые могут носить жгучий, тупой, либо ноющий характер, или проявляться в ощущении сдавливания. Часто это говорит о том, что плоскоклеточный рак пищевода или другая форма онкопатологии распространилась за черту органа и сдавливает нервные окончания. Чем дальше, тем боль становится сильнее.
Характерный признак рака – дисфагия только усиливается, глотание даже полужидкой пищи становится невозможным и человек переходит на питание бульонами. При нарушении глотания потеря веса является естественной, так как больной практически ничего не есть. Дальше пищевой ком провоцирует рвоту и постоянные срыгивания слюной и слизью. Пищевые остатки приводят к тошноте, неприятному запаху изо рта и налету на языке. Из-за недостаточного питания возникает анемия и истощение организма. На этом этапе у мужчин и у женщин с раком возникает слабость, чувство постоянного голода.
- голосовые связки или возвратный нерв – осиплость голоса;
- трахею и бронхи – пищеводно-трахеальный или пищеводно-бронхиальный свищ, что приводит к кашлю при употреблении жидкости, пневмония, абсцесс, гангрена легкого;
- легкие – болевой синдром в грудной клетке, набухание ямки под ключицей, одышка;
- органы средостения – перикардит или медиастинит;
- узлы симпатической нервной системы – сужение зрачков, нарушение их реакции на световой раздражитель, опущение века, западение глазного яблока, краснота кожного покрова на лице и другие признаки синдрома Бернара-Горнера.
Так как выраженная симптоматика возникает только на поздних стадиях болезни, необходимо периодически проходить обследование, что позволит выявить патологию на самом начальном ее этапе.
Для постановки диагноза необходимо проведение всестороннего полноценного обследования. Только совокупность лабораторных и инструментальных исследований помогает выявить патологию, позволяет добиться понимания стадии развития болезни, а также определиться с выбором методов терапии.
Диагностика рака пищевода подразумевает следующие виды исследований:
- Рентгеноскопия – исследование проводится с использованием контрастного вещества (жидкого бария), которое пациент должен выпить. Метод позволяет увидеть сужение просвета пищевода, состояние его стенок, язвы.
- Эзофагоскопия – при помощи тонкой трубки с маленькой камерой на конце врач осматривает внутреннюю поверхность органа. С помощью процедуры можно также взять биологический материал для дальнейшего исследования.
- Бронхоскопия – с помощью эндоскопа доктор определяет, в каком состоянии находятся голосовые связки, бронхи и трахея. Во время проведения манипуляции возможно увидеть метастазы, находящиеся в этих органах.
- Компьютерная или магнитно-резонансная томография – в момент диагностики рака пищевода при помощи КТ или МРТ врач составляет точную картину изменений, произошедших не только в пищеводе, но и во всех отделах организма, куда пошло метастазирование.
- УЗИ – с помощью ультразвукового исследования можно выявить новообразование, определить, каких оно размеров, а также найти участки вторичного поражения в других органах и лимфоузлах.
- Диагностическая лапароскопия – при помощи лапароскопа, введенного в брюшину в области пупка, врач осматривает органы, находящиеся в брюшной полости, а также проводит пункционную биопсию новообразования.
Обязательными лабораторными методами диагностики являются общеклинические анализы крови и мочи, биохимический анализ крови. Также сдаются онкомаркеры на рак. Онкомаркеры – это специфические белки, которые вырабатывает опухоль, их можно найти в венозной крови, которая сдается натощак. Когда врач будет уверен в диагнозе, он может назначать терапию.
Как лечить рак решается в зависимости от стадии болезни. Также врач учитывает, есть ли метастазы и каково общее состояние больного. Лечение рака пищевода часто проводится при помощи лучевой терапии и химиотерапии, но самым эффективным лечением рака пищевода является проведение операции в гастроэнтерологии. Эти методы терапии проводят как отдельно друг от друга, так и в совокупности, в каждом конкретном случае врач индивидуально подходит к выбору тактики избавления от онкологического процесса.
Операция при раке пищевода проводится, если новообразование локализовано внизу или посредине органа. Хирургическое вмешательство помогает в восстановлении просвета и нормализации питания человека. Операция может проводиться двумя способами:
- Пораженная часть пищевода вырезается вместе с опухолью. При этом врач захватывает по пять сантиметров здорового органа с обеих сторон. В тяжелых случаях может проводиться резекция верхнего отдела желудка. Часть органа, которая осталась, подшивается к желудку.
- Если поражен средний отдел, то спереди брюшины доктор делает отверстие для зонда, который вставляется в желудок для введения пищи, а пищевод удаляется полностью. Во время операции врач также может удалить лимфоузлы, если их поразили метастазы. Спустя год после успешной операции при условии отсутствия метастазов проводится повторное хирургическое вмешательство по созданию искусственного пищевода, используя для него участок тонкого кишечника. Если не выдержать такой большой перерыв, то могут возникнуть тяжелые последствия.
После оперативного вмешательства восстановительный период длится около полугода.
Оперативное вмешательство проводится при помощи эндоскопа, введенного через ротовую полость пациента. На конце аппарата находится небольшая камера, а также хирургическая петля. Чтобы расширить просвет врач бужирует его с помощью специальных инструментов цилиндрической формы. Такой вид операции менее травматичен, чем традиционное оперативное вмешательство.
Хорошим методом лечения является лучевая терапия. При небольших опухолях она может выступать как самостоятельный вид лечения или проводиться в несколько курсов до и после хирургического вмешательства. Ионизирующее облучение приостанавливает рост опухоли и не дает делиться раковым клеткам. Постепенно новообразование становится меньше. Облучению поддается само новообразование, а здоровые ткани остаются нетронутыми.
Химиотерапию проводят совместно с облучением, отдельно химическая терапия не дает положительного эффекта. Клетки опухоли погибают под воздействием токсических и ядовитых препаратов, но в то же время могут погибать и здоровые клетки.
С помощью комбинации лучевой и химической терапии за две или три недели до операции можно существенно уменьшить размер новообразования и улучшить прогноз хирургического вмешательства. Также больному ежедневно колют витаминные комплексы и препараты белка. Если естественное питание нарушено не сильно, то человеку перед операцией необходимо принимать в пищу высококалорийные белковые продукты. Если пациент не может кушать самостоятельно, то питание при раке проводится при помощи зонда.
Часто осложнения рака пищевода возникают уже на второй стадии болезни. Чаще всего у человека начинается обструкция пищевода. Новообразование закупоривает просвет, нарушая проходимость пищи в желудок. У пациента истощается организм, что без лечения может привести к летальному исходу. Еще одним осложнением является кровоизлияние по причине распада опухоли. Иногда этот процесс приводит к возникновению перфорации стенок пищевода.
Прогноз рака пищевода зависит от того, на какой стадии заболевания было начато лечение, как организм воспринял терапию и как сильно развита дисфагия. Пятилетняя выживаемость при лечении на первой стадии составляет девяносто процентов. Сколько живут при раковой опухоли пищевода 2 степени зависит от методики лечения. При успешной операции пятилетняя продолжительность жизни составляет пятьдесят процентов. На третьей стадии успешность лечения составляет около десяти процентов.
Рак 4 степени очень неблагоприятный в плане прогноза. Человек не может долго жить с метастазами и только десять процентов больных после химиотерапии и облучения могут прожить один год. Своевременная диагностика и новейшие методики лечения позволяют успешно бороться с раком.
На сегодняшний день нет стопроцентных методов, позволяющих избежать онкологического процесса. Профилактика рака пищевода заключается в ведении здорового образа жизни, избегании предрасполагающих факторов и периодическом обследовании у гастроэнтеролога.
источник
Абсцесс легкого — гнойно-деструктивная наполненная гноем полость, окруженная участком воспалительной перифокальной инфильтрации легочной ткани.
Абсцесс легкого — заболевание полиэтиологическое. Острые легочно-плевральные нагноения возникают в результате полимикробного инфицирования аэробно-анаэробными ассоциациями микроорганизмов. Среди них преобладают пневмококк, неспорообразующие анаэробные микроорганизмы (бактероиды, пептококк и др.), золотистый стафилококк, грамотрицательная аэробная палочковая микрофлора (протей, реже кишечная палочка и др.).
Стафилококк, пневмококк встречаются в ассоциации с клебсиеллой, энтеробактером, серрацией, бактероидами. При абсцессах легкого отмечается высокая бактериальная обсемененность (1,0 х 10 4 — 1,0 х 10 6 микробных тел в 1 мл).
К развитию острых абсцессов или гангрены легкого приводят заболевания следующих групп:
• крупозная или вирусная пневмония. Это наиболее частая, если не основная причина образования абсцессов легкого;
• аспирация инородных тел, опухоли или рубцы, суживающие просвет бронха и нарушающие тем самым его дренажную функцию с условиями для развития микрофлоры, проникающей из бронхов;
• септикопиемии, тромбофлебит, другие гнойные заболевания, которые могут привести к поражению легких гематогенным или лимфогенным путем с развитием пневмонического очага;
• травматические повреждения (открытые и закрытые) легочной ткани с первичным или вторичным инфицированием.
Эмболические абсцессы легкого чаще бывают множественными и локализуются в периферических отделах обоих легких. Асептические инфаркты легких абсцедируют крайне редко.
При острых гнойных поражениях легких инфицирование происходит наиболее часто аэрогенным путем. Это трансбронхиальное попадание микроорганизмов с развитием пневмонии, когда инфекционный агент перемешается в направлении респираторных отделов с потоком воздуха. Редко встречается аспирационный путь инфицирования, а гематогенно-эмболическое инфицирование наблюдается крайне редко.
Процесс абсцедирования в легком может протекать по-разному. И.С. Колесников, М.И. Лыткин (1988) выделяют три возможных варианта (типа) развития деструктивного процесса в легком.
Абсцедирование 1-го типа развивается на фоне обычной благоприятной динамики воспалительного процесса в легком через 1,5-3 нед от начала пневмонии. После улучшения состояния больного вновь повышается температура тела, увеличиваются боли в груди, ухудшается общее состояние с проявлениями нарастающей интоксикации. Это все заканчивается выделением гнойной мокроты.
Абсцедирование 2-го типа обычно происходит в течение 3-4 нед от начала пневмонии и клинически проявляется как затянувшаяся пневмония при безуспешности лечения. Сохраняются постоянно высокая температура тела на протяжении всего периода болезни, выраженная интоксикация, потом появляется гнойная мокрота, количество которой увеличивается.
Абсцедирование этих типов приводит к постпневмоническим абсцессам.
Абсцедирование 3-го типа приводит к аспирационным абсцессам. В этих случаях деструкция в легком начинается с первых дней, а абсцесс формируется через 5-10 дней от начала болезни.
Деструктивные заболевания легких часто поражают социально неустроенных людей, многие из которых страдают алкоголизмом. В последние годы обращает на себя внимание увеличение числа больных молодого возраста, употребляющих наркотики. Больные поступают в больницу, как правило, поздно, до госпитализации лечение либо не проводится, либо проводится неадекватно.
Заболевание возникает преимущественно у мужчин (80-85 %), наиболее часто в возрасте 20-50 лет (80-90 %). Чаще поражается правое легкое. Абсцесс может локализоваться в различных отделах легких, но наиболее часто встречается в верхней доле правого легкого. Клинические проявления абсцесса развиваются на фоне предшествующего патологического процесса в легком. Чаще всего это крупозная, гриппозная пневмония или ателектаз легочной ткани. Семиотика острого абсцесса определяется многими факторами, но в первую очередь фазой развития процесса, общим состоянием организма, вирулентностью флоры.
Формирование абсцесса сопровождается гнойной инфильтрацией и расплавлением легочной ткани, когда сообщения полости гнойника с просветом бронхов еще нет. В этой фазе клиническая картина абсцесса легкого весьма сходна с клинической картиной тяжелой пневмонии. Абсцесс легкого сопровождается общим тяжелым состоянием, болями при дыхании на пораженной стороне грудной клетки, высокой температурой тела, кашлем, притуплением перкуторного звука и бронхиальным, а иногда ослабленным дыханием над абсцессом; лейкоцитоз нарастает до 16-30 х 109/л, отмечается выраженный сдвиг лейкоцитарной формулы влево.
При рентгенологическом исследовании видна ограниченная тень различной интенсивности и величины.
Описанные явления нарастают в течение 4-10 дней, затем обычно гнойник прорывается в бронх и начинается вторая фаза острого абсцесса с кашлем и выделением обильной (до 200—800 мл/сут) зловонной гнойной мокроты, содержащей множество лейкоцитов, эритроцитов, бактерий и эластических волокон, а также тканевой детрит. При преобладании некроза в полости абсцесса мокрота бывает особенно зловонной, нередко с примесью крови. При отстаивании мокрота делится на три слоя: нижний из гноя и распавшихся тканей, средний из желтоватой прозрачной жидкости и верхний из пенистой жидкости.
Количество отделяемой мокроты при абсцессе легкого не соответствует размеру полости гнойника. При малых абсцессах мокроты может быть много и, наоборот, при большой полости гнойника количество мокроты может быть незначительным. Количество отделяемой мокроты зависит от сопутствующего бронхита, от распространенности пневмонических изменений, проходимости дренирующих бронхов.
Диагностика абсцесса легкого представляет трудности в ранней фазе развития до прорыва в бронх. Нередко абсцесс смешивают с очаговой пневмонией и другими заболеваниями. Наиболее постоянные симптомы: кашель с мокротой, боли в груди, усиливающиеся по мере вовлечения плевры в воспалительный процесс, высокая температура, постоянная или с большими колебаниями и проливными потами. В крови высокий лейкоцитоз с нейтрофилезом, повышенная СОЭ.
Данные перкуссии, аускультации и рентгенологического исследования хотя и не патогномоничны для острого абсцесса легкого, в ряде случаев позволяют предположить диагноз до вскрытия абсцесса в бронх или плевральную полость. КГ, выполненная в эту фазу развития абсцесса, часто разрешает диагностические сомнения, так как выявленная неоднородная структура воспалительного инфильтрата с участками разной плотности указывает на начинающийся процесс деструкции в легком.
После вскрытия абсцесса в бронх его диагностика значительно облегчается: диагноз устанавливают на основании отхождения обильной мокроты, чему предшествовал тяжелый воспалительный процесс в легком. Физикальные методы обследования обычно подтверждают диагноз абсцесса легкого. Большую роль в уточнении характера и локализации процесса играют рентгенологическое исследование, КТ, позволяющие точно определить полость в легком с газом и жидкостью.
Основной метод диагностики гнойных заболеваний легких — рентгенологический, установление очага деструкции в легком при этом играет основную, но не исчерпывающую роль. Важное значение имеют топическая диагностика — определение локализации патологического процесса в легком, состояние легочной ткани.
Рентгенологические изменения при абсцессе легкого бывают различными. Наиболее частый вариант (до 70 % наблюдений) — это одиночная полость в легком с жидкостью и воспалительной инфильтрацией легочной ткани вокруг. Полость чаще округлой формы с четкими контурами внутренних стенок, но возможны и неправильная форма и неровные контуры стенок.
В 10—14 % случаев острого абсцесса определяется массивное затемнение легочной ткани, обусловленное воспалительным процессом без признаков распада инфильтрата. Также изменения бывают при затянувшейся пневмонии с выраженным гнойным пневмонитом, поражением интерстициальной ткани и нарушением дренажной функции бронхов, выраженным региональным лимфаденитом в корне легкого.
В подобных случаях КТ позволяет выявить полости деструкции легочной ткани в зоне воспалительной инфильтрации. В клиническом плане такие изменения соответствуют длительному, хроническому воспалительному процессу в легком. В сомнительных случаях КТ увеличивает диагностические возможности рентгенологического исследования.
Все эти методы не дают четкой информации о состоянии бронхиального дерева исследуемого легкого. Отсутствие каких-либо изменений легочного рисунка при рентгенологическом исследовании и КТ служит основанием для отказа от бронхографии. При «закрытых» (не сообщающихся с бронхом) абсцессах разрешить сомнения в отношении наличия деструкции легочной ткани в зоне воспалительной инфильтрации помогает КТ.
Контрастирование бронхов (бронхография) позволяет определить состояние бронхов, но метод малоэффективен для выявления гнойников в легком, так как полости абсцессов не заполняются контрастным веществом из-за отечности слизистой оболочки дренирующих бронхов, а также из-за заполнения гнойника гноем, тканевым детритом.
Переход острого абсцесса легкого в хронический характеризуется не только временным фактором, но и определенными морфологическими изменениями в самом абсцессе, окружающей легочной ткани и прилежащих бронхах, сосудах.
Рентгенологическая семиотика длительных как одиночных, так и множественных абсцессов включает в себя тени неравномерной интенсивности и различной распространенности. Окружающая полость абсцесса легочная ткань имеет среднее уплотнение с резко деформированным легочным рисунком и соединительнотканными тяжами.
Состояние лимфатических узлов при неспецифическом лимфадените выявляют при рентгенологическом исследовании. Определяют расширение тени корня легкого, смазанность его структуры. Томография, КТ позволяют дифференцировать такие изменения и определить увеличение лимфатических бронхопульмональных узлов. Подобные изменения регионарных лимфатических узлов являются постоянным признаком абсцесса легкого.
Подобная картина не играет существенной диагностической роли, но изменения в узлах в процессе лечения оценивают как показатель эффективности проводимой терапии. Уменьшение размера, исчезновение узлов — благоприятный прогностический критерий. Лимфатические узлы остаются увеличенными еще в течение 1—2 мес после рубцевания абсцесса.
Бронхоскопия позволяет оценить состояние бронхов, определить дренирующий бронх, взять материал для бактериологического исследования, провести санацию абсцесса или катетеризировать дренирующий бронх.
Современные методы исследования (КТ, бронхоскопия) практически исключают необходимость диагностической пункции, так как риск развития осложнений, в частности, гнойного плеврита, значительно превышает диагностическую ценность метода.
Абсцесс легкого в 30 % случаев осложняется эмпиемой плевры или пиопневмотораксом. В этих случаях выполняют торакоскопию, которая часто выявляет бронхоплевральные свищи и позволяет определить их локализацию и размеры, сделать биопсию плевры или легкого для уточнения этиологии заболевания. Плевроабсцессография отражает состояние полости эмпиемы.
Для верификации возбудителя, установления бактериологического диагноза используют посевы бронхиальных смывов и пунктата из зоны деструкции легкого. Среди выделенной флоры преобладают пневмококк, стафилококк, протей (1 х 10 4 — 1 х 10 6 микробных тел в 1 мл) в ассоциации с клебсиеллой, энтеробактером, серрацией, бактероидами, в ряде случаев выявляют кишечную палочку. К результатам микробиологического исследования откашливаемой мокроты необходимо относиться критически ввиду ее смешивания с содержимым ротовой полости.
Острые абсцессы легкого необходимо дифференцировать с кавернозным туберкулезом, актиномикозом, эхинококкозом, нагноением кисты легкого, междолевым осумкованным плевритом, очаговой пневмонией, а также вторичными абсцессами при опухолях легкого. Кавернозный туберкулез обычно исключают при выяснении анамнеза заболевания, отсутствии туберкулезных микобактерий и характерных рентгенологических и КТ изменений в легких за пределами полости, содержащей жидкость.
При актиномикозе в мокроте находят возбудителя друз. Однако обнаружить их нелегко, в связи с чем требуются повторные тщательные исследования. При актиномикозе в процесс вовлекаются соседние органы, стенка трудной клетки.
При нагноившихся паразитарных (эхинококк) и врожденных кистах легких состояние больного не бывает таким тяжелым, как при остром абсцессе, не отмечается предшествующего воспаления легкого; при рентгенологическом исследовании определяются ровные, круглые, четкие контуры тени без перифокального воспаления. Обнаружение в мокроте хитиновой оболочки, дочерних пузырей и крючьев делает диагноз бесспорным.
Особенно трудна дифференциальная диагностика абсцесса при междолевых плевритах, вскрывшихся в бронх, и при других осумкованных плевритах. В таких случаях большую пользу оказывает КТ, позволяющая уточнить истинную природу заболевания.
Дифференцировать абсцесс легкого приходится с распадающимся периферическим раком легкого. Следует отметить, что по виду полости распада при рентгенологическом исследовании дифференцировать абсцесс и рак легкого не всегда представляется возможным. Стенка полости при раке толще, гнойной мокроты нет, но есть кровохарканье. В дифференциальной диагностике распадающегося периферического рака и абсцесса легкого важнее не вид полости и состояние ее внутренних стенок, а наружные очертания затемнения в легких и клинические проявления болезни.
Полость при распаде опухоли, по данным рентгенографии, КТ содержит мало жидкости, но это учитывают лишь при бугристости окружающих полость ткани и толстой стенке полости распада. Играют роль выявляемые при раке отводящие «дорожки», связывающие опухоль с корнем легкого, как раковую имплантацию по пути лимфооттока.
В дифференциальной диагностике абсцесса легкого и туберкулеза с каверной играет роль микробиологическое исследование.
Абсцесс легкого приходится дифференцировать также с аспергиллезом. Распад аспергиломы приводит к образованию полости. Мицелий гриба в мокроте, промывных водах при бронхоскопии, содержимом полости распада позволяет уточнить диагноз аспергиллеза легких.
В дифференциальной диагностике абсцесса легкого учитывают данные комплексного обследования больных: анамнез, клинические проявления, течение болезни, данные инструментальны и лабораторных исследований. Определенную роль играют результаты бактериологического исследования. Исследуют также биоптаты, полученные при бронхоскопии, торакоскопии, транспариетальной пункции. Цитологическому исследованию подвергают промывные воды и мазки-отпечатки, полученные при бронхоскопии.
При острых гнойно-деструктивных заболеваниях легких показана активная комплексная консервативная терапия. Показания к хирургическому лечению возникают при безуспешности консервативной терапии, переходе заболевания в хроническую форму, развитие осложнений (прорыв абсцесса в плевральную полость, средостение с развитием эмпиемы плевры или пиопневмоторакса, гнойного медиастинита, образование бронхиальных свищей, легочное кровотечение).
Комплексная интенсивная терапия включает:
• оптимальное дренирование и санацию полости распада в легком;
• антибактериальную терапию, подбор антибиотиков с учетом чувствительности к ним выделенной микрофлоры;
• коррекцию волемических, электролитных нарушений, устранение гипо- и диспротеинемии;
• дезинтоксикационную терапию: форсированный диурез, плазмаферез, непрямое электрохимическое;
• окисление крови с помощью гипохлорита натрия, УФО крови, гемофильтрацию;
• иммунотерапию;
• калорийное сбалансированное питание, по показаниям — парентеральное питание и инфузию компонентов крови;
• симптоматическое лечение.
Рациональная антибиотикотерапия наряду с активным местным лечением (бронхоскопическая аспирация, санация и т.п.) — основа эффективной консервативной терапии и предоперационной подготовки больных гнойными заболеваниями легких. Применение протеолитических ферментов, обладающих некролитическими и противовоспалительными свойствами, улучшило результаты консервативного лечения и предоперационной подготовки больных гнойными заболеваниями легких. Растворение густого содержимого бронхов и полостей и противоотечное действие энзимотерапии способствуют восстановлению дренажной функции бронхов, нарушение которой играет ведущую роль в патогенезе легочных нагноений.
Таким образом, сочетание антиибиотико- и энзимотерапии представляет собой удачное объединение этиотропного и патогенетического лечения.
Для восстановления проходимости дренирующих абсцесс бронхов осуществляется комплексная бронхологическая санация, ведущая роль в которой принадлежит бронхоскопии. С учетом данных предварительного рентгенологического исследования бронхоскопия позволяет выполнить катетеризацию дренирующего гнойный очаг бронха, промыть его и ввести антисептики, протеолитические ферменты, антибиотики.
При необходимости лечебные бронхоскопии повторяют, что позволяет в большинстве случаев добиться положительного эффекта Для улучшения отхождения мокроты используют протеолитические ферменты, отхаркивающие средства, муколитики. Протеиназы дают протеолитический эффект — разжижают мокроту и лизируют некротические ткани. Протеиназы оказывают противовоспалительное действие и влияют на дренажную функцию бронхов.
При остром абсцессе легкого эндобронхиальное применение ферментов и антисептиков (наряду с общей антибиотикотерапией) быстро устраняет гнойную интоксикацию. Курс комплексных бронхологических санаций, как правило, приводит к полному клиническому выздоровлению с рубцеванием абсцесса. Энзимотерапия дает выраженный эффект и при гигантских гнойниках легкого, когда мало надежды на излечение без хирургического вмешательства.
Одним из компонентов комплексной бронхологической санации является ингаляционное введение лекарственных препаратов. В ингаляциях вводят муколитики, антисептические препараты, протеолитические ферменты и др. Ингаляционная терапия обладает рядом ценных свойств, но играет только вспомогательную роль при консервативном лечении и подготовке к операции больных гнойными заболеваниями легких.
Основными преимуществами эндотрахеальных вливаний лекарственных препаратов являются простота и отсутствие необходимости рентгенологического контроля. Для правильного введения препарата нужно точно знать локализацию гнойного процесса и тщательно соблюдать соответствующие положения грудной клетки. При эндотрахеальном введении лекарственных препаратов, к сожалению, не удается точно доставлять препараты в дренирующий бронх, но при этом препараты распределяются по всей слизистой оболочке бронхов, что важно при диффузном бронхите.
Ингаляции, эндобронхиальные вливания протеолитических ферментов, муколитиков, антисептиков — простые методы санации, но по своей эффективности, скорости достижения результата они уступает лечебной бронхоскопии. Бронхоскопия — основной метод бронхологической санации.
Санационные бронхоскопии выполняют под местной анестезией. Лечебная бронхоскопия с аспирацией содержимого бронхиального дерева, его промыванием и введением лекарственных веществ широко применяется в хирургической клинике и входит в состав комплексной бронхологической санации.
Современные бронхоскопии позволяют выполнять трансназальное введение фиброскопа и производить непрерывное промывание бронхов с инстилляцией лекарственного вещества через один канал и аспирацией через другой. Анестезию производят аэрозольным препаратом 10 % лидокаина.
У больных, выделяющих гнойную мокроту, аспирацию содержимого бронхов производят уже в ходе диагностической эндоскопии, чтобы обеспечить условия для осмотра. Следующим этапом санации является удаление фибринозных наложений и гнойных пробок из устьев бронхов.
Следующий этап бронхоскопической санации — промывание бронхов раствором ферментов. Положение стола изменяют на противоположное дренажному. В бронх, дренирующий гнойные полости, вводят специальную трубку и вливают 25—30 мг химопсина или трипсина, химотрипсина, рибонуклеазы или 1 дозу террилитина на 4—10 мл стерильного изотонического раствора хлорида натрия.
Число промываний зависит от распространенности гнойного процесса и общего состояния больного. Лечебная бронхоскопия должна быть максимально эффективной, а риск, связанный с гипоксемией и гиперкапнией во время повторных эндобронхиальных манипуляций, — минимальным. У тяжело больных лечебную бронхоскопию следует проводить под контролем оксигемографии или оксигемометрии.
Санационные бронхоскопии с катетеризацией абсцесса через сегментарный бронх показаны при неэффективности обычных санационных бронхоскопий. Их проводят под рентгеновским, компьютерно-томографическим контролем.
Дренирование абсцесса при бронхоскопии в определенной мере заменяет обычные бронхоскопические санации.
В ряде случаев выполнить бронхоскопическую санацию не удается (отсутствие бронхоскопа, технические трудности, категорический отказ больного). Это служит показанием к санации бронхиального дерева через микротрахеостому.
Особую тактику применяют у наиболее тяжело больных с декомпенсацией внешнего дыхания, выраженной легочно-сердечной недостаточностью, когда тяжелая одышка и гипоксемия в состоянии покоя являются препятствием для эндотрахеального введения лекарственных веществ. Этим больным противопоказана бронхоскопия, у некоторых из них одна только ингаляция аэрозоля вызывает усиление одышки и цианоз.
В подобной ситуации наряду с парентеральным введением антибиотиков, дезинтоксикационной терапией и т.д. местную ферментную и антибактериальную терапию осуществляют путем транспариетальной пункции абсцесса с аспирацией гноя, промыванием полости раствором антисептика и последующим введением протеолитических ферментов. Благодаря этому обычно уменьшается гнойная интоксикация, улучшается общее состояние больного, частично компенсируются внешнее дыхание и гемодинамические нарушения, что позволяет постепенно перейти к комплексной бронхологической санации.
Пункции острых абсцессов производят при полной непроходимости дренирующего бронха («блокированный абсцесс») или недостаточной эвакуации гноя по нему в случае неэффективной бронхоскопической санации. Точку для пункции намечают под рентгеновским контролем или во время УЗИ, которое визуализирует положение иглы непосредственно во время пункции.
Путем транспариетальной пункции в полость гнойника можно вводить ферментные препараты: химопсин, трипсин, химотрипсин, рибонуклеазу, террилитин. В качестве антисептиков используют растворы гипохлорита натрия, диоксидина, фурагина калия, хлоргексидина.
Транспариетальные пункции, аспирация гноя и введение лекарственных препаратов повторяют ежедневно в течение 3-4 дней. Если улучшается состояние больного, переходят к бронхологической санации. Неэффективность пункционного метода при комплексном лечении служит показанием к наружному дренированию абсцесса. Противопоказанием к введению протеолитических ферментов пункционным методом служит обильное кровохарканье или легочное кровотечение.
Транспариетальное дренирование абсцесса или полости распада при гангрене легкого проводят при недостаточном или полностью нарушенном бронхиальном дренаже, когда бронхоскопическая санация не дает должного эффекта.
Дренирование производят под местной инфильтрационной анестезией под многоосевым рентгенологическим контролем. В связи с инвазивностью дренирование выполняют в рентген-операционной. Возможно попадание гноя или крови (при повреждении легочного сосуда) в бронхиальное дерево, поэтому необходимо предусмотреть оборудование для экстренной бронхоскопии или интубации трахеи.
Микродренирование применяется при абсцессах легких диаметром до 5—8 см с недостаточным или полностью нарушенным бронхиальным дренажем. Дренаж вводят по леске, проведенной через просвет пункционной иглы, и фиксируют его швом к коже. Дренирование при абсцессах легких диаметром более 8 см и гангрене легкого с полостью распада осуществляют с использованием троакара или специальной иглы.
Дренирование с помощью троакара применяют при крупных поверхностно расположенных внутрилегочных гнойных полостях. Дренажную трубку проводят через гильзу троакара.
Дренирование длинной пункционной иглой диаметром 2 мм, на которую надета дренажная трубка, применяют при глубоко расположенных внутрилегочных гнойниках.
После дренирования гнойной полости ее содержимое полностью эвакуируют. Полость промывают раствором антисептика и протеолитических ферментов. Свободный конец дренажа можно оставить открытым под толстой ватно-марлевой повязкой или соединить с трубкой, опушенной под раствор асептической жидкости по Бюлау— Петрову. Применение постоянной вакуум-аспирации зависит от размера гнойной полости. Разрежение при вакуум-аспирации не должно превышать 50 мм вод. ст., чтобы не спровоцировать аррозивное кровотечение.
Гнойную полость промывают через дренаж 3-4 раза в сутки. Количество одномоментно вводимого через дренаж раствора зависит от размеров полости, но при первых промываниях не более 20—30 мл.
Дренаж можно удалить после нормализации температуры тела, прекращения отделения гнойной мокроты и гноя через дренаж. При рентгенологическом исследовании следует убедиться в исчезновении воспалительной инфильтрации вокруг полости, в уменьшении ее размеров и в отсутствии в полости горизонтального уровня жидкости.
Осложнениями пункции и дренирования абсцессов легких являются кровохарканье, пневмоторакс и флегмона стенки грудной клетки, но они наблюдаются редко.
Сочетание лечебной фибробронхоскопии с пункциями или дренированием абсцесса легких создает оптимальные условия для удаления гнойного содержимого и купирования воспаления, а в результате для рубцевания абсцесса. Двойной вариант санации эффективен при секвестре в полости деструкции в легком: санацию выполняют через дренажную трубку при транспариетальном дренировании полости абсцесса и через дренирующий бронх.
Для больных с острыми деструкциями легких, поступивших в торакальное хирургическое отделение, трудно подобрать антибиотики, так как большинство из них получали массивную антибактериальную терапию в терапевтических отделениях или амбулаторно. До выделения верификации и возбудителя проводят эмпирическую антимикробную терапию препаратами широкого спектра действия.
В дальнейшем подбор антибиотиков зависит от чувствительности возбудителей. При тяжелом течении заболевания рекомендуют внутривенное введение антибиотиков, а для создания максимальной концентрации в очаге воспаления возможна катетеризация бронхиальных артерий с последующей региональной антибиотикотерапией.
Важное место в комплексном лечении занимает дезинтоксикационная терапия, которую проводят по общим правилам для больных с тяжелыми гнойными заболеваниями. Эффективность терапии значительно выше, если сеансу плазмафереза, гемофильтрации, непрямого электрохимического окисления крови предшествуют дренирование гнойного очага, удаление гноя, некрэктомия. Плазмаферез имеет явные преимущества перед другими методами, но его применение не всегда возможно по экономическим соображениям.
Иммунотерапию проводят с учетом иммунокорригирующего действия препаратов — гипериммунная специфическая плазма, гамма-глобулины, пентаглобин, габриглобин.
Вариант комплексной консервативной терапии, санации острого абсцесса легкого зависит от дренажной функции бронхов. Можно выделить больных с хорошим, недостаточным бронхиальным дренажем и с полностью нарушенным бронхиальным дренажем.
Показаниями для операции служат неэффективность консервативной терапии и малоинвазивных хирургических манипуляций и развитие осложнений. Комплексная терапия до и после операции позволяет выполнять как резекционные операции, так и разработанный в нашей клинике оригинальный вариант торакоабсцессостомии с последующими некрсеквестрэктомиями и санациями полости распада с применением различных методов химической и физической некрэктомии и использованием видеоскопических технологий. Торакоабсцессостома является основной операцией при гангренозных абсцессах.
При успешном лечении острых абсцессов легкого с применением комплексной терапии гнойник замещается рубцом, полностью исчезают клинические симптомы, а при рентгенологическом исследовании на месте полости абсцесса определяют фиброзные ткани. Если удалось полностью ликвидировать клинические проявления, но при рентгенологическом исследовании определяют небольшие тонкостенные полости в легком, результат лечения считают удовлетворительным (клиническое выздоровление).
Этих больных выписывают из стационара под амбулаторное наблюдение. Оставшиеся полости закрываются самостоятльно через 1—3 мес. Хорошие и удовлетворительные результаты мы наблюдали у 86 % больных, процесс перешел в хроническую форму в 7,8 % случаев.
В хирургическом лечении нуждаются 13,3 % больных.
Показания к оперативному лечению острых абсцессов легких: неэффективность комплекса консервативных и малоинвазивных хирургических методов лечения в течение 6—8 нед, развитие осложнений (легочное кровотечение, рецидивирующее кровохарканье, стойкие бронхоплевральные свищи), переход в хронический абсцесс.
Прогноз при острых абсцессах легких, если своевременно начато комплексное консервативное лечение, для большинства больных (до 90 %) благоприятен. У остальных больных успешное лечение возможно с использованием хирургических методов.
Профилактика острых абсцессов легких тесно связана с предупреждением пневмонии (крупозной, гриппозной), а также со своевременным и адекватным лечением пневмонии.
источник
Рак пищевода – это онкологическое заболевание, при котором на стенке пищевода появляется злокачественная опухоль. Болезнь распространена довольно широко и занимает шестое место среди раковых опухолей. Первыми признаками болезни являются затруднения при глотании грубой пищи, вызванные сужением пищевода.
От рака пищевода чаще страдают люди пожилого возраста. Среди больных больше мужчин. Это связано с тем, что появлению опухоли способствует курение и употребление крепких спиртных напитков. Такие вредные привычки повышают риск развития болезни в десятки раз.
Раковые опухоли чаще всего возникают в среднем и нижнем отделах пищевода. Самая распространенная форма рака пищевода развивается из клеток плоского эпителия. На втором месте аденокарцинома, которая образуется из железистых клеток. В 10% случаев эта форма рака сопровождается опухолью в ротовой полости: рак губы, неба, миндалин, гортани.
На планете существуют районы, где вероятность развития опухоли очень высокая – это «пояс рака пищевода», который находится в Азии. Сюда входят Иран, республики Средней Азии, некоторые районы Сибири, северные области Китая и Японии. Такую особенность связывают с тем, что в этой местности традиционно употребляют много маринованных блюд, а свежих овощей и фруктов значительно меньше. А вот представители негроидной расы болеют в 6 раз реже, чем европейцы.
- Экзофитные опухоли, растущие в просвет пищевода и возвышающиеся над слизистой оболочкой.
- Эндофитные опухоли, растущие в подслизистом слое, в толще стенки пищевода.
- Смешанные опухоли склонны к быстрому распаду и появлению на их месте язвы.
- Плоскоклеточный рак – опухоль развивается из клеток плоского эпителия.
Разновидности:
- поверхностный, в виде эрозии или бляшки на стенках пищевода. Отличается более легким течением, не достигает больших размеров.
- глубоко-инвазивный, поражающий глубокие слои пищевода. Может иметь форму гриба или язвы. Склонен к образованию метастазов в трахею, бронхи и сердце.
0 стадия. Раковые клетки лежат на поверхности пищевода и не проникают вглубь его стенок.
I стадия. Опухоль растет вглубь слизистого слоя, но не затрагивает мышечный. Метастазы отсутствуют. Больной не ощущает никаких признаков болезни, но опухоль хорошо видна при проведении эндоскопии.
II стадия.В некоторых случаях может проявляться нарушение глотания, но чаще болезнь протекает бессимптомно.
Подстадия IIА. Опухоль проросла в мышечный и соединительнотканный слой пищевода, но не затронула окружающие органы и не образовала метастазы.
Подстадия IIВ. Опухоль проросла в мышечную оболочку пищевода, но не поразила наружный слой, однако в ближайших лимфоузлах образовались метастазы.
III стадия. Выражены нарушения глотания, потеря веса и другие признаки рака. Опухоль проросла насквозь все слои пищевода. Она пустила метастазы в окружающие органы и ближайшие лимфатические узлы.
IV стадия. Если метастазы обнаруживаются в отдаленных лимфатических узлах и органах, независимо от размера опухоли, диагностируется IV стадия. На этом этапе лечение затруднено и прогноз неблагоприятный.
На начальных этапах, когда опухоль еще незначительных размеров, человек не ощущает никаких признаков болезни.
Первым симптомом рака пищевода является дисфагия – затруднение при глотании. Появляется ощущение, что проглоченная порция застряла в пищеводе и ее необходимо запить большим количеством воды. В отличие от сужения пищевода при спазме, в этом случае нарушение глотания ощущается постоянно и усиливается со временем.
Некоторые не придают значения такому симптому. Но если провести тщательное обследование на этом этапе, то больной имеет хорошие шансы на выздоровление.
Постепенно опухоль увеличивается в размерах и сужает просвет пищевода. Человек испытывает неприятные ощущения во время еды, он вынужден отказаться от грубой пищи: мясо, яблоки, хлеб. Больной начинает употреблять полужидкие перемолотые блюда: каши, супы-пюре. Но из-за того, что просвет пищевода постепенно сужается, остается возможность глотать только жидкость: бульон, молоко, кисель. Человек почти полностью отказывается от еды и это вызывает сильное истощение. Организм не получает достаточное количество пищи, начинается сильное похудение. Больной ощущает постоянный голод и сильную слабость.
Пищеводная рвота или срыгивание возникает в результате закупорки пищевода, и пища возвращается обратно.
Застой остатков пищи в пищеводе вызывает неприятный запах изо рта, который особенно заметен по утрам. Язык обложен, больной жалуется на тошноту.
Если опухоль распространилась на другие органы грудной полости, то возникают характерные симптомы. Если метастазы (вторичные раковые опухоли) возникли в легких, то появляются тупые боли в груди, одышка, кашель, набухание надключичной ямки.
Если опухоль проросла в возвратный нерв или метастазы распространились на голосовые связки, то наблюдается осиплость голоса.
В результате общей реакции организма на раковую опухоль незначительно поднимается температура до 37,5. У больных отмечается упадок сил и апатия, быстрая утомляемость.
Если возникло подозрение на рак пищевода, то врач назначает исследование для подтверждения диагноза, определения местоположения опухоли, ее степени и наличия метастазов.
Рентгенологическое обследование.
Для того чтобы получить точную картину изменений в пищеводе больному дают выпить контрастное вещество – жидкий барий. Он обволакивает стенки пищевода и орган хорошо видно на снимке. Таким образом, можно выявить сужение просвета пищевода, утолщение или истончение стенок, язву. Выше сужения обычно заметно расширение пищевода.
Эзофагоскопия.
С помощью эндоскопа, тонкой трубки, на конце которой есть крошечная камера, можно осмотреть пищевод изнутри. Трубку осторожно вводят больному через рот, а картинка выводится на экран монитора. При этом удается увидеть все изменения на слизистой оболочке, отличить спазм пищевода от раковой опухоли. Эндоскоп позволяет не только определить размеры поражения, но и взять образец ткани для биопсии.
Бронхоскопия.
Эндоскоп вводят в дыхательные пути, чтобы определить состояние голосовых связок, трахеи и бронхов. Это делается для выявления метастазов в дыхательных органах.
Компьютерная томография (КТ).
Метод основан на действии рентгеновских лучей. Датчик вращается вокруг пациента, лежащего на специальном столе, и делает множество снимков. Потом они сопоставляются в компьютере, и таким образом удается составить подробную картину изменений во внутренних органах. Этот метод позволяет оценить размеры опухоли и прорастание рака в близлежащие органы. А также наличие метастазов в лимфатических узлах и отдаленных органах.
Ультразвуковое исследование (УЗИ).
Пациент лежит на кушетке, а врач водит датчиком по животу. На кожу наносится специальный гель, чтобы улучшить проводимость ультразвука. Излучатель посылает звуковые волны высокой частоты, а датчик улавливает эти волны, отраженные от внутренних органов. Из-за того, что разные ткани по-разному поглощают излучение, удается выявить опухоль. УЗИ помогает определить ее размер и наличие вторичных новообразований в брюшной полости и лимфоузлах.
Лапароскопия. 
Хирургическое лечение применяют в том случае, когда опухоль находится в нижней или средней части пищевода. Его преимущество в том, что в ходе операции удается восстановить просвет пищевода и нормализовать питание.
Первый тип операций: вырезают пораженный участок пищевода, отступая вверх и вниз не менее чем по 5 см. Иногда при этом удаляют и верхний отдел желудка. Оставшуюся часть пищевода подшивают к желудку.
Второй тип операций выполняется при раке среднего отдела пищевода. На передней брюшной стенке создают отверстие в желудок для питания через зонд. После этого полностью удаляют пищевод. Часто одновременно удаляют и пораженные раком лимфатические узлы. Если операция прошла успешно, и не обнаружились метастазы, то примерно через год создают искусственный пищевод из участка тонкого кишечника. Такое растянутое во времени лечение проводят потому, что больной может не пережить обширного вмешательства.
У некоторой группы больных с раком пищевода хорошие результаты дает дистанционная гамма-терапия. Она может применяться самостоятельно или курсами до и после операции. Облучение опухоли ионизирующей радиацией приводит к приостановлению роста и деления раковых клеток. Рак постепенно уменьшается в размерах.
Излучение разрывает связи в молекулах ДНК, которые отвечают за передачу генетической информации дочерним клеткам. Лучевая терапия не так опасна для окружающих здоровых тканей в связи с тем, что она действует преимущественно на раковые клетки, которые активно делятся.
Хорошо себя зарекомендовала комбинация лучевой терапии с химиотерапией. Опухоли значительно уменьшаются в размерах, снижается вероятность появления метастазов. Этот метод используют для лечения больных, которым невозможно сделать операцию.
Курс химиотерапии и лучевой терапии проводится за 2-3 недели перед операцией. Такая схема позволяет значительно повысить шансы на успех лечения.
Большое внимание уделяется подготовке больных к операции. Пациенты бывают сильно истощены, поэтому им ежедневно вводят витамины, питательные жидкости, белковые препараты. Если возможно питание через рот, то дают небольшие порции белковой высококалорийной пищи, соки, морсы. В другом случае больного кормят через зонд.
Полное излечение от рака пищевода возможно. Чем раньше пациент обратился за помощью, тем выше шансы, что опухоль удастся полностью уничтожить и не допустить рецидивов.
Рак пищевода имеет относительно медленное течение и, по сравнению с другими онкологическими заболеваниями, и среднюю степень злокачественности. Часто болезнь проявляет себя только на поздних стадиях и когда больной обращается за помощью, то заболевание уже запущено. Если его не лечить, то прогноз всегда неблагоприятный и срок жизни составляет около 6-8 месяцев. От момента возникновения болезни продолжительность жизни без лечения составляет 5-6 лет.
Если опухоль сильно разрослась и пустила метастазы, то оперировать ее уже нет смысла. В этом случае лучевая терапия продлевает жизнь до 12 месяцев в 10% случаев. Современные методики позволяют улучшить эти показатели.
У больных, которым сделали операцию и провели курс химио- и лучевой терапии, выживаемость более 5 лет составляет:
- на I стадии более 90%;
- на II стадии — 50%;
- на III стадии — около 10%.
Операция при раке пищевода – это единственный шанс на полное выздоровление для больных с I, II и III стадиями. Лучшие результаты наблюдаются у тех пациентов, которые прошли курс лучевой терапии до и после операции.
Операции проводятся пациентам младше 70 лет. При условии, что у них не обнаружены метастазы в других органах.
Противопоказаниями для операции являются:
- Метастазы в лимфатические узлы
- Метастазы в легкие и печень
- Прорастание опухоли в возвратный нерв, аорту, сердце, трахею
- Тяжелые сопутствующие заболевания
- Проблемы в работе сердечно-сосудистой и дыхательной системы.
Таким больным назначается поддерживающее лечение, направленное на улучшение качества жизни.
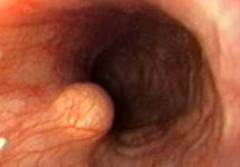
Самыми опасными считаются опухоли среднего отдела. Это объясняется тем, что они имеют особенность прорастать в сердце, трахею и другие органы. Наиболее легкой считается поверхностная форма рака. Такая опухоль имеет вид бляшки, возвышающийся над поверхностью слизистой. Она не достигает больших размеров и не склонна к прорастанию.
Симптомы заболевания:
- Затруднение глотания
- Срыгивание
- Неприятный запах изо рта
- Жгучие боли за грудиной
- Учащение сердцебиения
- Похудание
Существует несколько видов плоскоклеточного рака пищевода.
- Высокодифференцированный рак – это зрелая форма. Клетки склонны к ороговеванию.
- Умеренно дифференцированный рак. Промежуточная форма, встречается чаще других.
- Малодифференцированный плоскоклеточный рак. Незрелая, неороговевающая форма.
Наилучшие результаты в лечении плоскоклеточного рака дает комбинация хирургических методов и лучевой терапии. Курсы гамма-терапии назначаются до и после операции. Если начать лечение болезни на ранних этапах, то вероятность полного выздоровления достигает 80-90%.
При раке пищевода 3-й степени опухоль проросла через все слои пищевода и затронула окружающие органы. На этой стадии обнаруживаются метастазы в ближайших лимфатических узлах.
Если по состоянию здоровья пациенту можно сделать операцию, то это будет обширное вмешательство. Хирург удалит значительную часть пищевода и лимфатические узлы. В этом случае около 10% больных живут более 5 лет.
Если же опухоль затронула жизненно важные органы, то назначается поддерживающее (паллиативное) лечение. В этом случае продолжительность жизни составляет 8-12 месяцев.
Народные методы лечения рака пищевода требует определенной предварительной подготовки. В первую очередь больной должен отказаться от:
- курения
- употребления алкогольных напитков
- острой, сладкой, соленой пищи
- мясных продуктов
- сладостей
- специй и других раздражающих продуктов питания
Во-вторых, в основу рациона должны составлять продукты из твердой пшеницы, сырые овощи, фрукты и различные соки.
В-третьих, необходимо настроиться только на положительный результат. Больной должен воздерживаться от излишних эмоциональных напряжений. Он обязан достичь духовного равновесия. После чего, можно приступать к курсу лечения рака пищевода народными методами.
- Чеснок, мед и подорожник.
Для начала необходимо приготовить сок чеснока. Берем несколько головок чеснока, очищаем их и душим с помощью чесночницы. Потом через марлю продавливаем мякоть, выжимая чесночный сок.
Следующий шаг – приготовить сок подорожника. Проблема заключается в том, что необходимы молодые листья этого растения. А они собираются в конце мая – начале июня. Поэтому заранее позаботьтесь об этом. Листья и стебли подорожника перемалываются на блендере, пересыпаются незначительным количеством сахара. Полученную кашицу настаивают в прохладном месте в течение 5-7 дней. Потом сок процеживается через марлю, и ставят в холодильник.
Помните, что сок подорожника нужно заготовить впрок.
Способ применения.
Сок чеснока пропивают один раз в день, с утра, перед приемом пищи. При этом соблюдается следующая последовательность:
- 1 неделя – 10 капель;
- 2 неделя – 25 капель;
- 3 неделя – 30 капель;
- С 4 недели по 1 ст.л.
Каждая доза сока чеснока запивается 100 гр. сока подорожника. После чего, через 20-30 минут, необходимо съедать 1 ст.л. меда.
Весь курс лечения длится 2 месяца. После чего необходимо сделать перерыв 2-3 недели и повторить курс. Но сок подорожника необходимо продолжать пить на протяжении года. Два раза в день по 1 ст.л. перед приемами пищи.
Лекарство из лопуха.
Для приготовления этого рецепта подойдет как свежий, так и высушенный корень лопуха большого. Корень этого растения перемалывают на мясорубку или в блендере. Далее в полученную массу подмешивают спирт и мед. Все ингредиенты берут в равных пропорциях. Полученную массу ставят в прохладное место на 5-7 дней. После чего средство готово к употреблению.
Лекарство из лопуха необходимо принимать трижды в день по 2 ст.л. за 20-30 мин. до приема еды. Длительность курса – 3 месяца.
Средство из цветков картофеля.
Основу этого народного средства для лечения рака пищевода составляют цветы картофеля. Для приготовления лекарства собирается свежие соцветья картофеля. Потом цветки сушатся в тени. Высушенное соцветие заливают крутым кипятком в пропорции: на 1 ч.л. – 100 гр. кипятка. Потом накрывают крышкой и дают настояться 3-5 ч.
Полученный настой необходимо принимать по 2 ч.л. трижды в день перед приемами пищи. Лечение длится 1 месяц. Помните, что цветы картофеля содержат токсичные вещества, которые и помогают бороться с недугом. При этом необходимо строго соблюдать указанную дозу, иначе возникает угроза пищевого отравления! В таком случае курс лечения цветками картофеля необходимо приостановить на 1-2 недели.
Травяные отвары.
В качестве усиления вышеперечисленных народных методов и профилактики рака пищевода, народная медицина предлагает разнообразные отвары и настойки. Наиболее эффективными считаются отвары из чистотела, мать-и-мачехи, календулы. Для приготовления этих средств необходимо залить 1 стакан, высушенной травы 1 л крутого кипятка. Дать настояться 2 ч. Пропивать по 150-200 гр. трижды в день.
Также рекомендуется пить зеленый чай, придерживаться диетического питания и здорового образа жизни. Вера, сильное желание и народные методы обязательно помогут побороть этот недуг!
Народная медицина помогает многим больным облегчить состояние и продлить жизнь. Однако помните, что операция и лучевая терапия являются более действенными методами. Поэтому, если онколог назначил вам такое лечение, то не стоит заменять его фитотерапией.
Опасность рака пищевода состоит в том, что 40% случаев болезни протекают бессимптомно. Опухоль обнаруживается случайно во время рентгена грудной клетки. Очень часто признаки болезни появляются на поздних стадиях, когда лечение затруднено. Поэтому очень важно не пропустить первые симптомы рака.
Первые признаки рака пищевода:
- Дисфагия – затруднение при проглатывании пищи. Появляется, когда опухоль на 70% перекрыла пищевод. Сначала неприятные ощущения возникают при прохождении через пищевод жесткой пищи, потом и при глотании жидкости. В отличие от спазма желудка, дисфагия носит постоянный характер.
- Боль за грудиной. Часто это ощущение жжения, которое появляется во время еды и отдает в спину. Это свидетельствует о том, что на поверхности опухоли появилась язва.
- Пищеводная рвота. Срыгивание небольших не переваренных порций пищи.
- Неприятный гнилостный запах изо рта. Его появление связано с тем, что пища застаивается в пищеводе.
- Похудание вызвано недостаточным поступлением питательных веществ в организм из-за сужения пищевода.

Степени дисфагии:
- Больной проглатывает жесткую пищу, запивая водой
- Трудности при проглатывании полужидкой пищи
- Нарушение глотания жидкости
- Пищевод полностью перекрыт и в желудок ничего не поступает
При раке желудка больной получает недостаточно питательных веществ. Это приводит к дефициту витаминов и микроэлементов, а также белков, жиров и углеводов. Организм сначала использует жировые запасы, потом начинает расходовать белок из мышц. Это приводит к сильному истощению, падению иммунитета и присоединению вторичных заболеваний. Поэтому важно, чтобы меню больного было полноценным и разнообразным.
Для облегчения прохождения пиши по пищеводу, блюда должны быть полужидкие, протертые. Без частичек, которые бы могли перекрыть просвет. Необходимо дробное питание: 8-10 раз в сутки, но небольшими порциями. Это позволит довести объем пищи до 2,5-3 килограммов и поддержать силы для борьбы с болезнью. Объем жидкости не должен превышать полутора литров.
В продаже есть готовые смеси для питания с необходимым составом полезных веществ. Они выпускаются в виде жидкостей и их удобно использовать в больницах. Они также есть в виде растворимого порошка, наподобие детского питания. Их можно употреблять в домашних условиях.
Необходимо полностью исключить из рациона жирные, копченые и жареные блюда, газированные и крепкие спиртные напитки. Не рекомендуется пить свежее молоко, которое может вызвать процессы брожения в желудке. Специи и приправы необходимо свести к минимуму.
Рекомендуется употреблять: мясные и рыбные бульоны, супы-пюре, протертые блюда из круп с добавлением яиц и сливочного масла, сливки, кисломолочные продукты. Мясные и рыбные блюда лучше готовить на пару, а потом протирать и добавлять немного жидкости. Фрукты и ягоды лучше употреблять в переработанном виде. Они должны быть очищены от кожуры и быть приготовлены в виде пюре, желе или киселей.
Пища должна быть слегка теплой. Это устранит дискомфорт и облегчит ее прохождение по пищеводу.
Для того чтобы предупредить развитие рака пищевода необходимо исключить факторы риска. Сюда входит отказ от вредных привычек: курения и употребления крепких спиртных напитков. Питание должно быть богатым овощами (особенно зелеными листовыми) и фруктами. Одним из методов профилактики признано систематическое употребление небольших доз аспирина.
Людям с высоким риском возникновения опухоли рекомендуется регулярно проходить эндоскопическое обследование. Это относится к пациентам с диагнозом ахалазия пищевода, пищевод Барретта, язвами пищевода, рубцами вследствие ожогов. Осторожность необходимо проявить тем людям, чьи родители страдали от этой формы рака.
Будьте внимательны к своему здоровью и сообщайте врачу обо всех изменениях самочувствия и затруднениях глотания.
источник